化学教学中数据分析能力的培养
邢新侠
(江苏省睢宁高级中学 江苏 睢宁 221200)
定量研究的方法是化学常用的,数据在定量研究中处于核心位置。每一数据出现,我们会结合相关知识分析:它意味着什么?它包含哪些可能性(能干什么)?怎么干?有的同学对数据处理游刃有余,有的则避之不及,如何帮助学生顺利驾驭数据,需要探讨和有计划、有意识地实施。
一、讨论的范围及价值
数据分析类问题有广义、狭义之分,广义的包含所有出现数据的问题,狭义的是给出一组或多组数据,围绕着应用进行分析。狭义的数据分析问题近年来高考试卷都有涉及,有的作为综合题相对独立的一个部分,有的是完整的一个题,以数据为中心展开讨论。
数据分析题有难易之分,容易题只要简单训练一下即可,如托盘天平物码倒置所得读数的处理;物质的量浓度溶液配制中俯视、仰视等对浓度的误差分析。难题占少数但往往令人百思不得其解。
数据分析方法有基本性和不确定性。在中学化学范围内,基本方法可以理解为计算题的常见解法,表现形式为守恒法、差量法、关系式法、极限法、讨论法、图像法等。这可在学习中逐步教给学生,它对新问题的解决有良好迁移作用。数据分析方法有不确定性。分析的目的不同会有不同方法,从同一组数据中会发掘出不同信息,得出不同结论。只要可以从数据中找出规律、趋势和联系,把已知和未知沟通,有关数据建立起有用关系。
教学中培养学生数据处理能力,从中发现不同意义,既减少学生对计算题畏惧,又养成数据分析习惯,培养学生严谨的科学态度、精密的头脑。本文拟面向全体学生,以例说理,便于认识数据基本特点、探讨解题基本规律、总结教学基本思路。
二、利用非典型数据分析题培养分析能力
非典型数据分析题属于广义数据分析。只要有数据,就存在数据分析,习惯上称之为“已知条件分析”。这类问题学生接触较早,教师有意识地引导学生会慢慢地积累许多经验。下面是几个例子。
1.科学家对数据分析的态度,对学生者良好的导向
例1:初中化学有一个元素氩的发现故事,很好地展示了科学家严谨、执着、抓住事实(数据)不放的科学精神。
19世纪80年代英国物理学家瑞利在测定一些气体的密度时发现从空气中得到N2每升重1.2572克,从氨气中得到的N2每升重1.2560克,后者比前者轻千分之一。一般人会忽略这一细微差别,但他确定自己的实验用品、方法没有问题后,反复实验还是这样,就向《自然》杂志的同行求助,得到一些人呼应。迪瓦尔让他看100年前化学家卡文迪许的实验材料,拉姆赛与他交流并研究,又用两年多时间于1894年他们共同发现空气中有新物质氩气,发现了氩元素,为人类做出新贡献,也为自己赢得巨大荣誉。
2.要想办法把数据间关系建立起来
例 2:X、Y、Z、R 分别代表四种元素, 如果aXm+、bYn+、cZn-、dRm-四种离子的电子层结构相同(a、b、c、d为元素的核电荷数),则下列关系式中正确的是( )
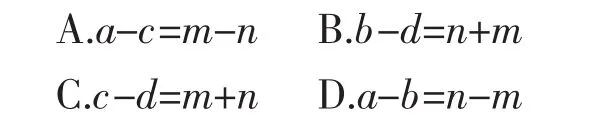
分析:初见此题,复杂的代数关系,从何理起?这就要千方百计建立数据之间关系。在知道符号意义前提下,分析“电子层结构相同”的意义是“电子层数相同且每层电子数也相同”,即离子核外电子数相同,可得数学模型为:a-m=b-n=c+n=d+m,答案 B。
三、利用典型数据分析题培养分析能力
这一类题属于狭义数据分析题。它提供若干实验数据,让我们在比较中看数据特点,找变化趋势、联系,从而发现规律解决问题。这类题与科研、生产、生活中数据分析情境非常接近,能给人许多启示。
1.真实的检验常常要作过量判断
实验室或工业生产中测定某成分含量时,往往不是恰好反应,必须尝试多次,用化学方程式计算就要作过量判断。这是真实的科研生活。
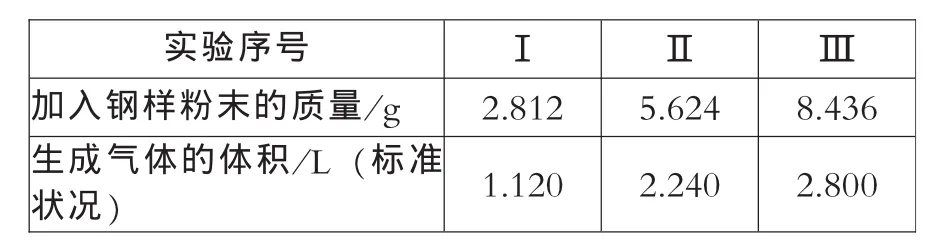
例1:(07年江苏卷第25题第2问)再取三份不同质量的钢样粉末分别加到100mL相同浓度的H2SO4溶液中,充分反应后,测得的实验数据如下表所示:
计算硫酸溶液的物质的量浓度为多少?
分析:这是综合题的一部分,本问关键是找出硫酸完全反应的数据。三次实验中硫酸的物质的量相同,但Ⅰ、Ⅱ加入样品的质量比等于生成氢气的体积比,说明这两次反应中硫酸是足量的,生成氢气的质量由金属的质量决定。Ⅲ加入样品的质量与氢气的体积和Ⅰ、Ⅱ不对应,说明Ⅲ生成氢气的体积由硫酸的量决定,即酸反应完全,金属未反应完。
根据实验Ⅲ可得:
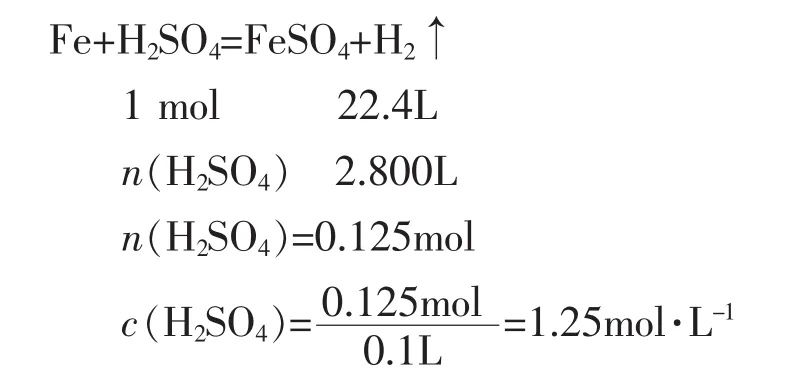
2.正常规律里有时要考虑个别因素
基础知识中的基本规律给我们推理的基础,但事实往往似乎与规律相悖,就要综合考虑各个相关因素了。
例2:(09年江苏卷第17题第3问)控制其他条件相同,印刷电路板的金属粉末用10%H2O2和3.0 mol·L-1H2SO4的混合溶液处理,测得不同温度下铜的平均溶解速率(见下表)。
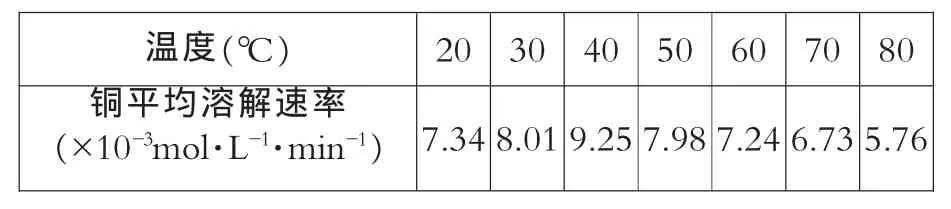
温度(℃) 20 30 40 50 60 70 80铜平均溶解速率(×10-3mol·L-1·min-1) 7.34 8.01 9.25 7.98 7.24 6.73 5.76
当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是________。
分析:这是影响速率变化因素的分析题,40℃前,速率随温度升高变大,符合所学知识。高于40℃,速率随温度升高变小了,不合规律,是浓度减小吗?不至于减小这么快!这时要把“当事人”都看看,悟出H2O2会分解,分解速率随温度升高加快,浓度迅速减小。
答案:H2O2分解速率加快。
3.类比是数据分析常借助的手段
例3:(07年高考理综宁夏卷)工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤。压强及温度对SO2转化率的影响如下表 (原料气各成分的体积分数为:SO27%,O211%,N282%):
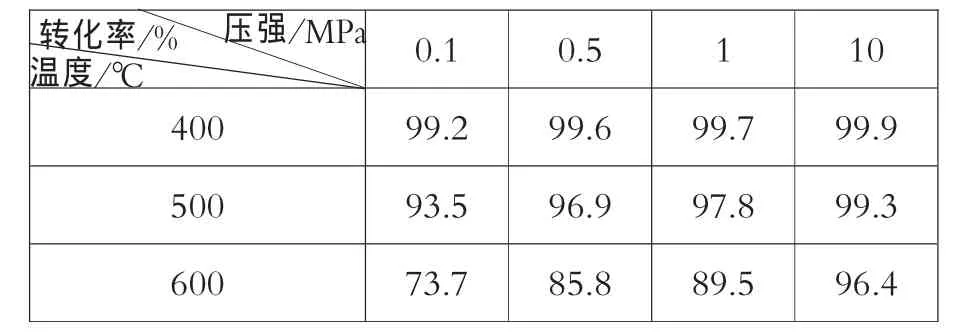
0.1 0.5 1 10 400 99.2 99.6 99.7 99.9 500 93.5 96.9 97.8 99.3 600 73.7 85.8 89.5 96.4压强/MPa温度/℃转化率/%
(1)已知SO2的氧化是放热反应,如何利用表中数据推断此结论? _______________________。
(2)在 400℃~500℃时,SO2的催化氧化采用常压而不是高压,主要原因是:______________。
(3)选择适宜的催化剂,是否可以提高SO2的转化率?___(填“是”或“否”),是否可以增大该反应所放出的热量? ______(填“是”或“否”)。
分析:本题似曾相识,细看就是“合成氨适宜条件选择”的翻版。让人感慨:基础好真是有利于能力提高。
答案:(1)压强一定时,温度升高,SO2转化率下降,说明升温有利于逆反应进行,所以正反应为放热反应;(2)由数据可见400℃或500℃时,增大压强对提高SO2转化率无显著影响,反而会增加成本; (3)否; 否。
4.难题中基础和悟性更显重要
实验序号 Ⅰ Ⅱ Ⅲ加入钢样粉末的质量 /g 2.812 5.624 8.436生成气体的体积/L(标准状况) 1.120 2.240 2.800
例4:(07年广东卷第22题)“碘钟”实验中,3I-+S2O82-=I3-+2SO42-的反应速率可以用 I3-与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,得到的数据如下表:
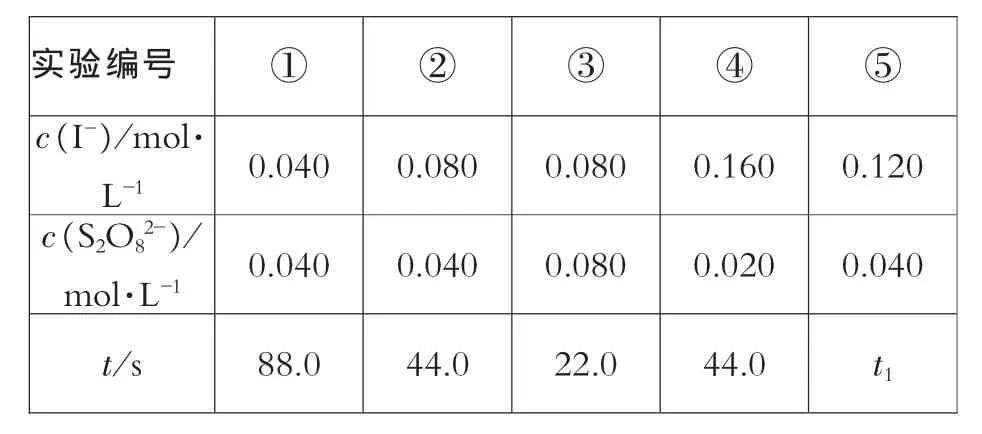
实验编号 ① ② ③ ④ ⑤c(I-) /mol·L-1 0.040 0.080 0.080 0.160 0.120 c(S2O82-) /mol·L-1 0.040 0.040 0.080 0.020 0.040 t/s 88.0 44.0 22.0 44.0 t1
回答下列问题:
(1)该实验的目的是__________________。
(2)显色时间 t1= ________。
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t的范围为_______(填字母)
A.<22.0s B.22.0~44.0s
C.>44.0s D.数据不足,无法判断
(4)通过分析比较上表数据,得到的结论是____________________。
分析:从测定的五组数据解答四个问题,目的不同,方法也不同。第(1)是问实验目的,从题干与数据对比可知答案是:研究反应物I-与S2O2-8的浓度对反应速率的影响。第(2)问显色时间t1,要费些周折,关键是要从数据变化判断出“反应速率与反应物起始浓度乘积成正比,显色时间与反应物起始浓度乘积成反比”。运用自己所得结论对未知实验数据作预测能力,这要基础知识厚实,更要悟性好,而悟性要靠多实践多思考磨砺。利用①、⑤两组数据中 c(S2O82-)相同,而⑤中 c(I-)是①中c(I-)的3倍关系,求出⑤所用显色时间是①的1/3,即 88s÷3=29.3s 。 第(3)问本身就有答案,答案为A,当然知识背景是我们已知的规律:温度越高反应速率越快。第(4)问是在第(2)问中解决的,答案:反应速率与反应物起始浓度乘积成正比(或显色时间与反应物起始浓度乘积成反比)。
数据承载着许多信息,数据在信息社会扮演着重要角色。化学专业的数据分析是学习、研究化学的必须,也是习得、驾驭其他领域数据能力的一个途径。在数据分析中可以了解数据的客观性、丰富性、规律性、多解性等特点。学会用基础知识、基本能力以逻辑的、直觉的、假设的、验证的、比较的、类比的等方法分析数据,提升数据分析能力,增加学习信心和乐趣。

