高产油脂酵母的筛选及发酵条件的研究
,李元,王常, ,, ,2,3
(1.湖北工业大学生物工程学院,湖北 武汉 430068;2.湖北工业大学发酵工程省部共建教育部重点实验室,湖北 武汉 430068;3.湖北工业大学湖北省工业微生物重点实验室,湖北 武汉 430068)
油脂按来源可分为动物油脂、植物油脂和微生物油脂。随着耕地的减少和人口的增加,动植物油脂越来越不能满足生产和发展的需求。微生物油脂由于得天独厚的优势条件(生产不受场地、季节等因素的影响),已引起各国研究者的关注。微生物油脂主要指由多不饱和脂肪酸(Polyunsaturated fatty acids,PUFAs)组成的甘油三酯。PUFAs具有很多生理功能,广泛用于食品、保健、医药、化工等领域。其工业化的最佳途径是发酵法[1]。
作者通过苏丹黑染色初筛及摇瓶发酵复筛,从6种酵母菌中筛选出油脂高产菌株,并对其发酵条件进行了优化。
1 实验
1.1 菌种
汉逊氏酵母(Hansenula)、啤酒酵母(S.cerevisiae)、假丝酵母(Candidaoleophila)、产酯酵母(Saccharomyceteesterproduced)、葡萄酒酵母(S.ellipsoideus)、路哥酵母(Saccharomycodesludwigiilog),自行保存。
1.2 培养基
斜面培养基(g·L-1):葡萄糖20,酵母膏10,蛋白胨20,琼脂20,pH值自然。
种子培养基(g·L-1):葡萄糖20,酵母膏5,蛋白胨6,pH值4.0。
发酵培养基(g·L-1):葡萄糖40,酵母膏4, MgSO4·7H2O 5, KNO39,(NH4)2SO46, NH4H2PO43, pH值5.5。
1.3 接种和发酵
从斜面取一环接种于50 mL(250 mL的三角瓶)种子液中,于28℃、120 r·min-1摇床培养1 d。然后取5 mL种子液接种于45 mL发酵培养基中,28℃、120 r·min-1摇床培养4 d。
1.4 菌种筛选及发酵条件优化
1.4.1 菌种初筛
采用苏丹黑染色法[2]进行初筛。用0.5%的苏丹黑对汉逊氏酵母、啤酒酵母、假丝酵母、产酯酵母、葡萄酒酵母、路哥酵母染色,用二甲苯洗去多余染色液,番红复染后镜检。显微镜下菌丝体呈粉红色,油脂颗粒呈蓝黑色。通过观察不同酵母菌中油脂颗粒的大小及多少,选出油脂产量较多的两种菌进行发酵复筛。
1.4.2 发酵复筛
取初筛得到的菌株发酵,测出各自的细胞量和油脂含量[1],算出油脂产量,确定油脂产量最高的菌种进行发酵条件优化。
1.4.3 发酵条件优化
以细胞量和油脂含量[3]为指标,对初始pH值、温度等培养条件和碳、氮源进行优化。
1.5 分析方法
1.5.1 生长曲线的绘制
取活化后斜面菌种一环,接种于50 mL液体种子培养基中,28℃培养24 h,取5 mL液体转移到45 mL液体种子培养基中,每隔一定时间取样,在600 nm处测定光密度值,以发酵周期为横坐标、OD600值为纵坐标,绘制菌体生长曲线。
1.5.2 细胞量的测定
取一定体积(V)的发酵液于恒重的离心管(m1)中,在3000 r·min-1下离心10 min,弃上清,沉淀用蒸馏水清洗2次,在3000 r·min-1下离心10 min,弃上清,于80℃烘干至恒重后取出,干燥器中自然冷却至室温后称量(m2)。细胞量(g·L-1)依下式计算:

1.5.3 菌体油脂含量的测定
(1)采用索氏提取法[1]。将一定量的干细胞用滤纸包裹放入提取管中,以石油醚为溶剂回流,细胞内油脂随石油醚进入平底烧瓶中,回流6~8 h后,回收石油醚并蒸干平底烧瓶,于电热鼓风干燥箱中烘干称量,计算平底烧瓶提取前后质量差值,可准确测得细胞油脂含量。
(2)采用苏丹黑比色法[3]。取一定体积的发酵液离心洗涤,用0.3%苏丹黑对细胞染色,用乙醇洗去多余染色液,并将细胞溶于同体积去离子水中,以未染色的细胞为参比,在OD580下测吸光度值,胞内油脂含量越高吸光度值越大,据此可快速直观地比较同种菌株不同条件下产油脂情况。吸光度值和油脂含量关系见图1。
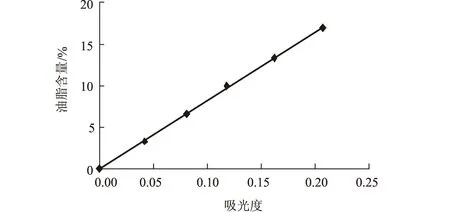
图1 油脂含量与吸光度值关系
2 结果与讨论
2.1 菌种初筛
用苏丹黑染色法[2]对6种酵母染色、镜检,显微镜照片见图2。
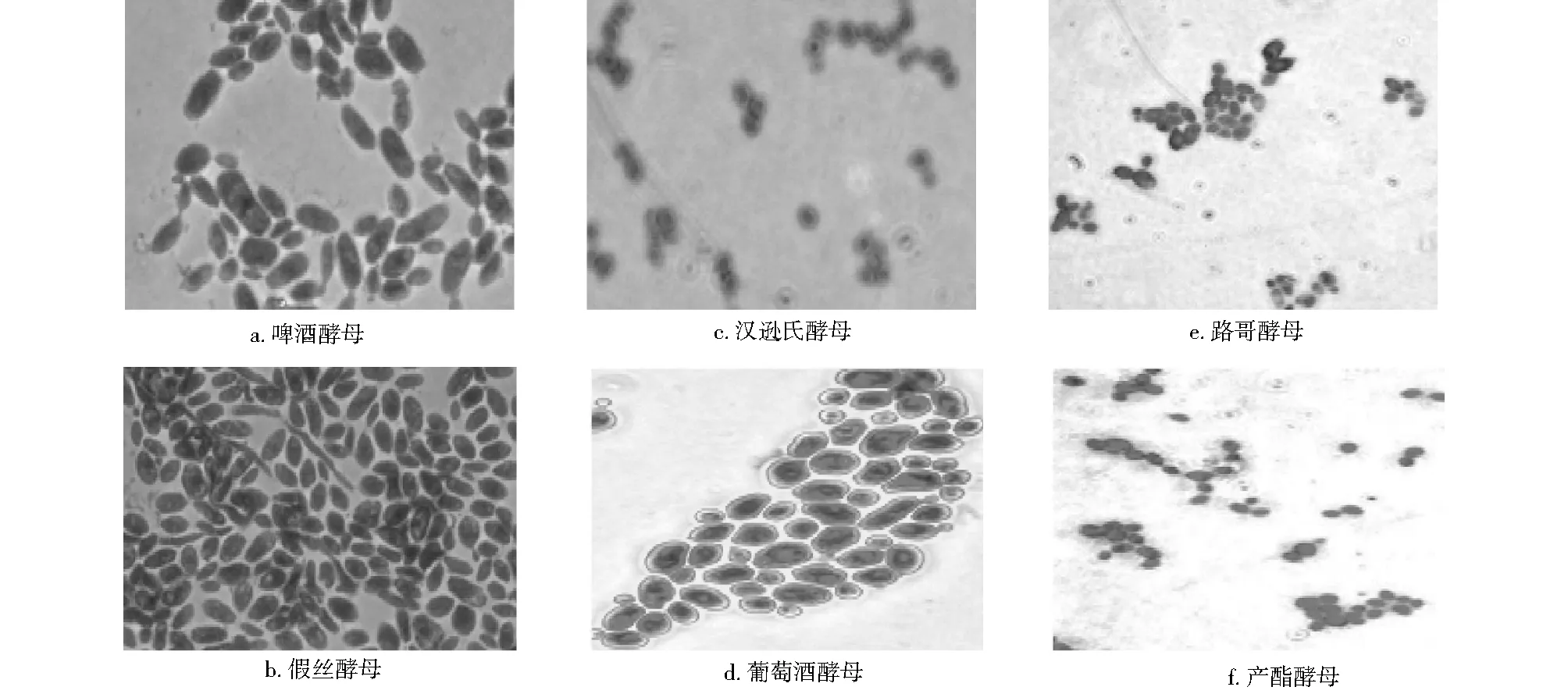
图2 6株苏丹黑染色酵母的显微镜照片
由图2可见,假丝酵母和啤酒酵母油脂颗粒较大,均呈油滴状。因此,选取假丝酵母和啤酒酵母进行发酵复筛。
2.2 发酵复筛
2.2.1 假丝酵母和啤酒酵母的生长曲线(图3)

图3 假丝酵母和啤酒酵母的生长曲线
由图3可见,假丝酵母在第6 h进入对数生长期,第20 h进入了稳定期;啤酒酵母在第6 h进入对数生长期,第12 h进入了稳定期。达到稳定期后假丝酵母的OD600比啤酒酵母高出很多。这说明同体积的发酵液假丝酵母能收获更多的细胞。
2.2.2 假丝酵母和啤酒酵母的细胞量和油脂含量
以相同的接种量(10%)对假丝酵母和啤酒酵母发酵培养4 d,测细胞量和油脂含量,计算油脂产量,结果见表1。

表1 假丝酵母和啤酒酵母细胞量和油脂产量
由表1可见,假丝酵母细胞量、油脂含量、油脂产量分别是啤酒酵母的1.64倍、1.14倍和1.87倍,故确定假丝酵母为油脂高产菌种进行发酵条件优化。
2.3 发酵条件优化
2.3.1 培养温度对假丝酵母细胞量和油脂含量的影响(图4)
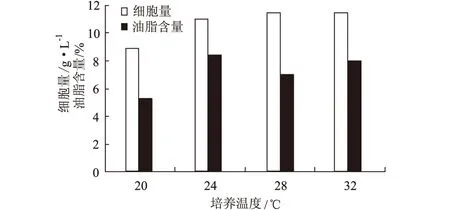
图4 培养温度对假丝酵母细胞量和油脂含量的影响
由图4可见,细胞量在20~28℃范围内,随着培养温度的上升而增加,而在28~32℃不再增加;油脂含量随培养温度的升高先上升后下降,24℃时油脂含量最高。这说明细胞生长和油脂合成的最适培养温度不同,为使最终油脂产量达到最大,可采用控温法来调节整个发酵过程,即发酵前期控制温度在28℃,待细胞量维持稳定后适当降低温度以促进油脂的合成。
2.3.2 初始pH值对假丝酵母细胞量和油脂含量的影响(图5)
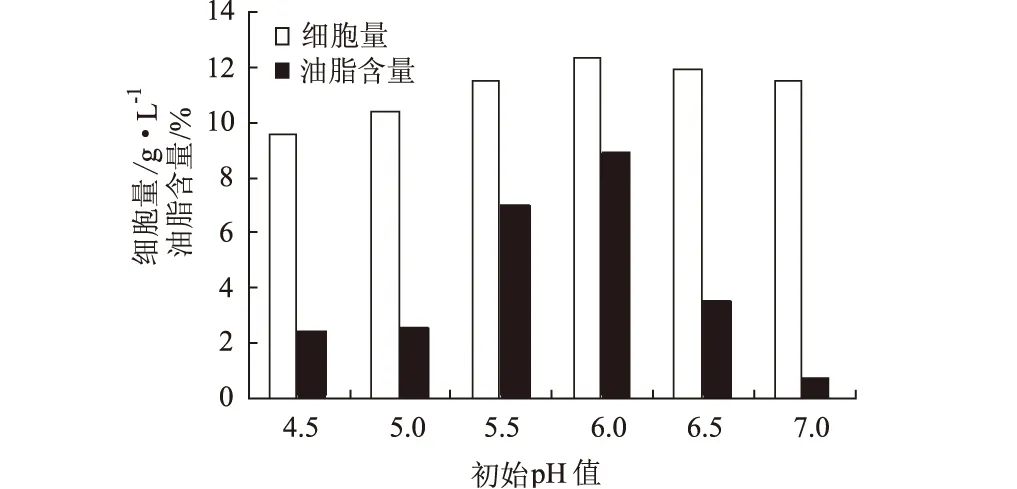
图5 初始pH值对假丝酵母细胞量和油脂含量的影响
由图5可见,在选取的初始pH值范围内,细胞量和油脂含量均先上升后下降,并均于初始pH值为6.0时达到最大,因此选择假丝酵母生长和油脂合成的初始pH值为6.0。
2.3.3 发酵周期对假丝酵母细胞量和油脂含量的影响(图6)

图6 发酵周期对假丝酵母细胞量和油脂含量的影响
由图6可见,细胞量和油脂含量均随着发酵周期的延长而增加,但发酵超过4 d以后,细胞量和油脂含量的增长非常有限。考虑经济因素,选择发酵周期为4 d。
2.3.4 接种量对假丝酵母细胞量和油脂含量的影响(图7)

图7 接种量对假丝酵母细胞量和油脂含量的影响
由图7可见,细胞量和油脂含量均随着接种量的增加先上升后下降,并都在接种量为10%时达到最大。因此,选择接种量为10%。
2.3.5 转速对假丝酵母细胞量和油脂含量的影响(图8)

图8 转速对假丝酵母细胞量和油脂含量的影响
由图8可见,转速从120 r·min-1提高到180 r·min-1,细胞量和油脂含量相应上升;转速超过180 r·min-1后,细胞量和油脂含量均趋于稳定。因此,选择转速为180 r·min-1。
2.4 碳、氮源选择
2.4.1 碳源对假丝酵母细胞量和油脂含量的影响
分别选择葡萄糖、乳糖、蔗糖、麦芽糖为碳源,添加量均为4%,其它成分不变,摇瓶发酵4 d,测细胞量和油脂含量,结果见图9。

图9 碳源对假丝酵母细胞量和油脂含量的影响
由图9可见,以葡萄糖为碳源时,细胞量和油脂含量都达到最大,即葡萄糖最有利于细胞生长和油脂合成,是最佳碳源。
2.4.2 氮源对假丝酵母细胞量和油脂含量的影响
氮源主要用于构成菌体细胞物质(氨基酸、蛋白质、核酸等)和含氮代谢物[4]。分别选取蛋白胨、酵母膏、硝酸钾、磷酸二氢铵、硫酸铵为氮源,添加量均为0.4%,其它成分不变,摇瓶发酵4 d,测细胞量和油脂含量,结果见图10。
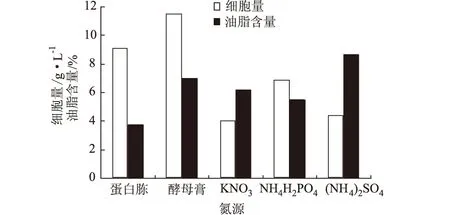
图10 氮源对假丝酵母细胞量和油脂含量的影响
由图10可知,酵母膏是菌体生长最佳氮源,硫酸铵有利于油脂合成,因此,选定酵母膏为氮源,并添加适量硫酸铵促进油脂合成。
2.5 验证实验
采用优化前、后的碳、氮源和培养条件进行发酵实验,结果见表2。

表2 优化前后发酵结果
由表2可见,发酵条件优化后,假丝酵母的细胞量、油脂含量、油脂产量分别是优化前的142%、171%、245%。
3 结论
对6种酵母菌进行初筛和复筛,选出假丝酵母为油脂高产菌株,确定其最适培养条件为:初始pH值6.0,转速180 r·min-1,接种量10%,发酵周期4 d,培养温度采用两阶段法即发酵前期温度控制在28℃,待细胞量维持稳定后适当降低温度以促进油脂的合成;最佳碳源为葡萄糖,最佳氮源为酵母膏,并添加适量硫酸铵促进油脂合成。优化后假丝酵母的细胞量、油脂含量、油脂产量分别是优化前的142%、171%、245%。
参考文献:
[1] 何东平,陈涛.微生物油脂学[M].北京:化学工业出版社,2006:228.
[2] 杜连祥,路福平.微生物学实验技术[M].北京:中国轻工业出版社,2005:107.
[3] Thakur M S,Prapulla S G,Karanth N G.Estimation of intracellular lipids by the measurement of absorbance of yeast cells stained with Sudan Black B[J].Enzyme Microb Technol,1989,11(4):252-254.
[4] 俞俊棠,唐孝宣.生物工艺学[M].上海:华东理工大学出版社,2002:101.

