纤维素分解菌的筛选及其紫外诱变
,,,
(东南大学化学化工学院,江苏 南京 210009)
纤维素是植物细胞壁的主要成分,约占植物干重的30%~50%,是自然界中分布最广的天然高分子化合物,也是地球上数量最丰富、最廉价的可再生资源[1,2]。自然界中广泛存在产纤维素酶的微生物,包括细菌、真菌、放线菌等。微生物产生的纤维素酶已经用于纤维素类生物质生产葡萄糖、饲料工业、纺织行业、环境保护、农产品加工等方面[3]。直接从环境中选育出来的野生型菌株产纤维素酶活性不高,菌种易退化,限制了其应用范围。因此,选育高产纤维素酶活性的微生物类群是人们研究的热点之一。作者从朽木、腐烂的竹叶和稻草中分离得到8株纤维素分解菌,并对其中酶活较高的菌株进行了紫外线诱变。
1 实验
1.1 材料与试剂
朽木、腐烂的竹叶与稻草从自然界中采集。
DNS试剂,pH值7.2的缓冲溶液,1%羧甲基纤维素钠(CMCNa)磷酸缓冲溶液。
1.2 培养基
霉菌斜面培养基:马铃薯200 g, 蔗糖20 g, 琼脂17 g, 蒸馏水1000 mL, pH值自然。
羧甲基纤维素钠培养基:(NH4)2SO42 g, MgSO40.5 g, KH2PO41 g, NaCl 0.5 g, 羧甲基纤维素钠10 g, 琼脂17 g, 蒸馏水1000 mL, pH值自然。
产酶液体培养基: 麦草粉40 g, 麦麸10 g,(NH4)2SO41.5 g, KH2PO41.0 g, MgSO40.5 g, NaCl 0.2 g, CaCl20.2 g, 蒸馏水1000 mL。
1.3 方法
1.3.1 菌株的分离与初筛
朽木、腐烂的竹叶与稻草等分别放入锥形瓶中,加入适量的灭菌生理盐水,振荡30 min,静置,各吸取上清液1 mL,分别稀释10、102、103倍,涂布在羧甲基纤维素钠培养基上,30℃培养7 d,挑取大的单菌落进行划线分离。将分离得到的菌株接种于新的羧甲基纤维素钠培养基上培养3 d,用刚果红染色法[3]测定菌落直径及透明圈直径,对其中8株产酶活性较高的菌株进行酶活性测定,从中筛选出产酶活性最高的菌株。
1.3.2 2#菌株孢子悬液制备
将初筛得到的2#菌株接种到霉菌斜面培养基上活化3 d,用无菌生理盐水洗下孢子,打散后用血球计数板计数,稀释孢子液浓度至1×106~1×108个·mL-1,得孢子悬液。
1.3.3 紫外线诱变处理
打开紫外灯将无菌操作箱灭菌20 min。取 8 个直径9 cm培养皿,每皿中加入5 mL孢子悬液,在20 W紫外灯下30 cm处分别照射0 s、6 s、12 s、18 s、24 s、30 s、40 s、50 s,将经过照射的孢子悬液适当稀释后涂布于羧甲基纤维素钠平板上,黑布包好后置于30℃恒温培养箱中培养3 d。菌落计数,绘制存活曲线。
1.3.4 突变株的筛选
选择致死率为60%~90%的紫外线剂量诱变。将诱变后的孢子悬液适当稀释后涂布于羧甲基纤维素钠平板上,按初筛方法筛选出产酶活性较高的突变株。将其接入产酶液体培养基中30℃培养3 d。用DNS比色法测定酶活性,进一步筛选出产酶活性较高的突变株,接种于斜面上,置于冷藏室保存。
1.3.5 纤维素分解菌的酶活性测定[4,5]
将菌株接种于产酶液体培养基中摇床培养3 d,培养液在3500 r·min-1离心10 min,上清液即为初酶液。移取含有1% CMCNa的磷酸缓冲溶液1.5 mL于试管中,加人初酶液0.5 mL,于50℃水浴中保温20 min后,按DNS法测糖含量。
2 结果与讨论
2.1 葡萄糖标准曲线
采用DNS法[4],在波长为530 nm条件下,测定一系列已知浓度葡萄糖的OD值,绘制葡萄糖标准曲线,结果见图1。

图1 葡萄糖标准曲线
2.2 菌株的初筛
涂布了样品水溶液的羧甲基纤维素钠培养基培养7 d后,培养基上长出很多大小不同的菌株,菌株颜色有乳白色、浅绿色、墨绿色、灰白色、黑色等。观察菌株形态,大部分为霉菌。用刚果红染色法选取8株透明圈直径(D2)和菌落直径(D1)的比值相对较大的菌株,结果见表1。
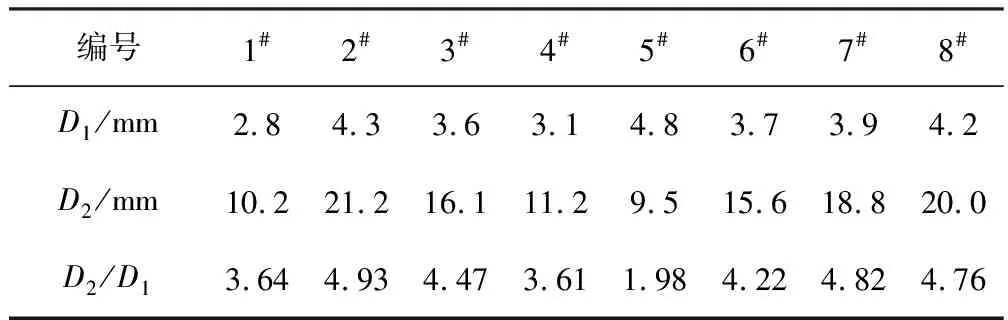
表1 8株菌株的透明圈直径和菌落直径
测定上述8株菌株的酶活性,结果见表2。

表2 8株菌株酶活性测定结果
从表2可以看出,2#、6#和8#菌的OD值及产酶活性较高,尤其是2#,这与刚果红染色法结果一致。但对于3#、4#、7#菌,刚果红染色法与OD法测定的酶活性大小不同。所以仅以D2/D1值作为菌株产纤维素酶活性大小的唯一定量指标不可靠。因为不同菌种、生长条件、纤维素酶系、产酶速度、菌苔大小及在平板上堆积情况的差异都可能造成D2/D1值与产酶活性结果的不完全一致[6]。综合两种方法结果,选择2#菌株进行紫外线诱变。
2.3 2#菌株紫外诱变存活率曲线(图2)

图2 存活率与紫外线照射时间的关系
从图2可以看出,在0~50 s照射时间内,随着紫外线照射时间的延长,2#菌存活率迅速下降。照射时间为5 s、6 s、12 s、19 s时其致死率分别为60%、70%、80%、90%。
2.4 突变株的筛选
以致死率60%~90%的紫外线剂量诱变2#菌株,得到了一系列突变株,结果见表3。

表3 致死率为60%~90%的突变株筛选情况
从表3可以看出,致死率为80%的M10菌株在所有突变株中产酶活性最大,其产酶活性相对于出发菌株提高了89.1%。
3 结论
(1)利用羧甲基纤维素钠为唯一碳源培养基从朽木、腐烂的竹叶与稻草中分离得到8株纤维素分解菌,测定了其产酶活性。对其中产酶活性较高的2#菌株进行紫外线诱变,进一步筛选得到突变株M10,相对酶活较出发菌株提高了89.1%。
(2)实验中发现,以水解圈直径/菌落直径比值判断菌株产纤维素酶活性大小并不可靠,需要进一步测定酶活。
参考文献:
[1] Munisiwaran P K A,Charyulu N C L N. Solid substrate fermentation of coconut coir pith for cellulase production[J].Enzyme Microb Technol,1994,16(5):436-440.
[2] Peter M,Zarnea G,Adrian P,et al. Biodegradation and bioconversion of cellulose wastes using bacterial and fungal cells immobilized in radiopolymerized hydrogels[J].Resources,Conservation and Recyling,1999,27(5):309-332.
[3] 刘春芬,贺稚非,蒲海燕,等.纤维素酶及应用现状[J].粮食与油脂,2004,(1):15-1.
[4] 魏亚琴,李永泉,李红玉.分解纤维素的三株真菌的筛选与鉴定[J].兰州大学学报,2008,44(S1):92-96.
[5] 傅力.纤维素酶测定方法的研究[J].新疆农业大学学报,2000,25(2):45-48.
[6] 房兴堂.秸秆纤维素分解菌的酶活力测定[J].生物技术通讯,2007,18(4):628-630.

