贝伐珠单抗联合标准化疗方案治疗对晚期结直肠癌患者凝血状态及毒副反应发生率的影响观察
【摘要】 目的:观察贝伐珠单抗联合标准化疗方案治疗对晚期结直肠癌患者凝血状态及毒副反应发生率的影响。方法:选取2022年12月—2023年12月宜春市人民医院肿瘤医院收治的80例晚期结直肠癌患者,按随机数字表法分为FOLFOXIRI组和FOLFIRI组,各40例。FOLFOXIRI组采用FOLFOXIRI方案(伊立替康+奥沙利铂+氟尿嘧啶)化疗联合贝伐珠单抗治疗,FOLFIRI组采用FOLFIRI方案(伊立替康+氟尿嘧啶)化疗联合贝伐珠单抗治疗。比较两组临床疗效、免疫功能、凝血状态及毒副反应发生率。结果:治疗4个周期后,FOLFOXIRI组客观缓解率为55.00%,明显高于FOLFIRI组的32.50%(Plt;0.05),且FOLFOXIRI组的疾病控制率为87.50%,明显高于FOLFIRI组的67.50%(Plt;0.05)。治疗4个周期后,两组CD4+/CD8+、CD4+水平均较治疗前升高,CD8+均较治疗前降低,FOLFOXIRI组CD4+/CD8+、CD4+水平均高于FOLFIRI组,CD8+低于FOLFIRI组,差异均有统计学意义(Plt;0.05)。FOLFOXIRI组骨髓抑制发生率为12.50%,高于FOLFIRI组的2.50%,差异有统计学意义(Plt;0.05);两组高血压、腹泻腹痛、恶心呕吐、蛋白尿、出血发生率比较,差异均无统计学意义(Pgt;0.05)。结论:与采用贝伐珠单抗联合FOLFIRI化疗治疗比较,贝伐珠单抗联合FOLFOXIRI化疗方案治疗晚期结直肠癌效果更佳,提高患者客观缓解率和疾病控制率,改善患者免疫功能,且不影响患者凝血状态,但骨髓抑制发生率提高。
【关键词】 结直肠癌 晚期 贝伐珠单抗 化疗 凝血状态
Observation on Effects of Bevacizumab Combined with Standard Chemotherapy Regimen on Coagulation State and Incidence of Toxicities in Patients with Advanced Colorectal Cancer/XIAO Chijin, ZHOU Aimin, FAN Song, QIU Meiqing, WANG Lichao. //Medical Innovation of China, 2025, 22(03): 0-075
[Abstract] Objective: To observe the effects of Bevacizumab combined with standard chemotherapy on coagulation status and incidence of toxic side effects in patients with advanced colorectal cancer. Method: A total of 80 patients with advanced colorectal cancer admitted to Yichun People's Hospital Cancer Hospital from December 2022 to December 2023 were selected and divided into FOLFOXIRI group and FOLFIRI group according to random number table method, with 40 patients in each group. FOLFOXIRI group was treated with FOLFOXIRI regimen (Irinotecan + Oxaliplatin + Fluorouracil) chemotherapy combined with Bevacizumab, and FOLFIRI group was treated with FOLFIRI regimen (Irinotecan + Fluorouracil) chemotherapy combined with Bevacizumab. The clinical efficacy, immune function, coagulation status and incidence of toxic and side effects were compared between the two groups. Result: After 4 cycles of treatment, the objective remission rate of FOLFOXIRI group was 55.00%, which was significantly higher than 32.50% of FOLFIRI group (Plt;0.05), and the disease control rate of FOLFOXIRI group was 87.50%, which was significantly higher than 67.50% of FOLFIRI group (Plt;0.05). After 4 cycles of treatment, the levels of CD4+/CD8+ and CD4+ in both groups were higher than those before treatment, and CD8+ were lower than those before treatment, the levels of CD4+/CD8+ and CD4+ in FOLFOXIRI group were higher than those in FOLFIRI group, and CD8+ was lower than that in FOLFIRI group, the differences were statistically significant (Plt;0.05). The incidence of myelosuppression in FOLFOXIRI group was 12.50%, which was higher than 2.50% in FOLFIRI group, the difference was statistically significant (Plt;0.05). There were no significant differences in the incidence of hypertension, diarrhea, abdominal pain, nausea and vomiting, proteinuria and bleeding between the two groups (Pgt;0.05). Conclusion: Compared with the treatment of Bevacizumab combined with FOLFIRI chemotherapy, the chemotherapy regimen of Bevacizumab combined with FOLFOXIRI is more effective in the treatment of advanced colorectal cancer, improves the objective response rate and disease control rate of patients, improves the immune function of patients, and does not affect the coagulation status of patients, but increases the incidence of bone marrow suppression.
[Key words] Colorectal cancer Advanced stage Bevacizumab Chemotherapy Coagulation state
First-author's address: Second Ward, Yichun People's Hospital Cancer Hospital, Yichun 336000, China
doi:10.3969/j.issn.1674-4985.2025.03.017
结直肠癌是常见的消化道恶性肿瘤,早期症状不典型,随着疾病进展,常表现为排便习惯改变、便血、腹痛、消瘦等症状,严重影响患者工作和生活[1]。中早期结直肠癌的治疗主要通过手术,患者预后较好,5年生存率可达67%~90%,而晚期结直肠癌失去手术根治的机会,多采用以化疗为主的综合治疗,伊立替康、氟尿嘧啶等是化疗常用药物,虽有一定效果,但药物毒副作用大,其长期生存还有待提高[2]。贝伐珠单抗是重组抗血管内皮生长因子(VEGF)的单克隆抗体,是一种靶向药物,被用于结直肠癌、肺癌等疾病中[3]。目前,贝伐珠单抗联合标准化疗已成为结直肠癌治疗的一线标准,其效果明显优于常规化疗,可延长患者总生存时间,改善患者生存质量,但还是有毒副反应和停药风险,且贝伐珠单抗联合化疗的最佳方案还在探索中[4-5]。基于此,本研究采用贝伐珠单抗联合标准化疗方案治疗,观察其对晚期结直肠癌患者凝血状态及毒副反应发生率的影响,以期为该类患者选择适合治疗方法及改善预后提供依据。
1 资料与方法
1.1 一般资料
选取2022年12月—2023年12月宜春市人民医院肿瘤医院收治的80例晚期结直肠癌患者。纳入标准:(1)符合结直肠癌的诊断标准[6],既往未接受过系统治疗的微卫星稳定(MSS)型或错配修复正常(pMMR)型不可切除局部晚期或转移性结直肠癌;(2)基因检测为RAS或BRAF突变型的转移性结直肠癌;(3)美国东部肿瘤协作组(ECOG)评分0~1分[7];(4)年龄18~75岁;(5)预计生存期gt;3个月;(6)主要脏器功能正常,无严重血液、心、肺、肝、肾、骨髓等功能异常和免疫缺陷。排除标准:(1)已经或正在接受额外化疗、放射治疗、靶向或免疫治疗;(2)患有任何形式的初级免疫缺陷;(3)一般情况差;(4)有内科系统性疾病和精神科疾病不适合化疗;(5)四周内参加过其他药物临床试验。按随机数字表法分为FOLFIRI组和FOLFOXIRI组,各40例。本研究经宜春市人民医院医学伦理委员会批准;患者或者患者家属知情同意本研究。
1.2 方法
FOLFIRI组采用FOLFIRI方案化疗联合贝伐珠单抗治疗,采用FOLFIRI方案(伊立替康+氟尿嘧啶)化疗,第1天,给予盐酸伊立替康注射液[生产厂家:齐鲁制药(海南)有限公司,批准文号:国药准字H20084572,规格:5 mL︰0.1 g]180 mg/m2溶于生理盐水中,静脉滴注1 h;静脉滴入亚叶酸钙注射液(生产厂家:江苏大红鹰恒顺药业有限公司,批准文号:国药准字H20010804,规格:3 mL︰30 mg)400 mg/m2,持续2 h;静脉推注注射用氟尿嘧啶(生产厂家:海南卓泰制药有限公司,批准文号:国药准字H20051627,规格:0.5 g)400 mg/m2,之后静脉泵入氟尿嘧啶2.4 g/m2,持续泵入48 h;两周为1周期,治疗4个周期。给予贝伐珠单抗治疗:将贝伐珠单抗注射液(生产厂家:齐鲁制药有限公司,批准文号:国药准字S20190040,规格:100 mg︰4 mL)5 mg/kg稀释于生理盐水中,静脉滴注30 min,每2周1次,治疗4次。
FOLFOXIRI组采用FOLFOXIRI方案(伊立替康+奥沙利铂+氟尿嘧啶)化疗联合贝伐珠单抗治疗,FOLFOXIRI方案,第1天,静脉滴注伊立替康165 mg/m2,滴注1 h,静脉滴注注射用奥沙利铂(生产厂家:Sanofi-Aventis France,批准文号:国药准字J20150117,规格:50 mg)85 mg/m2,滴注2 h,静脉滴注亚叶酸钙400 mg/m2,之后持续泵入氟尿嘧啶48 h,总量2.4 g/m2,每两周1次,治疗2次;贝伐珠单抗的用法用量与FOLFIRI组保持一致,两周为1个疗程,均治疗4个周期。
1.3 观察指标及评价标准
(1)近期疗效:治疗4个周期后,参照实体瘤疗效评价标准[8],分为完全缓解、部分缓解、稳定、进展;客观缓解率=完全缓解率+部分缓解率,疾病控制率=完全缓解率+部分缓解率+稳定率。(2)凝血状态:治疗前和治疗4个周期后,采集患者肘静脉血5 mL,检测活化部分凝血酶原时间(APTT)、凝血酶原时间(PT)、纤维蛋白原(FIB)、D-二聚体(D-D)水平。(3)免疫功能:治疗前和治疗4个周期后,取5 mL空腹静脉血,采用流式细胞仪检测CD4+、CD8+细胞水平,计算CD4+/CD8+。(4)毒副反应:记录两组治疗期间毒副反应发生情况,包括高血压、腹泻腹痛、恶心呕吐、蛋白尿、出血、骨髓抑制等。
1.4 统计学处理
本研究数据采用SPSS 24.0统计学软件进行分析和处理,计量资料以(x±s)表示,组间比较采用独立样本t检验,组内比较采用配对t检验;计数资料以率(%)表示,采用字2、Fisher检验。以Plt;0.05为差异有统计学意义。
2 结果
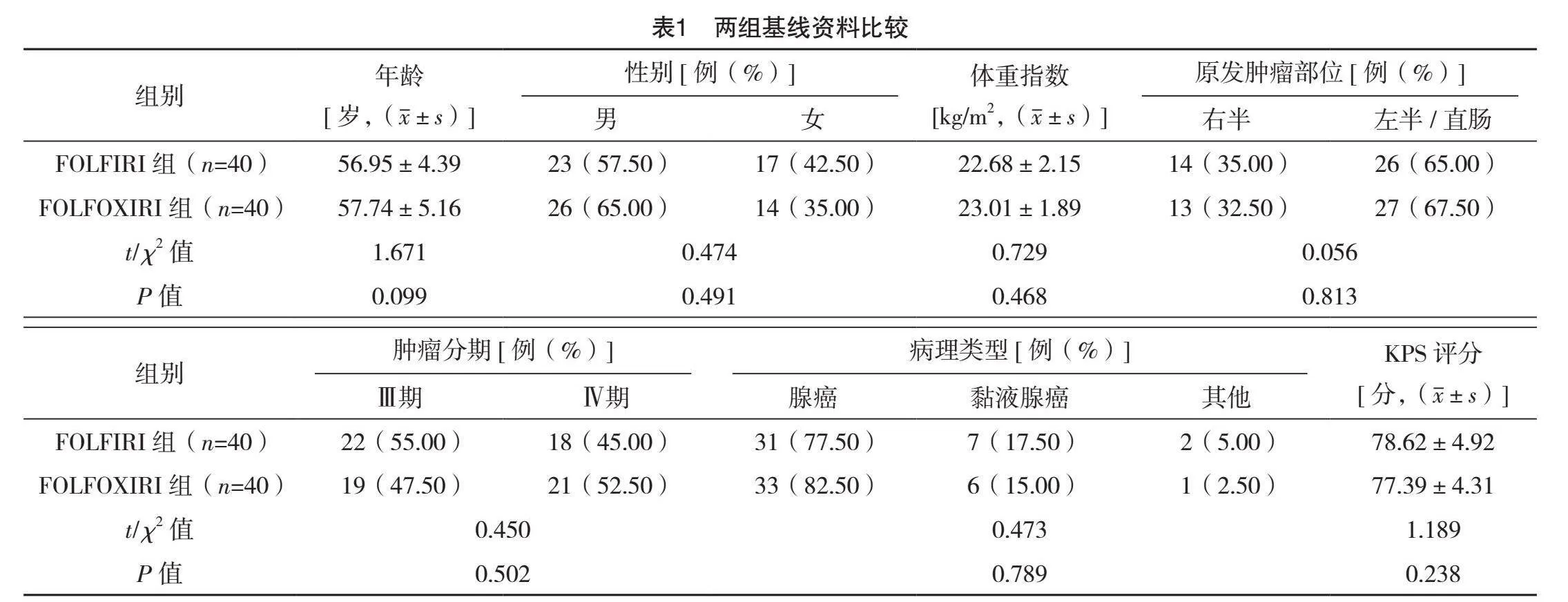
2.1 两组基线资料比较
两组年龄、性别、原发肿瘤部位等基线资料比较,差异均无统计学意义(Pgt;0.05),有可比性,见表1。
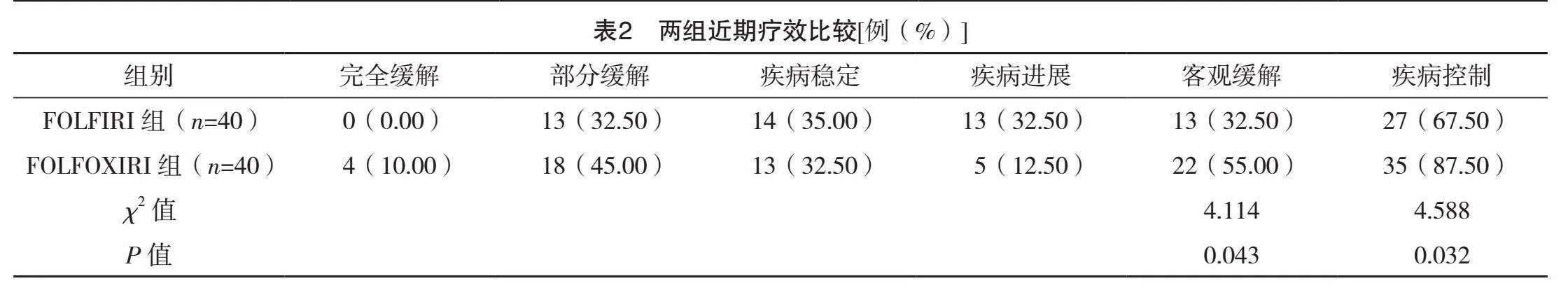
2.2 两组近期疗效比较
FOLFOXIRI组客观缓解率为55.00%,高于FOLFIRI组的32.50%,FOLFOXIRI组的疾病控制率为87.50%,高于FOLFIRI组的67.50%,差异均有统计学意义(Plt;0.05),见表2。
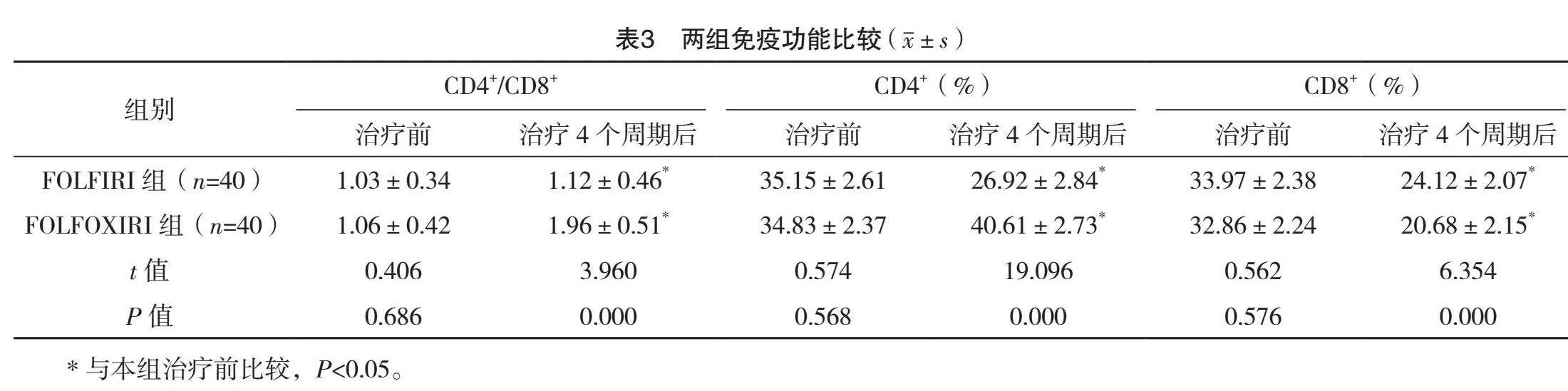
2.3 两组免疫功能比较
治疗前,两组CD4+/CD8+、CD4+、CD8+比较,差异均无统计学意义(Pgt;0.05);治疗4个周期后,两组CD4+/CD8+、CD4+水平均较治疗前升高,CD8+均较治疗前降低,FOLFOXIRI组CD4+/CD8+、CD4+水平均高于FOLFIRI组,CD8+低于FOLFIRI组,差异均有统计学意义(Plt;0.05)。见表3。
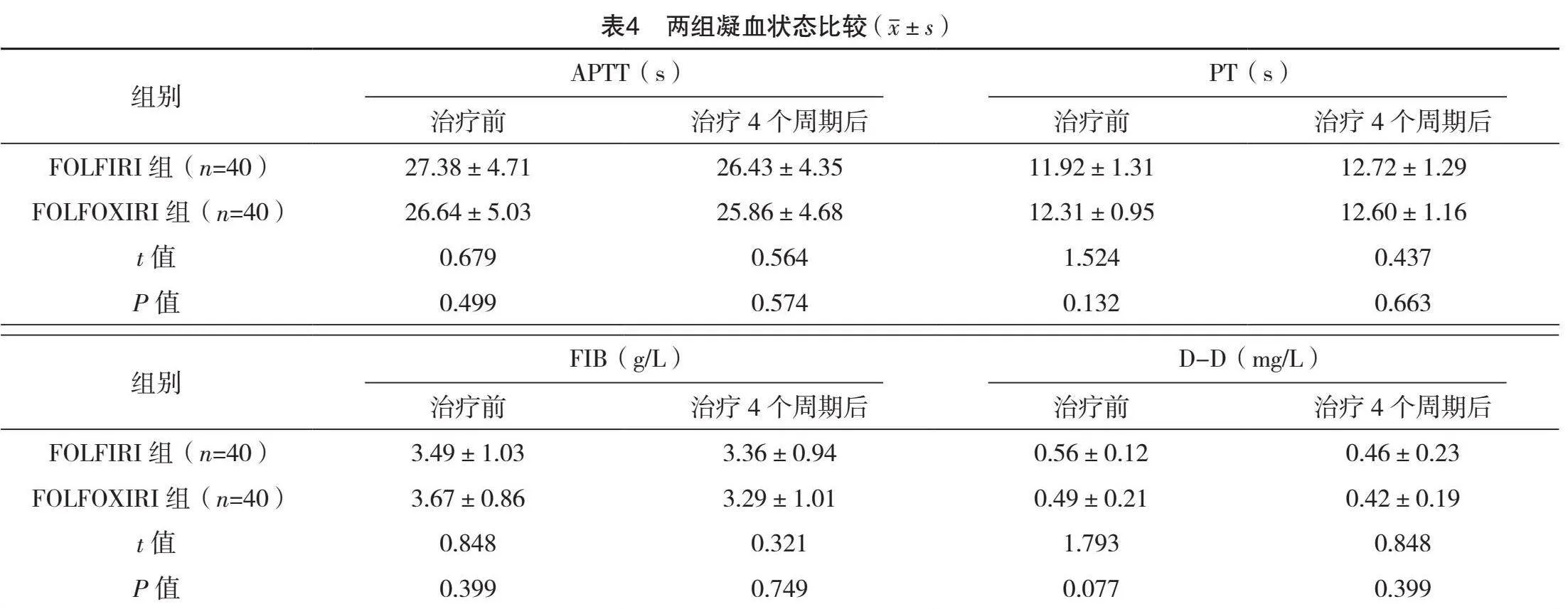
2.4 两组凝血状态比较
治疗前、治疗4个周期后,两组APTT、PT、FIB、D-D比较,差异均无统计学意义(Pgt;0.05),见表4。
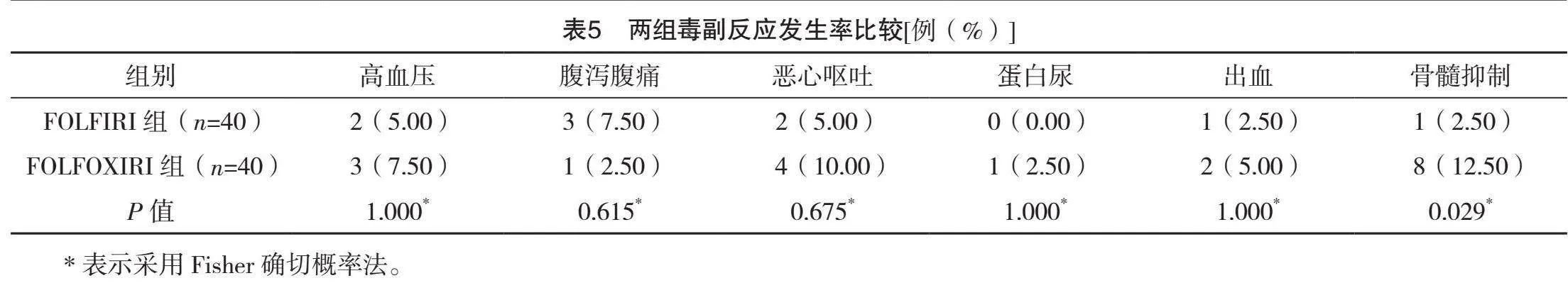
2.5 两组毒副反应发生率比较
FOLFOXIRI组骨髓抑制发生率为12.50%,高于对照组的2.50%,差异有统计学意义(Plt;0.05);两组高血压、腹泻腹痛、恶心呕吐、蛋白尿、出血发生率比较,差异均无统计学意义(Pgt;0.05),见表5。
3 讨论
随着经济的发展和生活水平的提高,结直肠癌的发病率呈上升趋势,在恶性肿瘤中名居前茅,大多发生在40岁以上中老年人,该病病因和机制尚不明确,但发病大多与生活方式、饮食习惯及遗传等有关[9-10]。该病起病隐匿,大多数患者确诊时都已进入中晚期,此时手术切除难以达到满意治疗效果,死亡率较高,严重影响患者的生活和健康[11-12]。临床往往采用化疗等方法治疗晚期结直肠癌,但肿瘤细胞易转移,患者复发率较高,且化疗毒副作用大,患者易发生恶心呕吐等胃肠道反应,和肝肾损伤等不良反应,目前,贝伐珠单抗联合化疗在临床中被广泛应用[13-14]。基于此,本研究采取贝伐珠单抗联合标准化疗方案治疗晚期结直肠癌,观察其对患者凝血状态及毒副反应发生率的影响。
本研究结果显示,治疗4个周期后,FOLFOXIRI组的客观缓解率和疾病控制率分别为55.00%、87.50%,明显高于FOLFIRI组的32.50%、67.50%;这与刘梅等[15]研究结果相似,表明贝伐珠单抗联合FOLFOXIRI化疗方案对晚期结直肠癌患者效果较好,客观缓解率和疾病控制率是优于贝伐珠单抗联合FOLFIRI化疗的。分析在于贝伐珠单抗是VEGF抑制剂,可特异性与VEGF结合,抑制其与受体结合,阻断血管生成的信号传导,抑制肿瘤新生血管生成,从而抑制肿瘤细胞的生长增殖,达到抗肿瘤作用[16-17]。采取贝伐珠单抗联合化疗方案,可使肿瘤新生血管退化,提高药物输送和利用率,抑制肿瘤血管形成,从而提高患者临床疗效,延长患者生存时间。相较于FOLFIRI两药方案联合贝伐珠单抗,FOLFOXIRI三药方案联合贝伐珠单抗对晚期结直肠癌效果更好,可显著提高疾病控制率。Cremolini等[18]的研究也显示,贝伐珠单抗联合FOLFOXIRI化疗方案治疗晚期结直肠癌疗效较好,提高患者长期生存。
本研究还显示,治疗4个周期后,FOLFOXIRI组CD4+/CD8+、CD4+水平较治疗前均升高,且均高于FOLFIRI组,而CD8+较治疗前均降低,FOLFOXIRI组水平低于FOLFIRI组;表明贝伐珠单抗联合FOLFOXIRI化疗方案治疗可改善晚期结直肠癌患者免疫功能,提高CD4+/CD8+水平,且安全性高。这可能是肿瘤的生长与免疫功能有关,晚期结直肠癌患者免疫功能异常,在疾病发展中,辅助T细胞CD4+减少,抑制T细胞CD8+增多,二者比值能反映免疫调节功能,一旦比值降低,则机体免疫力下降[19-20];贝伐珠单抗联合标准化疗方案治疗可有效改善患者免疫状态,提高免疫功能,提高CD4+/CD8+等的水平。
另本研究中,FOLFOXIRI组治疗4个周期后的APTT、PT、FIB、D-D水平与治疗前比较均无明显差异,且与FOLFIRI组比较无明显差异;提示贝伐珠单抗联合化疗治疗可改善晚期结直肠癌患者凝血功能,但贝伐珠单抗联合FOLFOXIRI化疗与贝伐珠单抗联合FOLFIRI化疗对凝血功能的影响相当,不会增加出血风险,这与沈玉静等[21]的研究结果一致;分析在于晚期结直肠癌患者存在凝血功能异常,出血或形成血栓依赖凝血与抗凝血系统,肿瘤细胞增殖、侵袭,会破坏凝血与抗凝血平衡,使患者血液呈现高凝状态,本研究中经贝伐珠单抗联合FOLFOXIRI化疗方案治疗后的APTT、PT水平,与贝伐珠单抗联合FOLFIRI化疗比较无明显差异,表明二者对患者凝血功能的影响相当。另本研究中,治疗期间,FOLFOXIRI组骨髓抑制发生率为12.50%,明显高于FOLFIRI组的2.50%;表明与贝伐珠单抗联合两药化疗方案相比,贝伐珠单抗联合三药化疗方案对晚期结直肠癌患者其骨髓抑制发生率升高,这也提示虽然贝伐珠单抗联合三药的效果要优于贝伐珠单抗联合两药,但患者因骨髓抑制不能耐受而选择两药化疗,建议增大研究样本量,来进一步研究贝伐珠单抗联合FOLFOXIRI化疗的疗效和安全性。
综上所述,贝伐珠单抗联合标准化疗方案治疗对晚期结直肠癌患者有一定疗效,其中贝伐珠单抗联合FOLFOXIRI化疗可提高疾病控制率,改善患者免疫功能,对患者凝血状态的影响较小,但骨髓抑制发生率较高。
参考文献
[1]中华医学会肿瘤学分会早诊早治学组.中国结直肠癌早诊早治专家共识[J].中华医学杂志,2020,100(22):1691-1698.
[2]杨冬阳,位俊敏,马冬,等.甲磺酸阿帕替尼在晚期结直肠癌标准二线治疗失败后三线治疗的疗效、安全性及疗效预测分析[J].实用医学杂志,2019,35(10):1607-1612.
[3]张智勇,丁昌利,郑盈,等.mFOLFOXIRI和mFOLFIRI联合贝伐珠单抗治疗转移性结直肠癌的疗效比较[J].中华肿瘤防治杂志,2023,30(13):806-811.
[4] MATSUOKA H,YAMADA T,OHTA R,et al.TAS CC4 Study Group.Biweekly TAS-102 and Bevacizumab as third-line chemotherapy for advanced or recurrent colorectal cancer: a phase Ⅱ, multicenter, clinical trial (TAS-CC4 study)[J].Int J Clin Oncol,2022,27(12):1859-1866.
[5]孔凡铭,王娜,谢红霞,等.消岩汤联合卡培他滨和贝伐珠单抗在结直肠癌维持治疗中的临床研究[J].中国肿瘤临床,2023,50(10):519-525.
[6]中华人民共和国国家卫生健康委员会.中国结直肠癌诊疗规范(2020版)[J].中华消化外科杂志,2020,19(6):563-588.
[7] CELLA D, TULSKY D S, GRAY G, et al. The functional assessment of cancer therapy scale: development and validation of the general measure[J]. Journal of Clinical Oncology, 1993, 11(3): 570-579.
[8]杨学宁,吴一龙.实体瘤治疗疗效评价标准-RECIST[J].循证医学,2004,4(2):85-90.
[9] PATEL S G,KARLITZ J J,YEN T,et al.The rising tide of early-onset colorectal cancer: a comprehensive review of epidemiology, clinical features, biology, risk factors, prevention, and early detection[J].Lancet Gastroenterol Hepatol,2022,7(3):262-274.
[10]邢国强,杨怀成,邓腾,等.结直肠癌患者的血清血管内皮生长因子、糖类抗原19-9、癌胚抗原水平及与临床特征和预后的关系[J].癌症进展,2023,21(4):424-427.
[11]陈思敏,唐诗宇,张智彬,等.循环外泌体微小RNA-10b表达及去甲基化状态在诊断结直肠癌肝转移及预测早期转化治疗反应中临床价值[J].创伤与急危重病医学,2021,9(4):247-252.
[12] WATANABE J,MURO K,SHITARA K,et al.Panitumumab vs Bevacizumab added to standard first-line chemotherapy and overall survival among patients with ras wild-type,left-sided metastatic colorectal cancer:a randomized clinical trial[J].JAMA,2023,329(15):1271-1282.
[13]蒋锐沅,蓝巧玉,李春姗,等.参一胶囊联合贝伐珠单抗+FOLFIRI方案对晚期转移性结肠癌患者的临床疗效及血清血管生成因子、T淋巴细胞亚群影响的观察[J].中药材,2021,44(6):1504-1510.
[14]石琪,赵洁敏,蒋敬庭,等.化疗联合肝动脉药盒治疗133例潜在可切除晚期结直肠癌疗效及影响因素分析[J].中华肿瘤防治杂志,2019,26(12):861-866.
[15]刘梅,李仲然,武翔.贝伐珠单抗联合化疗对晚期结直肠癌患者的近远期疗效及肿瘤标志物和免疫功能的影响[J].中国临床医生杂志,2023,51(9):1063-1067.
[16]谢兴旺,柯超,周红见,等.雷替曲塞联合西妥昔单抗或贝伐珠单抗治疗晚期结直肠癌临床疗效[J].中国老年学杂志,2022,42(14):3431-3434.
[17]黄志荣,曹齐生,杜成荣,等.贝伐珠单抗注射液联合奥沙利铂注射剂和卡培他滨片治疗晚期结肠癌患者的临床研究[J].中国临床药理学杂志,2020,36(19):2993-2995.
[18] CREMOLINI C,ANTONIOTTI C,ROSSINI D,et al.Upfront FOLFOXIRI plus Bevacizumab and reintroduction after progression versus mFOLFOX6 plus Bevacizumab followed by FOLFIRI plus Bevacizumab in the treatment of patients with metastatic colorectal cancer (TRIBE2): a multicentre, open-label,phase 3, randomised, controlled trial[J].Lancet Oncol,2020,21(4):497-507.
[19]刘萍,骆学新.肠益方联合XELOX化疗方案对老年晚期结直肠癌患者近期疗效及对血清SDC2、SEPT9和免疫功能的影响[J].中国老年学杂志,2022,42(5):1085-1087.
[20]刘杰锋,何苗,曾心雨,等.老年结直肠癌患者术后早期微生态肠内营养对肠道菌群及免疫功能的影响[J].中华老年医学杂志,2020,39(4):435-438.
[21]沈玉静,吴红卫,董南.贝伐珠单抗联合化疗对晚期结肠癌患者治疗后的临床疗效及对凝血功能的影响[J].血栓与止血学,2022,28(1):104-105.
(收稿日期:2024-05-31) (本文编辑:马娇)

