金盏花苷E通过自噬途径下调GPX4 和SLC7A11 抑制肝癌细胞的增殖和迁移

摘要:目的 探讨金盏花苷E抑制肝癌细胞增殖和迁移的分子机制。方法 金盏花苷E处理肝癌细胞,CCK-8 检测细胞活力;Western blotting检测GPX4、SLC7A11、LC3、P62的表达以及Akt/mTOR的磷酸化。自噬抑制剂LY294002和激活剂Rapamycin与金盏花苷E联合处理肝癌细胞,EdU和Transwell 实验分别检测肝癌细胞的增殖和迁移能力。TCGA数据库分析GPX4 和SLC7A11 在肝癌及正常肝组织中的表达水平,以及与肝癌患者存活之间的关系。Western blotting 和qPCR分别检测GPX4 和SLC7A11 在肝癌细胞和正常肝细胞中的表达水平。结果 金盏花苷E 能够显著抑制肝癌细胞的存活(Plt;0.05);GPX4 和SLC7A11在肝癌组织和肝癌细胞中均显著高表达;GPX4和SLC7A11的表达与肝癌患者存活呈显著负相关(Plt;0.001);金盏花苷E显著抑制GPX4 和SLC7A11 蛋白的表达,激活Akt-mTOR通路,增强LC3 Ⅱ的表达(Plt;0.01);自噬激活剂Rapamycin 显著增强金盏花苷E 对GPX4 和SLC7A11 的抑制作用,而自噬抑制剂LY294002 则明显逆转了金盏花苷E 对GPX4 和SLC7A11的抑制作用(Plt;0.05);抑制自噬途径能够逆转金盏花苷E对肝癌细胞增殖和迁移的抑制作用,增强自噬途径则发生相反的变化(Plt;0.01)。结论 金盏花苷E经自噬途径下调GPX4和SLC7A11抑制肝癌细胞的增殖和迁移。
关键词:金盏花苷E;谷胱甘肽过氧化物酶4;溶质转运蛋白第7 家族11 成员;自噬;肝细胞癌
肝癌是我国常见的一种消化系统恶性肿瘤,也是癌症患者死亡的常见原因之一,其中肝细胞癌(HCC)占原发性肝癌的70%~80%[1-3]。大多数肝癌患者由于确诊时就已经处于中晚期,故治疗效果和预后相对较差。因此,寻找影响HCC发生、发展的潜在生物学标记物,并以其为靶点进行治疗是改善肝癌患者治疗和预后的重要策略。
自噬是机体重要的生物学过程,不仅在细胞调节中发挥蛋白质降解、维持细胞器稳态、代谢稳态等作用[4],也和肿瘤的发生发展息息相关,调控自噬可作为癌症治疗的重要方法之一[5]。PI3K/Akt/mTOR通路不仅影响细胞增殖、分化、凋亡、转移和血管生成,也是调节肿瘤细胞自噬的重要途径之一,常被作为肿瘤治疗的关键信号途径[6-9]。溶质载体第7家族成员11(SLC7A11)也被称为xCT,是一种细胞跨膜蛋白,组成xc-系统的轻链,负责将细胞外胱氨酸转运至胞内,用于产生半胱氨酸,参与谷胱甘肽的生物合成[10]。SLC7A11在各种人类癌症高表达,并调节肿瘤的发展、增殖、转移、微环境和治疗耐药性[11, 12],被认为是癌症治疗的一个潜在靶点[13]。它下游的调节因子谷胱甘肽过氧化物酶4(GPX4)作为胞内的一种非常重要的抗氧化酶,在细胞存活和功能中发挥关键作用[14],抑制GPX4也已被证明是一种很有前途的癌症治疗方法[15]。如天然产物姜黄素通过激活自噬途径,下调GPX4和SLC7A11的表达,抑制非小细胞肺癌的增殖[16]。
金盏花苷E(CE)作为一种天然五环三萜皂苷,具有抗炎、缓解缺血再灌注损伤和非酒精性脂肪肝等作用[17-19]。我们已有的研究表明,金盏花苷E能够抑制肝癌HepG2细胞的增殖和迁移[20],但金盏花苷E调控肝癌进展的分子机制尚需进一步探明。在本研究中,我们发现金盏花苷E能够通过下调Akt/mTOR信号途径,促进肝癌细胞自噬,增强GPX4和SLC7A11蛋白降解,抑制肝癌细胞增殖和迁移。
1 材料和方法
1.1 主要药品和抗体
金盏花苷E(CE,HPLC≥95%,上海源叶生物科技有限公司),兔单克隆抗体β-actin(1∶3000)、辣根过氧化物酶标记的山羊抗兔(鼠)IgG(H+L)抗体(1∶10000)(ABclonal) ,p-Akt(Ser473)(1∶ 1000) 、p-mTOR(Ser2448)(1∶500)、SQSTM1/P62(1∶500)以及GAPDH(1∶1000)单克隆抗体(Cell Signaling Technology),SLC7A11(1∶1000)以及GPX4(1∶1000)抗体(BOSTER),LC3(1∶500)抗体(Sigma),环己酰亚胺(CHX,MCE),自噬激活剂(Rapamycin,Selleck Chemicals),自噬抑制剂LY294002和细胞裂解液(RIPA)(碧云天),自噬双标慢病毒mRFP-GFP-LC3和助转剂polybrene(通用生物),CCK-8 试剂盒(迈珂生物),EdU检测试剂盒(锐博生物),Transwell小室(Falcon),总RNA提取试剂盒(天根生化),cDNA合成及qPCR检测试剂盒(百时美生物)。
1.2 细胞培养
Huh7肝癌细胞购自中国科学院细胞库,用含10%胎牛血清(Lonsera),1%青霉素-链霉素(碧云天)的DMEM完全培养基,HepG2肝癌细胞(赛库生物)用含10%胎牛血清(Lonsera),1%NEAA(碧云天),1%青霉素-链霉素(碧云天)的MEM完全培养基,置于37 ℃,5% CO2条件下培养。
1.3 CCK-8检测细胞活力
将Huh7细胞按1×104/孔接种于96孔板,细胞贴壁后使用不同浓度金盏花苷E处理细胞并设置空白对照(无细胞的完全培养基),金盏花苷E作用24 h 后加入CCK-8工作液10 μL/孔,置于37℃,5% CO2培养箱中反应2 h,使用全波段酶标仪在450 nm波长处测量每孔A值,并根据如下公式计算细胞存活率。存活率(%)=(A实验组-A空白组)/(A对照组-A空白组)×100%。
1.4 RT-qPCR 检测SLC7A11 和GPX4 mRNA 的表达水平
提取肝癌细胞Huh7、HepG2 和正常肝细胞HL-7702中的总RNA,先通过逆转录合成cDNA,之后进行qPCR,具体操作根据cDNA合成及qPCR检测试剂盒说明书进行。热扩增条件如下:首先95 ℃预变性30 s,然后进行循环扩增,95℃变性10 s,60℃退火和延伸30 s,共40 个循环,2-ΔΔCT 法进行结果分析。qPCR 中所需的SLC7A11、GPX4以及GAPDH上下游引物如表1所示。
1.5 Western blotting检测蛋白表达量
分组处理Huh7 和HepG2 细胞后,弃去培养基,预冷PBS 清洗1 遍,加入含有PMSF 预冷的RIPA 细胞裂解液,4 ℃摇床裂解10 min,12 000 r/min,4 ℃离心10 min,收集细胞裂解上清,加入2×Loading buffer100 ℃金属浴煮沸5 min。取等量蛋白进行SDS-PAGE,将电泳后的蛋白转移至聚偏二氟乙烯膜(PVDF)膜上,用5%脱脂奶粉室温封闭2 h,1×TBST清洗3次,相应一抗4 ℃摇床孵育过夜。次日1×TBST清洗3次后,加入对应二抗后室温孵育2 h,1×TBST清洗后加入化学发光液和底物孵育后,使用化学发光成像系统(上海勤翔)进行结果检测, Image J进行吸光度分析。
1.6 mRFP-GFP-LC3慢病毒感染
将状态良好的Huh7和HepG2细胞接种到6孔板,接种密度保证在第2 天进行病毒感染的时候细胞汇合率介于30%~50%,放37 ℃,5% CO2 培养箱中培养过夜。感染前从冰箱取出并在冰上慢慢融化病毒,吸去细胞原有培养基,加入5 TU/mL 的病毒以及5 μg/mLpolybrene 进行感染,感染后第2 天(24 h),弃去含有病毒的培养液,换上新鲜的完全培养液并使用20 μg/mL以及15 μg/mL 金盏花苷E分别刺激Huh7 和HepG2细胞24 h,通过荧光显微镜观察并拍照。
1.7 EdU检测细胞的增殖能力
将Huh7 以及HepG2 细胞接种于24 孔板,待细胞贴壁后使用20 μmol/L Rapamycin 和30 μmol/LLY294002 分别预处理细胞1 h,再用20 μg/mL 以及15 μg/mL 金盏花苷E 分别刺激Huh7 和HepG2 细胞24 h,之后进行EdU实验检测细胞增殖能力。实验操作按试剂盒说明书进行,荧光倒置显微镜(Olympus)观察并拍照。使用Image J软件分析EdU阳性染色细胞(红色荧光)与Hoechst 染色细胞(蓝色荧光)数量,并计算EdU阳性染色细胞在总细胞中所占的比例。
1.8 Transwell实验检测细胞的迁移能力
细胞分组及处理同1.6 部分。处理后的细胞分别使用无血清的DMEM以及MEM培养基重悬,取细胞悬液200 μL 接种于Transwell 小室上层,500 μL 含有20%胎牛血清的完全培养基置于Transwell小室下层,置于37 ℃,5% CO2培养箱中培养24 h。取出小室,用脱脂棉签轻轻擦去小室上层细胞,之后将小室放入4%多聚甲醛中固定30 min,PBS清洗1遍后放入0.1%结晶紫中室温染色15 min,PBS清洗3次,使用荧光倒置显微镜观察并拍照。
1.9 统计学分析
所有数据以均数±标准差表示。通过SPSS 17.0 软件进行数据分析,Student's t 检验进行两组之间的比较,使用单因素方差分析进行多组间比较,Plt;0.05表示差异具有统计学意义 。
2 结果
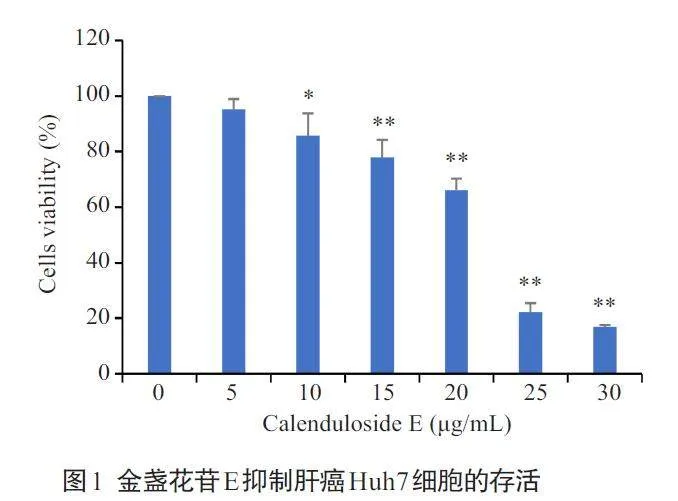
2.1 金盏花苷E对肝癌细胞活力的影响
本研究选取Huh7肝癌细胞为研究对象,金盏花苷E≥10 μg/mL作用Huh7细胞24 h,细胞活力被明显抑制;选取浓度为10、15和20 μg/mL的金盏花苷E处理Huh7细胞(图1,Plt;0.05)。
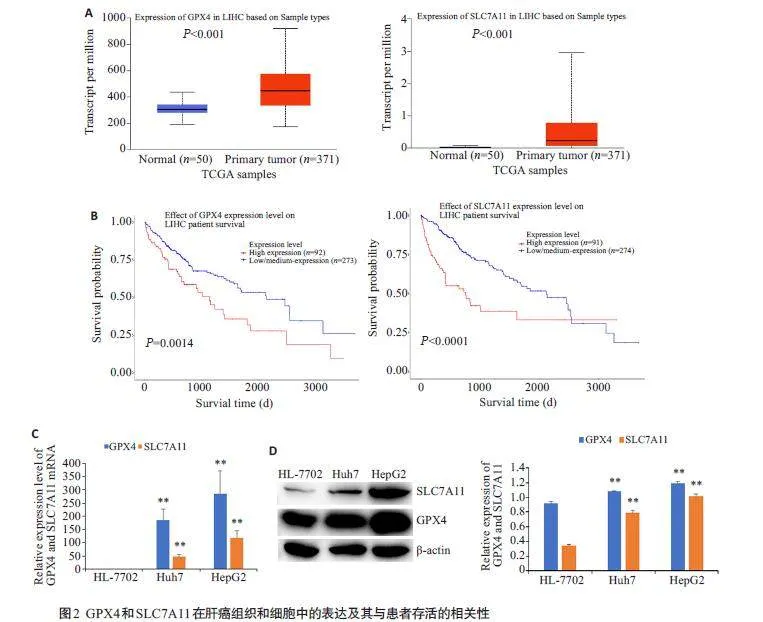
2.2 GPX4 和SLC7A11 在肝癌组织和细胞中的表达及其与肝癌患者存活之间的关系
TCGA数据库分析发现,GPX4 和SLC7A11 在肝癌组织中的表达均显著高于正常肝组织(图2A);它们的表达水平与肝癌患者存活之间的相关性分析显示,GPX4 和SLC7A11 高表达的患者,其存活时间和存活率均显著降低(Plt;0.001,图2B)。检测肝癌细胞和正常肝细胞HL-7702 中GPX4 和SLC7A11 的表达显示,无论是mRNA水平还是蛋白水平,两者在肝癌细胞系中的表达均显著高于正常肝细胞(Plt;0.01,图2C、D)。
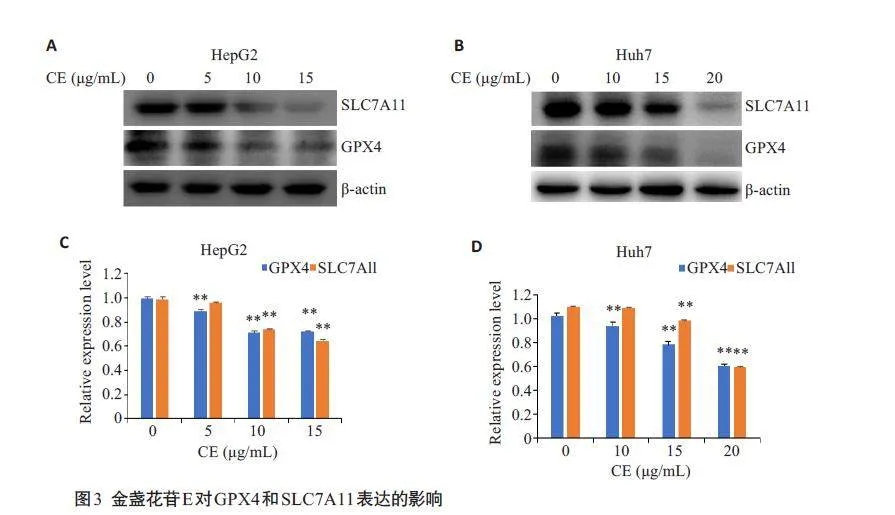
2.3 金盏花苷E对GPX4和SLC7A11表达的影响
金盏花苷E刺激肝癌细胞24 h后,Western blotting检测GPX4和SLC7A11蛋白水平显示金盏花苷E可浓度依赖性的抑制上述蛋白的表达(Plt;0.01,图3)。
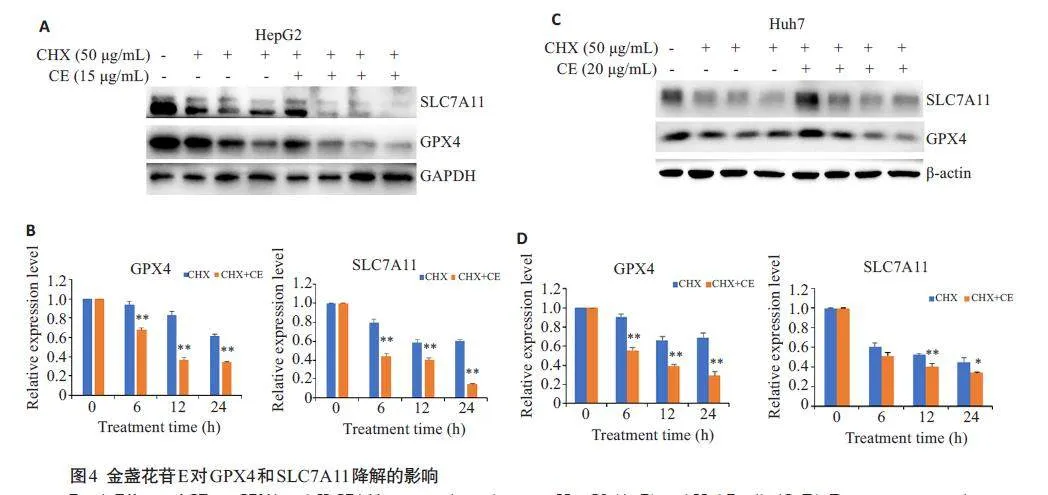
2.4 金盏花苷E对GPX4和SLC7A11降解的影响
检测金盏花苷E对GPX4和SLC7A11蛋白降解的影响,与CHX单独处理组相比,金盏花苷E能够明显促进GPX4和SLC7A11蛋白的降解(Plt;0.05,图4)。
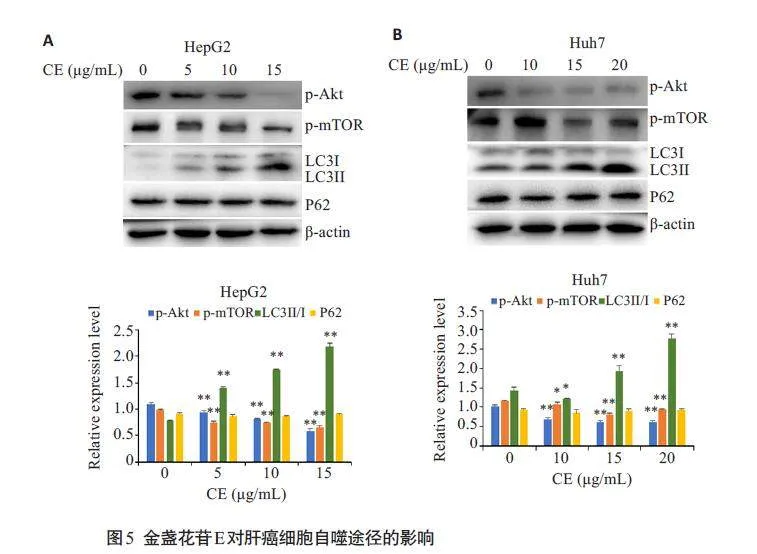
2.5 金盏花苷E对自噬途径的影响
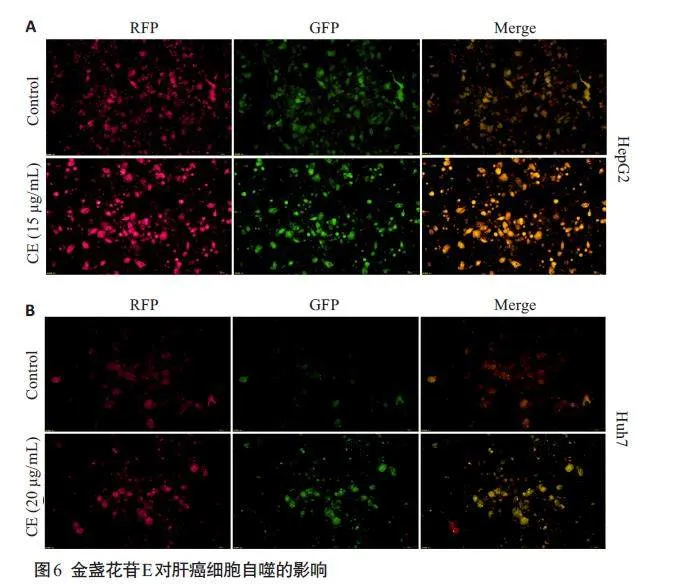
检测金盏花苷E对自噬途径的影响,使用不同浓度的金盏花苷E处理肝癌细胞24 h,自噬标志蛋白LC3Ⅱ的表达明显增强;Akt 和mTOR的磷酸化被显著抑制,但P62的表达并未受明显影响(图5)。mRFP-GFP-LC3慢病毒转染结果显示,金盏花苷E作用24 h 后自噬体(黄色斑点)明显增加,自噬溶酶体(红色斑点)无明显变化(图6)。
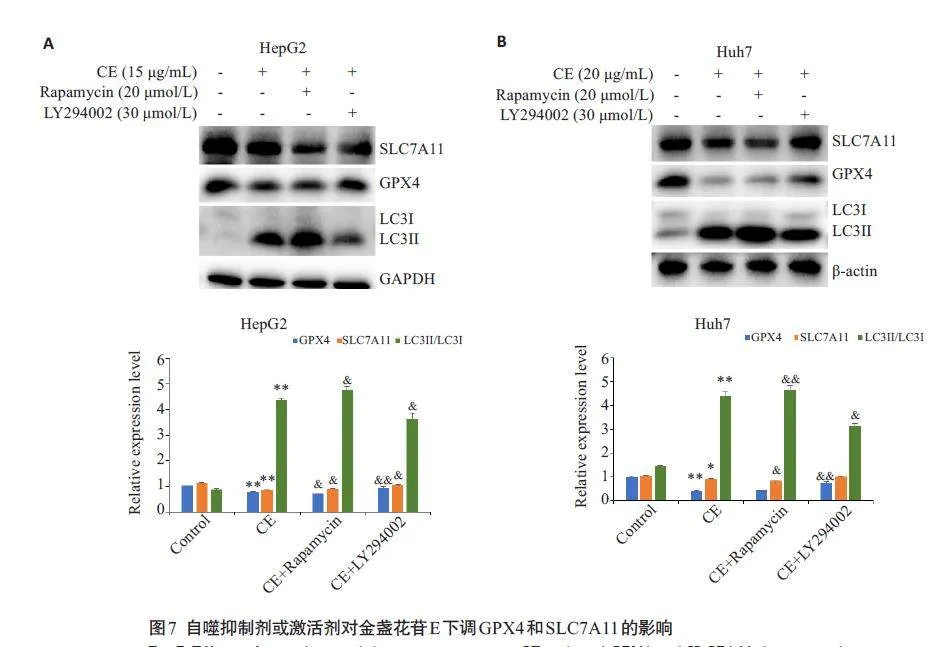
2.6 自噬途径抑制或激活对金盏花苷E下调GPX4 和SLC7A11表达的影响
使用自噬抑制剂LY294002 和自噬激活剂Rapamycin分别与金盏花苷E联合处理肝癌细胞,发现与金盏花苷E单独处理组相比,Rapamycin预处理能够进一步下调SLC7A11的表达;而LY294002预处理组则能够逆转金盏花苷E对GPX4和SLC7A11的抑制作用。而且LC3Ⅱ的表达水平也进一步证明了Rapamycin对自噬途径的激活作用,以及 LY294002对自噬途径的抑制作用(图7)。
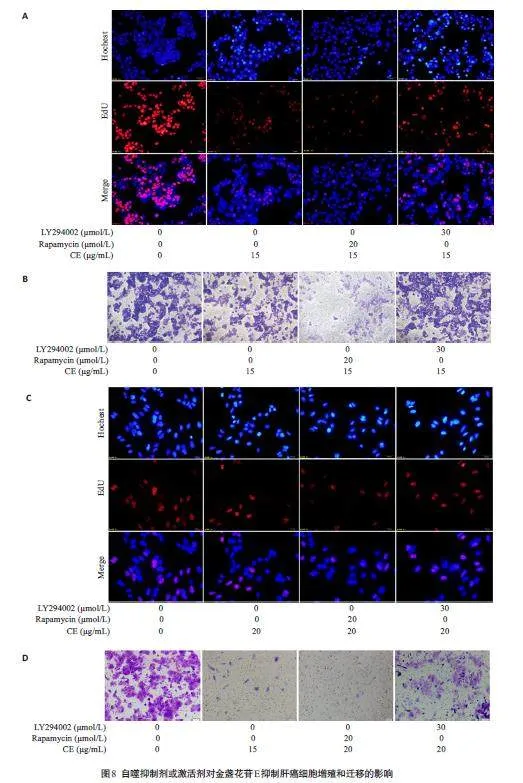
2.7 自噬途径抑制或激活对金盏花苷E抑制肝癌细胞增殖和迁移的影响
检测Rapamycin 和LY294002 与金盏花苷E 联合作用对肝癌细胞增殖和迁移的影响,结果显示,金盏花苷E单独处理的肝癌细胞,EdU阳性染色细胞占比明显低于对照组;Rapamycin 与金盏花苷E联合作用,EdU阳性染色细胞数量显著低于金盏花苷E单独处理组,而LY294002与金盏花苷E联合处理组EdU阳性染色细胞数量较金盏花苷E组明显增加(图8A、C)。Transwell实验发现金盏花苷E单独处理的肝癌细胞迁移能力与对照组相比显著降低。与金盏花苷E 处理组相比,Rapamycin 与金盏花苷E联合处理能够进一步抑制肝癌细胞的迁移能力;而LY294002 则逆转了金盏花苷E对肝癌细胞迁移的抑制作用(图8B、D)。
3 讨论
肝癌作为消化系统常见的恶性肿瘤,发病率和死亡率均较高。虽然已有研究表明,在肝癌HepG2细胞中,天然活性产物金盏花苷E能够通过下调HMGB1 的表达抑制肝癌细胞增殖和迁移[20]。鉴于肿瘤发生、发展在分子机制方面的复杂性,本文以两种肝癌系HepG2 和Huh7 为研究对象,深入探讨了金盏花苷E抑制肝癌细胞增殖和迁移的新机制。本研究结果表明,金盏花苷E通过激活自噬途径促进GPX4 和SLC7A11 蛋白降解,抑制肝癌细胞的增殖和迁移。
本研究在肝癌细胞系Huh7中,通过CCK-8实验验证了金盏花苷E对肝癌细胞活力的抑制作用。该结果不仅进一步证明了我们前期结果的可靠性,也证明了金盏花苷E对肝癌的抑制作用并非HepG2细胞特异性的,但是金盏花苷E抑制肝癌细胞增殖和迁移的分子机制尚不完全清楚。
越来越多的研究表明,抑制GPX4 和SLC7A11 可达到治疗肿瘤的目的[21-23]。本研究通过TCGA数据库分析和细胞水平检测均发现,GPX4 和SLC7A11 在肝癌组织和肝癌细胞中均显著高表达,且它们的表达水平与肝癌患者存活呈现明显负相关。金盏花苷E能否通过影响GPX4 和SLC7A11 的表达,抑制肝癌细胞的增殖和迁移呢? 金盏花苷E处理的肝癌细胞中GPX4和SLC7A11 蛋白表达被明显抑制。然而,我们在转录水平并未获得和蛋白水平一致的实验结果。我们猜想,金盏花苷E 可能通过调控蛋白降解途径抑制GPX4 和SLC7A11 的表达。本研究结果显示,金盏花苷E 和CHX 联合处理的肝癌细胞,无论是GPX4 还是SLC7A11 蛋白降解速度均明显高于CHX组。该结果意味着金盏花苷E能够通过促进蛋白降解下调GPX4和SLC7A11的表达。
自噬降解途径是体内蛋白降解的主要方式之一[24, 25], Akt/mTOR是调节自噬的重要信号途径,参与肿瘤发生、发展的一系列病理学过程,且很多研究证明天然产物能够通过靶向Akt/mTOR介导的自噬抑制肿瘤的增殖[26]。因此,靶向Akt/mTOR介导的自噬是许多肿瘤治疗的重要策略[27, 28]。本研究结果显示,金盏花苷E处理肝癌细胞24 h 能够明显抑制Akt 和mTOR的磷酸化,并显著诱导自噬标志蛋白LC3Ⅱ的表达,但不影响P62的表达水平。自噬发生时,定位在胞浆的LC3Ⅰ与磷脂酰乙醇胺(PE)结合形成LC3Ⅱ,P62与泛素化的蛋白质结合,再与LC3Ⅱ蛋白形成复合物,在自噬溶酶体内降解。当自噬流畅通的时候, LC3Ⅱ增加,P62降低。但我们的结果显示,金盏花苷E作用肝癌细胞后LC3Ⅱ表达增加,但P62并无明显改变。造成该现象的原因可能是金盏花苷E仅影响自噬体的形成,对自噬溶酶体的形成并无明显作用。
CQ和3-MA 是经典的自噬抑制剂,CQ主要通过影响自噬溶酶体的形成,3-MA作为PI3KⅢ家族的特异性抑制剂,通过阻断自噬体的形成,发挥自噬抑制作用。LY294002是一种非特异性的PI3K抑制剂,可广泛阻断细胞内PI3K信号通路的磷酸化过程,从而抑制自噬体的形成。已有研究表明, LY294002能够阻断 HER2 阳性的胃癌细胞中 T-DM1 诱导的自噬[29];LY294002能够逆转紫胶桐酸对HepG2 细胞自噬的诱导作用[30];LY294002通过抑制自噬参与 gracillin的抗黑色素瘤作用[31]。本实验证明金盏花苷E处理后显著诱导LC3Ⅱ的表达,但不影响P62 的表达水平,意味着金盏花苷E主要影响自噬体的形成。因此,本文选取LY294002作为自噬抑制剂进行后续研究。
为进一步证明自噬途径在金盏花苷E抑制GPX4和SLC7A11表达中的作用,本研究采用了自噬激活剂Rapamycin[32]和自噬抑制剂LY294002[33]联合金盏花苷E处理肝癌细胞,检测GPX4和SLC7A11蛋白的表达。结果显示,Rapamycin确实能够进一步增强金盏花苷E对GPX4和SLC7A11蛋白的抑制作用,而LY294002则明显逆转了金盏花苷E的上述效应。为证明自噬途径在金盏花苷E抑制肝癌细胞增殖和迁移中的作用,我们通过EdU和transwell实验检测自噬抑制剂和激活剂对金盏花苷E调控细胞增殖和迁移的影响,结果同样支持金盏花苷E通过激活自噬途径抑制肝癌细胞增殖和迁移的结论。
总之,本研究在肝癌HepG2 和Huh7 细胞中证明,金盏花苷E通过增强自噬途径介导的GPX4和SLC7A11降解,抑制肝癌细胞的增殖和迁移。本研究不仅在另一肝癌细胞系中验证了金盏花苷E对肝癌细胞增殖和迁移的抑制作用,还提示了金盏花苷E发挥抗癌作用的新机制。
由于GPX4和SLC7A11是铁死亡的重要负性调节因子[22, 34, 35],而铁死亡作为2012年发现的一种新型细胞死亡形式,已经成为很多肿瘤治疗的重要策略[36, 37]。在本研究中,金盏花苷E能够抑制GPX4和SLC7A11的表达提示我们,铁死亡可能在金盏花苷E抗肿瘤作用中发挥一定的作用。我们接下来的工作将重点关注金盏花苷E对肝癌细胞铁死亡的影响及可能的分子机制。
参考文献:
[1] Xia CF, Dong XS, Li H, et al. Cancer statistics in China and UnitedStates, 2022: profiles, trends, and determinants[J]. Chin Med J,2022, 135(5): 584-90.
[2] Wang SN, Wu XW, Wu XM, et al. Systematic analysis of the role ofLDHs subtype in pan-cancer demonstrates the importance of LDHDin the prognosis of hepatocellular carcinoma patients[J]. BMCCancer, 2024, 24(1): 156.
[3] 谢思雨, 李淼生, 江峰乐, 等. EHHADH是肝细胞癌脂肪酸代谢通路的关键基因: 基于转录组分分析[J]. 南方医科大学学报, 2023, 43(5): 680-93.
[4] Metur SP, Lei YC, Zhang ZH, et al. Regulation of autophagy geneexpression and its implications in cancer[J]. J Cell Sci, 2023, 136(10): jcs260631.
[5] Jain V, Singh MP, Amaravadi RK. Recent advances in targetingautophagy in cancer[J]. Trends Pharmacol Sci, 2023, 44(5):290-302.
[6] Chow AK, Yau SW, Ng L. Novel molecular targets in hepatocellularcarcinoma[J]. World J Clin Oncol, 2020, 11(8): 589-605.
[7] Wang Y, Deng BC. Hepatocellular carcinoma: molecularmechanism, targeted therapy, and biomarkers[J]. Cancer Metastasis Rev, 2023, 42(3): 629-52.
[8] Glaviano A, Foo ASC, Lam HY, et al. PI3K/AKT/mTOR signalingtransduction pathway and targeted therapies in cancer[J]. MolCancer, 2023, 22(1): 138.
[9] He PZ, He Y, Ma JJ, et al. Thymoquinone induces apoptosis andprotective autophagy in gastric cancer cells by inhibiting the PI3K/Akt/mTOR pathway[J]. Phytother Res, 2023, 37(8): 3467-80.
[10]Lee J, Roh JL. SLC7A11 as a gateway of metabolic perturbation andferroptosis vulnerability in cancer[J]. Antioxidants, 2022, 11(12):2444.
[11] Liu JY, Xia XJ, Huang P. xCT: a critical molecule that links cancermetabolism to redox signaling[J]. Mol Ther, 2020, 28(11): 2358-66.
[12]Huang Y, Dai ZY, Barbacioru C, et al. Cystine-glutamate transporterSLC7A11 in cancer chemosensitivity and chemoresistance[J].Cancer Res, 2005, 65(16): 7446-54.
[13]Li SJ, Lu ZY, Sun RB, et al. The role of SLC7A11 in cancer: friendor foe[J]? Cancers, 2022, 14(13): 3059.
[14]Zhang W, Liu Y, Liao Y, et al. GPX4, ferroptosis, and diseases[J].Biomed Pharmacother, 2024, 174: 116512.
[15] Jia CX, Zhang X, Qu TT, et al. Depletion of PSMD14 suppressesbladder cancer proliferation by regulating GPX4[J]. PeerJ, 2023,11: e14654.
[16]Tang X, Ding H, Liang ML, et al. Curcumin induces ferroptosis innon-small-cell lung cancer via activating autophagy[J]. ThoracCancer, 2021, 12(8): 1219-30.
[17]Le YF, Guo JN, Liu ZJ, et al. Calenduloside E ameliorates nonalcoholicfatty liver disease via modulating a pyroptosis-dependentpathway[J]. J Ethnopharmacol, 2024, 319(Pt 2): 117239.
[18]Li JX, Bu YJ, Li B, et al. Calenduloside E alleviates cerebralischemia/reperfusion injury by preserving mitochondrial function[J]. J Mol Histol, 2022, 53(4): 713-27.
[19]汤 托, 王胜男, 蔡田雨, 等. 金盏花苷E通过ROS介导的JAK1-stat3信号途径抑制LPS诱发的炎症反应[J]. 南方医科大学学报, 2019,39(8): 904-10.
[20]Wang SN, Chen XL, Cheng J, et al. Calunduloside E inhibits HepG2cell proliferation and migration via p38/JNK-HMGB1 signallingaxis[J]. J Pharmacol Sci, 2021, 147(1): 18-26.
[21]Zhang W, Jiang BP, Liu YX, et al. Bufotalin induces ferroptosis innon-small cell lung cancer cells by facilitating the ubiquitination anddegradation of GPX4[J]. Free Radic Biol Med, 2022, 180: 75-84.
[22]Li DB, Wang YH, Dong C, et al. CST1 inhibits ferroptosis andpromotes gastric cancer metastasis by regulating GPX4 proteinstability via OTUB1[J]. Oncogene, 2023, 42(2): 83-98.
[23]Wang XB, Chen YQ, Wang XD, et al. Stem cell factor SOX2 confersferroptosis resistance in lung cancer via upregulation of SLC7A11[J]. Cancer Res, 2021, 81(20): 5217-29.
[24]Hanzl A, Winter GE. Targeted protein degradation: current andfuture challenges[J]. Curr Opin Chem Biol, 2020, 56: 35-41.
[25]Wang Y, Le WD. Autophagy and ubiquitin-proteasome system[J].Adv Exp Med Biol, 2019, 1206: 527-50.
[26]Xu ZR, Han X, Ou DM, et al. Targeting PI3K/AKT/mTORmediatedautophagy for tumor therapy[J]. Appl MicrobiolBiotechnol, 2020, 104(2): 575-87.
[27]Zhang M, Liu SH, Chua MS, et al. SOCS5 inhibition inducesautophagy to impair metastasis in hepatocellular carcinoma cells viathe PI3K/Akt/mTOR pathway[J]. Cell Death Dis, 2019, 10(8): 612.
[28]Li H, Zhao SF, Shen LW, et al. E2F2 inhibition induces autophagyvia the PI3K/Akt/mTOR pathway in gastric cancer[J]. Aging, 2021,13(10): 13626-43.
[29]Zhang JH, Fan JJ, Zeng X, et al. Targeting the autophagy promotedantitumor effect of T-DM1 on HER2-positive gastric cancer[J]. CellDeath Dis, 2021, 12(4): 288.
[30]Yi H, Wang K, Du BY, et al. Aleuritolic acid impaired autophagicflux and induced apoptosis in hepatocellular carcinoma HepG2 cells[J]. Molecules, 2018, 23(6): 1338.
[31]Li JK, Zhu PL, Wang Y, et al. Gracillin exerts anti-melanoma effectsin vitro and in vivo: role of DNA damage, apoptosis and autophagy[J]. Phytomedicine, 2023, 108: 154526.
[32]Yu WX, Lu C, Wang B, et al. Effects of rapamycin on osteosarcomacell proliferation and apoptosis by inducing autophagy[J]. Eur RevMed Pharmacol Sci, 2020, 24(2): 915-21.
[33]Chen WS, Xian GY, Gu MH, et al. Autophagy inhibitors 3-MA andLY294002 repress osteoclastogenesis and titanium particlestimulatedosteolysis[J]. Biomater Sci, 2021, 9(14): 4922-35.
[34]Ouyang SM, Li HX, Lou LL, et al. Inhibition of STAT3-ferroptosisnegative regulatory axis suppresses tumor growth and alleviateschemoresistance in gastric cancer[J]. Redox Biol, 2022, 52: 102317.
[35]Zeng C, Lin J, Zhang KT, et al. SHARPIN promotes cellproliferation of cholangiocarcinoma and inhibits ferroptosis via p53/SLC7A11/GPX4 signaling[J]. Cancer Sci, 2022, 113(11): 3766-75.
[36]Dixon SJ, Lemberg KM, Lamprecht MR, et al. Ferroptosis: an irondependentform of nonapoptotic cell death[J]. Cell, 2012, 149(5):1060-72.
[37]Mou YH, Wang J, Wu JC, et al. Ferroptosis, a new form of cell death:opportunities and challenges in cancer[J]. J Hematol Oncol, 2019,12(1): 34.
(编辑:经 媛)
基金项目:安徽高校自然科学研究项目(KJ2020ZD54,2022AH051212);安徽省学科(专业)拔尖人才学术资助项目(gxbjZD2021060);活性生物大分子研究安徽省重点实验室项目(1306C083008);国家级大学生创新创业训练计划项目(202310368002)

