柑橘皮提取液绿色合成纳米Fe3O4及其吸附水中孔雀石绿的性能研究



摘 要:以柑橘皮提取液为还原剂和稳定剂,绿色合成Fe3O4纳米材料,利用扫描电子显微镜(SEM)、X射线衍射图谱(XRD)、傅立叶变换红外光谱(FT-IR)等手段对材料进行表征,并考察了其对孔雀石绿(MG)的吸附性能。结果表明:绿色合成纳米Fe3O4呈不规则圆球体,分散性和结晶度较好。在投加量为1.0 g/L、初始pH为4、温度为25 ℃、初始浓度为20 mg/L时,对孔雀石绿的吸附率达到95.33 %。纳米Fe3O4对MG的吸附过程分别符合准二级动力学方程和Langmuir等温方程。热力学研究表明,纳米Fe3O4吸附MG是自发吸热过程。绿色合成纳米Fe3O4重复利用4次吸附率仍在70%以上。
关键词:柑橘皮;绿色合成;纳米Fe3O4;孔雀石绿;吸附
中图分类号:TB383.1 文献标识码:A 文献编号:1007 - 9734 (2024) 03 - 0081 - 07
孔雀石绿(Malachite Green,MG),是一种三苯甲烷类阳离子染料,广泛用于印染、造纸、食品、化妆品等行业[1]。除了在工业上的应用外,MG还是常用于治疗鱼类鱼霉病等各种菌类感染的有效抗菌剂、杀菌剂和杀虫剂[2]。但MG具有致突变性、致畸形和致癌性[3],其经鱼体等迅速代谢后,以毒性更强的隐色孔雀石绿(leuco malachite green,LMG)贮藏在肌肉组织中,食用后可对人类的生命健康造成严重伤害[4]。因此,水体中MG的去除引起了人们的广泛关注。
去除孔雀石绿废水的方法通常有生物法[5]、光催化法[6,7]、吸附法[8,9]等。吸附法由于操作简单、效率高、无二次污染、经济实用等优点,越来越受到人们的重视[10]。其中吸附剂是影响吸附法去除污染物效率和成本的核心因素。目前,大部分吸附剂在使用过程中或多或少存在吸附容量低、再生困难等问题,限制了吸附法在污废水处理中的应用。
磁性Fe3O4纳米材料由于具有较高的比表面积,生物相容性好、表面功能化作用强、饱和磁化强度与磁响应性高,在外加磁场作用下具有良好的固液分离能力,而被广泛应用于水中各种污染物的吸附[11-14]。目前磁性Fe3O4纳米材料的制备常用化学还原法,但还原剂 (硼氢化钠或水合肼) 具有毒性,会对环境造成危害。为了实现纳米Fe3O4颗粒制备过程的绿色环保,利用植物提取物中的活性成分如酚类、黄酮类作还原剂及分散剂成为一种新兴的制备方法[15,16]。
柑橘是世界第一大宗水果,也是世界上重要的经济作物之一。2020年我国柑橘产量达5121.9万吨,其皮渣(占果重的20%—50%)年产量达1200多万吨,并且柑橘皮渣中含有类黄酮、类胡萝卜素、精油等多种功能性成分[17]。利用柑橘皮提取液替代有害的还原剂,绿色合成磁性Fe3O4纳米材料,应用于水体有机污染物的吸附,不仅可以减少环境污染,还可以实现生物资源的再利用,达到以废治废的目的。本文以柑橘皮提取液作为还原剂和稳定剂,绿色合成Fe3O4纳米材料,并应用于MG染料的吸附,探讨其吸附性能,以期为纳米Fe3O4的绿色制备,以及柑橘皮的资源化利用提供新思路。
1 材料与方法
1.1" 实验材料与仪器
实验材料:柑橘皮(广西宽皮柑橘购自超市,取皮自然干燥),硝酸铁(Fe(NO3)3∙9H2O)购自北京化工集团,孔雀石绿(C23H25CIN2)购自天津市科密欧化学试剂有限公司,均为分析纯。
仪器:扫描电子显微镜(JSM-7001F)、X射线衍射仪(Bruker D8 Advance)、红外光谱仪(IS5)、紫外可见分光光度计(T9CS)、箱式马弗炉(XL-1800)、恒温磁力搅拌器(78HW-1)、高速离心机(JW-2019H)。
1.2" 材料的制备
清洗柑橘皮,干燥至恒重,破碎成为粉末。称取1 g粉末加入50 mL蒸馏水搅拌3 h,60 ℃的水浴60 min,离心5 min,取上清液,即为柑橘皮提取液。
将1g Fe(NO3)3·9H2O与40 mL柑橘皮提取液混合搅拌60 min,置于60 ℃的水浴中60 min,转至鼓风干燥箱内,120 ℃干燥,转入马弗炉中300 ℃热处理1 h,所得粉末为绿色纳米Fe3O4材料。
1.3" 材料的表征
利用扫描电子显微镜分析材料表面结构形态,利用X射线衍射仪分析材料的物相组成,利用红外光谱仪分析材料的表面官能团特征。
1.4" 吸附实验
1.4.1 吸附率的计算
准确称取一定量绿色制备Fe3O4纳米材料于锥形瓶中,加入20 mL一定浓度 MG溶液,用1 mol/L的HCl或NaOH溶液调整pH到指定值。密封置于恒温磁力搅拌器中,搅拌2 h后用离心机分离。取上清液在617 nm 波长测定吸光度,根据标准曲线计算MG浓度,利用公式(1)计算吸附率。
[R=1-CtC0×100%] (1)
式中:[R]表示污染物去除率;[Ct]表示吸附结束时污染物浓度mg/L;[C0]表示吸附初始时污染物浓度mg/L。
1.4.2 吸附动力学
称取20 mg吸附剂,加入20 ml 20 mg/L的MG溶液中,分别吸附5、10、20、30、60、90、120 min后取样,测试样品中MG浓度。采用准一级动力学方程(2)和准二级动力学方程(3)对吸附过程进行拟合。
[lnQe-Qt=lnQe-K1t]" (2)
[t/Qt =1/(K2 Q 2e)+(1/b)lnt] (3)
式中:[t]表示吸附时间,min;[Qt、Qe]表示吸附在t时刻和平衡时的吸附量,mg/g;[K1、K2]表示吸附常数。
1.4.3 吸附等温线
称取20 mg吸附剂置于不同浓度的MG模拟废水中,待吸附达到平衡时,测试样品中MG浓度。采用Langmuir(4)和Freundlich(5)吸附等温线模型来拟合Fe3O4对模拟MG的吸附平衡量。
[Ce/Qe=Ce/Qm+1/kLQm] (4)
[lnQe=lnkF+(1/n)lnCe] (5)
式中:[Ce]表示吸附平衡时溶液中MG浓度mg/L;[Qe]、[Qm]表示吸附平衡时的实际吸附量与理论吸附量mg/g;[kL][、kF]表示常数。
1.4.4 吸附热力学
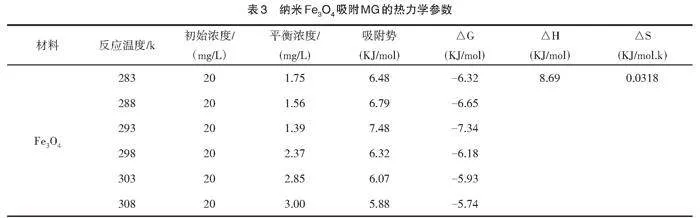
由Clausius-Clapeyron方程(6)和Gibbs方程(7)可以计算出吸附过程的焓变△H和自由能△G;吸附过程的熵变可由Gibbs-Helmholtz方程(8)计算得出;吸附势由Polanyi公式(9)计算得出。
[lnCe=△H/RT+lnK0] (6)
[△G=-RT0xQedx]" (7)
[△S=(△H-△G)/T]" " (8)
[E=-RTln(Ce/C0)]" "(9)
式中:[C0]、[Ce]表示溶液中MG的初始浓度和吸附平衡浓度,mg/L;[T]表示反应温度,K;[R]表示理想气体状态常数;[K0]表示常数;[x]表示溶液中MG的摩尔分数;[Qe]表示吸附平衡时的吸附量,mg/g。
1.5" 吸附—脱附再生实验
用抽滤机将吸附完全的Fe3O4吸附剂分离取出,用0.1 mol/L的H2SO4和去离子水交叉洗涤进行脱附,脱附完成后,用去离子水反复冲洗至中性,在 80 ℃恒温干燥箱中烘干并用于下一次吸附。重复上述实验,将每次实验中Fe3O4吸附剂对MG的去除率作为评价吸附剂再生性能的指标。
2 结果与讨论
2.1" 材料的表征
2.1.1 SEM分析
利用SEM对绿色合成纳米Fe3O4材料的表面形貌进行分析,如图1所示,纳米Fe3O4颗粒较好地分散在柑橘皮生物质炭上,形貌为不规则圆球状,粒径大约在100 nm—200 nm范围,与化学还原法合成Fe3O4球体材料相比,粒径增大。绿色合成Fe3O4球体的表面呈现不同大小的突起,这些突起增加了材料的比表面积,提高了对MG染料废水的吸附面积。
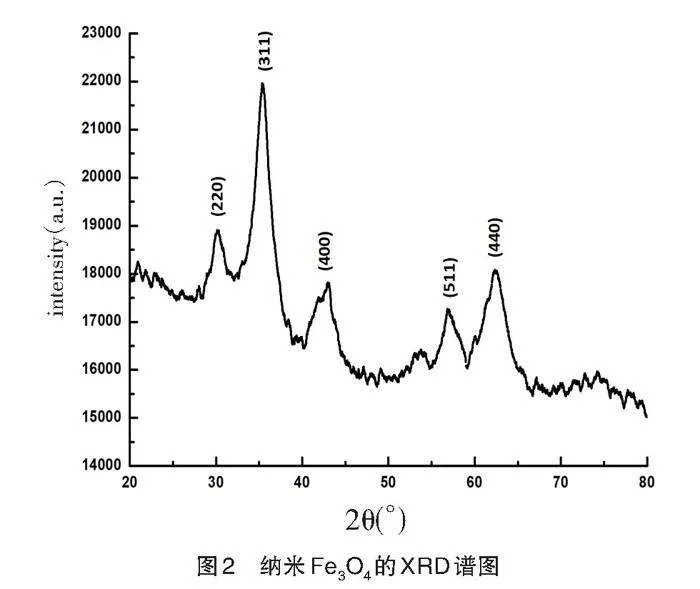
2.1.2 XRD分析
图2为Fe3O4纳米颗粒的XRD谱图,在2θ=30.2°、35.5°、43.4°、57.2°和62.8°处表现出明显的特征衍射峰[18]。特征峰分别对应于Fe3O4标准谱中的(220)(311)(400)(511)(440)晶面,表明合成的纳米Fe3O4材料结晶度良好,呈立方反尖晶石结构,这种结构在尖晶石单元的基础上增加了一个反推的层,使得整个晶体结构变得更加密集,因此具有优异的热稳定性和化学稳定性。
2.1.3 FTIR分析
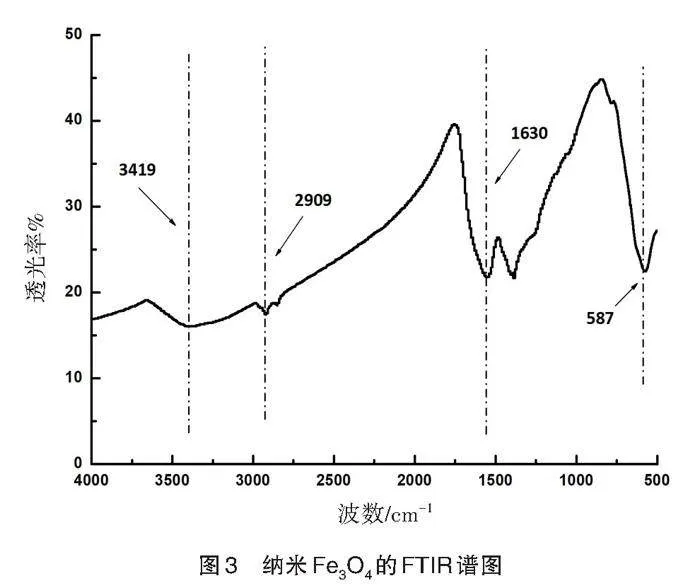
图3为Fe3O4纳米材料的红外光谱图。如图3所示,纳米Fe3O4的FTIR谱图在587 cm-1处出现Fe-O伸缩振动峰[19],1630 cm-1处为Fe3O4束缚水的伸缩振动峰,在2909 cm-1和3419 cm-1处的吸收峰强而宽,是由于表面吸附水、碳水化合物和多酚过多引起的羟基O-H伸缩振动与弯曲振动模式[20],表明以柑橘皮提取液作为还原剂和稳定剂,可以成功合成Fe3O4纳米材料。
2.2" 纳米Fe3O4的吸附性能
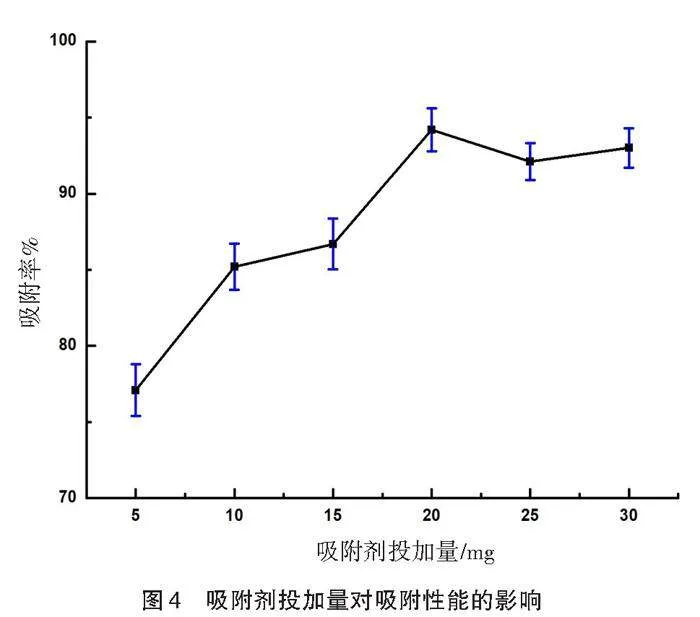
2.2.1 吸附剂投加量对吸附性能的影响
在MG溶液初始浓度为20 mg/L,吸附时间为2 h时,选取纳米Fe3O4投加量为0.25、0.5、0.75、1.0、1.25、1.5 g/L,探究不同吸附剂添加量对吸附性能的影响。由图4可知,随着吸附剂投加量的增加,MG吸附率逐渐增大,当吸附剂添加量为1 g/L时,材料对MG吸附达到最大,再增加材料用量,MG的去除率基本保持稳定,这可能是因为增大Fe3O4用量提供了更多可利用的吸附位点和更大的比表面积,去除率会因此而提高,但过多地增加吸附剂用量会导致吸附位点的饱和。因此,选择1 g/L作为最佳吸附用量。
2.2.2 初始pH对吸附性能的影响
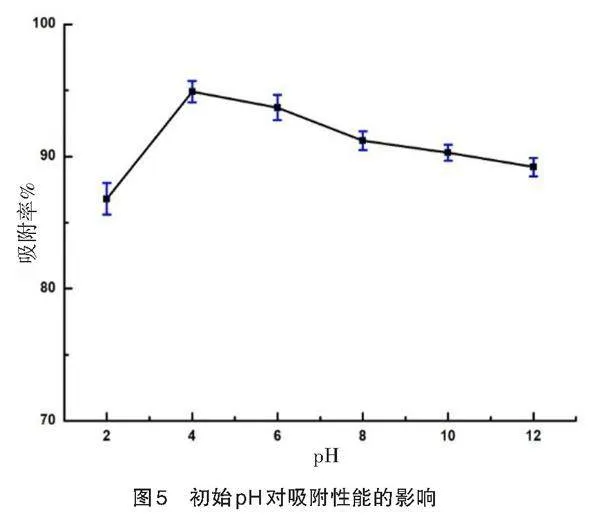
在MG溶液浓度为20 mg/L,吸附时间为2 h,材料投加量为20 mg时,选取初始pH为2、4、6、8、10、12,探究了pH对吸附性能的影响。如图5所示,随着pH的增加,吸附率增大,当pH为4时达到最大,随后逐渐降低。表明在酸性条件下,纳米Fe3O4对MG的吸附效果更好。这是由于当溶液pH较高时,溶液中的OH-容易和MG分子的氨基结合,从而降低纳米Fe3O4对MG的吸附量[8]。因此,选择MG溶液初始pH为4。
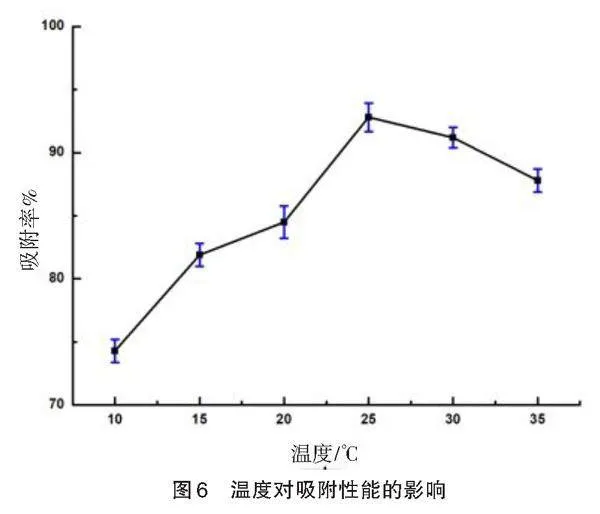
2.2.3 温度对MG吸附性能的影响
在MG初始浓度为20 mg/L,反应时间为2 h,吸附剂投加量为20 mg,溶液pH为4时,控制吸附温度为10℃、15℃、20℃、25℃、30℃、35℃,探究了不同温度对吸附效率的影响。由图6可知,随着温度的增加,Fe3O4纳米颗粒对MG溶液的吸附率逐渐增加,在温度为25 ℃时吸附率最高,后稍有下降,说明适当升温有利于吸附进行,即该反应应该是吸热的过程,继续增加吸附温度,吸附率减小,可能是因为温度升高导致染料的解吸速率变快,吸附率降低[21]。因此选择25 ℃作为最适吸附温度。
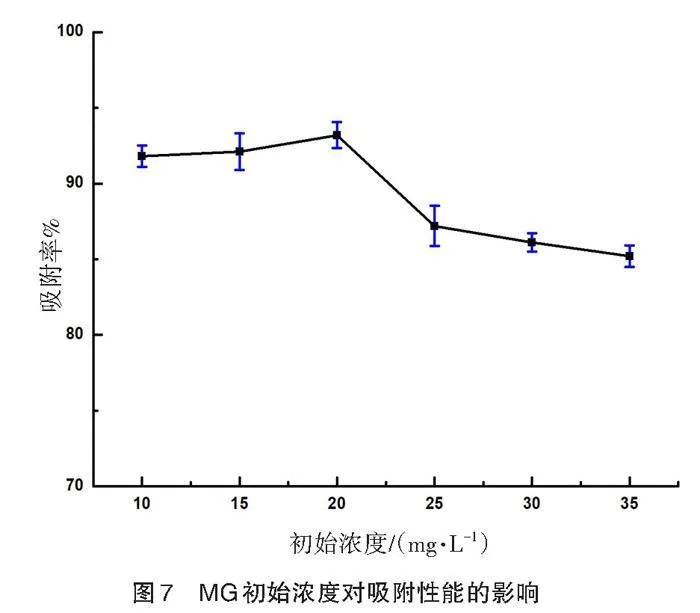
2.2.4 MG初始浓度对吸附性能的影响
在反应时间为2 h,材料投加量为20 mg,溶液pH为4,反应温度为25 ℃时, 选取MG初始浓度为10、15、20、25、30、35 mg/L,探究了MG的初始浓度对吸附性能的影响。如图7所示,在MG溶液浓度低于20 mg/L时,吸附率稍有增加,在20 mg/L时吸附率达到最大,随后略有下降。这是因为MG的浓度增加,使得 MG与Fe3O4材料能充分混合,增大了吸附面积,提高了吸附效率,但是如果过分增加MG浓度,会加重 Fe3O4中吸附位点的载荷能力,导致吸附率的下降。因此,选择20 mg/L 作为MG溶液初始浓度。
2.2.5 吸附时间对吸附性能的影响
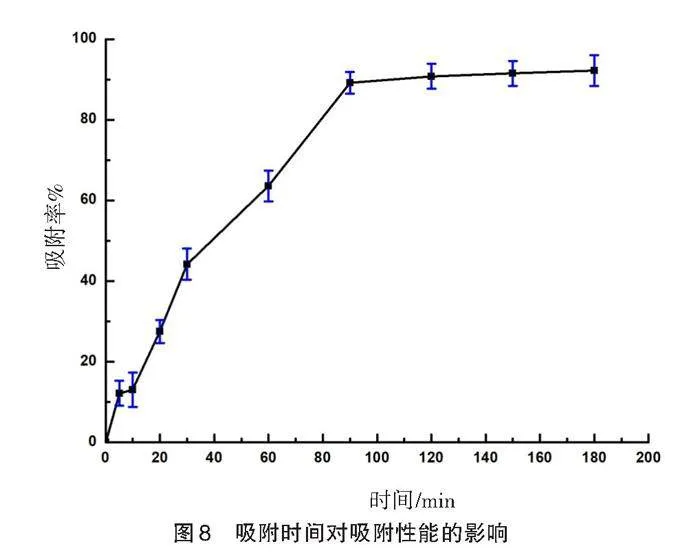
在MG初始浓度为20 mg/L,材料投加量为20 mg,溶液pH为4,反应温度为25 ℃时,探究了吸附时间对吸附率的影响,如图8所示。
当吸附时间从5 min延长至90 min 时,吸附率迅速提高,继续增加吸附时间,吸附率趋于平缓。这可能是因为绿色合成吸附剂Fe3O4用量一定时,吸附位点的数量有限,吸附初始阶段,吸附剂表面有相对充足的活性吸附位点,MG可被快速的吸附。随着吸附时间的增长,活性吸附位点减少,不利于吸附,吸附率也趋于恒定。基于吸附效率和省时节能双重角度考虑,选择120 min为吸附时间。
2.3" 吸附动力学
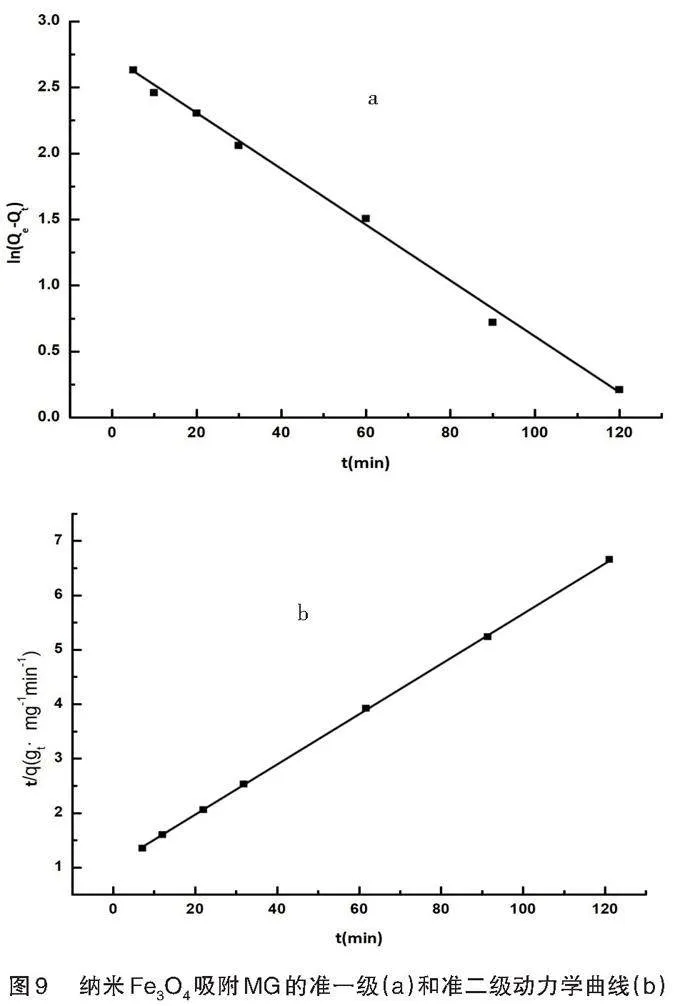
采用准一级动力学方程和准二级动力学方程来评估纳米Fe3O4吸附MG的动力学过程,拟合曲线如图9所示。表1为纳米Fe3O4吸附MG的动力学模型拟合数据结果。从图9和表1的拟合结果可知,准二级动力学模型的拟合程度更高,准二级动力学模型拟合的R2 大于0.99,因此,准二级动力学模型可以更准确地描述纳米Fe3O4对MG的吸附过程。拟合结果表明,吸附过程以化学吸附为主,Fe3O4对MG的吸附速率主要受染料分子与吸附剂活性中心之间的化学键控制[22]。
2.4" 吸附等温线
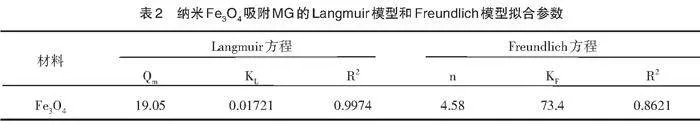
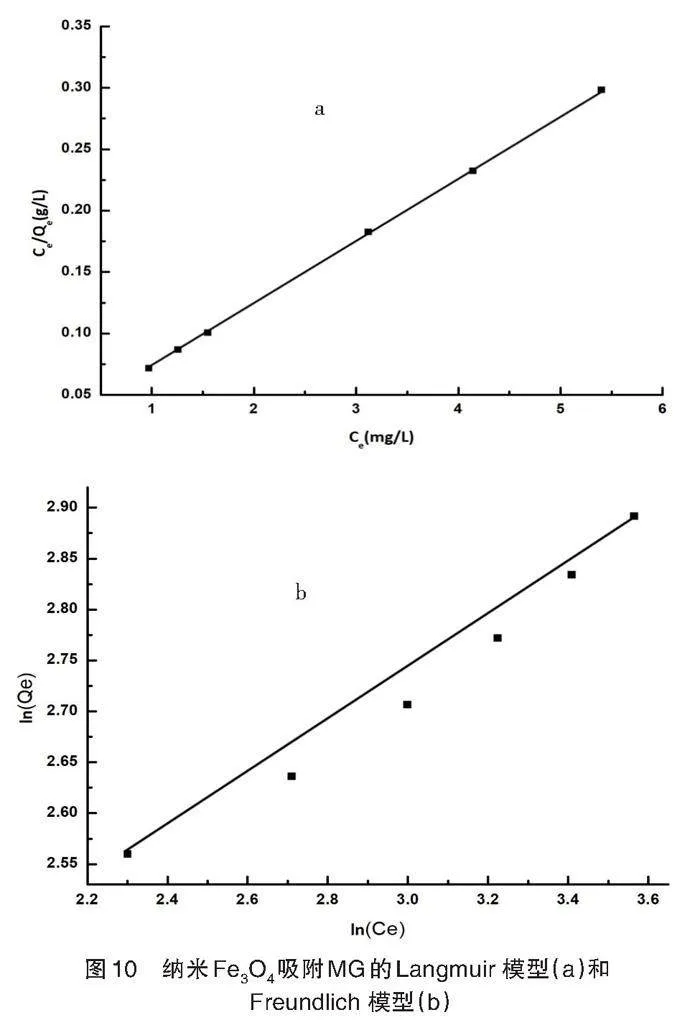
采用 Langmuir 和 Freundlich 等温吸附模型对纳米Fe3O4吸附MG过程进行拟合,结果如图10和表2所示。Fe3O4材料的Langmuir吸附等温线的相关系数R2为0.9974,大于Freundlich 等温线的R2值。因此,Langmuir等温线模型较好地预测了Fe3O4对MG的吸附过程。说明吸附发生在均匀的吸附剂表面,属于单层吸附。
2.5" 吸附热力学
通过热力学计算发现(表3),纳米Fe3O4材料对MG吸附过程的吉布斯自由能△G<0,说明吸附过程自发进行[23]。焓变△H>0,说明吸附过程伴随着吸热现象,温度升高,有利于吸附的进行;Fe3O4的△H=8.69,说明吸附过程主要受氢键影响[24]。熵变△S>0,说明在吸附过程中无序性增加[25]。
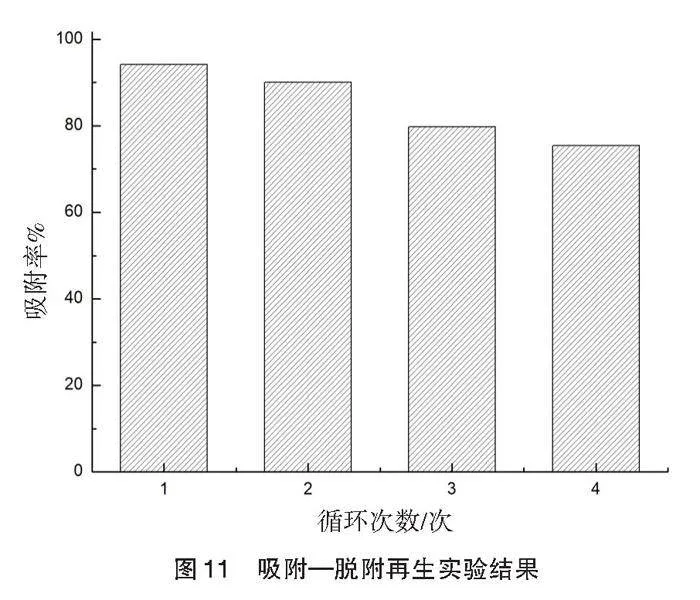
2.6" 吸附—脱附再生实验结果
纳米Fe3O4材料对MG的吸附—脱附再生实验结果见图11。由图11可知,第一次吸附时,纳米Fe3O4材料对MG去除率为95.5%,经过3次再生后,第四次吸附时,去除率仍为70.3%,表明Fe3O4纳米材料具有较好的重复使用性。
3 结 论
(1)利用柑橘皮提取液绿色合成Fe3O4纳米材料,形貌为不规则圆球体,分散性较好,呈立方反尖晶石结构,结晶度高。
(2)将制备得到的Fe3O4纳米材料应用于MG的吸附去除研究。探究了吸附剂添加量、pH、温度、MG溶液初始浓度等因素的影响,在最佳条件下,Fe3O4对MG的吸附率达95%以上。
(3)通过吸附动力学、吸附等温线和吸附热力学拟合发现吸附过程以化学吸附为主,属于单分子层吸附,吸附过程为吸热自发的反应。通过循环实验,证实绿色合成的纳米Fe3O4具有较好的循环利用性能。
参考文献:
[1]肖勇, 郝慧茹, 李军, 等. 不同晶型二氧化锰去除孔雀石绿的研究[J]. 工业水处理, 2022, 42(8):142-148.
[2]秦丽, 李东东, 田景升, 等. 融合多种技术的隐色孔雀石绿印迹传感器的制备及其应用[J]. 化工进展, 2022, 41(11):6018-6028.
[3]YANG J, WANG Z, LIN Y, et al. Immobilized Cerrena sp. laccase: Preparation, thermal inactivation, and operational stability in malachite green decolorization[J]. Scientific Report, 2017, 7(1): 16429.
[4]孟二琼, 念琪循, 李峰, 等. 磺酸化磁性氮化碳固相萃取超高液相色谱—串联质谱筛检淡水鱼中孔雀石绿和隐色孔雀石绿[J]. 色谱, 2023, 41(8):673-682.
[5]田小丽, 李绪鹏, 李春生, 等. 微生物降解孔雀石绿的研究进展[J]. 中国渔业质量与标准, 2021, 11(6):34-44.
[6]马旭光. α-SiW11Ni/PANI/ZnO三元复合催化剂的制备及光催化性能[J]. 印染助剂, 2023, 40(7):14-19.
[7]李大军, 杜倩, 贺惠, 等. GO-PPy/TiO2复合物的制备及降解废水中的复合物的制备及降解废水中的孔雀石绿[J]. 水处理技术, 2022, 48(11): 88-93.
[8]韩志勇, 杜承臻, 张 娟, 等. 玉米秸秆生物炭的制备改性及其对孔雀石绿染料的吸附效果[J]. 石油化工, 2023, 52(2):199-208.
[9]江晨浩, 王杰, 龚亮, 等. 磁性蟹壳碳吸附材料对溶液中孔雀石绿吸附性能研究[J]. 中南大学学报(自然科学版), 2021, 52(5): 1446−1455.
[10]蔡婉玲, 张建森. 高岭土负载绿色合成纳米铁的制备及其对孔雀石绿和铅离子的去除性能研究[J]. 西昌学院学报(自然科学版), 2023, 37(3):61-67.
[11]梁文婷, 黄昱, 文朝朝, 等. 功能化Fe3O4磁性纳米材料的制备及在水中污染物处理中的应用[J]. 山西大学学报(自然科学版), 2023, 46(2):405−415.
[12]赵峰滔,李宣镜,李恩泽, 等. 磁性纳米Fe3O4吸附材料的制备及在废水处理中的应用[J]. 日用化学工业, 2022, 52(8):882-891.
[13]邹成龙,徐志威,聂发辉,等. Fe3O4@SA/GO凝胶球的制备及对亚甲基蓝的吸附性能[J].环境工程学报,2022, 16(1):121-132.
[14]CHEN D, XU R. Hydrothermal synthesis and characterization of nanocrystalline Fe3O4 powders[J].Materials Research Bulletin, 1998, 33(7):1015-1021.
[15]刘清,邓真宁,滑熠龙,等. 纳米铁的绿色合成及其在环境中的应用研究进展[J]. 化工进展, 2020, 39(5): 1950-1963.
[16]林珺娥,赵紫苗,郭会琴,等. 基于油茶果壳的络合生物质对水中氨氮的吸附特性及机制[J]. 南昌航空大学学报(自然科学版), 2023,37(3):39-49.
[17]唐清苗, 王鲁峰. 柑橘皮渣的功能组分及加工应用现状[J]. 食品与机械, 2022, 38(6):180-185,218.
[18]SONG W, GAO B, XU X, et al. Adsorption-desorption behavior of magnetic amine/Fe3O4 functionalized biopolymer resin towards anionic dyes from wastewater[J]. Bioresource Technology, 2016(210): 123-130.
[19]HONG D Y, HWANG Y K, SERRE C, et al. Porous chromium terephthalate MIL-101 with coordinatively unsaturated sites: surface functionalization, encapsulation, sorption and catalysis[J]. Advanced Functional Materials, 2010, 19(10): 1537-1552.
[20]PADMANATHAN N, SELLADURAI S. Shape controlled synthesis of CeO2 nanostructures for high performance supercapacitor electrodes[J]. Royal Society of Chemistry Advances, 2014(4): 6527-6534.
[21]高海荣, 王亚鑫, 黄振旭, 等. Fe3O4/菹草磁性材料的制备及对刚果红吸附研究[J]. 化学研究与应用, 2021, 33(2):284-289.
[22]CHEN S X, HUANG Y F, HAN X X, et al. Simultaneous and efficient removal of Cr(VI) and methyl orange on LDHs decorated porous carbons[J]. Chemical Engineering Journal, 2018(352): 306-315.
[23]PRISCIANDARO M, PIEMONTE V, GMD CELSO, et al. Thermodynamic features of dioxins' adsorption[J]. Journal of Hazardous Materials, 2017(324): 645-652.
[24]L AF I R, CHARRADI K, DJ EB BI M A, et al. Adsorption study of Congo red dye from aqueous solution to Mg–Al–layered double hydroxide[J]. Advanced Powder Technology, 2016, 27(1):232-237.
[25]李见云,崔节虎,郑宾国,等. 秸秆掺杂与煅烧改性沸石吸附铜锌离子的特性[J]. 应用化工, 2019, 48(7): 1558-1562.
责任编校:陈 强,裴媛慧
Green Synthesis of Fe3O4 Nanomaterials Using Citrus Reticulata Peels Extract and its Application in Removal of Malachite Green
ZHANG Mengfan, LI Chunguang, WANG Cong, WANG Qiang, DU Chenyang, LIU Yuqing,
YANG Jie, WANG Hanrui
(Zhengzhou Key Laboratory of environmental functional materials, Zhengzhou University of Aeronautics,"Zhengzhou 450046, China)
Abstract: The Fe3O4 nanomaterials were green-synthesized by the peels extract of Citrus reticulata as the reducing agent and stabilizer. The physical and chemical properties of Fe3O4 nanomaterials were characterized with scanning electron microscope(SEM), X-ray diffraction(XRD), Fourier transform infrared spectroscopy (FTIR), and the adsorption performance of Malachite Green was investigated. The results show that green synthetic nano-Fe3O4 is an irregular sphere with good dispersion and crystallinity. The adsorption rate of MG can reach 95.33% when the adsorption time of 2 h, solution pH of 4, material dosage of 20 mg, MG concentration of 20 mg/L, at 25 ℃. The results showed that the adsorption kinetics and adsorption isotherm of MG adsorption by nano-Fe3O4 were mainly inaccordance with the pseudo-second-order kinetics model, and Langmuir model. Thermodynamic studies showed that the adsorption process of MG onto nano-Fe3O4 was an endothermic process with spontaneous. The adsorption rate can reach more than 70% after reuse for 4 times.
Key words: citrus reticulata peels; green synthesis; nano-Fe3O4; malachite green; adsorption
收稿日期:2024-01-13
基金项目:国家自然科学基金项目(21771165);河南省科技攻关基金资助项目(222102310285);郑州航院研究生教育创新计划基金项目(2023CX73)
作者简介:张梦凡,河南焦作人,硕士,研究方向为环境功能材料制备及应用。
∗通讯作者:李春光,河南确山人,教授,博士,研究方向为环境污染治理技术及材料研发。

