基于可视化的“空气中氧气含量测定”实验的改进与扩展





化学是一门以实验为基础的学科,化学实验是重要的组成部分,它不仅是洞察自然界的窗口,也是化学学习与科学探究的基本方式。本篇文章主要针对人教版“空气中氧气含量测定”的实验进行改进,该实验在教师演示过程中效果不佳,步骤繁杂,以及产物五氧化二磷会造成空气污染。现以焦性没食子酸的碱性溶液替代红磷进行氧气含量测定,可以弥补教材实验的不足,且该实验还迁移至常规气体制备与喷泉现象相关的实验。这符合新课标的要求,重视开展以化学实验为主的多种探究活动,用以激发学生的学习兴趣,培养他们的创新精神和实践能力。
人教版的教材在九年级上册出现有关于空气中氧气含量的测定的实验,是初中第一个定量实验,该实验能引导学生初步了解测定混合物中某物质的一般思路和方法,从化学视角研究物质。本实验的教学目标是通过设计实验,从实验现象中获取证据,基于证据得出空气中氧气约占1/5体积的结论,进一步得出空气是一种混合物。在教学过程中,教师引导学生观察实验现象,通过实验现象,进一步感受像空气这种无形的物质的存在,与此同时引入纯净物和混合物的概念,认识空气的组成并进一步了解空气的组成。
一、教材的实验设计
(一)教材的装置和原理
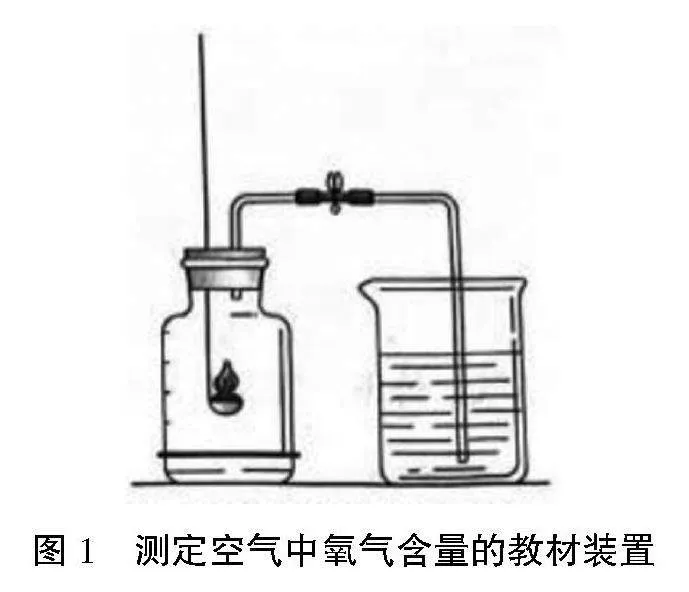
人教版中有关于图1的实验操作步骤如下:第一步:在大小合适的集气瓶内加入少量水,并将水面上方做上标记空间分为5等份。用止水夹夹紧胶皮管,防止漏气,在集气瓶口把燃烧匙内的红磷点燃后,迅速伸入集气瓶中并把橡胶塞塞紧,防止漏气,观察集气瓶内红磷燃烧的现象并记录。红磷熄灭后等待其冷却,打开止水夹,仔细观察集气瓶中的实验现象以及水位的变化情况。由实验现象可以得出结论:氧气约占空气体积的1/5,且空气的组成不是只有氧气,还有其他组成成分。
■
图1 测定空气中氧气含量的教材装置
(二)教材实验的不足
1.红磷燃烧的产物五氧化二磷有毒,反应开始时需要在外部点燃红磷再立即伸入瓶中,不可避免白烟逸出,污染空气。具有毒性的白烟在被人体吸入一定量后就能引起中毒。此外,实验的操作环境要求也比较高,需借助通风橱来操作实验,所以在教室演示实验不方便,也不安全。有将红磷改为白磷,并借助激光或放大镜聚光引燃白磷的设计方案,但白磷的毒性更强,能自燃,现在大多实验室都不采购,该方法不宜推广。
2.燃烧结束后冷却的时间较长,对于正常的教学秩序也会受影响。
3.实验操作步骤不仅多而且杂,再者对装置的气密性要求高,装置气密性不好或操作不当都可能导致实验失败或产生较大误差。
二、实验改进
(一)实验器材以及药品
图2为塑料洗瓶、橡胶管、玻璃导管、弹簧夹、烧杯、纸槽、焦性没食子酸、氢氧化钠溶液、蒸馏水等。
■
图2
(二)实验原理
实验利用焦性没食子酸碱性溶液来吸收空气中的氧气,引起密闭容器内气体压强减小,烧杯中的水被吸入容器内,吸入水的体积等于消耗氧气的体积。根据教材实验装置上对气密性存在的不足,在装置上寻找替代的装置,在装置上把常规的利用双孔橡胶塞活塞塞紧于集气瓶中用以测定空气中氧气含量的装置替换成塑料材质的洗气瓶,洗气瓶都带有尖嘴部分,可以直接与橡胶管连接,而洗气瓶的螺旋纹的瓶塞口保证了装置瓶口的气密性。
(三)实验过程
■
图3
■
图4
■
图5
(1)如图3所示,往本身就有标记刻度的塑料洗瓶内加入约50 mL10%的氢氧化钠溶液和约3 g的焦性没食子酸粉末,关闭止水夹,盖上瓶盖并旋紧。
(2)如图4所示,不断振荡塑料洗瓶,直至不再发生更大程度形变且等溶液冷却到室温时,将导管插入装有不少于200 mL水的烧杯中。
(3)如图5所示,打开止水夹,烧杯中的水吸入塑料洗瓶中,记录液面上升的位置,根据进入的水的液面上升的体积计算相对于空气体积的占比。
实验数据处理:利用公式O2%=■×100%可估算出氧气相对于空气的占比。
(四)数据分析
实验按照步骤进行操作,按顺序加入约3 g焦性没食子酸和50 mL10%的氢氧化钠溶液,关闭止水夹以及旋紧塑料瓶塞,观察读数作为V1,此时可以得出装置中的空气含量为瓶身的总体积525 mL减去V1,下一步震荡塑料瓶约为1分钟后冷却至室温,打开止水夹,等液面上升到不再上升时观察读数,作为V2,此时可以通过V2-V1得出氧气的体积,利用公式O2%=■×100%进行计算,实验平行操作3次,最终取平均值。具体数值从表1可以看到每次的实验数据都是接近21%,而且对于教师在课堂上进行读数和计算都方便。
表1 实验数据
■
(五)焦性没食子酸碱性溶液对氧气的吸收率
试剂方面选用焦性没食子酸用作药品主要基于其在常温下容易被氧化,特别是在碱性溶液中,对氧气的吸收率很高。焦性没食子酸是一种白色固体,易被氧化,也是一种多取代的芳基化合物,分子式为C6H6O3,常应用于制备金属胶状溶液,皮革着色,毛皮毛发等的染色,蚀刻等;并可用作电影胶片的显影剂、红外线照相热敏剂;在医疗中以及染料使用制备过程中常被用作中间体以及分析用试剂等。在可视化的仪器选择方面,优选传感器技术来进行实验过程中的实时观测。在探究物质的性质及其变化的过程中经常遇到反应无明显现象的情况,如吸收氧气的过程、酸与碱的反应等,我们应该结合化学学科的发展趋势扬长避短,结合现有的更新的现代技术进行课堂展示。现代科学希望在教学中能够更加直观地让学生感知实验过程中看不见摸不着的有关于气体的吸收过程视觉化,所以我们准备使用传感器。传感器技术是一种与实验以及科学相关的实用技术,为了进一步说明焦性没食子酸对氧气的吸收率,采用氧气传感器对氧气含量进行检测与实时监控数据变化。自动测量氧气浓度需要一个完全集成的氧气传感系统,该系统通常是由一个探头、一个控制器和计算机接口组成,操作过程中可以实时观察到有关于氧气浓度和时间的曲线变化。在这个过程中通过曲线上数据连续变化的测量,使实验过程从看不见摸不着的观察状态变为可观测的状态。有了质的飞跃,从“定性”分析,走向“定量”分析。有关于以“空气中氧气含量测定”的实验为教学主题的内容,进行可视化的传感器技术的有效探究,有利于学生的发展,且能够激发学生对实验的兴趣。利用这个手段进行定量分析,从侧面说明此实验准确率高的原因。为了使实验结果简明直观,我们会以图像的形式进行呈现,引导学生结合已有的经验和将要经历的社会生活来学习化学的原理和方法,形成化学学科的核心观念。如图6和图7,图6是氧气传感器在检测塑料瓶中氧气的含量的片段截取,横坐标为时间,纵坐标为氧气含量;图7是3组平行数据中第1组最终氧气含量的显示数值。此过程中,学生可以直观地看到氧气浓度的下降,以及最终用焦性没食子酸消耗氧气的余量为1.3%。我们通过这个数值也可以知道焦性没食子酸碱性溶液用来吸收空气中的氧气含量精确度高。
■
图6 图7
(六)实验拓展与迁移
1.本实验的装置气密性良好可以作为常用气体的制备,如氢气、二氧化碳、氧气等。
2.在洗气瓶的内部安装一根玻璃导管就可以改装成喷泉实验装置,如图8。
■
图8
三、本实验改进的优点
(一)实验装置简单、直观
本实验所需的实验装置是实验室常见的仪器装置,便于取用,不需要再进行复杂的加工和连接组装。对老师来说操作起来方便而且可以反复使用,便于提高课堂效率;对学生来说也便于开展分组实验,实验的使用率会高。学生参与实验的意识也会增强,利于激发兴趣。
(二)实验操作便捷
本实验操作简单,洗气瓶本身自带刻度,无需提前做标记,也无需加热,更加节约能源,也不用考虑操作过程中燃烧匙伸入快或者慢的问题,只需加药品后进行震荡冷却后即可进行读数,得出数据以及结论,与此同时能为学生检验化学理论,验证化学实验提供实验事实证据。
(三)实验误差小,更精准
实验所利用的焦性没食子酸对于氧气的吸收率很高,放热也少,恢复至室温也快,在测定数据方面有很大的优势,测得的数据误差小,更精准,在教学过程中也便于分析。
(四)实验的拓展应用范围广
塑料洗瓶耐酸耐碱,且带螺旋纹的塑料塞让整套装置在使用过程中基本保持良好的气密性,在常见气体的制备中可以经常使用,也可改造成喷泉实验,视觉上更为直观,应用更为广泛。
(作者单位:福建省厦门集美中学)
编辑:曾彦慧

