低温等离子下声门上成形术治疗婴幼儿喉软化症的效果
乾恩乐,姜岚,任红波,王晓东
(郑州大学附属儿童医院/河南省儿童医院郑州儿童医院 耳鼻咽喉头颈外科,河南 郑州 450018)
喉软化症(laryngomalacia)是一种常见的先天性疾病,临床表现以吸气性喉鸣为主,是新生儿及婴幼儿喉鸣的主要原因[1-2]。根据吸气性喉鸣的程度,分为轻、中、重度,对于轻、中度喉软化症患者无需手术也可通过保守治疗自愈[3-4]。重度喉软化症患儿表现为较严重的呼吸困难、睡眠质量不佳、喂养困难、发育迟缓,同时伴有反复的呼吸道感染,阻碍婴幼儿的生长发育,使婴幼儿的生存质量降低[5-7]。本文主要研究的低温等离子技术,是已经在喉外科推广使用的一种微创技术,治疗其他喉外科疾病疗效确切[8-10]。低温等离子技术治疗喉软化症的效果在文献中报道较多,但关于低温等离子手术对患儿免疫功能的影响鲜有报道,本文就这一热点问题进行研究,并总结报告如下。
1 对象与方法
1.1 研究对象
研究纳入郑州大学附属儿童医院2018年6月至2022年2月就诊的55例重度喉软化症患儿。其中男32例,女23例;出生时间为30~317 d,年龄(159.63±14.15)d,所有患儿的一般资料差异无统计学意义(见表1)。纳入标准:病历资料完整,随访记录详细,可查找到各项检查结果,包括肝、肾功能,血常规,生化指标等;血液学参数无异常;能够配合医生行喉镜检查;未合并其他系统疾病。排除标准:伴有较严重的气道其他病变,如后鼻孔闭锁、声门下狭窄、喉蹼、喉裂、气管或支气管软化等;早产儿;合并其他严重的先天性疾病,如新生儿肺发育不良、心脏病、神经性综合征、下颌畸形等;伴有严重感染性疾病或免疫功能不全;存在手术禁忌证。按照治疗方式分为等离子组和对照组,低等离子组患儿接受低温等离子下声门上成形术治疗,对照组患儿家长拒绝手术要求保守治疗。等离子组30例,对照组25例。在研究开始前所有患儿家属均由护理人员充分沟通,使家属能够对治疗过程当中的操作流程有所了解,熟记有关注意事项,并能够对相关风险有一个充分的认识,选择治疗方式后签署知情同意书。本研究经医院医学伦理委员会审批通过。
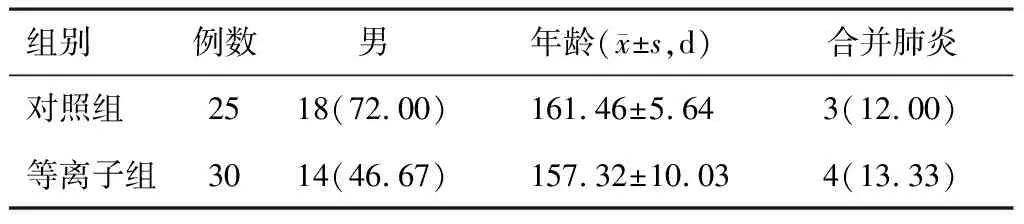
表1 两组患儿基本情况
1.2 研究方法
1.2.1诊断
本研究中诊断重度喉软化症的方法借鉴Roger等标准,主要依据临床表现吸气性喉鸣并伴有以下任意1条者即可诊断:(1)需要干预的发绀及呼吸困难;(2)喂养困难(频繁呛咳、反流、进食中断或需要胃管注食);(3)身高和体重增长迟缓;(4)危及生命的呼吸暂停;(5)因阻塞性窒息行气管插管史;(6)继发漏斗胸,肺动脉高压或肺心病[8-10]。根据喉软化症分型标准,将纳入病例进行分型。Ⅰ型:杓区黏膜过度肥厚脱垂。Ⅱ型:杓会厌襞短缩。Ⅲ型:会厌后移陷入声门。Ⅳ型:混合存在2种及2种以上。
1.2.2手术方法
对于接受手术治疗的等离子组,术前行手术麻醉准备,常规消毒、铺巾、包头,保持患儿头处于正中后仰位。麻醉插管前再次行支气管镜检查,此时保留患儿自主呼吸,并再次确认符合纳入标准。等离子组患儿均接受等离子辅助下声门上成形术,术中使用等离子刀头(型号施乐辉,7071)辅助操作。Ⅰ型:切除多余杓区脱垂黏膜,注意保护杓间区黏膜。Ⅱ型:切除部分杓会厌皱襞,深度达会厌下咽韧带水平,使会厌形态明显显现,增加杓状软骨与会厌间距离,增加会厌抬举幅度及空间。Ⅲ型:等离子烧灼会厌舌面下部2/3黏膜,做点状创面,增加会厌软骨硬度,减少其向声门塌陷,行会厌成形术。Ⅳ型:按照声门上塌陷部位处理。术后将患儿送入ICU,全过程均带气管插管,由医护定时观察和评估患儿情况,达到拔管标准后即可将患儿送回普通病房。
1.2.3保守治疗
对于未接受手术治疗的对照组,给予患儿体位指导及其家属相应的喂养指导等,如增加食物的黏稠度,尽量给予患儿立位时喂液体食物和药物,尽量保持患儿侧卧位睡。若口腔分泌物较多,可取侧卧位,有利于分泌物和呕吐物的引流,同时亦可将患儿置于半卧位,以减少胃食管反流,同时半卧位时也可减轻患儿呼吸困难;口服益生菌及抑酸药物治疗。另外,若患儿出现其他疾病时也应给予相应治疗。
1.3 观察指标
1.3.1观察临床症状相关指标
比较两组患儿呼吸困难、吸气性喉喘鸣、呼吸道感染、喂养困难的发生比例。治愈标准[1]:患儿喉喘鸣、呼吸困难、喂养困难等临床症状完全消失或显著改善,各实验室指标恢复正常;否则视为未治愈。
1.3.2观察体液免疫指标
等离子组手术后1个月及对照组患儿保守治疗1个月后均抽血进行体液免疫功能检查,检查内容包括血清IgG、IgM和补体C3、C4水平,由专人于晨时8点左右采集股静脉血2 mL,收集于干燥管内,标本均于1 h内送检。
1.4 统计学方法
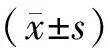
2 结果
2.1 治愈率
等离子组于术后1个月治愈22例,对照组保守治疗1个月后治愈0例,等离子组高于对照组(P<0.01);等离子组于术后3个月治愈30例,治愈率为100.0%,对照组于保守治疗3个月后治愈2例,等离子组高于对照组(P<0.01)。见表2。
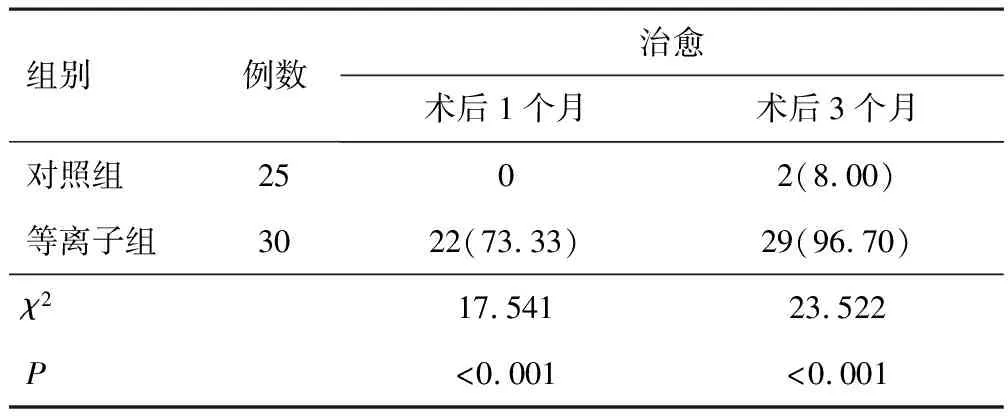
表2 两组患儿治愈率比较[n(%)]
2.2 免疫功能指标
对照组保守治疗1个月后的血清IgG和补体C3、C4水平高于等离子组术后1个月的血清IgG和补体C3、C4水平(P<0.05);对照组血清IgM水平低于等离子组(P>0.05)。见表3。
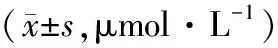
表3 术后1个月两组患儿免疫功能比较
2.3 临床症状相关指标
对照组在保守治疗3个月后,仍有7例出现呼吸困难,17例有吸气性喉喘鸣,14例出现反复呼吸道感染,22例有喂养困难;等离子组在手术3个月后,1例有吸气性喉喘鸣,呼吸困难较前改善,2例出现反复呼吸道感染,2例有喂养困难。等离子组手术后3个月呼吸困难、喉鸣、呼吸道感染、喂养困难的发生率较对照组保守治疗3个月后降低(P<0.05)。见表4。
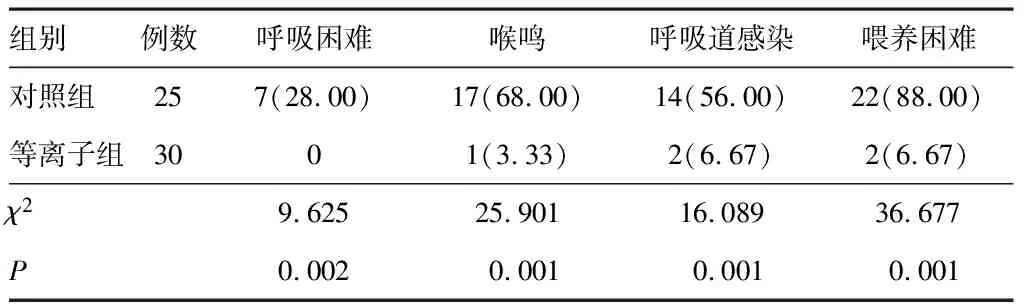
表4 术后3个月两组患儿观察指标比较[n(%)]
3 讨论
喉软化症是一种常见的先天性疾病,临床表现以吸气性喉鸣为主,喉软化症的突出症状为上呼吸道梗阻,出生1个月内会出现上述症状,喉喘鸣平均的发作年龄为2.2周,症状出现的高峰年龄为6~8个月,较为严重者可以提前发病。对于轻、中度的喉软化症患儿,无需手术,可采取留置胃管、吞咽评估并康复、喂养指导、抑酸治疗、体位治疗等保守治疗方式,一般在12~18个月后可自愈,有研究发现喉软化患儿仰卧时喘鸣表现明显,俯卧时减轻或消失[11];对于部分重度的喉软化症患儿,需手术治疗,手术率约16%。重症患儿常伴有较严重的呼吸和喂养困难以及发育迟缓等问题。喉软化的研究历史可以追溯至1897年,Sutherland发现了一种幼儿声门上组织塌陷的疾病,影响患儿生存质量,如何解决声门上组织塌陷的问题一直困扰着医者[12-15]。显微手术在20世纪80年代开始发展和流行,重度喉软化症第一次得到了有效治疗,如1984年报道的杓突成形术联合杓会厌襞切开术,1987年报道的会厌成形术,2002年报道了激光气化黏膜后会厌固定术[16-19]。新型术式的发现为重度喉软化症患儿的治疗打开了希望之窗,重症喉软化症的治愈率得到了有效提高。
本文主要研究的是低温等离子技术,是目前在喉外科采用的一种微创治疗技术,对于其他喉外科疾病有着确切的疗效,低温等离子技术治疗新生儿喉软化症的效果在文献中报道较多,可减少婴幼儿呼吸道感染概率,缓解缺氧症状,从而避免发生免疫功能紊乱状态,但关于对患儿免疫功能的影响鲜有报道。纳入郑州大学附属儿童医院2018年6月至2022年2月就诊的重度喉软化患儿55例,所有患儿的一般资料,差异无统计学意义。按照治疗方式的选择分为等离子组和对照组,等离子组患儿接受低温等离子下声门上成形术治疗,对照组患儿家长拒绝手术要求保守治疗。等离子组与对照组相比,术后1个月,等离子组患儿治愈率为73.33%,而对照组治愈率为0;术后3个月,等离子组患儿治愈率达到96.7%,对照组治愈者为2例,治愈率为8%;术后3个月,等离子组呼吸困难、喉鸣、呼吸道感染、喂养困难的发生率较对照组低。可见,等离子组的治愈率和患儿恢复情况优于对照组,治疗重度喉软化的效果确切,本研究结果与国外以往研究结果[20-21]相似。因此,诊断为重症喉软症患儿,应尽早接受手术治疗,低温等离子技术辅助下声门上成形术为首选。另外,低温等离子技术优点多,如术中出血少,切割损伤小,并发症少,且刀头的前段可以弯曲,便于术者调节手术角度,可广泛应用于重度喉软化症患儿。
婴幼儿由于免疫器官尚未发育完全,其免疫功能尚未完善,特异性免疫力较低下,出生后1个月婴幼儿的免疫力才能相对增高[22]。出生时通过母体胎盘输入可获得的免疫球蛋白IgG,对患儿起到保护作用,正常婴幼儿IgG水平会随着月龄增加而减少,且IgA、IgM、 C3、C4水平较低,但在感染情况下接触强抗原刺激后IgA、IgM、C3、C4水平上升,出现免疫功能紊乱状态。本研究中,等离子组患儿接受手术后1个月时,对等离子组和对照组患儿均进行血清免疫功能检查,结果显示接受保守治疗的重度喉软化症患者IgG和补体C3、C4水平较高,差异有统计学意义,说明接受低温等离子技术治疗的患儿免疫功能处于正常水平,而保守治疗的患儿免疫功能处于紊乱状态,因此对于重度喉软化患儿,保守治疗效果不佳尽早选择手术治疗,以避免发生免疫功能紊乱状态。
4 结论
低温等离子技术能够较高效地治愈重度喉软化症患儿,且属于微创手术,患儿恢复快,同时并发症少,联合血清免疫球蛋白以及补体C3、C4检测可评估重度喉软化患者的免疫功能恢复情况,建议尝试临床推广使用。本研究存在的局限性,纳入病例数较少,免疫功能监测随访时间较短,计划未来纳入更多病例,对喉软化症患儿的免疫功能的发展变化进行更加深入的研究,以及进行长期的随访。

