原理题的命题特点与复习备考策略
王 丽
(广州市玉岩中学,广东 广州 510530)
1 试题分析
化学反应原理模块涵盖了高中化学的基本原理,是发展微粒观、变化观、平衡观、守恒观等核心素养的良好载体.原理题是基于生产实际,考查了学生基于基本原理分析反应过程,进行反应调控等问题解决能力,是高考化学的必考题型.
1.1 考查形式
原理题的情境多以工业生产、废气利用等气态多反应体系为主,引导学生关注与化学有关的社会问题,培养学生的社会责任感[1].题目信息常以“文字+图像”的形式呈现,其中图像包含平衡体系中物质变化曲线和装置图等,以此体现学生多种形式信息的阅读、获取和分析能力.
1.2 考查内容
从考查内容上来看,主要包含了“反应热”“反应速率、反应限度与反应方向”“水溶液中的离子平衡”“电化学”四部分内容.设问方式有反应热的计算、平衡状态的判断、反应速率大小对比和计算、平衡移动方向和原因分析、反应条件控制、反应方向判断、平衡状态计算、各种类型平衡常数的计算和电极反应式书写等.有对反应速率、平衡状态和平衡移动的定性分析,更有对基本原理的定量分析,如平衡时转化率、平衡常数的计算.
1.3 考查能力
在关键能力方面,主要侧重于信息获取、情境转化和逻辑推理能力,能从文字和图像中获取关键信息,基于核心知识体系和方法体系进行情境转化,匹配问题解决模型,熟练应用归纳、演绎和归因等逻辑论证方法,实现问题的解决.在问题解决的过程中,重点考查了“证据推理与模型认识”“变化观念与平衡思想”,同时也落实了“科学探究与创新意识”和“科学态度与社会责任”的培养.
2 备考策略
新的高考评价体系指出,高考命题理念从知识立意、能力立意向价值引领、素养导向、能力为重、知识为基转变,题目的呈现具有基础性、综合性、应用性、创新性.据此提出原理题“关联经典试题,建立常规题型方法体系”的备考建议,供大家参考.
反应原理这一模块的考查更加注重应用性和综合性,根据试题呈现,结合模块知识的特征,原理题的设问有3种类型(表1):基于概念的理解辨识、基于原理的定性分析和基于原理的定量计算.

表1 原理题常规题型及方法体系
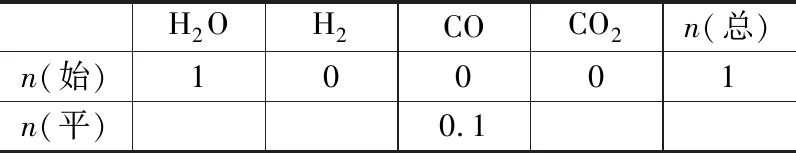
表2 守恒法物质的量分析表(初表)
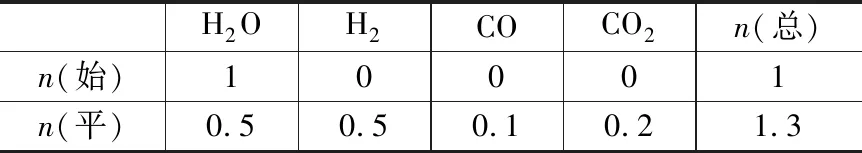
表3 守恒法物质的量分析表(完整)
本文重点讨论定量型设问方法体系的建立.
原理题中的计算题不管是转化率还是平衡常数的计算,是逻辑推理能力体现,依据求算的定义式,通过三段式或守恒法来找数据并代入计算,找数据是解题的关键.在复习时,可引导学生形成“三段式”和“守恒法”数据推理框架,突破找数据的难点,建立定量的基本方法体系.
2.1 三段式法
以2022年湖南卷的Kp计算为例,展示以定义式为出发点的计算过程(如图3).

图3 三段式解题模型
在进行多反应三段式计算时,习惯上在“在其中一个反应充分反应后,再进行第二个反应”的假设下,使用极限值的思维,2个反应单独列三段式.这与学生“2个反应不是同时进行”的认知相互冲突.在实际的反应体系中,反应1和2是同时进行的.
在单一反应三段式的基础上,笔者采用“多反应合并三段式”,综合考虑了多个反应进行合并数据处理,将原三段式进阶为总体系三段式,更加符合反应实际.“三段”分别为“体系的起始总投料量”“反应的总转化量”“体系的总平衡量”.具体解题过程如图4.

图4 总体系三段式解题模型
2.2 守恒法
三段式是常规找数据的方式,对于一些复杂的反应情境,可使用“守恒法”进行数据处理.“守恒法”是利用反应前后元素质量守恒的简化计算方法,在计算过程中,只需要关注反应的起始状态和平衡状态原子数目的变化情况,降低了多反应体系计算的难度,具体解题步骤如下.
步骤一:列出体系起始和平衡状态物质的量表;
步骤二:根据元素质量守恒和题示信息,列出信息关系式和守恒关系式,联立方程求算其他未知量;
守恒关系式:
氢原子守恒2n(H2O)+2n(H2)=2 mol
氧原子守恒n(H2O)+n(CO)+2n(CO2)=1 mol
题干信息:n(H2O)=0.5mol,n(CO)=0.1mol
求得:n(H2)=0.5mol,n(CO2)=0.2
步骤三:补充物质的量表;
另外,在《高中化学选择性必修1(2020版)》中,新增了方法指引栏目.归纳出了“图像分析”“定性分析与定量分析”“电解质溶液中的电荷守恒与元素质量守恒”“化学方程式中的变化与守恒”“电化学过程的系统思想与方法”等,这些都是解决化学问题的重要方法体系,值得师生重点研究.
3 结束语
化学不仅改善了人类的生活,给生活带来极大的便利,也是人类利用自然资源和解决环境问题的科学依据.在复习中,素材体现化学的应用价值,呈现在绿色化学思想和循环经济原则下的科学、安全、有效自然资源利用过程,帮学生树立对化学学科的正确认识.

