BCR-ABL 融合基因检测在慢性粒细胞白血病诊断中的价值
郭 竑,林 江,马吉春,刘嫣方,闻向梅,钱 军
(江苏大学附属人民医院中心实验室,江苏 镇江 212000)
血液肿瘤已成为高度危及人类生命的疾病,如急/慢性淋巴细胞白血病、急/慢性髓系白血病等。其中,血液系统骨髓增殖性肿瘤(MPN)在血液系统疾病中占据较高发病比例,MPN 为造血干细胞克隆增生性疾病,根据诊断标准,粒红巨三系呈现不同程度的增生,分为慢性粒细胞白血病、慢性中性粒细胞白血病、真性红细胞增多症、原发性骨髓纤维化、原发性血小板增多症、慢性嗜酸性粒细胞白血病、肥大细胞增生症和无法分类的MPN[1],而临床上以慢性粒细胞白血病(CML)、真性红细胞增多症(PV)和原发性血小板增多症(ET)居多,本研究针对这三种类型的MPN 进行研究。其中,CML为起源于多能干细胞的恶性克隆增殖性疾病[2]。通过对BCR-ABL融合基因进行定量检测,实现对CML 各个病程(慢性期、加速期与急变期)的监测,使BCR-ABL融合基因成为一个有价值的指标,为进一步临床用药提供指导依据[3]。
1 资料与方法
1.1 研究对象
收集2016 年1 月至2022 年6 月期间,江苏大学附属人民医院的96 例MPN 患者标本。其中,包含59 例CML患者(初发30例,加速期和急变期11例,缓解18例),37 例非CML 骨髓增殖性肿瘤患者(PV16 例和ET21 例),所有患者均已确诊。本研究经江苏大学附属人民医院伦理委员会批准。患者一般资料见表1。
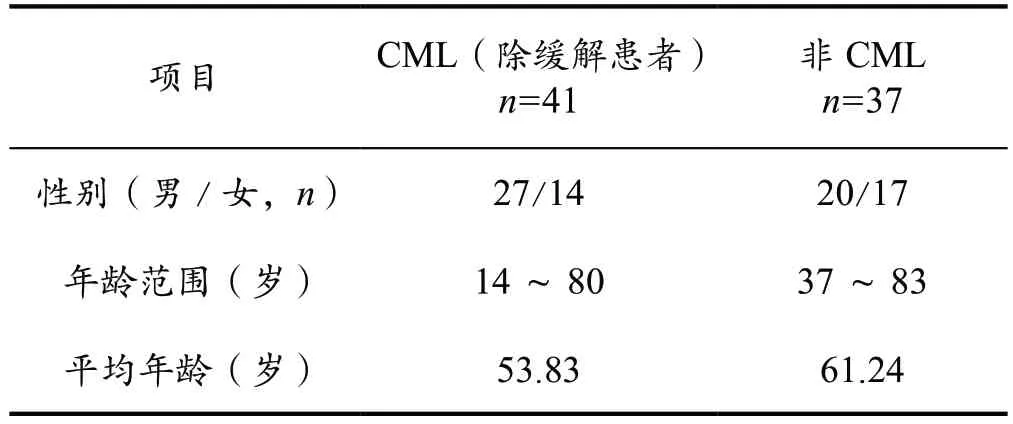
表1 CML(除缓解患者)与非CML 患者性别及年龄参数
1.2 方法
1.2.1BCR-ABL定量检测
进行BCR-ABL融合基因定量检测,留取骨髓或者外周血(5 mL),应用实时荧光定量PCR 方法,试剂为上海源奇生物医药科技有限公司提供,仪器名称和型号为ABI 7500。
1.2.2 统计学处理
统计学处理和图形分析采用Graphpad Prism 7.00 和SPSS 24.0。组间分类变量的差异采用Fisher's 确切检验和卡方检验;组间连续变量的差异则采用Mann-Whitney U 检验。以P<0.05(双侧分布)为差异具统计学意义。
2 结果
2.1 CML 初发患者与非CML 的MPN 患者对比
在CML 初发患者中,BCR-ABL融合基因水平均值为167.93%,结果均为阳性;而非CML 的MPN 患者其BCR-ABL融合基因均为阴性。
2.2 比较CML 患者各个病程中BCR-ABL 融合基因的水平
30 例初发CML 患者,与11 例加速期和急变期的患者的标本进行BCR-ABL融合基因水平及临床参数的比较(见表2),结果显示在白细胞计数、血红蛋白含量和血小板计数中,CML 初发患者与加速期和急变期的患者间差异具统计学意义,P值分别为0.046、0.039 和0.001(见图1、图2 和图3),而BCR-ABL融合基因水平差异无统计学意义。结果表明当病程发生进展,处于加速期与急变期时,患者BCR-ABL融合基因水平增高,但与未治疗的初发患者水平无明显差异。
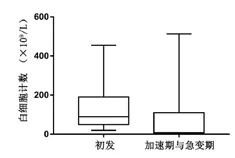
图1 CML 初发患者和加速期与急变期患者的白细胞计数
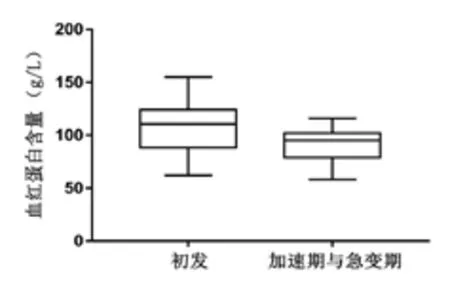
图2 CML 初发患者和加速期与急变期患者的血红蛋白含量
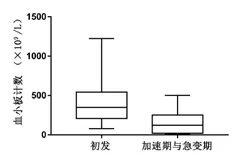
图3 CML 初发患者和加速期与急变期患者的血小板计数
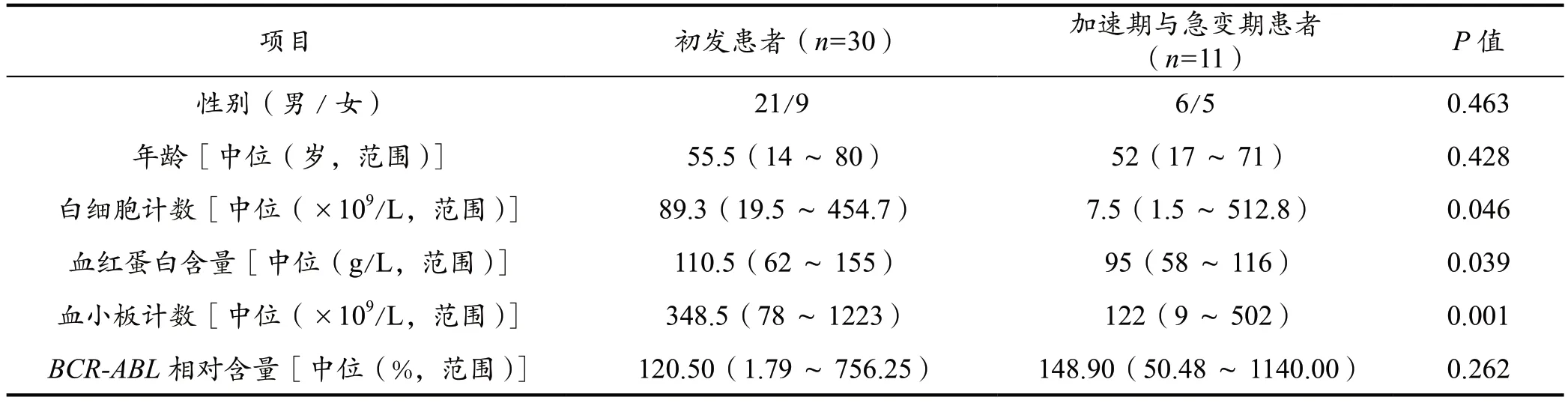
表2 CML 初发患者与加速期和急变期患者BCR-ABL 融合基因水平及临床参数
2.3 CML 初发与缓解后患者BCR-ABL 融合基因水平的变化
分别检测18 组CML 初发与缓解后患者的BCR-ABL融合基因水平(见表3),结果表明差异具有统计学意义(P<0.0001),证实BCR-ABL融合基因水平对于疾病的诊断及监测是一个较好指标,见图4。
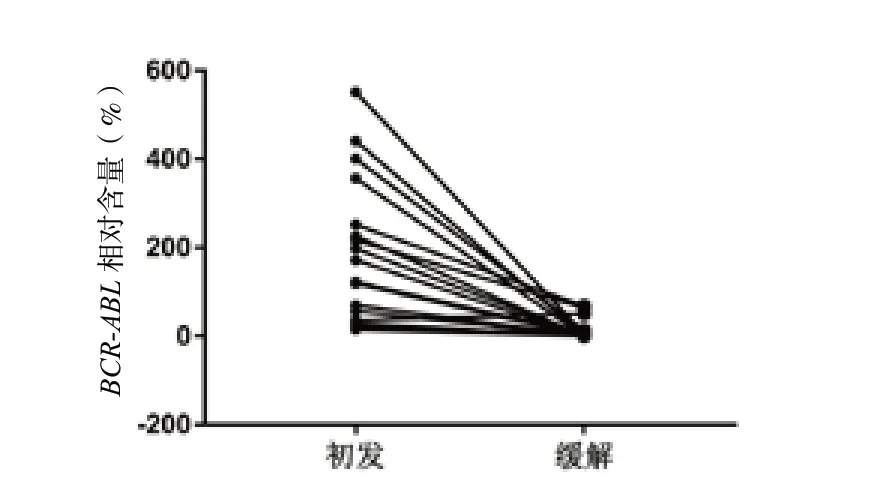
图4 CML 患者中初发患者及缓解后患者的BCR-ABL 融合基因相对含量
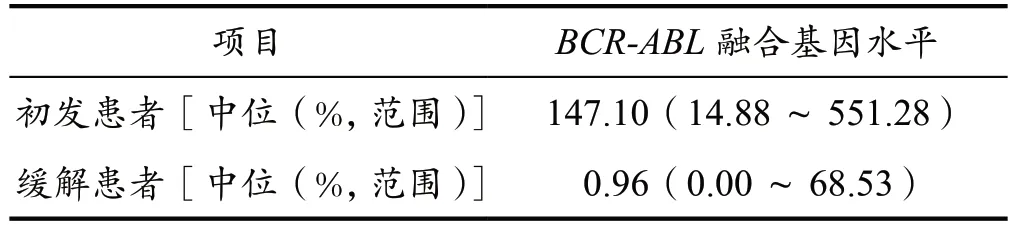
表3 18 组CML 初发与缓解后患者的BCR-ABL 融合基因相对含量水平
3 讨论
MPN 在临床上常见类型为CML、PV 及ET,PV 和ET 治疗的主要目的是预防血栓出血并发症。对其早期诊断,可将疾病控制在低风险层,有效阻止疾病进程。Tefferi A 等人证实在PV 和ET 患者的血栓形成风险分层中,骨髓虽有不同程度增生,但均不出现BCR-ABL融合基因改变[4]。Lu T 等人证实酪氨酸激酶由BCR-ABL融合蛋白激活,是CML 驱动因子,其阳性见于大多数CML患者中[5]。因此本研究通过对BCR-ABL融合基因的检测,证实了该基因在PV及ET增生性疾病中其水平均为阴性,提高了MPN 诊断率。
CML 常伴有染色体t(9;22)易位[6]。在起病初期,部分Ph 染色体发生隐匿性易位,约5%的Ph 染色体出现阴性状态[7],而BCR-ABL融合基因检测灵敏度高于染色体,因此其在CML 的发病机制中起着重要作用。这种异常信号的激活,导致细胞不受控制增殖,如果未实施有效干预,病程将从慢性期向加速期与急变期发展[8]。
本研究结果表明,在CML 患者中,随着病程发展,经治疗缓解后,BCR-ABL融合基因水平明显下调,而病程处于加速期与急变期时,其水平又明显增高,与未治疗的初发患者水平相当。Zhang XS 等人也得出同样的结论[9]。诊断明确后及时进行靶向药物治疗,使用酪氨酸激酶抑制剂(TKI)治疗CML,是现代靶向治疗的规范用药。重要的是,通过对BCR-ABL融合基因水平进行监测,来评估治疗有效性和量化,是目前监测CML 的主要决定因素[10]。部分患者经靶向药物治疗后BCR-ABL融合基因水平明显下调,经TKI 治疗,CML 的患者进展到加速期或急变期的百分比从每年20%以上降至1%至1.5%[11],国际血液骨髓移植研究中心同样建议使用实时定量聚合酶链反应定期监测BCR-ABL融合基因水平,对CML 病程监测及用药是一个较好的诊疗指标[12]。
BCR-ABL融合基因可以对MPN 类型做鉴别诊断,并对CML 病程进行监测,是一个有价值的指标,可为进一步临床用药提供指导依据。

