高岭土制备聚氯化铝的实验研究
王 焜,廖秋实,肖林波,田承涛,孟 洋,黄 琴,张芷紫,刘燕琴
(1.湖北三宁化工股份有限公司,湖北 枝江 443206;2.宜昌市磷资源循环利用重点实验室,湖北 枝江 443206)
随着工业的迅速发展以及人们消费能力的不断提高,产生的废弃物量也日益增多[1-2]。聚氯化铝(PAC)是一种含有羟基的多核无机高分子高效混凝剂[3],市场需求量巨大[4]。高岭土中的铝含量很高,因此可作为铝源而应用于絮凝剂的制备。目前,以高岭土为主要原料制备的絮凝剂,主要有聚硅酸铝铁、聚硫酸铝铁、聚合氯化铝、聚氯化铝铁等无机高分子絮凝剂。天然高岭土的结构稳定,反应活性很低,以它为原料提取硅铝活性成分时,必须进行活化处理。高岭土的改性方法主要有机械粉碎法、煅烧改性[5]、酸碱改性[6-7]等。
根据生产原料的不同,制备PAC 的方法可分为4 大类,即金属铝法、氢氧化铝法、氯化铝法和含铝矿物法[8]。本文采用直接酸浸高岭土[9]的方法,提取煤系高岭土中的活性成分,用于制备聚合氯化铝絮凝剂。絮凝的作用机理主要有压缩双电层与电中和作用、高分子絮凝剂的吸附架桥作用和絮体的卷扫沉淀机理。在絮凝过程中,胶体颗粒失去稳定,小的悬浮粒通过各种作用絮凝成较大的颗粒,在液体中沉降下来[10]。
1 实验部分
1.1 原料和仪器设备
高岭土(800℃煅烧)、盐酸(分析纯)。
集热式恒温加热磁力搅拌器、分析天平、循环水式真空泵、电热鼓风干燥箱、500mL 烧杯、温度计(0~120℃)、量筒(100mL)、尾气吸收装置。
1.2 实验原理
高岭土在800℃下煅烧2h,脱掉其中的水分,形成具有一定活性的“脱稳高岭石”[11]。取出冷却后,与一定浓度的盐酸反应,得到的上层透明液体即为高纯聚氯化铝溶液。反应方程式如下:
1.3 实验步骤
准确称取800℃下煅烧的高岭土50g 于500mL烧杯中,加入一定量的盐酸溶解后,置于500mL 四口烧瓶中,于水浴锅中加热反应一段时间。之后连接尾气吸收装置,用氢氧化钠溶液吸收逸出的酸性气体。反应完成后将溶液过滤,滤液置于烧杯中蒸发浓缩,滤渣用水清洗。收集滤液进行蒸发浓缩,取样分析所得固体中的Al2O3含量。实验装置图见图1。

图1 实验装置图
2 实验结果分析
2.1 最佳的反应物浓度
准确称取800℃煅烧的高岭土50g,分别置于编号为①~⑤的300mL 烧杯中,加入200g、浓度分别为16%、18%、20%、22%、25%的盐酸,配置成料浆,置于500mL 四口烧瓶中,于集热式恒温加热磁力搅拌器中水浴加热,升温至90℃反应3h。反应完成后,将溶液于室温下冷却、过滤,滤液于170℃下蒸发浓缩。浓缩得到的晶体即为聚氯化铝固体。取样分析固体中的Al2O3含量,分析结果见表1。

表1 不同盐酸浓度下AlCl3的分析结果
图2 是盐酸浓度对AlCl3中Al2O3含量的影响曲线。从图2可以看出,随着盐酸浓度增加,固体产品中Al2O3的含量逐渐上升;盐酸浓度为20%时,产品中的Al2O3含量达到27.2%,已达到国家标准;之后随着盐酸浓度上升,Al2O3含量逐渐降低。原因是高浓度的盐酸溶液会使氯化铝溶液中的有效成分酸解,进而降低了Al2O3的含量。综合考虑确定最佳的盐酸浓度为20%。
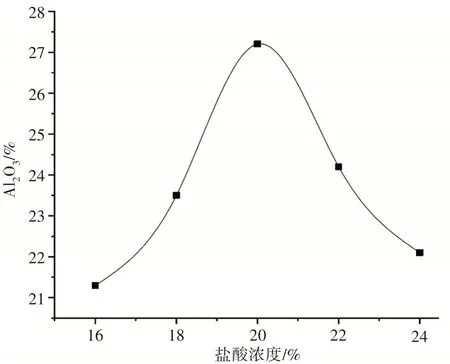
图2 盐酸浓度对AlCl3中Al2O3含量的影响曲线
2.2 最佳反应时间
准确称取800℃煅烧的高岭土50g,置于编号为①~⑤号的300mL 烧杯中,加入200mL、20%盐酸配成料浆,置于500mL 四口烧瓶中,于集热式恒温加热磁力搅拌器中水浴加热,升温至90℃,分别反应90min、120min、150min、180min、210min。反应完成后,将溶液于室温下冷却并过滤,将滤液于170℃下蒸发浓缩,得到的晶体即为聚氯化铝固体。取样分析固体中的Al2O3含量,结果见表2。

表2 不同反应时间下AlCl3的分析结果
图3 是反应时间对AlCl3中Al2O3含量的影响曲线。从图3可以看出,随着反应时间延长,产品纯度呈先升后降的趋势,180min 时氯化铝中Al2O3含量为27.5%,达到聚氯化铝的国家标准。盐酸对高岭土中的Al2O3分解完全后,继续延长反应时间,水分会大量蒸发,使得溶解的AlCl3重新析出,会在过滤时随滤渣一起被滤出,导致成品有少量损耗。由此确定180min为最佳反应时间。
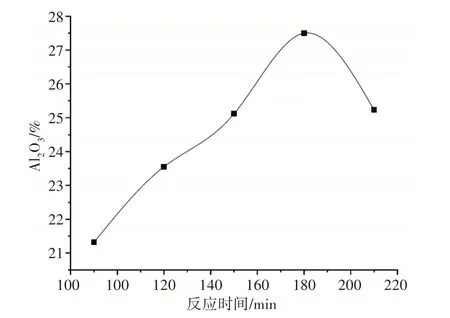
图3 反应时间对AlCl3中Al2O3含量的影响曲线
2.3 最佳反应温度
准确称取800℃煅烧的高岭土50g,置于编号为①~④号的300mL 烧杯中,加入200mL、20%盐酸配成料浆,置于500mL 四口烧瓶中,于集热式恒温加热磁力搅拌器中,分别水浴加热至70℃、80℃、90℃、100℃,反应3h。反应完成后,将溶液于室温下冷却并过滤,滤液于170℃下蒸发浓缩,得到的晶体即为聚氯化铝固体。取样分析固体中的Al2O3含量,结果见表3。

表3 不同反应温度下AlCl3的分析结果
图4 是反应温度对AlCl3中Al2O3含量的影响曲线。从图4 可以看出,随着反应温度升高,AlCl3中的Al2O3含量增加,温度达到90℃时,Al2O3含量达到最高。适当的高温可促进高岭土中的Al2O3与盐酸发生反应,因此确定实验的最佳反应温度为90℃。

图4 反应温度对AlCl3中Al2O3含量的影响曲线
2.4 最佳搅拌速度
准确称取800℃煅烧的高岭土50g,置于编号为①~④号的300mL 烧杯中,加入20%盐酸200g 配成料浆,置于500mL 四口烧瓶中,于集热式恒温加热磁力搅拌器中水浴升温至90℃,控制搅拌速度分别为200、250、300、350r·min-1,反应180min。反应完成后,将溶液于室温下冷却并过滤,滤液于170℃下蒸发浓缩,得到的晶体即为聚氯化铝固体。取样分析固体中的Al2O3含量,分析结果见表4。

表4 不同搅拌转速下AlCl3的分析结果表
图5 是搅拌速度对AlCl3中Al2O3含量的影响曲线。从图5可以看出,随着搅拌速度升高,AlCl3中的Al2O3含量持续增加,转速达到300 r·min-1之后,AlCl3中的Al2O3含量基本保持不变。适当的高转速有助于促进高岭土中的Al2O3溶出,但转动过程中,液体与搅拌桨的碰撞剧烈,反应液容易飞溅,因此确定实验的最佳搅拌速度为300r·min-1。
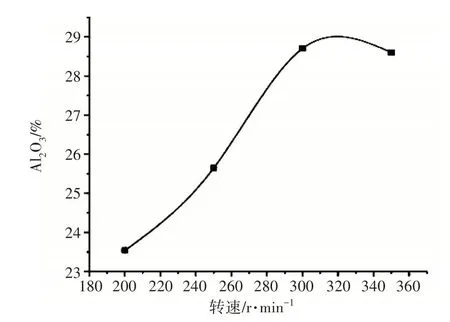
图5 搅拌速度对AlCl3中Al2O3含量的影响曲线
3 结论
本文采用单因素优化法,以轻烧高岭土和盐酸为原料,探究了不同的反应条件对制备的氯化铝溶液中Al2O3含量的影响,得到了最佳的反应条件。随着盐酸浓度升高,氯化铝中的Al2O3含量先升后降;随着反应时间延长,氯化铝中的Al2O3含量呈先升后降的趋势;随着反应温度升高,氯化铝产品中的Al2O3含量增加;随着搅拌速度提高,氯化铝产品的纯度及Al2O3含量逐渐升高。最终得到的最佳反应条件为:800℃下煅烧的高岭土与20%盐酸溶液,按照固液比1∶4,在90℃下以300r·min-1的搅拌速度反应3h。此条件下制备的的氯化铝固体中,Al2O3含量为28%,达到了生活用水的聚氯化铝指标。

