脑膜炎球菌多糖结合疫苗的研究进展
孟清霞,许项可 综述,安文珏,张珂,2 审校
1.华兰生物疫苗股份有限公司,河南 新乡 453003;2.华兰生物工程股份有限公司,河南 新乡 453003
流行性脑脊髓膜炎(简称流脑)是由脑膜炎球菌[学名脑膜炎奈瑟球菌(Neisseria meningitidis,Nm)]感染引起的一种呼吸道传染病,该病传染性强、起病急、病情重,从发现病因至今已有百余年历史,因其发病率和病死率高而备受关注[1-2]。在脑膜炎球菌13个血清群中,引起疾病最主要的血清群为A、B、C、W135、X和Y群[3-6]。
由于脑膜炎球菌荚膜多糖大多具有良好的抗原性,将其提纯制备多糖疫苗,能有效预防流脑[7-8]。但多糖抗原一般属于T 细胞非依赖性抗原,其免疫效果与接种人群年龄相关[9]。因2 岁以内婴幼儿免疫系统未发育完全,接种多糖疫苗后,不能有效激活Th 细胞和记忆性T 细胞,因此不能诱导免疫记忆产生,机体免疫保护时间较短,即使2 次接种也不能加强免疫反应。为解决该问题,研究人员将多糖与载体蛋白制备成多糖结合物原液,再配制成多糖结合疫苗,接种后能刺激B 细胞对多糖产生抗体应答,并促使T细胞产生免疫记忆,从而使B细胞产生更多的特异性抗体[10-12]。
本文就脑膜炎球菌多糖结合疫苗制备的影响因素、多糖与载体蛋白的结合方式、国内外研究以及制备过程中存在的问题进行综述。
1 影响因素
1.1 多糖结构 多糖是由糖苷键结合的糖链组成的碳水化合物。很多研究表明,糖链长度与其抗原性和免疫原性相关[13-14]。结构较长的糖链能够容易形成构象表位,刺激B细胞,从而产生数量较多的抗体;结构较短的糖链易激活T 细胞,使Th 细胞更好地辅助B细胞产生特异性抗体[15]。每种多糖结构不同,糖链长短不一,发生化学反应时,可能有些暴露在外部的位点与蛋白结合,还有些可能自身发生化学反应。
1.2 载体蛋白在制备多糖结合疫苗时,选取的载体蛋白有破伤风类毒素(tetanus toxoid,TT)、白喉类毒素(diphtheria toxoid,DT)、白喉毒素自然突变体CRM-197、脑膜炎球菌外膜蛋白(outer membrane protein,OMP)、流感嗜血杆菌D 蛋白(protein D,PD)等。这些蛋白与多糖按一定比例结合后,能显著提高多糖免疫原性。佟巍等[16]研究结果显示,以TT 及DT 为载体制备的A、C、Y、W135群四价脑膜炎球菌多糖结合疫苗均具有良好的免疫原性,TT略优于DT。
CRM197 为野生型白喉毒素的第52 位甘氨酸突变为谷氨酸的产物,突变后的CRM197保留了T辅助表位且毒性消失。该载体蛋白最早应用于C 群脑膜炎球菌多糖结合疫苗。接种后的结果表明,C 群脑膜炎的发病率在各年龄阶段均降低,表明该疫苗对预防C 群脑膜炎具有显著效果[17]。在近年临床免疫原性研究中,多糖与CRM197 结合后的免疫效果不如TT。JONKER 等[18]研究了在成人体中注射A、C、Y、W135-CRM197和A、C、Y、W135-TT群脑膜炎球菌多糖结合疫苗的安全性和免疫原性,结果显示,注射A、C、Y、W135-TT 群脑膜炎球菌多糖结合疫苗的人群抗体水平更高。
MICOLI 等[19]报道了MeNZB 外膜囊泡(outer membrane vesicle,OMV)疫苗成功控制了新西兰B 型脑膜炎的暴发后,又开发了含有OMV 的4 组分4CMenB,针对B 型菌株脑膜炎球菌提供了更广泛的保护。SEMCHENKO 等[20]在新西兰接种MeNZB 后,不仅降低了B 型脑膜炎的发病率,同时还降低了淋病发病率。研究表明,MeNZBOMV 抗原之间与淋球蛋白具有高度相似的序列。接种MeNZB 后,同时在体内诱导抗淋球菌抗体产生,阻碍了淋病发病。
王丽婵等[21]研究了PD 作为A 群脑膜炎球菌多糖蛋白结合疫苗蛋白载体的免疫效果,发现PD 与A群多糖结合后能增强多糖免疫原性,既可提高体液免疫反应能力,又可激发细胞免疫反应,提示PD 具备作为A群脑膜炎球菌多糖蛋白载体的潜力。
1.3 多糖与蛋白比值 当多糖与蛋白比值较低时,诱导抗体应答的效率也较低,而比值较高时,可能会掩盖部分载体表位,导致反应不充分[22-23]。主要应注意以下几点:①每种多糖与载体蛋白结合时,应有最适比值;②应根据最适比值确定加量;③反应结束后,去除未参与反应物质;④长期存放的多糖结合物可能会部分解离,进而改变多糖与蛋白比值。
2 结合方式
目前上市的多糖结合疫苗基本采用化学结合方式,主要的化学反应包括还原胺化、酰胺缩合和硫醚缩合等。多糖与载体蛋白结合最常用的方式为酰胺缩合反应,是利用溴化氰(CNBr)活化多糖,即在碱性条件下CNBr与多糖分子上的邻位顺式羟基(-OH)反应,形成氰酸酯,再与加入的己二酰肼(ADH)反应,氰酸酯中的碳氧键断裂,与ADH 的氨基发生加成反应,将酰肼基团导入多糖分子,形成多糖衍生物。多糖蛋白结合时,在碳二亚胺(EDAC)的催化作用下,连接在多糖分子上ADH 一端的氨基(-NH2)与TT一端的羧基(-COOH)共价结合,形成多糖-蛋白结合物。酰胺缩合反应通过CNBr 活化多糖引入了酰肼基团,该基团比多糖的氨基具有更高的亲核反应性,更易与蛋白分子上的羧基缩合,且由于多糖与蛋白以共价键形式结合,制备的结合疫苗稳定性较高,具有明显的技术优势。
除CNBr活化多糖外,还可采用高碘酸盐氧化[24]。高碘酸盐氧化是采用高碘酸钠(NaIO4)作用于糖上的邻位羟基,将邻位羟基氧化成C=O,同时切断C-C单键。国外使用的活化剂除上述2种试剂,还包括1-氰基-4-(二甲氨基)吡啶四氟硼酸盐(CDAP),在pH为7 ~9时活化多糖羟基[25]。
结合方式除化学结合外,还有生物合成法。疫苗主要通过工程菌株的诱导表达以及一步纯化制备,多糖与蛋白的偶联由细菌自身完成[26]。王磊[27]应用生物合成法“一站式”制备宋内志贺菌多糖蛋白结合疫苗,即利用基因工程手段敲除宋内菌S7 株的O-抗原连接酶基因(waaL)构建S7waaL 表达菌株,将糖基化系统质粒pET28a-PglL-CTB4573C导入表达菌株,经诱导表达后制备CTB-OPS 宋内志贺菌多糖蛋白结合疫苗。结果显示,CTB-OPS 可在S7waaL 内成功表达,经纯化后获得高纯度样品。BALB/c 小鼠免疫试验证明,CTB-OPS 具有约72.5%的保护力。但生物合成法也存在问题,如糖基转移酶的适用性、载体蛋白的选择和优化以及多糖的表达等。
3 国内外现状
3.1 国内现状 我国上市国产流脑多糖结合疫苗见表1,在研国产流脑多糖结合疫苗见表2。国产及国内在研流脑多糖结合疫苗大部分采用酰胺缩合方法制备,即先活化多糖,ADH 为连接剂,在EDAC 催化下共价结合载体蛋白,结合所用活化剂为CNBr,载体蛋白为TT和CRM197。

表1 国内上市流脑多糖结合疫苗Tab.1 Polysaccharide conjugate vaccines of Nm approved in China

表2 国产在研流脑多糖结合疫苗Tab.2 Polysaccharide conjugate vaccines of Nm under development in China
3.2 国外现状 国外流脑多糖结合疫苗上市情况见表3[28-31]。国外流脑多糖结合疫苗上市时间均早于国内,大多数采用还原胺化和酰胺缩合制备,使用的载体也为DT、TT和CRM197。
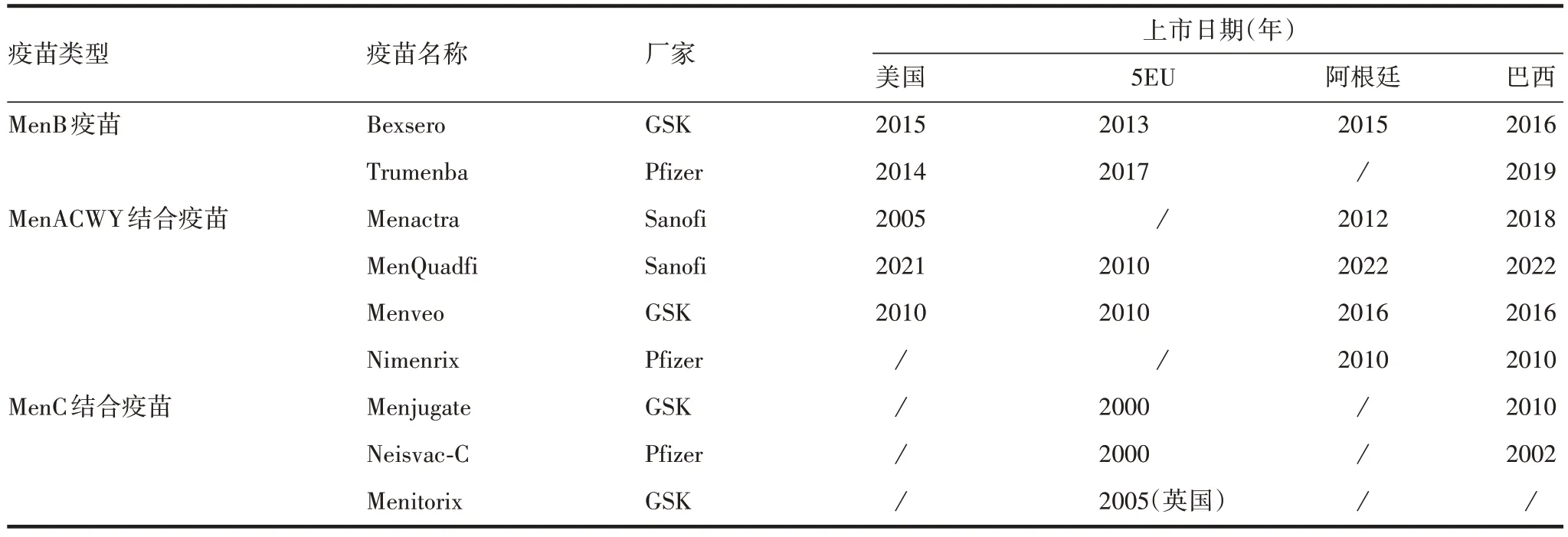
表3 国外上市流脑多糖结合疫苗Tab.3 Polysaccharide conjugate vaccines of Nm in international market
根据GlobalData数据,国外上市的脑膜炎球菌多糖疫苗,除B 群脑膜炎球菌为单群多糖疫苗外,还有MenC 和MenACWY 结合疫苗。葛兰素史克(GSK)研制的Bexsero 疫苗是唯一可用于常规儿童免疫的疫苗。其他大部分脑膜炎球菌疫苗主要来自GSK、辉瑞(Pfizer)和赛诺菲(Sanofi)3 家公司。在大多数国家接种的脑膜炎球菌多糖疫苗或多糖结合疫苗,至少是2个不同种类的疫苗。
四价MenACWY 疫苗主要包括Sanofi 的Menactra、GSK 的Menveo 和Pfizer 的Nimenrix。Sanofi 的Menactra 是美国疫苗市场主要销售的疫苗,目前约占75%的销售额。Menactra 疫苗结合的载体为DT,Menveo疫苗结合的载体蛋白为CRM197,Nimenrix疫苗结合的载体为TT。在流脑暴发初期,Menveo 和Nimenrix疫苗均有免疫效果,但注射Nimenrix疫苗后能产生更高、更持久的抗体。
近两年Sanofi 进行了利用TT 作为载体的Men-Quadfi 疫苗的研制,相较于Menactra 疫苗,会提供更长久的保护。
国外对流脑多糖结合疫苗的研究除A、C、Y、W群,还增加了B 和X 群,见表4。正在研发的五价ABCWY 疫苗均为市场上MenACWY 和MenB 疫苗的组合,分别由GSK 的Menveo 和Bexsero 及Pfizer 的Nimenrix 和Trumenba 组成。GSK 从诺华公司获得了五价候选疫苗(GSK3536819A),至今已完成7 项Ⅱ期临床研究,结果表明,MenABCWY 诱导的抗体水平与Menveo差异较小,且安全性好,可预防多种B群脑膜炎球菌引起的疾病[32];在接种2 剂疫苗后4 年,抗体水平下降,但仍高于接种前水平,4 年后加强免疫可快速提高体内抗体水平[33]。
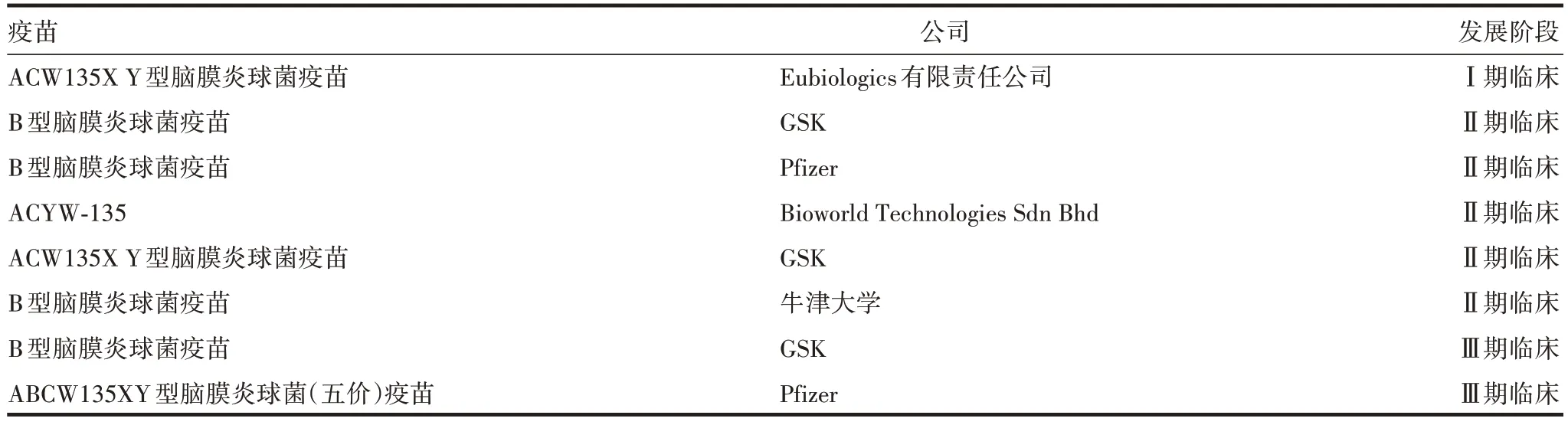
表4 国外部分在研流脑多糖结合疫苗Tab.4 Some foreign polysaccharide conjugate vaccines of Nm under development
Pfizer 公司正在进行MenABCWY 疫苗的Ⅲ期临床研究,预计将成为全球首款五价脑膜炎球菌疫苗。
4 存在问题
随着多糖结合疫苗的应用,流脑的发病率已大大降低[34-37]。我国2015—2019年流脑报告病例540例,年均发病率为0.78/1 000 万[38],2020 和2021 年报告病例分别为50 和63 例[39-40]。但在疫苗生产中仍面临较多问题:在制备方面,涉及超滤、层析、过滤等多步纯化,导致产率较低,生产成本增加,疫苗价格较高,不能在发展中国家和非发达国家普及应用;在产品质量方面,多糖糖链长短不一,每种多糖抗原性不同,多糖与蛋白间的连接位点及数量也不明确,有可能自身发生交联反应,质量控制相对较难;在环保方面,大规模培养致病菌和使用活化剂CNBr 对环境可能造成不可逆改变。因此,虽然多糖结合疫苗已取得了巨大成就,但面临的上述问题仍亟待解决。
5 小结与展望
目前国内主要接种的为脑膜炎球菌多糖疫苗,随着A 群C 群和ACYW135 群脑膜炎球菌多糖结合疫苗的上市,选择结合疫苗,不仅能减少接种次数,还能提供更好、更持久的保护。国际市场上已经从接种MenC 疫苗转向接种多价结合的MenACWY 和MenB 疫苗。随着流脑结合疫苗研究的不断深入,开发多价结合疫苗可能成为以后的趋势。GlobalData数据显示,GSK 和Pfizer 的MenABCWY 疫苗预计在2024年上市。
在疫苗研发过程中,应在充分考虑疫苗生产规模放大、生产工艺变更、产品质量和产品特征指标等基础上,确保变更后工艺对疫苗安全性和有效性不造成影响。除此之外,还应考虑纯化工艺对杂质去除效果以及疫苗主要成分结构的变化[41]。对于结合疫苗,可进行官能团状态和功能的研究分析,如测定从多糖活化开始至多糖/蛋白结合物形成后各步骤的多糖结构,分析每一步多糖结构的变化;测定未结合的活化基团含量;分析多糖与蛋白的结合方式等。
mRNA 疫苗特别是其脂质纳米粒(lipid nanoparticles,LNP)递送功能在开发蛋白、多肽抗原靶抗原疫苗上具有巨大潜力[42]。2022 年9 月29 日,印度尼西亚国家食品药品监管局宣布,授予由云南沃森生物技术股份有限公司和苏州艾博生物科技有限公司2家公司采用生物技术共同研发的mRNA疫苗AW-corna紧急使用授权(Emergency Use Authorization,EUA),用于18 周岁及以上人群通过主动免疫预防新型冠状病毒感染。现有mRNA 疫苗技术虽暂不能直接用于多糖、多糖结合靶抗原疫苗研制,但由于机体内多糖均由具体酶促反应合成,多糖与载体蛋白结合理论上也可借酶促反应实现[43-45]。未来将进一步开发编码多糖合成过程所需各种酶的mRNA 技术、体内直接偶联多糖与载体蛋白的酶,从而一步合成多糖蛋白结合疫苗。

