弱约束条件下氢气含量对甲烷/空气燃爆特性的影响研究
张蓓蓓, 程扬帆,, 夏 煜, 钱家祺, 韦 箫
(1.安徽理工大学 土木建筑学院,安徽 淮南 232001; 2. 安徽理工大学 化学工程学院,安徽 淮南 232001)
甲烷(CH4)是结构最简单的烷烃,在自然界中分布广泛,是天然气、坑气和沼气的主要成分。甲烷具有独特的物理和化学性质,可广泛用于燃料是化工、医疗合成的生产原料。然而,甲烷的燃烧速度较慢,并且甲烷燃烧时会产生大量的氮氧化物,对大气造成严重污染[1]。因此,许多学者为提高燃料的利用效率,提高其应用能力,尝试将氢气与甲烷混合使用,并为此做了大量的试验研究。Di Sarli等[2]开发了大涡模型来模拟富氢/甲烷/空气预混火焰的非定常燃烧,模拟结果表明,非等扩散效应对非定常火焰传播的作用可忽略不计,其主要是由氢富集引起的火焰反应活性增加所决定。Shen等[3]研究了20 L球形容器中氢气/甲烷/空气混合物的爆炸参数,结果表明,随着氢气的添加,混合物中甲烷的可燃性下限和可燃性上限均显著下降,层流火焰速度的变化规律与最大压力上升速率相似,且主要由二元燃料混合物的总当量比控制。Fairweather等[4]研究了氢气/甲烷/空气混合物在湍流环境中的燃烧特性,发现氢的添加通常会导致湍流和层流燃烧速度增加,并降低马克斯坦长度。Yu等[5]研究了氢气和甲烷混合物在矩形管道中的传播行为,研究发现,当氢气体积分数小于50%时,添加氢气可明显提高火焰传播速度,但当氢气体积分数超过50%时,对火焰传播速度的影响较弱。Cao等[6]研究了点火位置对氢气/空气爆炸泄放的影响,结果表明,外部的爆炸促进了内部压力的增长,中部点火时内部压力产生的峰值压力最大,前部点火产生的峰值压力最小,后部点火压力峰值介于两者之间。Hu等[7]研究了氢气/甲烷/空气的层流火焰燃烧特性,结果表明,马克斯坦长度随当量比的增加而增大、随氢分数的增加而减小,并且预混火焰反应区的燃烧速度与H、OH的自由基浓度有很强的相关性。
然而,混合气体燃料具有反应性高、燃烧温度高等特点[8],这使得混合燃料比单一燃料更加危险。混合气体燃料在储运及使用过程当中可能会发生泄漏,在开敞空间与空气形成爆炸云团,因此,研究弱约束条件下可燃气体的燃爆特性对预防气体泄漏发生的爆炸事故具有重要作用。专家学者们在以前的研究中通常采用聚乙烯膜、气泡和乳胶气球作为反应容器测试可燃气体的爆炸风险性,如:Zhou等[9]在1 m3和27 m3的立方体聚乙烯膜中对贫燃料和富燃料的氢气进行燃爆特性测试,可以很直观地观测到气体火焰的传播过程。Kim等[10]在肥皂泡中研究了可燃气体/空气混合物的燃爆特性,可以很明显地观测到火焰的胞格结构,并详细分析了火焰传播过程。Li等[11]选用不同尺寸的透明乳胶气球作为反应容器研究甲烷/空气的燃爆特性,相比较聚乙烯膜和肥皂泡,乳胶气球更加稳定。
本文采用自制的可视化气体爆炸试验设备,以乳胶气球为反应容器模拟弱约束空间,研究弱约束条件下氢气/甲烷/空气预混气体的爆炸火焰温度场、爆炸压力以及火焰传播速度等特征参数;结合试验测试和Chemkin软件模拟结果,详细分析了氢气浓度对甲烷/空气爆炸特性的影响规律。研究结果可为弱约束空间内氢气/甲烷/空气预混气体的意外爆炸防控提供基础数据,也可为其他可燃气体爆炸特性的研究提供试验方法。
1 试验装置和方法
1.1 试验材料及装置
氢气/甲烷/空气预混气体燃爆测试系统如图1所示,主要包括自制可视化等压测试装置、高速相机、示波器、PCB压力传感器和混气罐,甲烷(纯度:≥99.9%)、氢气(纯度:≥99.9%)和空气(体积分数:21%O2+79%N2)均由合肥恒隆电气有限公司提供。首先,使用真空泵将混气罐抽至真空,然后按照道尔顿分压法先后通入甲烷、氢气和空气,静置5 min以确保气体充分混合,随后通过气体体积流量计通入乳胶气球中直至气球半径大约为17 cm。在气球中静置6 min确保预混气体分布均匀,再进行点火,点火电极两端放电距离为2 mm,放电电压为15 kV,采用高速相机(MEMRECAM HX-3)记录预混气体燃爆火焰传播过程,拍摄帧率为5 000 fps,采用2个PCB压力传感器(型号为106B52)记录预混气体燃爆压力,放置在与电极同一高度,并分别距离点火电极1 m和3 m,并通过示波器(HDO4034)进行采集。试验初始温度为298 K,初始压力为101.325 kPa。
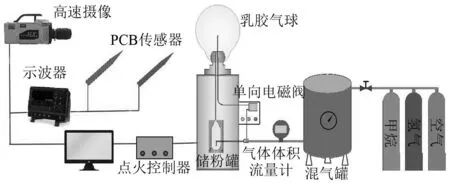
图1 氢气/甲烷/空气预混气体燃爆测试系统Fig.1 Hydrogen/methane/air premixed gas explosion test system
氢气/甲烷/空气预混气体燃爆反应方程式如式(1)所示,其中,可燃气体的当量比控制为1,当改变氢气/甲烷/空气混合物中氢气的百分比时,调整空气浓度以保持当量比恒定。氢气体积分数由式(2)计算
(2)
式中:X为氢气/甲烷/空气混合气体中氢气的体积分数;VH2和VCH4分别为氢气和甲烷的体积。试验工况如表1所示,每组工况进行3次试验,降低试验误差及偶然性。
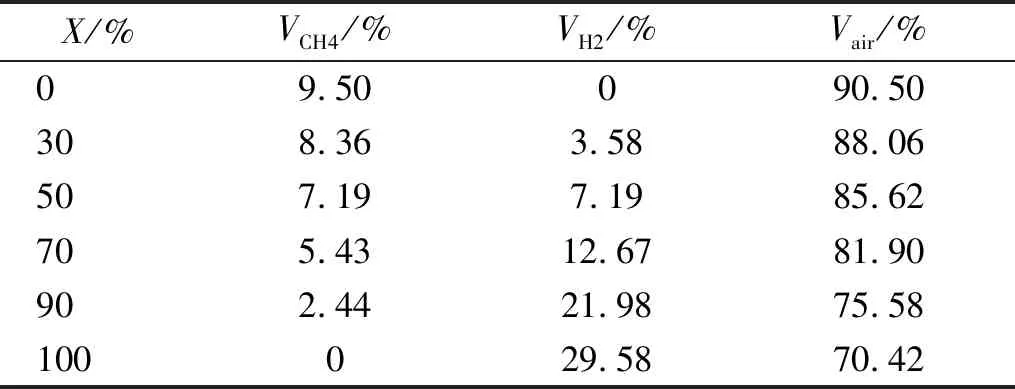
表1 氢气/甲烷/空气预混气体试验工况Tab.1 Test condition of hydrogen/methane/air premixed gas
1.2 比色测温原理及标定
图2中红色、绿色和蓝色分别用R、G和B符号表示,由于每个像素点的绝对R/G/B值无法计算,因此借助两种颜色对应像素的比值得到每个像素的温度[12],其中每个像素的平均R/G比由周围的3×3矩阵计算得出[13]。比色测温方法由钨卤灯(Newport, QTH 50 W)从1 600 K到3 000 K校准,拟合曲线如图3(a)所示,并编写Python代码来计算每个1 080×1 080像素的图片。Python代码主要做了3个工作:首先,对灰色图像进行插值运算,重构出彩色图像;然后根据相关R、G像素值计算各像素点的R/G值,得到温度与R/G值的关系;最后,利用代码的绘图功能对温度场云图分布进行显示。

图2 GRBG模式的拜耳滤波器Fig.2 The Bayer filter of GRBG pattern.
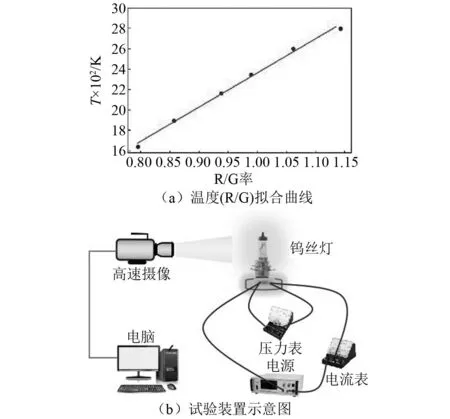
图3 高温钨丝灯标定试验Fig.3 Calibration experiment of high temperature tungsten filament lamp
利用比色测温方法测量预混气体的爆炸温度场,需要先对温度进行标定和校准(如图3(b)所示)。钨丝的温度会随加载电压的变化而规律性改变,试验选用钨丝灯进行温度标定(钨是世界上熔点最高的金属,其熔点高达3 695 K)[14],为避免可见光对结果的影响,标定试验在黑暗环境中进行。温度标定的具体步骤如下:使用高速相机拍摄钨丝灯的发光照片,标定出R/G比值随温度的变化规律,接着采用曲线拟合方法对温度数值的变化规律进行拟合计算,如图3(a)所示,得到修正系数与温度的拟合曲线关系。
2 弱约束条件下氢气添加量的影响
2.1 氢气添加量对火焰温度的影响
温度是评估爆炸输出特性的关键参数,能够反应可燃气体的热毁伤性能和能量释放规律[15]。本研究通过高速摄像捕捉火焰传播图像,并结合比色测温法对混合气体进行温度测量,根据课题组前期的研究工作,与固体物质燃烧不同的是,甲烷和氢气等可燃气体燃烧过程一般不伴随有黑体物质产生,故选用钨粉作为辅助灰体介质(每次试验的钨粉质量为0.2 g,粉尘浓度58.8 g/m3,D50≈4 μm),测量了不同氢气添加量下氢气/甲烷/空气混合气体燃烧火焰动态温度场分布,并与模拟结果进行比较。
不同氢气添加量下氢气/甲烷/空气混合气体燃爆火焰动态温度图,如图4所示。可以看出:在点火初期,受电极点火影响,火焰中心温度较高;氢气的燃烧热值为282 kJ/mol,甲烷的燃烧热值较高(889.5 kJ/mol),从而主导混合气体的燃烧,导致温度的不均匀分布,且高温区域集中在火焰中心位置。在气球破裂前的最后阶段,内部高温区位置上升,这可能是由于氢气相对于空气的密度较低,产生了水蒸气。当X>70%时,由于氢气的热扩散系数远高于甲烷(氢气:0.128 9 W/(m·K),甲烷:0.030 0 W/(m·K)),在火焰膨胀过程中,氢气多集中于外部,并且氢气的含量显著高于甲烷,反应生成的大量水吸收热量转换成水蒸气,导致火焰内部的温度降低,形成了中心温度低、边缘温度高的温度场结构。随着氢气浓度增加,燃烧越激烈,火焰外部的温度就越高。
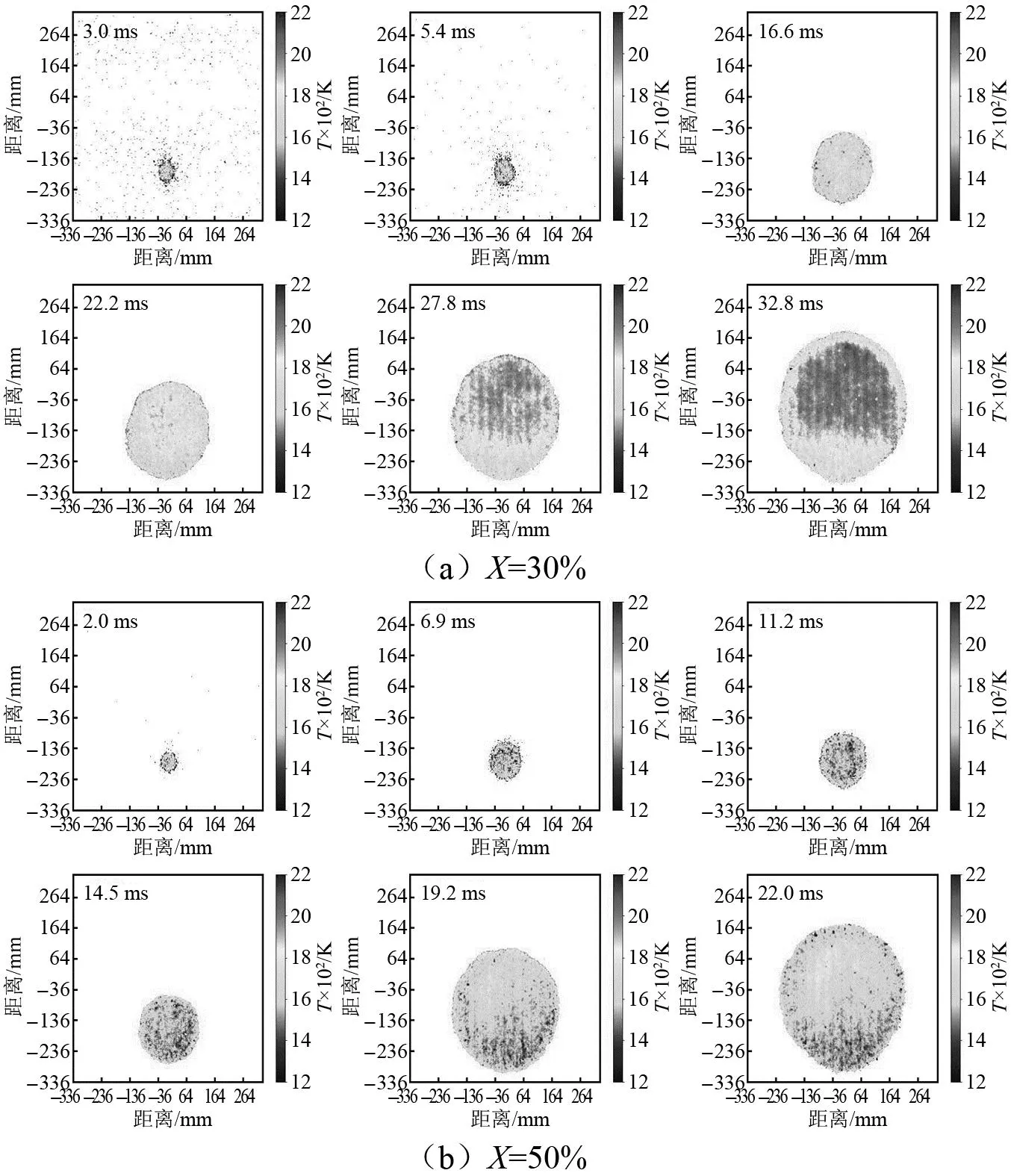
图4 不同氢气添加量下氢气/甲烷/空气混合气体爆燃动态温度Fig.4 Dynamic temperature diagrams of hydrogen/methane/airdeflagration under different hydrogen addition
2.2 氢气添加量对爆炸压力的影响
爆炸压力是衡量可燃气体爆炸毁伤效应的重要指标,能够有效设计建筑物结构及安全距离[16]。图5是不同氢气添加量下甲烷/氢气/空气混合气体的峰值超压和最大压力上升速率柱状图,与纯甲烷/空气混合气体相比[17],氢气/甲烷/空气混合物具有更高的爆炸压力。不同氢气添加量下混合气体的峰值超压值分别为0.424、0.623、0.738、0.765、0.86 kPa,可以看出X=100%时的峰值超压最高,X=30%时最低,并且混合气体的氢含量越高,其峰值超压越大,这是由于氢气在空气中的热扩散率、高反应性和火焰不稳定性的影响,最大压力上升速率也表现出相似的规律[18]。但通过计算发现在X<50%时,混合燃料中氢气含量增加对最大压力上升速率的影响非常显著,提高了11%,此时添加氢气会极大增加混合气体的爆炸威力;当X提高时,氢气在燃料中的作用较小,最大压力上升速率分别增长了7%(X=70%)、5.7%(X=90%)和2.5%(X=100%),因此可以认为最大压力上升速率的敏感性随着X的增加而降低。
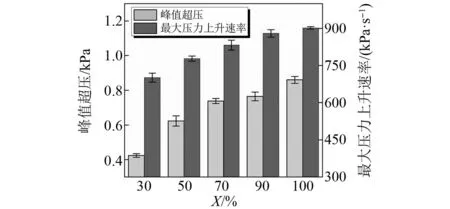
图5 峰值超压和最大压力上升速率参数Fig.5 Peak overpressure and maximum pressure rise rate parameters
为了深入了解自由基相互作用在观察到的现象中的作用,利用Chemkin软件对爆炸压力做敏感性分析(模拟方法:单一反应器模型;反应器模型:等压反应模型;反应机理:GRI-Mech 3.0)[19-20],如图6所示。不同氢气添加量下混合气体的关键基元大致相同,氢气/甲烷/空气爆炸链式反应中关键基元反应如表2所示。可以发现,随着氢气的增加,氧气和甲烷的体积分数减小,氧气、甲烷作为R170、R119和R158中主要的反应物质,其体积分数减小导致R170、R119和R158在爆炸反应中的重要程度降低。R11、R52、R53和R98的敏感性系数为负值,并且随着X的增大,敏感性系数的绝对值增大,对爆炸压力的抑制作用增大,其主要是通过H、OH和O自由基攻击甲烷分子形成CH3基团,进而引发链反应。添加氢气后,R3反应中H自由基浓度增大,促进R3反应正向进行,增大了O自由基的消耗速率和H、OH自由基的生成速率,同时也增加了R84和R3中的H、OH自由基的反应速率,从而促进了R38反应正向进行,因此R3、R38和R84对爆炸反应有促进作用[21]。虽然甲烷和氢气都是与活性自由基反应,但甲烷分子与自由基结合的基元反应敏感性系数为负,与氢气相反,此时甲烷和氢气存在竞争关系,说明甲烷的存在一定程度上抑制了氢气的燃烧,间接抑制了爆炸压力的升高。

表2 氢气/甲烷/空气爆炸链式反应中关键基元反应
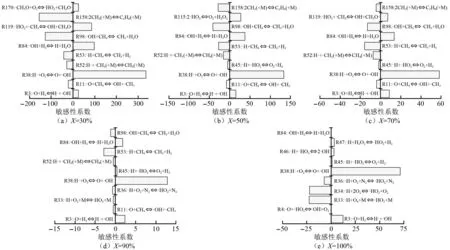
图6 不同氢气添加量下爆炸压力的敏感性系数Fig.6 Sensitivity coefficient of explosion pressure at different amounts of hydrogen added
2.3 氢气添加量对火焰传播速度的影响
图7列出了不同氢气添加量下混合气体的火焰半径和传播速度随时间的变化情况,氢气含量越少,火焰传播速度越低。整体上看火焰传播速度是不断振荡的,分析认为:当半径较小时,火焰表面的强拉伸作用抑制了火焰湍流化发展,火焰稳定传播;随着半径的增大,拉伸率减小,湍流增强了火焰的不稳定性,火焰锋的表面积增加,并且湍流加速了燃烧区和未燃烧区之间的物质输送,火焰速度增加[22]。此外,观察到在火焰传播后期振幅增大,说明火焰不稳定性会随着火焰半径的增加而增加。
3 结 论
文章利用乳胶气球为反应容器,通过向甲烷/空气混合物中添加氢气的一系列试验,并结合比色测温技术和Chemkin敏感性分析,研究了不同氢气添加量下氢气/甲烷/空气预混气体的火焰温度场分布、爆炸压力、火焰传播速度等特征参数,分析氢气对甲烷爆炸特性的影响规律,得到的相关结论如下:
(1)添加氢气量不同导致的火焰的温度分布状态不同,当X≤70%时,甲烷主导混合气体的燃烧,形成了火焰内部温度高于锋面温度的火焰结构,并且受水蒸气的影响,内部高温区位置上升;当X≥90%时,氢气主导混合气体的燃烧,形成了内部温度低、边缘温度高的温度场结构,随着氢气浓度增加,火焰边缘的温度就越高。在低氢气含量下(X≤70%)和高氢气含量下(X≥90%),H、O和OH自由基的生成速率较快;当70% (2)与甲烷相比,甲烷/氢气/空气混合物具有更高的爆炸压力,随着氢含量的增加,峰值超压和最大压力上升速率均逐渐增大,当X=100%时取得最大值,当X=0时获得最小值。当X<50%时,氢气含量增加导致最大压力上升速率提高了11%,并且最大压力上升速率的敏感性随着X的增加而降低,分别增长了7%(X=70%)、5.7%(X=90%)和2.5%(X=100%)。 (3)通过对爆炸压力敏感性分析发现,R11、R52、R53和R98的敏感性系数随着X的增大而增大,对压力升高的抑制作用增大,R3、R38和R84对爆炸反应有促进作用。混合物中甲烷和氢气都是与活性自由基反应,但实际的作用结果却完全相反,说明甲烷的存在一定程度上抑制了氢气的燃烧。

