蒙药京大戟奶制前后肠道毒性变化及成分分析
刘璐,郁红礼,2,3,吴皓,2,3,王欣之,崔小兵,曹玉,林伟豪,沈昌丽,曹杰
(1.南京中医药大学药学院,江苏 南京 210023;2.江苏省中药炮制重点实验室,江苏 南京 210023;3.国家教育部中药炮制规范化及标准化工程研究中心,江苏 南京 210023;4.南京市食品药品监督检验院,江苏 南京 211198)
蒙药巴格-塔日努(京大戟)为大戟科植物京大戟EuphorbiapekinensisRupr.的干燥根,首载于《神农本草经》,历版《中国药典》均收录。京大戟性寒,味苦,归肺、脾、肾经,具有泻水逐饮、消肿散结的作用[1]。但是生品京大戟泻下作用峻烈,使用不当容易引起强烈的胃肠道刺激反应,主要表现为腹痛腹泻、恶心呕吐[2]。故临床上常用其炮制品,以缓和其偏性。根据《中国民族药炮制集成》《四部医典》等著作记载,蒙医、藏医多采用“牛奶制”“诃子汤制”等技术炮制京大戟,《内蒙古蒙药饮片炮制规范》收载了奶制京大戟饮片,奶制可缓和生品京大戟的峻烈之性,减缓生品引起的腹痛腹泻等症状[3-5]。但未见有奶制京大戟炮制减毒机制的研究报道。课题组前期研究发现生品京大戟95%醇提物可以导致肠道炎症的产生,萜类成分是京大戟中主要的毒性成分[6-8]。本文通过采用小鼠肠道毒性模型,比较京大戟奶制前后的泻下作用及肠道致炎毒性变化,并采用高效液相色谱-四极杆-飞行时间串联质谱法(HPLC-Q-TOF-MS/MS)和多元统计学方法对生品和奶制京大戟的化学成分进行鉴定和组成变化分析,鉴定辅料残液中成分,研究奶制京大戟肠道毒性变化与成分变化的相关性,以期为奶制京大戟炮制减毒机制研究提供依据。
1 材料
1.1 动物
SPF级ICR雄性小鼠40只,体质量18~22 g,购自江苏华创信诺医药科技有限公司,许可证号:SCXK(苏)2020-0009,饲养于南京中医药大学实验动物中心,动物实验通过伦理审查,动物伦理号:202305A073。
1.2 药材
京大戟生品饮片购于安徽鑫泰药业有限公司(批号:20220311),产地为云南,经南京中医药大学陈建伟教授鉴定为大戟科植物京大戟EuphorbiapekinensisRuper.的干燥根。
1.3 试剂
95%乙醇(分析纯,南京晚晴化玻仪器有限公司);小鼠肿瘤坏死因子-α(TNF-α)、白细胞介素-1β(IL-1β)ELISA试剂盒(上海酶联生物科技有限公司,批号:YM-02323M1、YM20230403);乙腈、甲酸(质谱级,德国Merck公司);纯牛奶[内蒙古蒙牛乳业(集团)股份有限公司,批号:20220817];水为实验室自制超纯水。
1.4 仪器
Spring实验室超纯水净化系统(厦门锐思捷科学仪器有限公司);AGF-200高效率粉碎机(温岭市奥力中药机械有限公司);KQ-250DE数显控温水浴锅(郑州长城科工贸有限公司);BUCHIV-855旋转蒸发仪(瑞士Buchi公司);FA1104电子天平(德国Sartorius公司);Tiss-24组织研磨仪(上海净信事业发展有限公司);1730R台式低温离心机(美国Thermo公司);SectraMax i3x多功能酶标仪(美国Molecular Devices公司);Triple TOFTM5600LC-MS/MS高分辨质谱系统(美国AB SCIEX公司);FreeZone 2.5L冷冻干燥机(美国Labconco公司)。
2 方法
2.1 京大戟奶制品、水制品的制备
奶制京大戟饮片的制备:按照《内蒙古蒙药饮片炮制规范》(2020年版)奶制京大戟[5]制备方法,取净京大戟(厚片),用牛奶室温浸泡至透心(约12 h),取出,低温干燥。每100 kg京大戟,用牛奶150 kg,辅料牛奶残液收集备用。
水制京大戟饮片的制备:同奶制品制备方法,用等量纯净水替换牛奶。
2.2 京大戟生品、奶制品及水制品总提物的制备
京大戟生品总提物制备:生品京大戟饮片用粉碎机粉碎后过60目筛,取10 g加100 mL 95%乙醇加热回流提取2次,每次1 h,合并提取液减压浓缩至干(含生品饮片10 g)。
京大戟奶制品、水制品总提物制备同京大戟生品(含生品饮片10 g)。
2.3 京大戟炮制前后肠道毒性变化研究
2.3.1 动物分组及模型建立 适应性饲养1周,将40只ICR雄性小鼠按体质量随机分成空白组、京大戟生品总提物(生品)组、京大戟奶制品总提物(奶制品)组、京大戟水提物总提物(水制品)组,每组10只。
2.3.2 给药 空白组灌胃5‰CMC-Na溶液。京大戟生品、奶制品、水制品总提物用5‰CMC-Na溶液混悬,京大戟生品总提物组、奶制品总提物组、水制品总提物组分别灌胃京大戟生品、奶制品、水制品总提物溶液,剂量为4.5 g·kg-1(按照2020版《中国药典》临床10倍剂量换算[1]),给药体积为20 mL·kg-1,给药1次。
2.3.3 小鼠粪便含水量的测定 实验前禁食不禁水24 h,灌胃给药后将每只小鼠分别放入单独的笼盒中,收集小鼠3 h内粪便置于干燥已称质量的西林瓶中,随时密闭。收集结束后称质量,随后放入105 ℃烘箱中过夜烘干,称质量,粪便含水量=(烘干前粪便质量-烘干后粪便质量)/烘干前粪便质量×100%。
2.3.4 ELISA法测定小鼠不同肠段炎症因子水平 小鼠处死后,取小鼠肠道并分离出十二指肠、空肠、回肠、结肠,用提前预冷的生理盐水洗净肠道内容物,并用滤纸吸干剩余水分后于液氮中快速冷冻,后转移至-80 ℃冰箱中低温保存,快速称取小鼠各肠段组织50 mg,剪碎后加10倍量预冷的PBS溶液低温研磨。在4 ℃,5 000×g离心10 min,取上清分装,保存至-20 ℃冰箱。按照炎症因子TNF-α和IL-1β的ELISA试剂盒说明书测定。
2.4 LC-MS/MS分析京大戟奶制前后成分组成变化
精密称取京大戟生品、奶制品粉末1 g,置于具塞锥形瓶中,各平行6份,精密加入95%乙醇50 mL,超声处理30 min,过滤,取续滤液,0.45 μm微孔滤膜过滤,13 000 r·min-1离心10 min,取上清液待测。
色谱条件:Agilent Eclipse XDB-C18色谱柱(4.6 mm×250 mm,5 μm);流动相A为0.1%甲酸水,B为乙腈(洗脱程序:0~5 min,12%~18%B;5~15 min,18%B;15~25 min,18%~24%B;25~35 min,24%~95%B;35~45 min,95%~100%B);柱温30 ℃;流速1.0 mL·min-1;进样量10 μL。
质谱条件:TOF-MS/MS;扫描方式为ESI+和ESI-,质量扫描范围m/z50~1 500,气帘气(CUR)40 psi(1 psi≈6.895 kPa),雾化气(GSI)60 psi,辅助气(GS2)60 psi,电喷雾电压(ISVF)-4 500 eV(负),5 500 eV(正);离子源温度600 ℃,去簇电压(DP)100 eV/-100 eV,TOF-MS模式下碰撞电压10 eV/-10 eV,IDA-MS/MS条件下碰撞电压(CE)40 eV/-40 eV。
2.5 PCA及OPLS-DA分析京大戟牛奶制前后差异性成分
将6份生品、奶制品的MS数据导入MarkerView1.2.1软件中,通过设置相应参数,去除同位素离子峰,归一化等操作,导出数据。再将处理过的数据导入SIMCA 14.1软件中进行PCA及OPLS-DA分析,筛选出京大戟奶制前后的差异性成分。
2.6 LC-MS/MS分析辅料牛奶残液成分组成
将辅料牛奶残液冻干,按照“2.4”项下相同方法制备样品,色谱条件及质谱条件见2.4。
2.7 统计学方法
3 结果
3.1 京大戟生品、奶制品、水制品对小鼠粪便含水量的影响
图1结果可知,与空白组相比,京大戟生品和水制品均能显著增加小鼠的粪便含水量(P<0.05),表明京大戟生品和水制品均能导致小鼠泻下。与生品组相比,奶制品组小鼠的粪便含水量显著下降(P<0.05),水制品组小鼠的粪便含水量没有显著性差异,表明奶制能缓和生品京大戟的泻下作用,水制则不能缓和泻下作用。
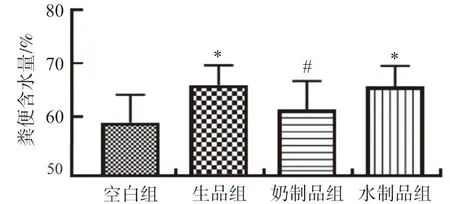
注:与空白组相比,*P<0.05;与生品组相比,
3.2 京大戟生品、奶制品、水制品对小鼠各肠段炎症因子TNF-α、IL-1β水平的影响
结果显示,与空白组比较,京大戟生品组和水制品组可致小鼠十二指肠、空肠、回肠、结肠的TNF-α、IL-1β水平显著升高(P<0.05),见图2~3,表明京大戟生品和水制品具有肠道致炎毒性。与生品组比较,奶制品组十二指肠、空肠、回肠、结肠的TNF-α、IL-1β水平显著降低(P<0.05),水制品组十二指肠、空肠、回肠、结肠的TNF-α、IL-1β水平无显著性差异,表明奶制可以降低生品京大戟的肠道致炎毒性,水制则不能降低毒性。牛奶是京大戟奶制后肠道毒性降低的关键辅料。
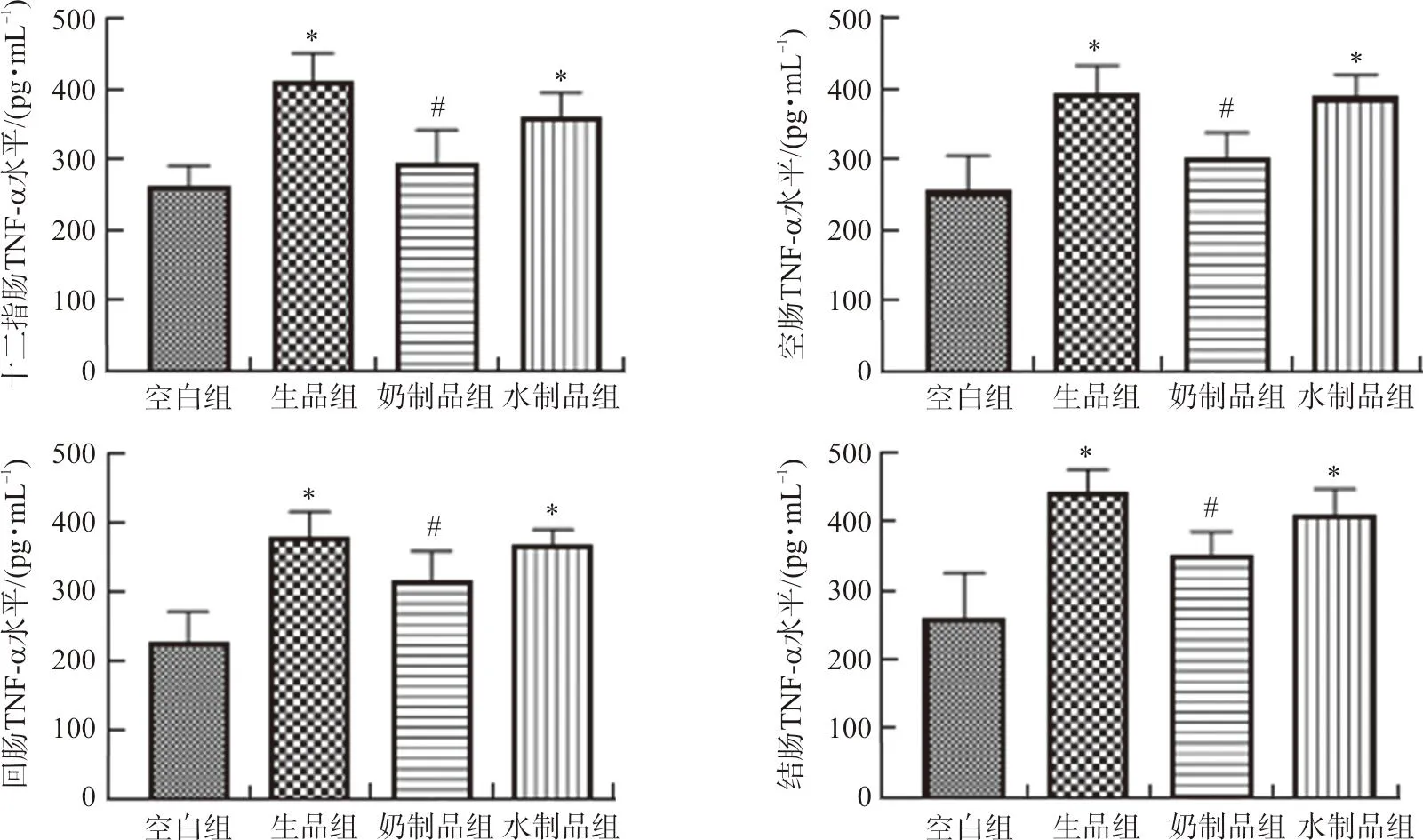
注:与空白组相比,*P<0.05;与生品组相比,
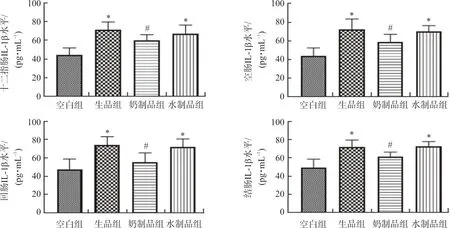
注:与空白组相比,*P<0.05;与生品组相比,
3.3 京大戟奶制前后95%醇提物成分分析
京大戟生品、奶制品正、负离子模式下的总离子流图,见图4。查阅相关文献及CAS Scifinder和PubChem等数据库,并建立京大戟化学成分库。采用Peak View软件得到保留时间、离子碎片等信息,结合成分库,对京大戟中成分进行鉴定。根据HPLC-Q-TOF-MS/MS结果显示,京大戟中共鉴定出50个成分,见表1,其中萜类成分38个,包括24个二萜、3个倍半萜及11个三萜,酚酸类成分6个,其它成分6个,化合物信息见表1。对比相同化合物的峰强度,发现各成分含量有不同程度下降。
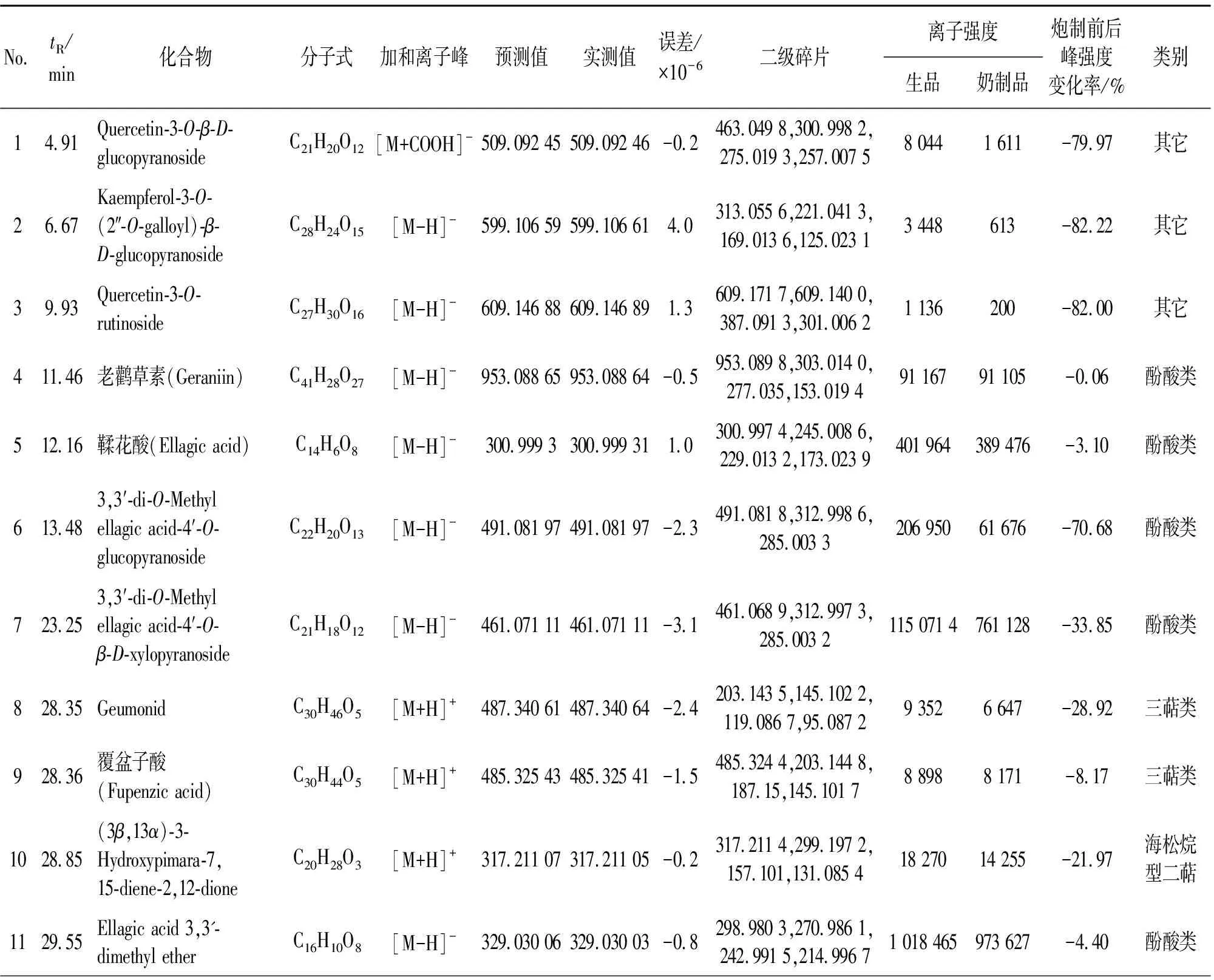
表1 京大戟中化学成分的鉴定结果及奶制前后峰强度变化率Table 1 Chemical components in Euphorbiae pekinensis Radix and peak intensitychange rate before and after milk processing
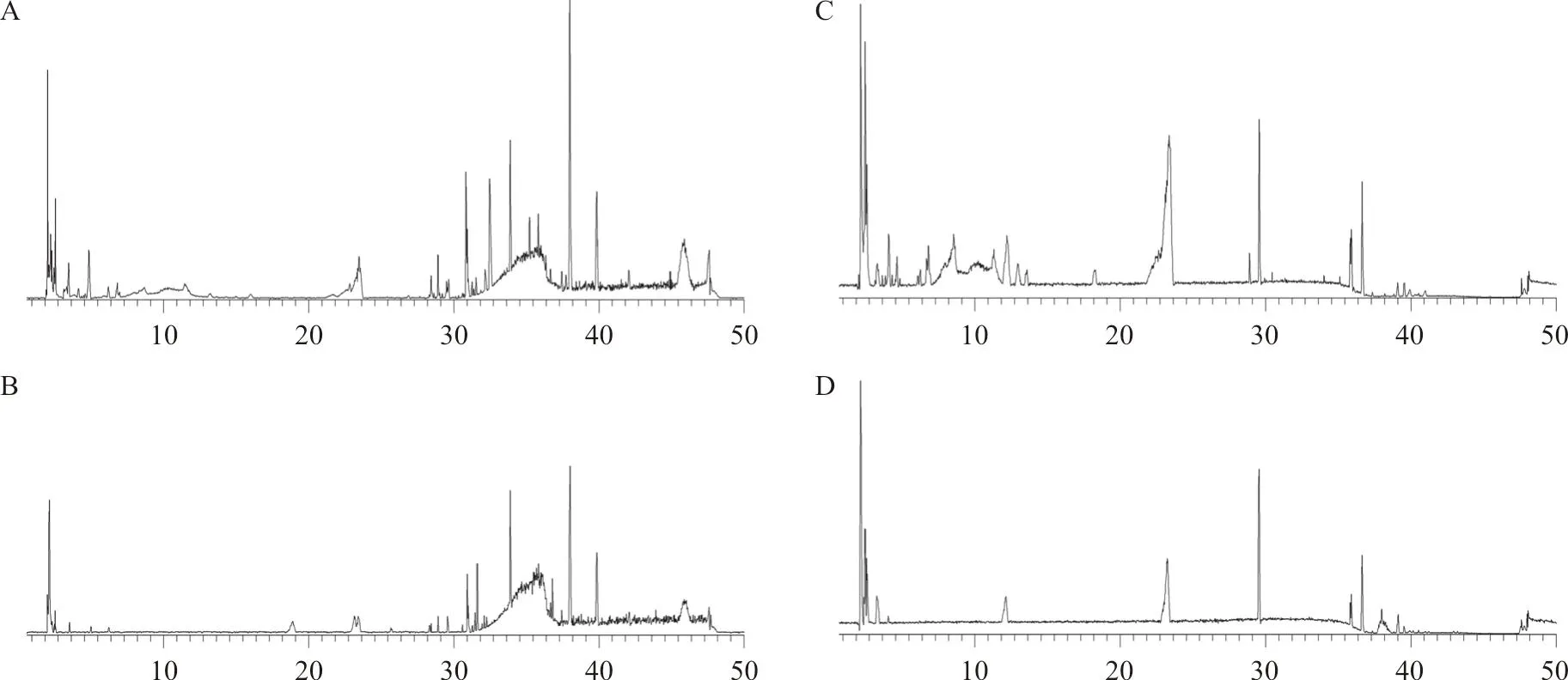
注:A.京大戟生品正离子;B.京大戟奶制品正离子;C.京大戟生品负离子;D.京大戟奶制品负离子
3.4 京大戟奶制前后差异性成分分析
将生品京大戟和奶制京大戟的MS数据导入多元数据处理软件MarkerViewTM1.21软件中进行去除同位素离子,归一化处理后导出。将处理后的数据导入SIMCA 14.1软件中进行无监督的PCA分析,见图5。结果发现在正、负离子模式下,生品、奶制品可明显聚为2类,表明炮制前后发生了明显的成分组成变化。进一步在有监督模式下的OPLS-DA分析,见图6,正离子模式下所建模型R2X(cum)=0.648,R2Y(cum)=0.996,Q2(cum)=0.673,负离子模式下所建模型R2X(cum)=0.85,R2Y(cum)=0.995,Q2(cum)=0.999,表明模型预测能力良好。OPLS-DA结果与PCA结果一致,生品京大戟与奶制京大戟明显聚为2类。进一步对变量重要投影(VIP)值进行分析,筛选出VIP值>1且t检验P<0.05的成分,同PeakView1.2中以匹配鉴定的化合物信息比对,筛选生品京大戟和奶制京大戟中的差异性成分。结果从已鉴定的50个成分中筛选出13个差异性成分,其中萜类成分11个,均为二萜类成分,酚酸类成分2个,其成分含量均下降,见表2。其中松香烷型二萜Helioscopinolide A、卡司烷型二萜Pekinenin A、海松烷型二萜(12α,13α)-12-Hydroxypimara-7,15-dien-3-one、海松烷型二萜17-nor-7α-Hydroxy-15-oxoabieta-8,11,13-triene这4个成分含量下降最多,下降率分别为56.78%、53.19%、43.36%、41.60%。
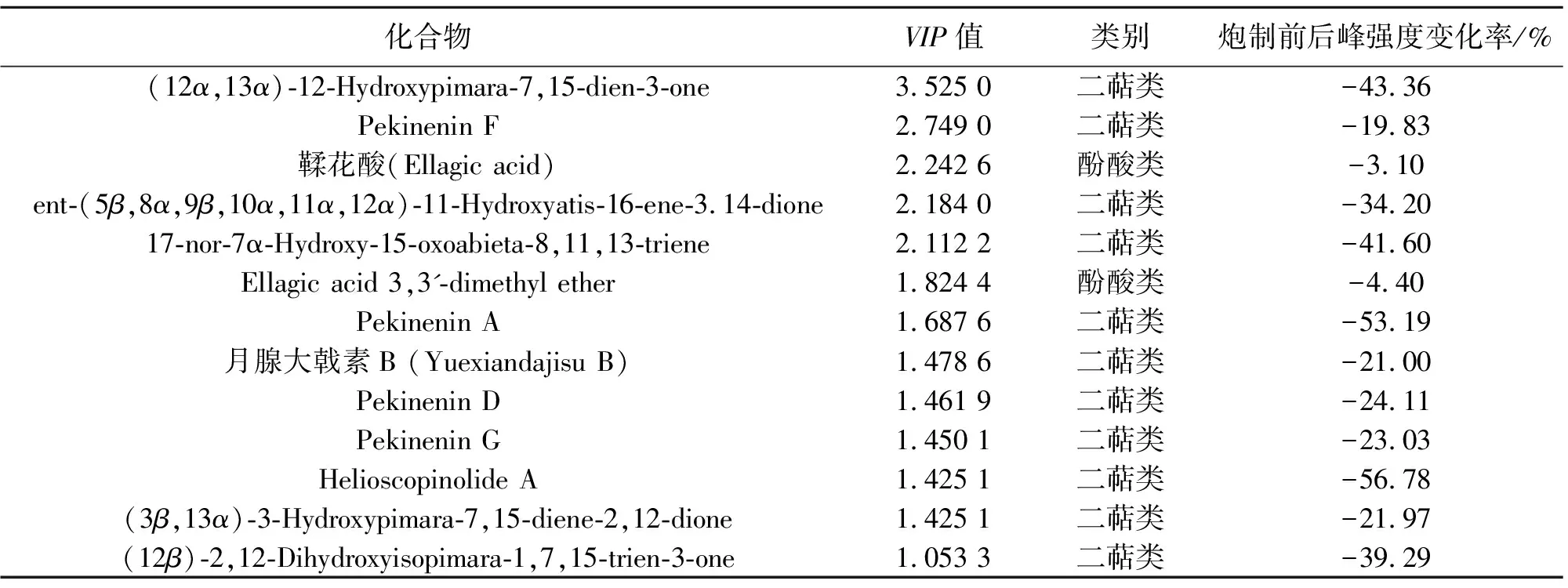
表2 京大戟奶制前后饮片中主要差异性成分Table 2 Differential components of Euphorbiae pekinensis Radix before and after processing with milk
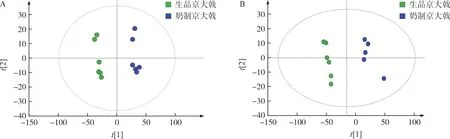
注:A.正离子模式;B.负离子模式
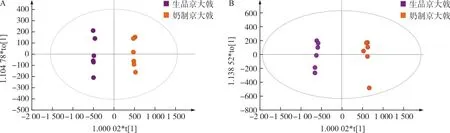
注:A.正离子模式;B.负离子模式
3.5 炮制后辅料牛奶残液中的成分鉴定
为了研究京大戟牛奶制后成分含量下降的原因。本文收集炮制后剩余的辅料牛奶,采用HPLC-Q-TOF-MS/MS对其中的成分进行分析,共检测到17个成分,其中16个是萜类成分(包括1个倍半萜类成分,13个二萜类成分,2个三萜类成分),1个是酚酸类成分,见表3。结果表明,在牛奶浸泡炮制过程中,京大戟中的萜类成分转移到牛奶中。
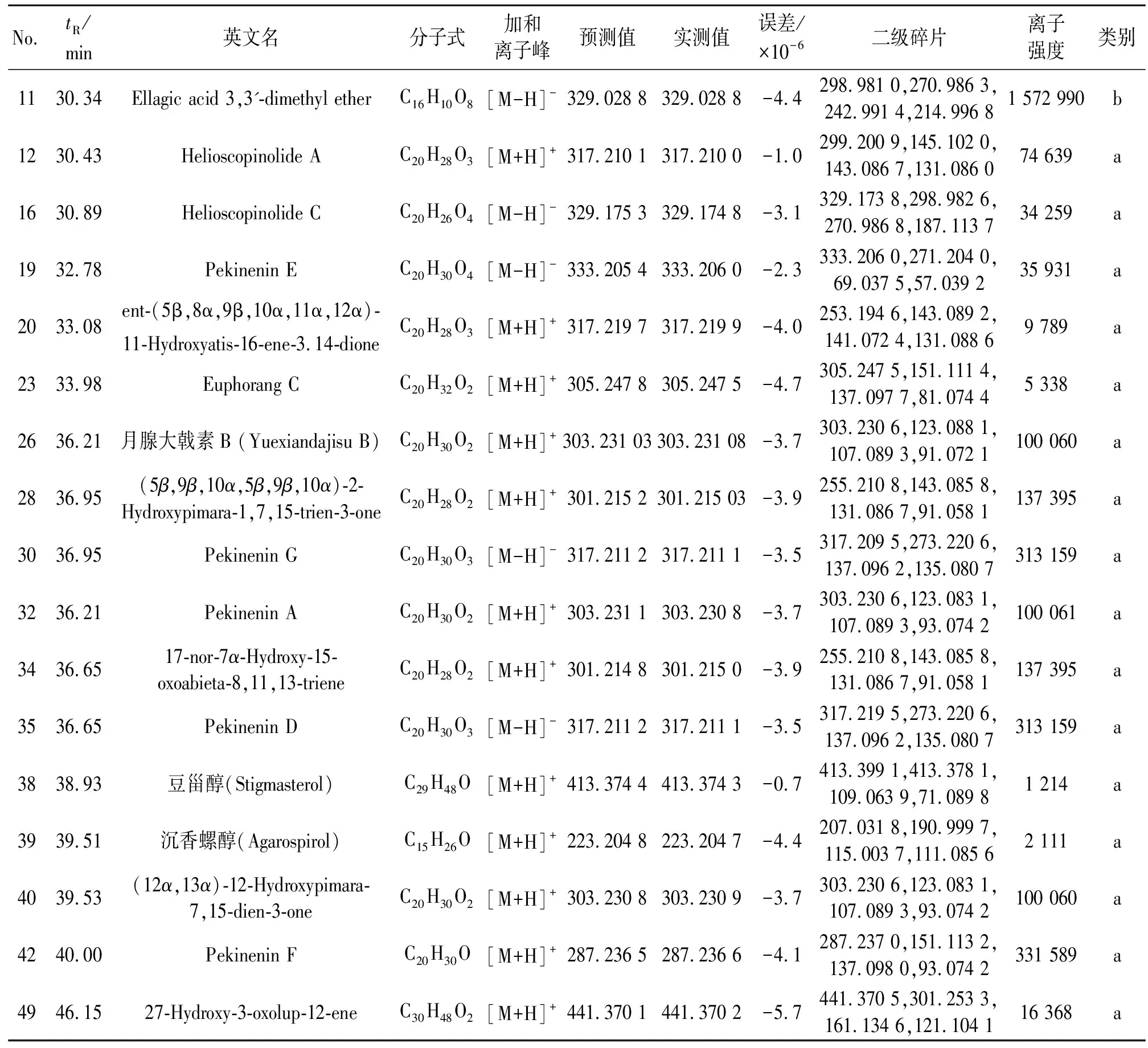
表3 辅料牛奶残液中成分鉴定结果Table 3 Identification of chemical components in residual milk
4 讨论
京大戟生品容易引起腹痛腹泻、恶心呕吐等不良反应,故临床上常用其炮制品,现多用醋制品,多以丸散剂入药,如十枣丸、消肿九味散、卫生散等。课题组前期研究发现,生品京大戟的毒性主要表现为胃肠道刺激,可以引起肠道黏膜损伤,引发肠道炎症[7-8],醋制可以减轻生品刺激性[9-10]。《内蒙古蒙药饮片炮制规范》中记载奶制京大戟。蒙医认为奶制京大戟可以缓和生品京大戟峻下作用,减弱京大戟的肠道毒性作用,故蒙医临床常用奶制京大戟[4],但是目前未见奶制京大戟减毒机制的相关研究。本文采用小鼠肠道致炎毒性模型,比较生品京大戟、奶制京大戟的致泻作用及肠道致炎毒性。因京大戟常以丸散剂入药,同时课题组前期对京大戟毒性部位进行筛选时发现,京大戟毒性部位主要富集了极性较低的成分[8],相较于水提,95%乙醇提取对小极性成分的提取效率更高,因此本研究选择比较生品与奶制品95%醇提物的肠道毒性变化。结果显示奶制可以改善生品引起的泻下反应,降低小鼠各肠段炎症因子水平,表明奶制可以降低京大戟的肠道致炎毒性。牛奶中含有大量的水,无法确定在炮制过程中起到作用的是水还是牛奶中的蛋白、脂质等物质,因此本文对比了水处理浸泡是否对京大戟的肠道毒性产生影响。结果显示,水制京大戟肠道毒性并未显著降低,表明在炮制浸泡过程中辅料牛奶是炮制解毒的关键辅料。
为进一步研究蒙药京大戟奶制前后毒性变化与成分变化的相关性,本文以质谱法解析奶制前后京大戟中化学成分组成,结果发现炮制前后京大戟95%乙醇提取物中成分组成发生显著变化,生品中共鉴定出50个成分,其中萜类成分38个(其中3个倍半萜类成分,24个二萜类成分和11个三萜类成分),酚酸类成分6个,其它成分6个。通过计算各成分峰强度的变化率,发现奶制后所有萜类成分的相对含量均有不同程度的下降。课题组前期研究发现,京大戟二氯甲烷提取部位中分离获得的二萜类成分如卡司烷型二萜Pekinenin A、Pekinenin G以及倍半萜Pernambucone成分具有显著致炎毒性[11-12],奶制后这些成分含量均下降,下降率分别为53.19%、23.03%、18.27%,故推测奶制后毒性降低与奶制后京大戟中萜类成分的含量下降相关。
采用PCA分析生品京大戟和奶制京大戟的质谱数据,发现生品和奶制品能明显聚为2类,表明京大戟炮制前后的成分组成发生显著变化。通过t检验筛选出的13个差异性成分, 其中11个萜类成分均为二萜类成分,这些二萜类成分中Helioscopinolide A(松香烷型二萜)、Pekinenin A(卡司烷型二萜)、(12α,13α)-12-Hydroxypimara-7,15-dien-3-one(海松烷型二萜)、17-nor-7α-Hydroxy-15-oxoabieta-8,11,13-triene(海松烷型二萜)4个成分含量下降最多,下降率分别为56.78%、53.19%、43.36%、41.60%。同时在炮制后辅料牛奶残液中检出了来源于京大戟的17个成分,其中16个为萜类成分,均为亲脂性小分子成分。文献研究显示,牛奶中含有大量的酪蛋白、脂质[13],由于其特殊的两亲性结构,可以作为天然载体[14-16],运载某些水溶性差的亲脂性成分,如酪蛋白可以作为β-胡萝卜素的载体[17-18]。推测牛奶中的这些两亲性结构物质与京大戟中极性小的萜类成分发生相互作用,促进萜类成分的转移,因此能在牛奶残液中检测到京大戟中的萜类成分。不同萜类成分的毒性差异以及牛奶中两亲性结构物质与萜类成分的相互作用机制正在开展深入研究。水浸泡京大戟可能也会在浸泡过程中损失部分成分,但实验结果表明,相较于生品,水制品的毒性并未显著降低,说明水制不能起到减毒的作用。
综上,京大戟奶制法炮制降低肠道毒副作用,可能是由于牛奶浸泡过程中辅料牛奶促进大量毒性萜类成分从饮片转移至牛奶中,使饮片中毒性成分含量下降,肠道毒性降低。本研究为牛奶制京大戟的减毒机制提供了基础。

