海藻酸钠载药口腔速溶膜的制备及性能研究
欧阳建梅,林艳霞
(深圳湾实验室,广东 深圳 518000)
随着生物医药技术发展,传统的药物传输方式如静脉注射、糖浆和缓释胶囊等广泛应用于医学领域,然而这些方式存在药物突释、利用率低等问题[1]。为了提高给药简便性和药物持续释放能力,开发新的给药方式具有重要的意义,如载药口腔速溶膜可通过将药物有效成分负载至聚合物薄膜制得,依靠唾液浸润水化使药物快速释放[2]。
高分子材料具有良好的化学稳定性且不易与药物发生反应,使其作为载药聚合物成为可能[3]。常见的载药聚合物主要有壳聚糖、海藻酸钠(SA)、淀粉和羟丙甲基纤维素(HPMC)等[4]。SA 作为一种天然高分子多糖,具有良好的成膜性、生物降解性和生物相容性,用作医用敷料时能吸收多余的伤口液体,减少细菌感染,是生物医学领域的研究热点[5]。HPMC 作为半合成的纤维素衍生物能够在口腔中快速溶胀,具有良好的机械性能和承载能力,不易与药物发生反应,在胃肠液的酸碱环境中依然保持化学稳定性,是一种稳定普遍的药物载体[6]。另外,阴离子聚合物可以调节其凝胶层的形成和厚度并加强黏膜粘附作用,笔者将HPMC 与阴离子聚合物SA 复合并负载BH 制备海藻酸钠载药口腔速溶膜,以期实现药物的控制释放。
1 实验部分
1.1 仪器与试剂
YJ1002 型电子天平,DF-101S 集热式恒温加热磁力搅拌器,DHG-9070A 台式电热恒温鼓风干燥箱,JC-QXS-2L超声波清洗仪,雷磁PHSJ-6L型pH 计,ZB-5000N 拉力试验机,Lambda 950 紫外分光光度计。
盐酸苄达明(BH)、SA,分析纯;HPMC,I型,黏度20 Pa·s;磷酸盐缓冲液(PBS),pH=7.2~7.4。
1.2 海藻酸钠口腔速溶膜的制备
溶液制备。将SA 和HPMC 分别溶于蒸馏水中,以500 r/min转速搅拌30 min至SA和HPMC全部溶解得到各自水溶液,2 者混合得到HPMC/SA水溶液,静置至气泡消失。
流延成膜。将SA/HPMC水溶液用浇铸刀在玻璃板表面均匀浇铸,在温度为50 ℃鼓风干燥箱内恒温蒸发溶剂,脱膜后获得海藻酸钠口腔速溶膜SA/HPMC。通过调整HPMC 和SA 的质量比分别为2∶1、1∶1、1∶2,得到相应的海藻酸钠口腔速溶膜H2S1、H1S1、H1S2。
1.3 海藻酸钠载药口腔速溶膜的制备
按照SA 和HPMC 最佳性能比例制备SA 水溶液和HPMC/BH水溶液,将SA水溶液和HPMC/BH水溶液充分混合、静置至气泡消失,按照流延成膜的方式制备海藻酸钠载药口腔速溶膜HPMC/SA/BH,通过调整BH 的质量分数,得到不同负载量的HPMC/SA/BH载药口腔速溶膜。
1.4 分析方法
1.4.1 拉伸性能测试
根据GB/T 228-2002 对膜的力学性能进行分析[7]。将膜制成样条(1 cm×5 cm),使用万能拉力机将样品拉断测试其拉伸强度,每组样品测量5次,取平均值。
1.4.2 红外测试与表征
利用傅里叶红外光谱仪对SA/HPMC口腔速溶膜表面的化学基团进行分析。将干燥后的样品置于红外光谱仪分析台上,通过膜对红外光的吸收来分析膜表面的存在的基团信息。
1.4.3 透光率测试
采用紫外分光光度计对SA/HPMC口腔速溶膜的透光率进行测试,测试条件:波长200~500 nm,分辨率5 nm。
1.4.4 水溶性测试
将SA/HPMC 口腔速溶膜裁成样品(20 mm×20 mm),放入温度37 ℃、体积20 mL 的水中搅拌,转速为150 r/min,记录薄膜完全溶解的时间。
1.4.5 载药量和包封率测试
配制模拟口腔唾液。准确量取25 mL PBS溶液加至200 mL 蒸馏水中,待完全溶解后,用盐酸溶液(浓度为0.1 mol/L)调节至pH=6.8,加水定容至500 mL。
绘制标准曲线。准确称取5 mg BH 加入到50 mL PBS 中,得到药物质量浓度为0.1 mg/mL 的溶液,再对速溶膜进行稀释,得到质量浓度分别为0.005、0.01、0.015、0.02、0.025、0.03、0.035、0.04 mg/mL的样品。采用紫外分光光度计在200~800 nm 的范围内进行测试,得到最大吸收的波长位置。在最大波长处对上述不同浓度的样品进行吸光度测试,通过回归分析得到浓度-吸光度标准曲线见图1。

图1 BH的浓度-吸光度标准曲线Fig 1 Concentration-absorbance standard curve of BH(benzylamine hydrochloride)
测定载药量。称取一定质量的HPMC/SA/BH载药口腔速溶膜样品溶于10 mL的模拟口腔唾液中并进行搅拌溶解。采用胶头滴管准确量取1 mL 含有样品的模拟口腔唾液置于10 mL比色管中,并用PBS溶液进行稀释,静置后取上层澄清液进行吸光度测试。BH的质量浓度根据浓度-吸光度标准曲线计算,通过公式计算载药效率S和包封率P:
式中,m为BH 的质量;M为样品的质量;m0为样品中BH的理论质量。
2 结果与讨论
2.1 海藻酸钠口腔速溶膜的性能
2.1.1 化学结构
对SA/HPMC口腔速溶膜进行红外测试,结果见图2。

图2 口腔速溶膜的红外光谱Fig 2 Infrared spectroscopy of oral instant film
由图2可知,HPMC在3 439 cm-1处出现了-OH峰,在2 904 cm-1处出现了-CH2的不对称伸缩振动峰,在2 834 cm-1处有-CH2的对称伸缩振动峰出现,在1 647 cm-处出现了羟丙基的骨架伸缩振动峰。SA 在3 000~3 700 cm-处出现了-OH 的伸缩振动峰,在1 596 cm-1处出现了羧基不对称伸缩振动峰,在1 408 cm-1处出现了羧基对称伸缩振动峰。比对SA/HPMC 口腔速溶膜红外吸收峰中SA和HPMC 特征峰均同时出现,说明口腔速溶膜中存在HPMC和SA,同时在3 000~3 700 cm-1处的-OH峰出现了移动,说明在流延成膜的过程中,SA和HPMC具有良好的相容性。
2.1.2 透光性
薄膜的透光度主要是指薄膜材料的透光程度,通常用雾度或者透光率来表示。对SA/HPMC口腔速溶膜的透光率进行测试,结果见图3。
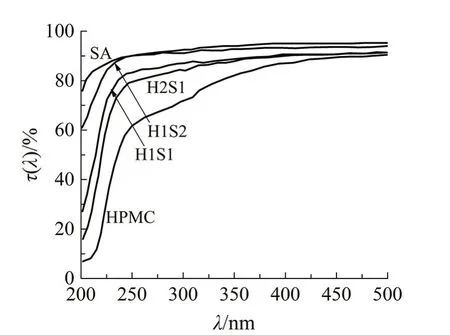
图3 口腔速溶膜的透光性能Fig 3 Transmittance performance of oral instant film
由图3 可知,在波长200~500 nm 范围内,HPMC的透光率较低,特别是在波长200~340 nm范围内透光率低于70%,而SA 透光率较高接近90%。随着SA含量的增加,SA/HPMC口腔速溶膜透光率提高,当w(SA)∶w(HPMC)=2∶1 时,在220~500 nm范围内,透光率高于80%,并接近纯SA 的透光率,说明SA 和HPMC 具有良好的相容性,起到了互补的作用。
2.1.3 水溶性
SA/HPMC 口腔速溶膜的水溶性影响到药物的释放速率,口腔速溶膜的水溶性较高即在水中的溶解时间短,会导致口腔速溶膜与唾液等接触时快速溶解,加快药物的释放,不利于药物的最佳使用。对SA/HPMC口腔速溶膜的水溶性平行测试3次(1#、2#、3#),结果如表1所示。

表1 口腔速溶膜的水溶性Tab 1 Water solubility of oral instant film
由表1 可知,纯SA 口腔速溶膜在水中的溶解时间约20 min,溶解速率极高,这将导致药物的快速释放,而纯HPMC 膜在水中的溶解时间约84 min,为纯SA口腔膜溶解时间的约4倍,有利于减缓药物的释放速率。通过将SA和HPMC结合,使得SA/HPMC口腔速溶膜在水中的溶解时间处于纯SA 口腔膜和纯HPMC 膜之间,其中H2S1 口腔速溶膜的溶解时间约46 min。分析原因为,SA 作为亲水性胶体易溶于水,而HPMC 含有的甲氧基疏水性强,在水中溶解较慢,通过提高HPMC 的含量可延长SA/HPMC 口腔速溶膜在水中的溶解时间,延迟药物的释放时间。
2.2 海藻酸钠载药口腔速溶膜的性能
2.2.1 分子结构
对HPMC/SA/BH 载药口腔速溶膜进行红外测试,结果见图4。
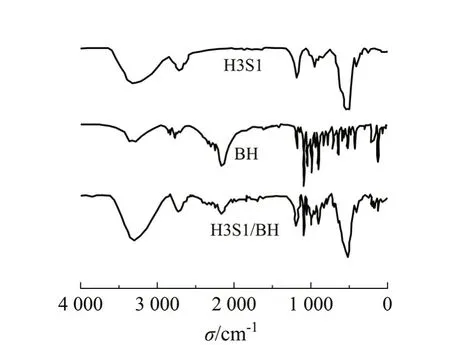
图4 载药口腔速溶膜的红外光谱Fig 4 Infrared spectroscopy of drug loaded oral instant film
由图4 可知,H3S1/BH 载药口腔速溶膜在1 462 cm-1、1 530 cm-1、1 575 cm-1和1 610 cm-1位置处均出现了苯环的C=C 骨架振动峰,药物BH 在相同的位置也出现了相应的峰,证明BH 在H3S1/BH载药口腔速溶膜上进行了有效负载,并保留了BH 药物本身的化学性质,在载药过程中,BH 未与口腔速溶膜发生化学反应,不存在其它物质的产生导致药物质量发生变化。
2.2.2 力学性能
对不同BH负载量的HPMC/SA/BH载药口腔速溶膜进行力学性能测试,结果如图5所示。

图5 载药口腔速溶膜的力学性能Fig 5 Mechanical properties of drug loaded oral instant film
由图5 可知,在HPMC/SA/BH 载药口腔速溶膜中,在低负载率的条件下,HPMC/SA/BH 载药口腔速溶膜的拉伸强度和断裂伸长率随着BH负载量的增加而增加;当负载率为30%时,拉伸强度和断裂伸长率达到最大值,分别为61.12 MPa 和51.12%;继续增加BH负载量,断裂伸长率和拉伸强度总体呈下降趋势。分析原因为,BH作为小分子物质在大分子链之间产生了应力节点,增加了大分子物质在拉伸过程中的受力点,从而使分子链不易断裂,使力学性能增加;当BH负载率大于30%时,随着BH 的增加,其分布在SA 和HPMC 大分子之间,减少了大分子之间的氢键作用,使大分子之间的流动性增加,拉伸过程中更容易变形。
2.2.3 载药效率和包封率
HPMC/SA/BH载药口腔速溶膜的BH负载量分别与载药效率S、包封率P的关系,如图6所示。
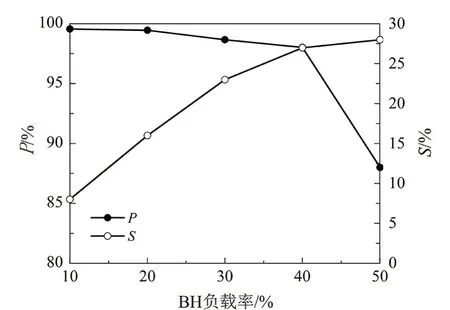
图6 载药口腔速溶膜的载药效率和包封率Fig 6 Drug loading efficiency and encapsulation efficiency of drug loaded oral instant film
由图6可知,随着药物负载量的增加,包封率呈下降趋势。总体上,BH 负载量低于40%时,包封率均大于98%;当药物负载量为50%时,包封率降至88%。分析原因为,各组分在水中的溶解性差异,BH粉末溶解于水中并与海藻酸钠溶液混合时,由于海藻酸钠亲水性极强,使得大量的水分子脱离BH,导致BH 在溶液中的饱和绝对值降低,固体析出。因此,随着负载量的增加,HPMC/SA/BH 载药口腔速溶膜包封率下降,载药效率增加。当负载率大于40%时,载药效率也达到极限值,继续增加负载量,载药效率无明显增加。综上所述,BH 的负载量以不高于40%为佳,避免造成HPMC/SA/BH 载药口腔速溶膜包封率下降、药物浪费和成本增加。
3 结 论
以SA和HPMC作为成膜剂,采用流延成膜的方法制备了SA/HPMC 口腔速溶膜,对其化学结构、透光性以及水溶性进行了分析,选择了最佳成膜比例。在此基础上,将BH 负载在SA/HPMC口腔速溶膜上,制备了不同负载率的HPMC/SA/BH 载药口腔速溶膜,对其分子结构、力学性能、包封率和载药效率进行分析,得出结果:
1)SA/HPMC 口腔速溶膜的红外光谱出现SA和HPMC的特征峰,说明2种成膜剂在分子间氢键作用下具有良好的相容性;当w(SA)>w(HPMC),在波长为220~500 nm 范围,SA/HPMC 口腔速溶膜透光率均高于80%,透光性能良好;当w(SA)∶w(HPMC)=1∶2,SA/HPMC 口腔速溶膜在水中的溶解时间为46 min,能够延迟药物的释放时间。
2)在w(SA)∶w(HPMC)=1∶2 的条件下,将BH负载至SA/HPMC口腔速溶膜制备了HPMC/SA/BH载药口腔速溶膜,红外测试结果表明BH得到有效负载;当BH负载量为30%时,HPMC/SA/BH载药口腔速溶膜力学性能最好,当BH 负载量为40%时,其包封率和载药效率较佳,经济成本更好。

