一种新型次氯酸响应型光敏剂的合成及其抗肿瘤活性
赵勇强,袁家英,匡思颖,吴仕萍,张宁峰,黄统辉
(徐州医科大学 江苏省新药研究与临床药学重点实验室,江苏 徐州 221000)
光动力疗法(Photodynamic therapy,PDT)通过光激发光敏剂产生活性氧(ROS)消融肿瘤细胞,是一种非侵入式的肿瘤治疗新方法,具有毒性小、选择性好、无耐药性和可重复治疗等突出优点,抗肿瘤效果优异[1-2]。已有多种光敏剂药物,如光福啉(photofrin)、5-氨基酮戊酸(ALA)、亚甲基兰(methylene blue)、血卟啉、喜泊芬和海姆泊芬等批准应用于临床治疗皮肤癌、口腔癌、宫颈癌以及膀胱癌等疾病,显示出良好的应用前景[3-5]。光敏剂经光触发后可发生2种类型的光化学反应,即I型和II型[6-7]。相较于I型光化学反应,II型光化学反应所产生的ROS寿命更长;相较于II型光化学反应,I型光化学反应所需氧量相对较低[8]。因此,能同时发生I型和II型光化学反应的光敏剂更有利于应用于复杂的肿瘤环境,特别是缺氧的肿瘤环境[9-10]。
与正常组织细胞相比,肿瘤细胞微环境具有H2O2、HClO/ClO-和谷胱甘肽(GSH)含量高,缺氧及特殊酶过量表达等特点[11]。例如,HClO/ClO-是生物体内的H2O2和Cl-在髓过氧化物酶(MPO)催化作用下产生的一种重要的活性物质,参与多种生理及病理过程,也是肿瘤等相关疾病的高表达物质之一,与肿瘤的发生发展密切相关[12-13]。因此,合理利用好这些区别,开发肿瘤环境响应型的光敏剂,可以极大提高光动力治疗的组织特异性,进而达到更加精准的诊断与治疗的目的,具有重要的临床应用价值[14]。
酚噻嗪是一种含有氮和硫杂原子的芳香杂环化合物,具有较强的给电子能力和良好的光物理特性,其结构中的硫原子能被HClO/ClO-选择性地氧化为亚砜结构[15]。基于此,本研究设计并合成了一种基于酚噻嗪结构的ClO-响应型光敏剂PTZPPy,响应机制如图1所示。其结构包含酚噻嗪作为给电子基团,同时作为ClO-识别的片段。使用吡啶盐片段作为强吸电子基团,使用C=C和苯环,将酚噻嗪与吡啶盐结构相连,形成具有D-π-A结构特征的分子结构,该化合物具有分子内电荷转移(ICT)效应,无明显荧光信号[16-17]。但当其与ClO-反应后,由于酚噻嗪中的硫原子被氧化为亚砜,导致ICT效应减弱,荧光增强[18-19],起到“点亮”肿瘤组织的作用,可应用于高表达ClO-的肿瘤检测[20]。光照后,PTZPPy具有较好的ROS产生效率。使用取代的酚噻嗪(S-1)为原料,经缩合、偶联、成盐等合成步骤得到目标产物PTZPPy(图2),其结构经NMR和HR-MS(ESI)表征,体外抗肿瘤活性结果表明PTZPPy具有良好的抗肿瘤活性[21]。
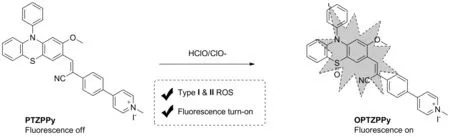
图1 PTZPPy对ClO-的响应机制
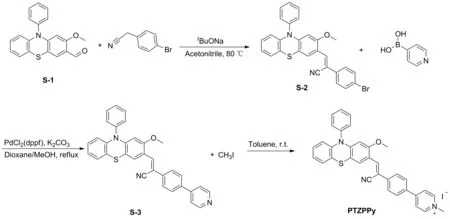
图2 化合物PTZPPy的合成路线
1 实验部分
1.1 仪器与试剂
F4600型荧光分光光度计;JNM-ECZR 400 MHz型核磁共振仪(DMSO-d6或CDCl3为溶剂,TMS为内标);Bruker maXis 4G UHR-TOF型质谱仪。
所有试剂皆为分析纯或化学纯。
1.2 合成
(1) 化合物S-2的合成
将2-甲氧基-10-苯基-10H-吩噻嗪-3-甲醛(1.665 g,5.0 mmol)、t-BuONa(480.5 mg,5.0 mmol)和2-(4-溴苯基)乙腈(980.0 mg,5.0 mmol)溶解于30.0 mL乙腈溶液,在80 ℃下回流反应3 h,薄层层析监测反应进程,待原料消耗完毕,将反应液倒入50 mL水中,使用二氯甲烷(3×25.0 mL)萃取,用饱和食盐水溶液洗涤有机层,有机层加入无水硫酸钠干燥后脱溶。粗品经硅胶柱层析纯化(洗脱剂:石油醚∶乙酸乙酯=20∶1,V∶V)得到化合物S-2,收率61%,1H NMR(400 MHz,CDCl3)δ:7.91(s,1H),7.76~7.60(m,3H),7.57~7.47(m,5H),7.42(d,J=8.0 Hz,2H),7.28~7.24(m,1H),7.05~6.99(m,2H),6.84(d,J=6.1 Hz,1H),6.17~6.10(m,1H),3.48(s,3H)。
(2) 化合物S-3的合成
将吡啶-4-硼酸(369.0 mg,3.0 mmol)溶解于5.0 mL甲醇溶液中,然后加入化合物1(1.020 g,2.0 mmol)、PdCl2(dppf)(146.0 mg,0.2 mmol)、K2CO3(29.2 mg,6.0 mmol)和1,4-二氧六环(25.0 mL),搅拌并在110 ℃下回流10 h。反应完全后,将反应液倒入50 mL水中,用二氯甲烷(3×25.0 mL)萃取,用饱和食盐水溶液洗涤有机层,加入无水硫酸钠干燥,粗品经硅胶柱层析纯化(洗脱剂:石油醚∶乙酸乙酯=2∶1,V∶V)得到化合物S-3,收率42%,1H NMR(400 MHz,CDCl3)δ:8.68(s,1H),7.96(s,0H),7.83(s,1H),7.76(d,J=8.4 Hz,1H),7.67(dd,J=12.8 Hz,8.0 Hz,1H),7.54(d,J=5.6 Hz,1H),7.42(d,J=7.0 Hz,1H),7.07~6.98(m,1H),6.90~6.76(m,1H),6.18~6.09(m,1H),5.73(s,1H)。
(3) 化合物PTZPPy的合成
将化合物S-3(254.8 mg,0.5 mmol)溶解于5.0 mL乙腈溶液中,加入碘甲烷(71.0 mg,0.5 mmol),搅拌并在80 ℃下回流12 h。反应完成后,过滤溶液。固体用乙酸乙酯洗涤并进一步真空干燥,得到黑色固体状的PTZPPy,收率36%,1H NMR(400 MHz,DMSO-d6)δ:9.02(d,J=6.8 Hz,2H),8.54(d,J=6.6 Hz,2H),8.19(d,J=8.6 Hz,2H),7.98(s,1H),7.89(d,J=8.4 Hz,2H),7.80(s,1H),7.75(t,J=7.6 Hz,2H),7.64(t,J=7.4 Hz,2H),7.53(d,J=7.4 Hz,1H),7.13(dd,J=7.2 Hz,2.0 Hz,1H),7.06~6.58(m,2H),6.12(dd,J=7.8 Hz,1.6 Hz,1H),5.82(s,1H),4.33(s,3H),3.49(s,3H);13C NMR(100 MHz,DMSO-d6)δ:158.17,153.04,147.58,145.69,142.13,139.36,137.63,136.99,133.31,131.37,130.43,129.34,128.92,127.49,126.79,126.44,125.22,124.62,123.95,123.65,118.90,118.08,116.40,109.44,106.33,99.33,55.50,47.14; HR-MS(ESI) Calcd for C34H26N3OS[M]+:524.1791,found 524.1795。
2 结果与讨论
2.1 光敏剂PTZPPy与ClO-响应机制验证及其光物理性质
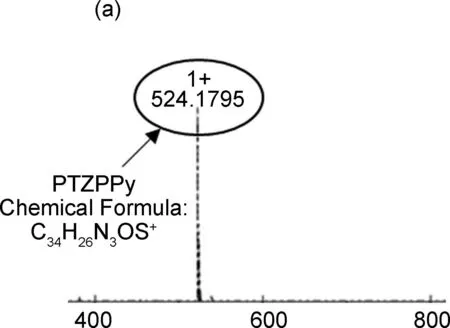
为探究光敏PTZPPy与ClO-的响应机理,将化合物PTZPPy(15.0 mg,2.8 μmol)加入1 mL乙腈中溶解,搅拌状态下逐滴加入NaOCl水溶液(其中含氯量5.5%~6.5%),使用365 nm紫外灯监测,直至观察到溶液由无荧光状态完全转变为黄色荧光状态。使用二氯甲烷(3×25.0 mL)萃取反应混合物,有机相用水洗涤,干燥,浓缩后得到棕色固体OPTZPPy。分别对PTZPPy与OPTZPPy进行高分辨质谱表征,如图3a所示,在m/z=524.1795处出现了PTZPPy的阳离子峰,如图3b所示,在m/z=570.1742处片段与OPTZPPy的阳离子峰一致,说明PTZPPy中的硫原子在ClO-的氧化下转化为亚砜结构OPTZPPy。同时对光敏剂PTZPPy与OPTZPPy的光谱性质进行了探究,将PTZPPy与OPTZPPy分别用乙腈配制成10 μM待测液后,测定二者的紫外-可见吸收光谱与荧光发射光谱(图3c),PTZPPy的最大吸收波长为475 nm,在300~800 nm范围内无明显荧光发射峰。相比较之下,OPTZPPy的最大吸收波长为410 nm,对应的最大发射波长为605 nm,显示出较大的Stokes位移(195 nm)。由于光敏剂PTZPPy与ClO-反应后,酚噻嗪中的硫原子被氧化亚砜,导致分子内电荷转移(ICT)效应减弱,荧光强度明显增加。
λ/nm
2.2 PTZPPy对ClO-的光谱响应
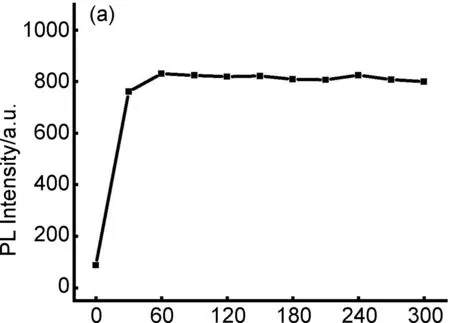
为确定PTZPPy与ClO-的最佳响应时间,在PTZPPy(10 μM)的PBS缓冲液(pH=7.4,PBS∶DMSO=99∶1,V∶V)中加入ClO-(1.0 mM),记录其在605 nm处的荧光强度变化。如图4a所示,随着孵育时间增加,605 nm处的荧光强度逐渐增强,1 min后荧光强度基本保持不变。说明能够在1 min内与ClO-完成响应。随后配制PTZPPy(10 μM)的PBS缓冲液(pH=7.4,PBS∶DMSO=99∶1,V∶V)并加入不同浓度的ClO-,记录荧光光谱变化,随着ClO-浓度的增加,溶液在605 nm处的荧光强度逐渐增强(图4b),并且ClO-的浓度在0~120 μM范围与605 nm处的荧光强度呈现良好的线性关系(图4c),线性方程y=4.607x+258.207,R2=0.999,说明PTZPPy具有较好的灵敏度和定量检测ClO-的能力。
Time/s
2.3 光敏剂PTZPPy的选择性及OPTZPPy稳定性
为验证PTZPPy特异性响应能力,向含有PTZPPy(5 μM)的PBS缓冲液中加入ClO-(100 μM)及其他干扰离子(100 μM)并分别测试其荧光光谱,如图5(a)所示,只有在ClO-存在时605 nm处显示出明显的荧光增强,此结果说明PTZPPy对ClO-的检测具有良好的特异性和抗干扰性,有助于观察生物体内ClO-在病理过程中的变化。为了验证PTZPPy在不同pH值下是否稳定,本文评估了其在不同pH值缓冲液中与ClO-的响应能力。如图5(b)所示,在pH=4~10范围内,PTZPPy对ClO-的响应基本稳定,表明PTZPPy能够应用于大多数生物环境。如图5(c)所示,使用20 mW cm-2的光照射OPTZPPy(5 μM)溶液,60 min后其荧光强度无明显变化,24 h后略有衰减,表明PTZPPy与ClO-响应后具有良好的光稳定性。
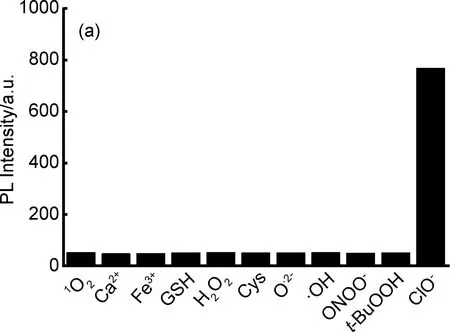
pH
2.4 PTZPPy和OPTZPPy的ROS生成能力及类型
为了进一步研究光敏剂PTZPPy和OPTZPPy的ROS产生能力,选择ROS指示剂2′,7′-二氯二氢荧光素二乙酸酯(2′,7′-Dichlorodihydrofluorescein diacetate,DCFH-DA)来验证二者在光照下产生的总ROS,如图6(a)所示,在20 mW cm-2的白光照射下,随着光照时间的增加,500~650 nm范围内的荧光逐渐增强。说明PTZPPy和OPTZPPy在光照下均能产生ROS。使用9,10-蒽二甲酰基-双(亚甲基)-二丙二酸(9,10-Anthracenediyl-bis(methylene)dimalonic Acid,ABDA)作为指示剂,测定了PTZPPy和OPTZPPy在光照下产生ROS的类型。ABDA被1O2氧化后会形成内过氧化物,吸光度下降,应用于II型ROS的检测。如图6(b)所示,随着照射时间的延长,PTZPPy和OPTZPPy的吸光度逐渐下降。说明PTZPPy和OPTZPPy在光照下,均能产生1O2且相较于临床上应用的光敏剂药物孟加拉玫瑰红(RB),能够更高效地产生1O2。使用二氢罗丹明123(DHR123)测试PTZPPy与OPTZPPy产生I型ROS能力,如图6(c)所示,添加PTZPPy与OPTZPPy后,随着照射时间的增加,DHR123荧光信号逐渐增强,加入清除剂VC后,随着时间的增加,荧光强度明显下降,说明PTZPPy与OPTZPPy具有产生I型ROS的能力。以上结果证明PTZPPy与OPTZPPy不仅具有产生ROS的能力,而且可以同时产生I型和II型ROS。
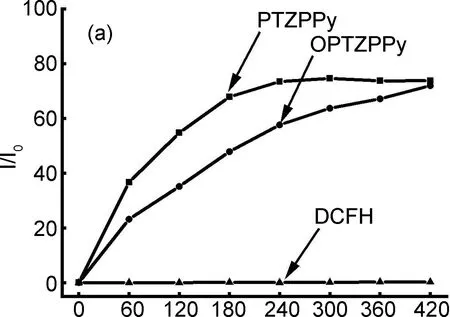
Time/s
2.5 抗肿瘤活性
采用CCK8法测试了PTZPPy与OPTZPPy对4T1细胞的光、暗毒性,将不同浓度的化合物加入到4T1细胞培养液中,孵育12 h后使用20 mW cm-2白光照射15 min,进一步孵育10 h后加入CCK8,2 h后使用酶标仪测定细胞液在450 nm处的吸光度。如图7所示,PTZPPy与OPTZPPy在黑暗条件下的细胞毒性相对较低,表明它们良好的生物相容性。相反,在白光照射下,细胞活力逐渐迅速下降,10 μM的PTZPPy与OPTZPPy均可导致大多数4T1细胞的死亡,说明PTZPPy与OPTZPPy均具有较好的PDT抗肿瘤活性。
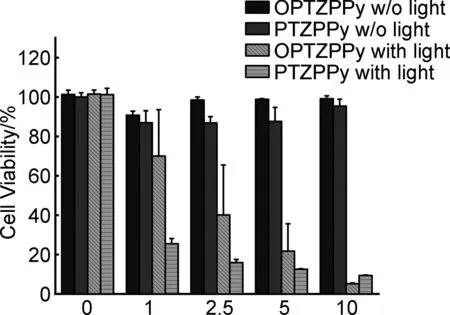
Concentration/μM
3 结论
本工作构建了一种基于酚噻嗪的ClO-响应型光敏剂PTZPPy,并将其应用于细胞水平上的光动力治疗研究。PTZPPy无荧光,当与ClO-反应后生成OPTZPPy,荧光强度明显增强,显示出一种荧光开启的效应,且具有较好的稳定性及较高的灵敏度。对PTZPPy及OPTZPPy的ROS产生能力测试结果表明:在光照条件下PTZPPy和OPTZPPy均能产生I型和II型2种类型的ROS,其中PTZPPy产生ROS以II型为主,OPTZPPy产生的ROS以I型为主。抗肿瘤活性结果表明,PTZPPy与OPTZPPy无光照条件下毒性较低,具有较好的生物相容性,在光照条件下具有良好的体外抗肿瘤活性。作为一种新的ClO-响应型光敏剂,PTZPPy在荧光引导的光动力治疗方面具有较大的应用潜力和研究价值。

