基于化学模式识别结合灰色关联度法的鲜地黄药材质量评价△
徐杰,姚晓璇,黄梦婷,黄瑶,潘玲,张正*
1.广东一方制药有限公司,广东 佛山 528244;
2.广东省中药配方颗粒企业重点实验室,广东 佛山 528244
鲜地黄为玄参科植物地黄Rehmannia glutinosaLibosch.的新鲜块根,秋季釆挖,除去芦头、须根及泥沙,具有清热生津、凉血止血的功效[1]。现代研究表明,鲜地黄在治疗上中焦温热病、消炎、抗菌、止血等方面疗效显著[2-3],其现代化制剂也越来越受到重视[4-5]。《中华人民共和国药典》(以下简称《中国药典》)2020 年版对鲜地黄仅进行了性状、鉴别项的要求,因此需要建立科学的鲜地黄质量综合评价体系。
灰色关联度分析是根据曲线间相似程度判断因素间的关联程度,可以为系统的发展变化态势提供量化的度量,基于“中药成分与中药质量是一种灰色关系”的认识,可以运用该方法评价药材质量[6]。近年来,灰色关联度法已广泛应用于中药质量综合评价领域[7-9]。本研究采集了河南、山西、河北的32 批鲜地黄药材,测定各批样品的总灰分、酸不溶性灰分、浸出物,以及梓醇、地黄苷D、铅、镉、砷、汞、铜含量,建立指纹图谱,通过化学模式识别结合灰色关联度法对不同产地鲜地黄进行综合质量评价,以期为鲜地黄药材质量评价与控制提供参考。
1 材料
1.1 仪器
Arc 型高效液相色谱仪、ACQUITY 型超高效液相色谱仪(美国Waters公司);Thermo ICAPQ型电感耦合等离子体质谱仪(美国Thermo Fisher Scientific公司);ME204E型分析天平、XP26型分析天平(瑞士Mettler-Toledo 公司);MiliQ Direct 8 型超纯水机(德国Merck Millipore公司)。
1.2 试药
对照品梓醇(批号:110808-201711,纯度:99.6%,中国食品药品检定研究院);地黄苷D(批号:ST11190120,纯度:98.0%,上海诗丹德标准技术服务有限公司);益母草苷(批号:17122601,纯度:99.6%,成都普菲德生物技术有限公司);色谱级甲醇、乙腈(德国默克股份有限公司);色谱级磷酸(天津市科密欧化学试剂有限公司);水为实验室自制超纯水。
32 批鲜地黄药材经广东一方制药有限公司孙冬梅主任中药师鉴定为玄参科植物地黄Rehmannia glutinosaLibosch.的新鲜块根,样品信息见表1。

表1 32批鲜地黄药材信息
2 方法与结果
2.1 灰分测定
按《中国药典》2020 年版通则2302 灰分测定法[10],测定32 批鲜地黄药材样品的总灰分和酸不溶性灰分,结果见表2。结果显示,以干燥品计,32批鲜地黄药材总灰分为1.5%~4.2%,均小于8%;32批鲜地黄药材酸不溶性灰分为0.1%~0.3%,均小于3%,表明收集的32 批鲜地黄药材均符合《中国药典》2020 年版地黄项下总灰分和酸不溶性灰分的限量要求。

表2 32批鲜地黄药材各指标测定结果
2.2 浸出物测定
按《中国药典》2020 年版通则2201 浸出物测定法第一法[10],测定32 批鲜地黄药材水溶性浸出物,结果见表2。结果显示,以干燥品计,32 批鲜地黄浸出物质量分数为84.7%~92.3%,均超过65%,符合《中国药典》2020 年版地黄项下浸出物的限量要求。
2.3 重金属及有害元素测定
按《中国药典》2020 年版通则2321 原子吸收分光光度法或电感耦合等离子体质谱法[10],测定32 批鲜地黄药材的重金属及有害元素,结果见表2。结果表明,32 批鲜地黄中铅、镉、砷、汞、铜的含量均符合《中国药典》2020 年版对重金属及有害元素的一般限量要求。
2.4 梓醇含量测定
2.4.1 供试品溶液的制备 取鲜地黄药材样品适量,切碎,取约2.0 g,精密称定,置具塞锥形瓶中,精密加入60%甲醇50 mL,称定质量,加热回流90 min,放冷,再称定质量,用60%甲醇补足减失的质量,摇匀,滤过,精密量取续滤液10 mL,蒸干,残渣用流动相溶解,转移至10 mL 量瓶中,加流动相定容至刻度,摇匀,用0.22 μm 的微孔滤膜滤过,取续滤液,即得。
2.4.2 对照品溶液的制备 精密称取梓醇对照品适量,加流动相溶解并定容,得到质量浓度为500.988 µg·mL-1的溶液,即得。
2.4.3 色谱条件 采用ZORBAX SB-C18色谱柱(150 mm×4.6 mm,5 μm);以甲醇-0.1%磷酸水溶液(1∶99)为流动相;检测波长为210 nm;流速为1.0 mL·min-1;柱温为30 ℃;进样量为10 μL。鲜地黄药材供试品溶液及梓醇对照品溶液的色谱图见图1。采用信噪比法计算梓醇的检测限为0.59 μg·mL-1,定量限为1.96 μg·mL-1。
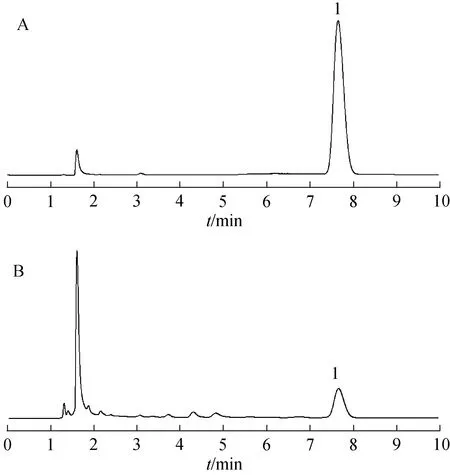
图1 梓醇对照品和鲜地黄药材样品的HPLC图
2.4.4 线性关系考察 精密吸取2.4.2 项下梓醇对照品溶液,分别加流动相稀释5、10、25、50 倍,摇匀,得不同质量浓度的梓醇对照品溶液。精密吸取上述不同质量浓度的梓醇对照品溶液10 μL,按
2.4.3 项下色谱条件进样测定。以对照品质量浓度为横坐标(X)、峰面积为纵坐标(Y),绘制标准曲线,回归方程为Y=2331X-4 895.4(r=1),表明梓醇质量浓度为10.020~500.988 μg·mL-1时与峰面积线性关系良好。
2.4.5 精密度试验 取鲜地黄药材供试品(S1)溶液,按2.4.3项下色谱条件连续进样测定6次,记录峰面积,6 次测定结果的RSD为0.29%,表明仪器精密度良好。
2.4.6 稳定性试验 取鲜地黄药材供试品(S1)溶液,分别在0、2、4、6、8、16、24 h,按2.4.3 项下色谱条件进样测定,记录梓醇峰面积,24 h 内供试品中梓醇峰面积的RSD为2.54%,表明供试品溶液在24 h 内稳定性良好。
2.4.7 重复性试验 分别取鲜地黄药材供试品(S1)6 份,按2.4.1 项下方法制备供试品溶液,按2.4.3 项下色谱条件进样测定,计算6 份供试品中梓醇含量的RSD为0.75%,表明该方法重复性良好。
2.4.8 加样回收率试验 取已知梓醇含量的鲜地黄药材供试品(S1)9 份,每份约1.0 g,精密称定,置于锥形瓶中,按高、中、低质量浓度分别加入梓醇对照品,按2.4.1 项下方法制备供试品溶液,按2.4.3 项下色谱条件进样测定,梓醇的加样回收率为100.87%,RSD为3.33%,表明该方法准确度良好。
2.4.9 梓醇含量测定 取32 批鲜地黄药材样品,分别按2.4.1项下方法制备供试品溶液,按2.4.3项下色谱条件进样测定,结果见表2。结果显示,32批鲜地黄药材梓醇质量分数为2.768%~5.876%,均值为4.090%,RSD为19.77%。
2.5 地黄苷D含量测定
2.5.1 供试品溶液的制备 取鲜地黄药材样品适量,切碎,取约2.0 g,精密称定,置具塞锥形瓶中,精密加入60%甲醇50 mL,称定质量,超声处理(250 W,频率40 kHz)30 min,放冷,再称定质量,用60%甲醇补足减失的质量,摇匀,滤过,精密量取续滤液10 mL,蒸干,残渣用流动相溶解,转移至10 mL 量瓶中,加流动相定容至刻度,摇匀,用0.22 μm 的微孔滤膜滤过,取续滤液,即得。
2.5.2 对照品溶液的制备 精密称取地黄苷D 对照品适量,加流动相溶解并定容,制成质量浓度为115.248 µg·mL-1的溶液,即得。
2.5.3 色谱条件 采用ZORBAX SB-C18色谱柱(150 mm×4.6 mm,5 μm);以乙腈-0.1%磷酸水溶液(5∶95)为流动相;检测波长为203 nm;流速为1.0 mL·min-1;柱温为30 ℃;进样量为10 μL。鲜地黄药材供试品溶液及地黄苷D 对照品溶液的色谱图见图2。采用信噪比法计算地黄苷D的检测限为0.17 μg·mL-1,定量限为0.58 μg·mL-1。

图2 地黄苷D对照品和鲜地黄药材样品的HPLC图
2.5.4 线性关系考察 精密吸取地黄苷D 对照品溶液适量,分别加流动相稀释4、10、25、50 倍,摇匀,得不同质量浓度的地黄苷D 对照品溶液。精密吸取上述不同质量浓度的地黄苷D 对照品溶液10 μL,按2.5.3 项下色谱条件进样测定。以对照品质量浓度为横坐标(X)、峰面积为纵坐标(Y),绘制标准曲线,回归方程为Y=5 563.7X-809.94(r=1),表明在地黄苷D质量浓度为2.305~115.248 µg·mL-1时与峰面积线性关系良好。
2.5.5 精密度试验 取鲜地黄药材供试品(S1)溶液,按2.5.3 项下色谱条件连续进样6 次,记录地黄苷D 的峰面积,6 次测定结果的RSD为0.38%,表明仪器精密度良好。
2.5.6 稳定性试验 取鲜地黄药材供试品(S1)溶液,分别在0、2、4、6、8、16、24 h 进样,按2.5.3 项下色谱条件进样测定,记录地黄苷D 峰面积,24 h内样品中地黄苷D峰面积的RSD为1.48%,表明供试品溶液在24 h 内稳定性良好。
2.5.7 重复性试验 取鲜地黄药材供试品(S1)6份,按2.5.1项下方法制备供试品溶液,按2.5.3项下色谱条件进样测定,6 份供试品地黄苷D 含量的RSD为0.38%,表明该方法重复性良好。
2.5.8 加样回收率试验 取鲜地黄药材供试品(S1)9份,每份约1.0 g,精密称定,置于锥形瓶中,按高、中、低质量浓度分别加入地黄苷D 对照品,按2.5.1项下方法制备供试品溶液,按2.5.3项下色谱条件进样测定,地黄苷D的加样回收率为98.11%,RSD为2.97%,表明该方法的准确度良好。
2.5.9 地黄苷D 含量测定 取32 批鲜地黄药材样品,分别按2.5.1 项下方法制备供试品溶液,按2.5.3 项下色谱条件进样测定,结果见表2。结果显示,32 批鲜地黄药材地黄苷D 质量分数为0.164%~0.432%,均值为0.288%,RSD为19.75%。
2.6 鲜地黄药材指纹图谱的建立
2.6.1 供试品溶液的制备 取鲜地黄药材样品(S1)适量,切碎,取约2.0 g,精密称定,置具塞锥形瓶中,精密加入60%甲醇50 mL,称定质量,加热回流90 min,放冷,再称定质量,用60%甲醇补足减失的质量,摇匀,滤过,精密量取续滤液10 mL,蒸干,残渣用0.1%磷酸水溶液溶解,转移至10 mL量瓶中,加0.1%磷酸水溶液定容至刻度,摇匀,用0.22 μm的微孔滤膜滤过,取续滤液,即得。
2.6.2 对照品溶液的制备 精密称取对照品梓醇、地黄苷D、益母草苷适量,加0.1%磷酸水溶液溶解并定容,制成混合对照品溶液。
2.6.3 色谱条件 Waters ACQUITY HSS T3 色谱柱(100 mm×2.1 mm,1.8 μm);流动相为乙腈(A)-0.1% 磷酸水溶液(B),梯度洗脱(0~5 min,100%B;5~7 min,100%~95%B;7~10 min,95%B;10~16 min,95%~89%B;16~18 min,89%~84%B;18~35 min,84%~70%B);检测波长为203 nm;流速为0.3 mL·min-1;柱温为30 ℃;进样量为2 μL。
2.6.4 方法学考察
2.6.4.1 精密度试验 取鲜地黄药材供试品(S1)溶液,按2.6.3 项下色谱条件连续进样6 次,以地黄苷D 相应的峰(4 号峰)为S 峰,计算各色谱峰与S 峰的相对保留时间和相对峰面积的RSD 分别为0~0.29%、0.35%~0.94%,表明仪器精密度良好。
2.6.4.2 稳定性试验 取鲜地黄药材供试品(S1)溶液,分别在0、2、4、8、12、24 h 进样测定,计算24 h 内供试品溶液各色谱峰与S 峰的相对保留时间和相对峰面积的RSD 分别为0~1.87%、0.51%~2.94%,表明供试品溶液在24 h 内稳定性良好。
2.6.4.3 重复性试验 取鲜地黄药材样品(S1)6份,按2.6.1项下方法制备供试品溶液,按2.6.3项下色谱条件进样测定,计算6 份供试品中各色谱峰与S 峰的相对保留时间和相对峰面积的RSD 分别为0~0.95%、1.27%~3.12%,表明该方法重复性良好。
2.6.5 指纹图谱的建立及色谱峰指认 取32 批鲜地黄药材样品,按2.6.1 项下方法制备供试品溶液,按2.6.3 项下色谱条件进样检测,记录各特征峰峰面积值并进行量化处理(峰面积/称样量),结果见表3。采用“中药色谱指纹图谱相似度评价系统”(2012 版)对采集的色谱信息进行数据处理,生成鲜地黄药材对照指纹图谱,并确立了10 个共有峰,见图3。通过对照品比对,指认了其中3个成分,分别为梓醇、地黄苷D、益母草苷,结果见图4。

图3 32批鲜地黄药材UPLC指纹图谱
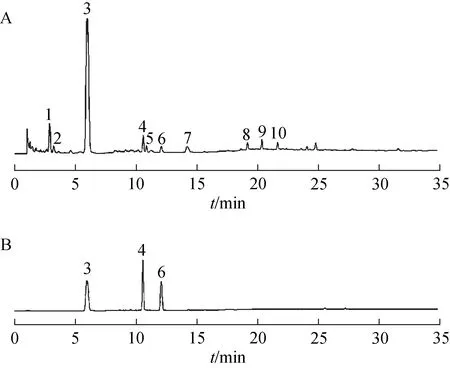
图4 鲜地黄药材样品及混合对照品溶液的色谱图
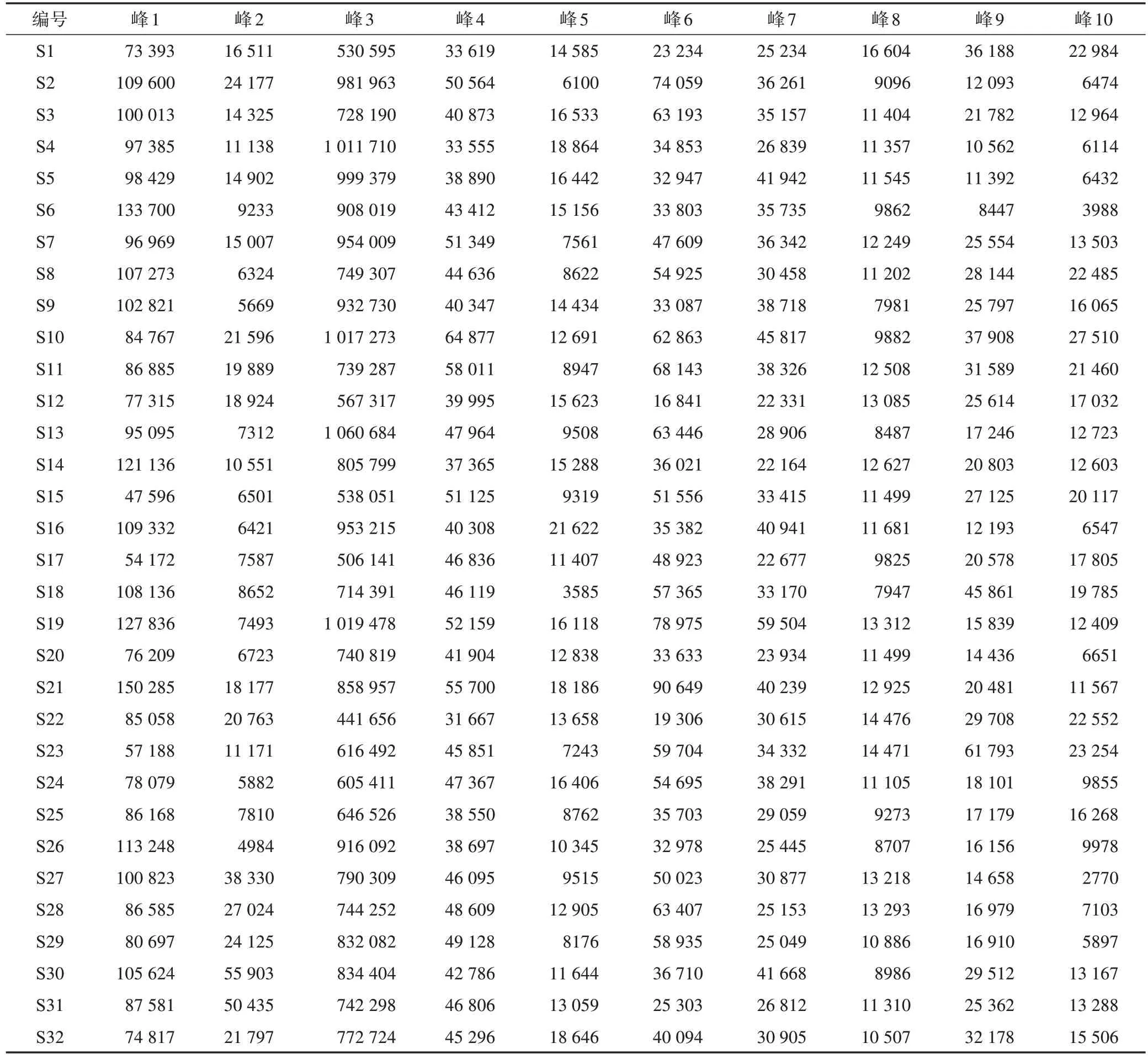
表3 32批鲜地黄药材各特征峰峰面积/称样量
2.6.6 相似度评价 采用“中药色谱指纹图谱相似度评价系统”(2012 版)计算32 批鲜地黄药材指纹图谱的相似度,结果显示,32 批鲜地黄药材的指纹图谱与对照指纹图谱的相似度均大于0.995,说明各产地鲜地黄药材指纹图谱差异不明显。
2.7 不同产地鲜地黄药材多指标成分的聚类分析(HCA)
将32 批鲜地黄药材的总灰分,酸不溶性灰分,浸出物、重金属及有害元素、梓醇、地黄苷D 质量分数及10 个特征峰的峰面积值作为变量,形成数据矩阵,导入SPSS 20.0 软件,以离均差平方和法为聚类方法、欧氏距离平方法为测量距离方法,进行HCA。聚类结果见图5,当距离为15 时,32 批鲜地黄药材可分为4 类。S2、S4~S6、S9、S14、S16、S20、S26~S32 聚为一类,S7、S10、S11、S13、S19、S21 聚为一类,S1、S12、S22 聚为一类,S3、S8、S15、S17、S18、S23~S25聚为一类。总体上未见明显的产地分类聚集现象,河南、河北、山西的鲜地黄药材整体质量较为接近。

图5 32批鲜地黄HCA
2.8 不同产地鲜地黄药材多指标成分的主成分分析(PCA)
将32 批鲜地黄药材的总灰分,酸不溶性灰分,浸出物、重金属及有害元素、梓醇、地黄苷D 的质量分数及10 个特征峰的峰面积值作为变量,采用SIMCA 14.1 软件对32 批鲜地黄药材进行PCA,以特征值>1为评判标准,共提取7 个主成分,累积方差贡献率为80.6%。提取方差贡献率最高的主成分PC1、PC2 绘制得分散点图,见图6。结果显示,32批鲜地黄药材聚类结果与2.7 项下HCA 结果基本一致。
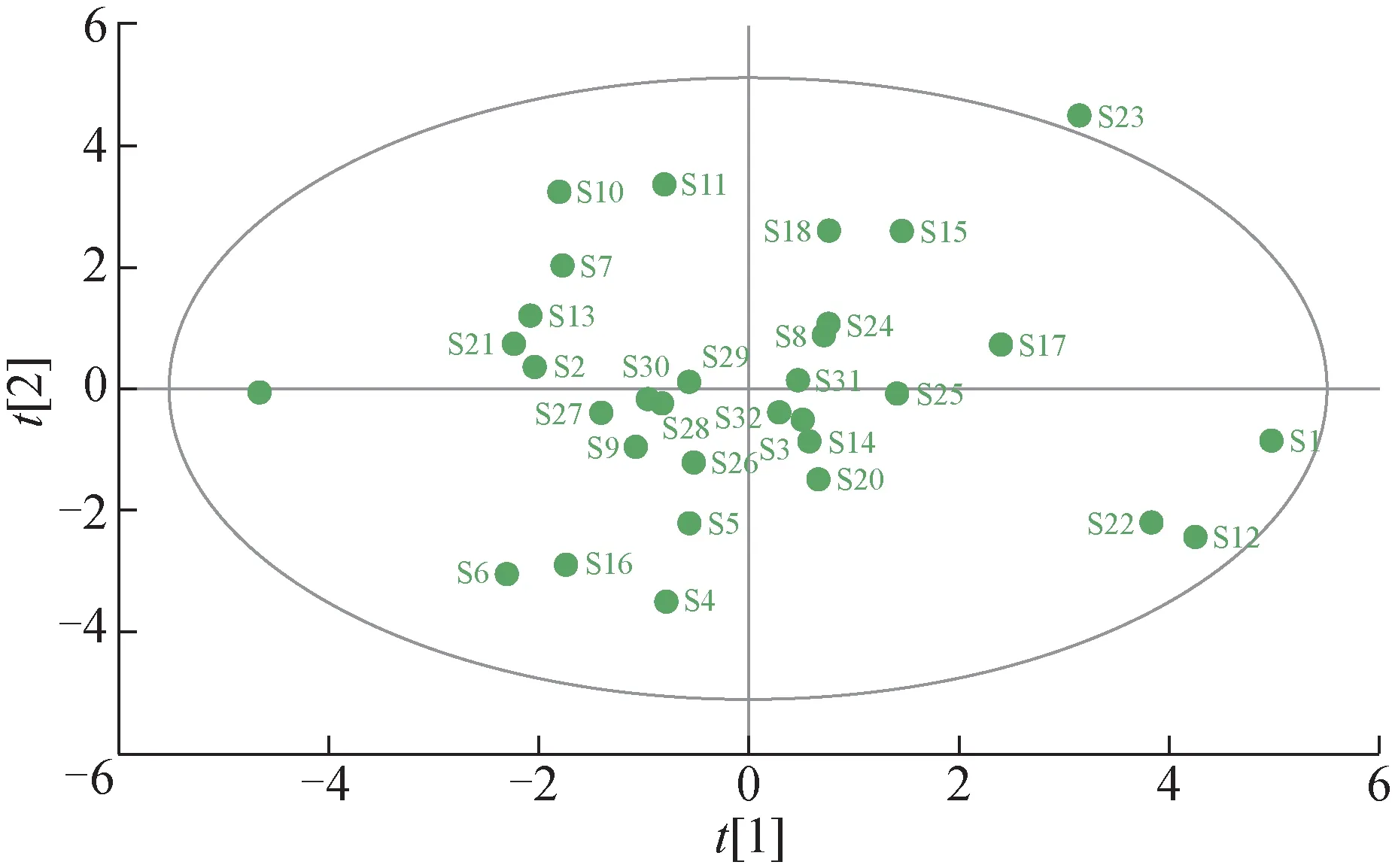
图6 32批鲜地黄PCA得分
2.9 不同产地鲜地黄药材多指标成分的正交偏最小二乘法-判别分析(OPLS-DA)
将32 批鲜地黄药材的总灰分,酸不溶性灰分,浸出物、重金属及有害元素、梓醇、地黄苷D 的质量分数及10 个特征峰的峰面积值作为变量,采用SIMCA 14.1软件对32批鲜地黄药材进行OPLS-DA,得分图见图7。分析OPLS-DA 模型中的变量重要性投影(VIP),结果见图8。对不同产区的鲜地黄药材各指标的VIP 值进行排列,选择VIP 值>1 的指标作为区分不同产地鲜地黄药材的主要差异性成分。结果显示,峰3(VIP 值为1.540)、峰2(VIP 值为1.533)、峰1(VIP值为1.366)、梓醇质量分数(VIP值为1.298)、浸出物质量分数(VIP值为1.248)、峰10(VIP值为1.216)、总灰分(VIP值为1.203)、峰9(VIP值为1.183)均大于1,说明以上指标对不同产地鲜地黄药材的分类影响较大,而其他指标对鲜地黄药材产地的区分影响较小。

图7 32批鲜地黄OPLS-DA

图8 32批鲜地黄VIP分析(±s,n=32)
2.10 灰色关联度分析
2.1 0.1 无量纲化处理 以32 批鲜地黄药材的总灰分,酸不溶性灰分,浸出物、梓醇、地黄苷D、铅、镉、砷、汞、铜的质量分数及指纹图谱10 个共有峰的峰面积值作为鲜地黄药材质量综合评价指标,按公式(1)采用均值法建立矩阵并进行无量纲化处理,结果见表4。
式中,i为待评样本数(i=0,1,2,3……m),k为评价指标数(k=1,2,3……n),在本研究中,m=32,n=20。
2.1 0.2 关联系数的确定 比较数列值与相对应的参考数列值差的绝对值,按公式(2)计算各指标的关联系数,ρ的取值通常为0.5,关联系数反映了待评指标与该指标理想值的吻合程度,越大说明越接近该指标的理想值,结果见表5。

表5 32批鲜地黄参评材料各质量指标的关联系数
2.1 0.3 关联度和权重的确定 按公式(3)、公式(4)计算各指标的关联度和权重,总灰分,酸不溶性灰分,浸出物、梓醇、地黄苷D、铅、镉、砷、汞、铜的质量分数,峰1~10 的峰面积值关联度分别为0.79、0.85、0.98、0.80、0.78、0.72、0.77、0.72、1.00、0.74、0.75、0.44、0.84、0.80、0.72、0.67、0.69、0.79、0.53、0.65,权重分别为0.05、0.06、0.06、0.05、0.05、0.05、0.05、0.05、0.07、0.05、0.05、0.03、0.06、0.05、0.05、0.04、0.05、0.05、0.03、0.04。
式中,r(k)为关联度,ω(k)为权重。
2.1 0.4 灰色综合评价值的确定 按公式(5)计算灰色关联度并对所得值大小进行排序,结果见表6。32 批鲜地黄药材灰色关联度分析结果表明,关联度排 序为S10>S21>S11>S30>S32>S6>S2>S16>S27>S4>S1>S28>S19>S29>S18>S20>S9>S5>S8>S7>S22>S23>S31>S13>S3>S26>S15>S17>S24>S25>S12>S14。河南产鲜地黄药材综合质量排名比较分散,最优的批次为S10,产自河南省焦作市武陟县;河北产的3 批鲜地黄药材有2 批分别排名第4、第5;山西产的3 批鲜地黄药材排名比较接近,排名第9、第12、第14。关联度为0.036~0.042,关联度差异为0~13.89%,说明32 批鲜地黄药材总体质量差异并不大,这与HCA 和PCA 的结果一致。

表6 32批鲜地黄参评材料的灰色关联度、排名及关联度差异
式中,r′(i)为灰色关联度。
3 讨论
《中国药典》2020 年版地黄项下规定了生地黄梓醇和地黄苷D 的含量限度,考虑鲜地黄的水分含量远高于生地黄,故本研究在《中国药典》2020 年版的基础上考察了不同提取溶剂、提取方式、提取时间及溶剂用量对鲜地黄梓醇和地黄苷D 提取效率的影响。结果表明,采用60%甲醇回流提取1.5 h,鲜地黄药材梓醇的提取效率最高;采用60%甲醇超声处理0.5 h,鲜地黄药材地黄苷D的提取效率最高。
本研究建立了鲜地黄药材UPLC指纹图谱,标定了10 个共有峰,并对梓醇、地黄苷D 和益母草苷色谱峰进行了指认。研究表明,梓醇为地黄环烯醚萜苷类成分,是发挥降血糖生物活性的主要药效物质基础[11],可以调节脂肪细胞的糖脂代谢(通过活化位于肾上腺髓质的肾上腺受体、促进β-内啡肽释放、提高葡萄糖运转蛋白-4 的表达)从而提高葡萄糖转运率、增加葡萄糖利用率、抑制糖异生、降低链尿佐菌素诱导的糖尿病大鼠血糖[12-13]。研究发现,地黄苷D 可能是地黄发挥抗抑郁作用的重要物质基础,该成分可有效缓解由高浓度皮质酮诱导的PC-12 细胞损伤,其作用机制可能为提高脑源性神经营养因子(BDNF)表达,并通过BDNF-酪氨酸激酶受体B(TrkB)通路发挥抗凋亡作用,最终保护神经细胞,发挥抗抑郁作用[14-15]。此外,地黄中的益母草苷可有效抑制食管癌细胞的增殖,细胞凋亡明显且细胞周期出现G2/M 期阻滞[16]。可见,本研究构建的指纹图谱可表征鲜地黄的主要活性成分,能为鲜地黄药材及其制剂的整体质量评价提供参考。OPLS-DA结果表明,指纹图谱中峰1~3、9、10 的峰面积均为影响各产地鲜地黄药材质量差异的主要因素,根据已指认的成分(峰3、峰4、峰6)初步判断上述色谱峰表征的可能为环烯醚萜苷类成分,是地黄的主要活性成分,后续研究需对以上共有峰进行进一步归属。
HCA 结果表明,32 批鲜地黄药材聚为4 类,但未见明显的产地聚集现象。分析原因为本研究收集的32 批鲜地黄药材产地较为集中,基本处在河南、河北、山西的交界处,经纬度相差不大,且均为人工种植,因此质量较为接近。由于采样、保鲜、运输、储藏条件的限制,本研究收集的鲜地黄药材样品未能覆盖大部分主产区,同时本研究建立的鲜地黄药材特征图谱主要表征的是鲜地黄药材中极性较大的环烯醚萜苷类成分,对于地黄中另一类活性成分苯乙醇苷类成分并未能有效表征,因此关于不同产地鲜地黄药材质量优劣评价的结果是否具有更广泛的代表性,还需要后续进一步扩大样本量进行系统深入的研究。
[利益冲突]本文不存在任何利益冲突。

