第二类医疗器械重组胶原蛋白液体敷料的性能测试
王晓晨 张璐 闫芳 王亚琳 柴谦 山东省食品药品审评查验中心 (山东 济南 250014)
内容提要: 重组胶原蛋白液体敷料进行第二类医疗器械注册申报时,按照《重组胶原蛋白创面敷料注册审查指导原则》进行关键性能测试。文章对产品的有效成分进行鉴别和含量检测、并对是否体外透皮吸收、成膜性、膜微观结构、孔隙率及平均孔径等进行性能测试,以此评价该液体创面敷料在注册申报第二类医疗器械时的安全性和有效性。结果表明,采用2,2’-联喹啉二羧酸(BCA)法测得该敷料所含有效成分(以重组胶原蛋白为有效成分计)含量平均值为2.01mg/mL,在0.5、1、2、6、12h时均未透过巴马香猪的新鲜离体缺损皮肤,判定不可被人体吸收。该液体敷料的成膜性良好,37°C下干燥1min后形成一层肉眼可见的膜状物。控制成膜厚度为3mm,45°C下放置12h干燥,在扫描电子显微镜下观察的膜微观形态,分别放大400倍和5000倍的膜状物表面分别呈现出不同孔隙状的物理屏障保护层,经计算孔隙率为7.645%,平均孔径为1.414μm。该液体敷料适用于切割伤等非慢性创面的护理,具有广阔的临床使用价值和市场前景。
在意外伤害、外科手术等多种原因造成的真皮浅层及其以上的浅表性小创口、擦伤中,创面敷料能否形成屏障保护或为创面愈合提供良好的护理基础,一直是临床应用急需考虑的问题[1,2]。重组胶原蛋白(Recombinant Collagen Protein,RCP)是近年来关注度较高的新兴生物材料,具有良好的人体同源性、亲水性和细胞黏附性,可制备成液体、凝胶、海绵等不同型式的创面敷料[3-5]。RCP创面敷料进行第二类医疗器械注册申报时,需符合国家药品监督管理局发布的《重组胶原蛋白创面敷料注册审查指导原则》[6]的关键性能,制定出产品技术要求,进行的研究能证明敷料在非慢性创面形成物理屏障作用,以保证医疗器械上市注册的安全性和有效性。本文测试了RCP液体敷料的有效成分鉴别和含量、是否体外透皮吸收、成膜性、膜微观结构、孔隙率及平均孔径等性能,以此评价该液体创面敷料在注册申报第二类医疗器械时的安全性和有效性,为各省的药品监管机构医疗器械审评审批人员、医疗器械生产研发人员、注册申请人等提供一些RCP敷料产品的数据参考和信息评估。
1.材料与方法
1.1 一般材料
试验起止时间:2022年1月~2023年10月。
原料试剂:重组胶原蛋白液体敷料(Recombinant Collagen Protein Liquid Dressing,RCPLD),实验室自制;重组人源胶原蛋白参比品(SYB),批号DA2290S009,江苏江山聚源生物技术有限公司;胰蛋白酶(Trypsin)(测序级),批号AS01589,Promega公司;生理盐水,批号20221514,信合援生制药股份有限公司;BSA牛血清白蛋白、BCA蛋白浓度检测试剂盒,批号均为P0011,碧云天生物技术有限公司。
仪器设备:高效液相色谱仪,型号Ultimate 3000,Thermo Fisher Scientific公司;透皮扩散仪,型号TK-12D,上海玉研科学仪器有限公司;多功能酶标仪,型号SpectraMax M2e,美谷分子仪器(上海)有限公司电热恒温培养箱,型号DNP-9082,上海精宏实验设备有限公司;扫描电子显微镜,型号SUPRA 55,德国蔡司Zeiss公司。
1.2 方法
1.2.1 鉴别试验
参考《中华人民共和国药典》[7](2020版)第四部通则3405通则肽图检查法的第一法“胰蛋白酶裂解-反相高效液相色谱法”进行测定。
1.2.2 体外透皮试验
巴马香猪经麻醉剃毛、常规消毒后,在背部脱毛部位用无菌针头或手术刀片划切,制备类似“井”字形创面,以渗血为宜,剔除皮下脂肪及组织冲净为离体猪皮创面模型(见图1)[8-11]。将其固定于透皮吸收扩散仪上,角质层朝上,真皮层与接收池内接收液完全接触,设定水浴温度为32°C,磁力搅拌子作用于接收液中,转速100r/min,向接收池内注满预温32°C±1°C的生理盐水8mL,排尽气泡。扩散液为受试物,接收池容积为8mL,接收液为生理盐水。皮肤涂覆面积为1.8cm2。

图1.新鲜离体巴马香猪创面模型
取1mLRCPLD作为试验组,均匀覆盖离体皮肤,每组设三个平行组,设置1mL生理盐水为对照组。参照有关暴露时间的规定,同时考虑到皮肤完整性超过24h就会变差,因此于第0.5、1、2、6、12h用注射器吸取全部接收液,采用2,2’-联喹啉二羧酸(BCA)法定量分析RCP含量,作为敷料产品有效成分是否被人体吸收的判断依据[8,12]。
1.2.3 成膜测试
吸取RCPLD约2~3滴均匀涂布于载玻片上,在37°C恒温箱中放置1min后翻转载玻片观察。以纯化水组做对照。肉眼观察是否能附着在载玻片上,且能否在载玻片上形成膜状物。
1.2.4 扫描电子显微镜和孔隙率测试
取RCPLD倒入底部平整的直径为3.8cm的干燥培养皿中,控制厚度为3mm,在45°C下放置12h待干燥、成膜。用扫描电子显微镜分别放大400倍和5000倍,观察以上条件形成的RCPLD膜的微观结构,测试孔隙率和平均孔径。
2.结果
2.1 鉴别试验结果
RCPLD主要特征肽段相对比例(响应强度)与参比品(SYB)基本一致。见图2。

图2.RCPLD 与参比品(SYB)主要特征肽段相对比例(响应强度)(注:2a.RCPLD;2b.参比品)
2.2 体外透皮试验结果
2.2.1 BCA法蛋白定量标准曲线
蛋白浓度线性检测范围为0~1mg/mL。标准曲线的制备是将蛋白标准品BSA 按照0、1、2、4、8、12、16、20μL依次加入96孔板中,然后每个孔依次加入20、19、18、16、12、8、4、0μL生理盐水,使其体积补足到20μL,按照BCA法处理后测定562nm处的吸光度,并以吸光度为横坐标,浓度(mg/mL)为纵坐标,绘制标准工作曲线,得回归方程为Y=1.7051X-0.1873,R2=0.9991。见图3。

图3.BSA 标准曲线(0~1mg/mL)
2.2.2 质控样品考察
以浓度为0.50mg/mL的BSA为质控样品,设置3个平行样品,在同一批次内进行测定,代入随行标准曲线求算测定浓度,试验结果见表1,平均值0.51mg/mL。
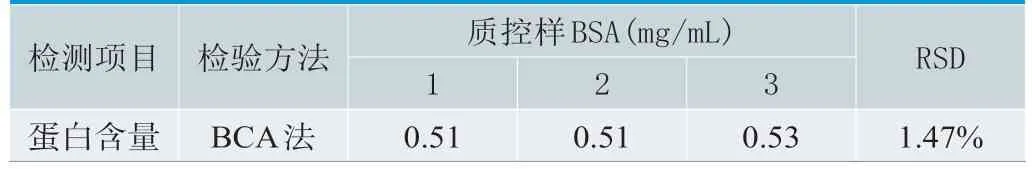
表1.质控样BSA胶原蛋白含量
2.2.3 RCPLD中胶原蛋白含量测定
将RCPLD稀释后检测胶原蛋白含量。试验结果见表2,RCPLD中胶原蛋白含量平均值为2.01mg/mL。

表2.验样RCPLD胶原蛋白含量
2.2.4 RCPLD体外透皮结果
采用BCA法测定RCPLD中胶原蛋白含量的方法灵敏度高,准确度好,在20~1000μg/mL浓度范围内有良好的线性关系,作用不同时间后接收液中胶原蛋白含量见表3,可以看出,不同透皮时间,生理盐水组和受试物组接收液中蛋白含量均增加,与对照组相比,受试物组的蛋白含量增加无统计学意义(P>0.05)。在0.5、1、2、6、12h时均未透过离体缺损皮肤。
表3.接收液中累计蛋白含量对比(n=3,±s,mg)
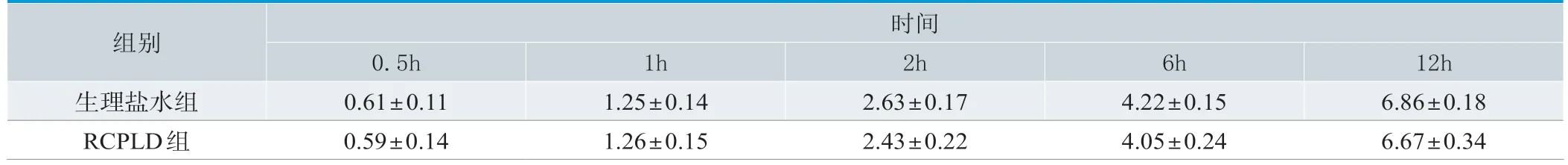
表3.接收液中累计蛋白含量对比(n=3,±s,mg)
组别时间0.5h 1h 2h 6h 12h生理盐水组0.61±0.11 1.25±0.14 2.63±0.17 4.22±0.15 6.86±0.18 RCPLD组0.59±0.14 1.26±0.15 2.43±0.22 4.05±0.24 6.67±0.34
体外透皮试验结果显示,生理盐水组接收液中检测出蛋白,认为来自离体皮肤,表明离体状态下皮肤中胶原蛋白有渗出。RCPLD组接收液中蛋白含量增加,但增加量与对照组相比差异无统计学意义(P>0.05),进一步表明RCPLD组接收液中蛋白来自离体皮肤。
2.3 成膜测试结果
分别取2、3滴RCPLD和纯化水均匀地涂抹于载玻片上,在37°C恒温箱1min后成膜对比图(见图4)。从试验结果可见,RCPLD溶液可附着在载玻片上并在载玻片上形成一层透明的膜状物,具备成膜性能。

图4.RCPLD 和纯化水在37˚C 恒温箱1min 后成膜对比图(注:4a.RCPLD 和纯化水涂覆载玻片的情况对比图;4b.试验条件下RCPLD 涂覆后形成膜状物;4c.试验条件下纯化水涂覆后的残留)
2.4 扫描电子显微镜和孔隙率测试结果
试验结果显示,45°C下干燥12h形成半透明RCPLD膜,可用镊子取下。其微观结构不是一个平滑表面,均呈多孔网状的纤维结构(见图5)。对RCPLD膜孔隙率和孔径的测试结果为,孔隙率为7.645%,孔径平均为1.414μm。由此可见,RCPLD具有一定的锁水性(结合水后相分离均匀)、机械性能及热稳定性。

图5.扫描电子显微镜下放大400 倍(5a)和放大5000 倍(5b)的RCPLD 成膜图像
3.讨论
RCP敷料的用途主要在于促进伤口愈合,增强受损皮肤的修复能力。为了模拟真实条件下RCP透皮吸收情况,选用具有浅表性伤口的猪皮作为离体供试皮肤。机械性伤口是各种外力作用的结果,根据受伤的深度又分为浅表性或上皮性损伤伤口、穿透性伤口、复合伤口。其中浅表性或上皮性损伤伤口是指伤口累及表皮层,因表皮具有再生能力,愈合后一般无瘢痕,如Ⅰ度烧伤或烫伤伤口、中厚皮片供皮区均可视为浅表性伤口,这类浅表性伤口为RCP敷料主要修复类型[13,14]。
本文对RCPLD,分别进行了有效成分含量、是否透皮吸收、成膜性、膜微观结构、孔隙率及平均孔径的性能测试。选择巴马香猪的新鲜离体缺损皮肤为测试模型,采用BCA法设定0.5、1、2、6、12h,测得该创面敷料所含胶原蛋白含量平均值为2.01mg/mL,均未透过测试模型,因此判定该敷料不可被人体吸收。此外37°C下干燥1min后该敷料能形成一层肉眼可见的膜状物,成膜性良好。在控制成膜厚度为3mm,45°C条件下放置12h干燥,观察扫描电子显微镜下放大400倍和5000倍的膜状物表面分别呈现出不同孔隙状的物理屏障保护层,测得孔隙率为7.645%,平均孔径为1.414μm。RCPLD进行第二类医疗器械注册申报时,符合了《重组胶原蛋白创面敷料注册审查指导原则》[6]的关键性能要求,通过以上对第二类医疗器械上市注册的安全性和有效性进行的相关测试,能证明该敷料形成物理屏障起到屏障修护作用,适用于切割伤、擦伤、浅表创口等非慢性创面的覆盖和护理。本文的测试结果可以为各省药品监管机构医疗器械审评审批人员、医疗器械生产研发人员、注册申请人等提供一些较为直观的数据参考,同时对RCP创面敷料产品的注册申报信息进行科学合理的评估提供一些帮助。

