二维斑点追踪技术评价代谢综合征患者右室收缩功能及其与心外膜脂肪厚度的关系
刘姝靖 万富鑫 吴 丹 马 鑫 潘 璐 井一淑 王 琴
代谢综合征(metabolic syndrome,MS)是一组以腹型肥胖、高血压、糖代谢异常及脂代谢异常为特点的复杂临床症候群,是导致心血管疾病的重要危险因素[1]。随着生活水平的提高,我国MS 的发病率呈逐年上升趋势。既往研究[2]表明,MS 会导致左室收缩功能障碍,且早期准确评价右室收缩功能对预防不良心血管事件发生和预后有着重要意义[3]。因此,早期评价MS 患者右室收缩功能至关重要。然而常规超声心动图在评价亚临床右室收缩功能障碍方面存有一定局限。二维斑点追踪技术(two-dimensional speckle tracking imaging,2D-STI)较常规超声心动图能更敏感、准确地评价右室收缩功能。研究[4]表明,内脏脂肪过度积累是MS 心肌收缩功能障碍的重要机制之一。近年来,心外膜脂肪组织被提议可用于评价内脏脂肪厚度,其释放的致动脉粥样硬化因子肿瘤坏死因子-α[5]会导致心脏形态和功能的改变。应用常规超声心动图能够测量心外膜脂肪厚度(epicardial fat thickness,EAT),且与MRI 测量的EAT有良好相关性[6]。基于此,本研究应用2D-STI 评价MS 患者右室收缩功能,并分析其与EAT 的关系,旨在为临床早期检测MS 患者亚临床右室收缩功能障碍,以及预测MS 患者右室收缩功能受损风险提供新的参考指标。
资料与方法
一、研究对象
选取2022 年9 月至2023 年5 月在宁夏医科大学总医院就诊的65 例MS 患者(MS 组),男38 例,女27 例,年龄30~52 岁,平均(42.52±5.77)岁。MS 诊断参考《中国2 型糖尿病防治指南(2020 年版)》[7]:①腹型肥胖(即中心型肥胖),腰围≥90 cm(男)或85 cm(女);②高血糖,空腹血糖(Glu)≥6.1 mmol/L 或糖负荷后2 h 血糖≥7.8 mmol/L 和/或已确诊为糖尿病并接受治疗者;③高血压(血压≥130/85 mmHg,1 mmHg=0.133 kPa)和/或已确诊为高血压并接受治疗者;④甘油三酯(TG)≥1.70 mmol/L;⑤高密度脂蛋白胆固醇(HDL-C)<1.04 mmol/L。上述条件满足3 项及以上即可诊断为MS。纳入标准:符合MS 诊断标准且年龄>18 岁。排除标准:先天性心脏病、心肌梗死、心肌病、慢性肺部疾病、严重心力衰竭、肝肾功能衰竭、心电图异常,以及经胸超声心动图显示不佳影响分析者等。另选同期性别及年龄与之匹配的健康志愿者35例作为对照组,男18例,女17例,年龄30~49 岁,平均(40.37±4.59)岁;既往无心肺疾病且心电图、超声心动图及实验室检查均正常。本研究经医院医学伦理委员会批准,所有研究对象均知情同意。
二、仪器与方法
1.常规超声心动图检查及图像分析:使用GE Vivid E95彩色多普勒超声诊断仪,M5s探头,频率1.4~4.6 MHz;配备EchoPAC 204AFI RV 软件。受检者取左侧卧位,于胸骨旁左室长轴切面常规测量右室流出道近端内径(RVOT prox),于心尖四腔心切面测量右室基底部内径(RV-B)、右室中部内径(RV-M)、右室长径(RV-L)、右室舒张末期面积和收缩末期面积,计算面积变化率(FAC);脉冲多普勒测量三尖瓣口舒张早、晚期峰值流速(E、A),计算E/A;将取样线置于三尖瓣环处,组织多普勒测量三尖瓣环侧壁舒张早期峰值运动速度(e’)、三尖瓣环收缩期峰值速度(S’),计算E/e’;M 型取样线置于三尖瓣环处测量三尖瓣前叶瓣环收缩期位移(TAPSE);选取胸骨旁左室长轴切面,以主动脉环和室间隔为解剖标记,确保测量方向与右室游离壁垂直,于收缩末期测量右室游离壁外EAT(图1)。采集以右室为主的四腔心切面图像,并储存5 个心动周期,将图像导入工作站。应用EchoPAC 204AFI RV 软件进行分析,手动标记心内膜点的位置,自动获取右室整体纵向应变(RVGLS)、右室游离壁应变(RVFWS)。图像采集均由同一经验丰富的高年资超声医师完成;后处理分析由2 名斑点追踪分析经验丰富的超声医师完成;所有参数均重复测量3 次取平均值。
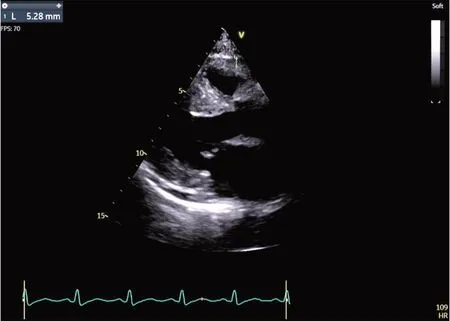
图1 EAT测量示意图
2.临床资料收集:获取心率及各代谢因素,其中各代谢因素包括年龄、性别、体质量指数(BMI)、腰围身高比(WtHR)、收缩压、舒张压、空腹血糖(Glu)、TG、HDL-C、低密度脂蛋白胆固醇(LDL-C)、总胆固醇(TC)。
3.一致性检验:从所有研究对象随机抽取20 例,再次进行2D-STI 图像分析获取RVGLS、RVFWS 进行一致性检验。
三、统计学处理
应用SPSS 26.0 统计软件,采用Shapiro-Wilk 检验计量资料的正态性,正态分布的计量资料以x±s表示,两组比较采用独立样本t检验;非正态分布的计量资料以M(Q1,Q3)表示,两组比较采用Mann-WhitneyU检验。计数资料以例或率表示,两组比较采用χ2检验。相关性分析采用Pearson 或Spearman 相关分析法。应用多元线性回归分析RVFWS 的独立影响因素;采用Bootstrap 自助抽样法分析临床指标是否介导EAT 与RVFWS 之间的关联。一致性检验采用组内相关系数(ICC)进行评估。P<0.05 为差异有统计学意义。
结果
一、两组心率及各代谢因素比较
与对照组比较,MS 组BMI、收缩压、舒张压、WtHR、Glu、TG、LDL-C、TC 均增高,HDL-C 减低,差异均有统计学意义(均P<0.05);两组年龄、性别、心率比较差异均无统计学意义。见表1。
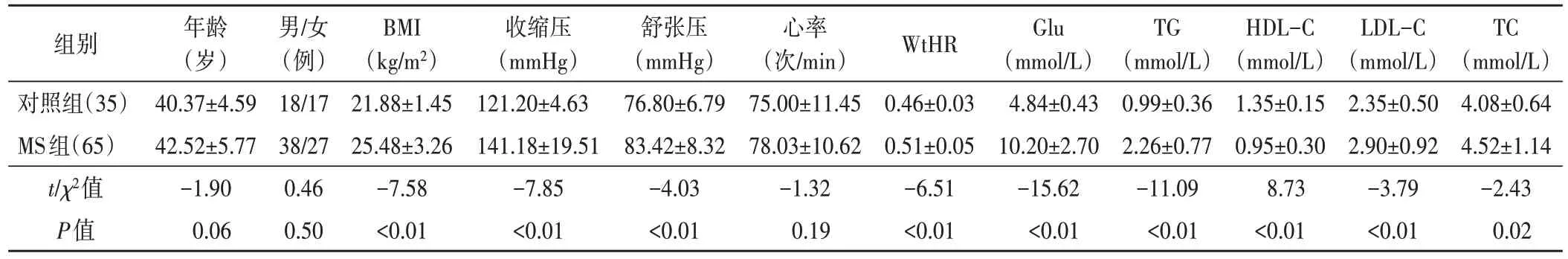
表1 两组心率及各代谢因素比较
二、两组常规超声心动图参数及2D-STI参数比较
与对照组比较,MS 组E/e’、EAT 均增高,TAPSE、RVGLS、RVFWS 均减低,差异均有统计学意义(均P<0.05);两组其余参数比较差异均无统计学意义。见表2和图2。
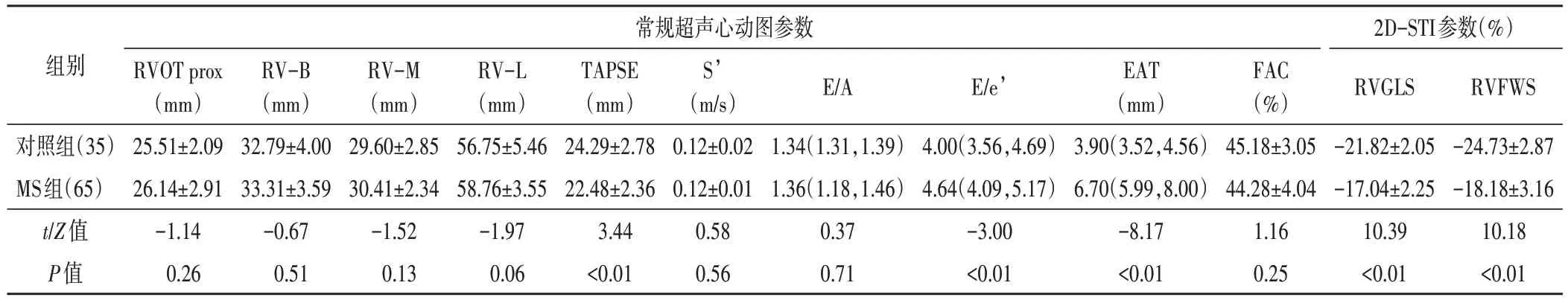
表2 两组常规超声心动图参数及2D-STI参数比较
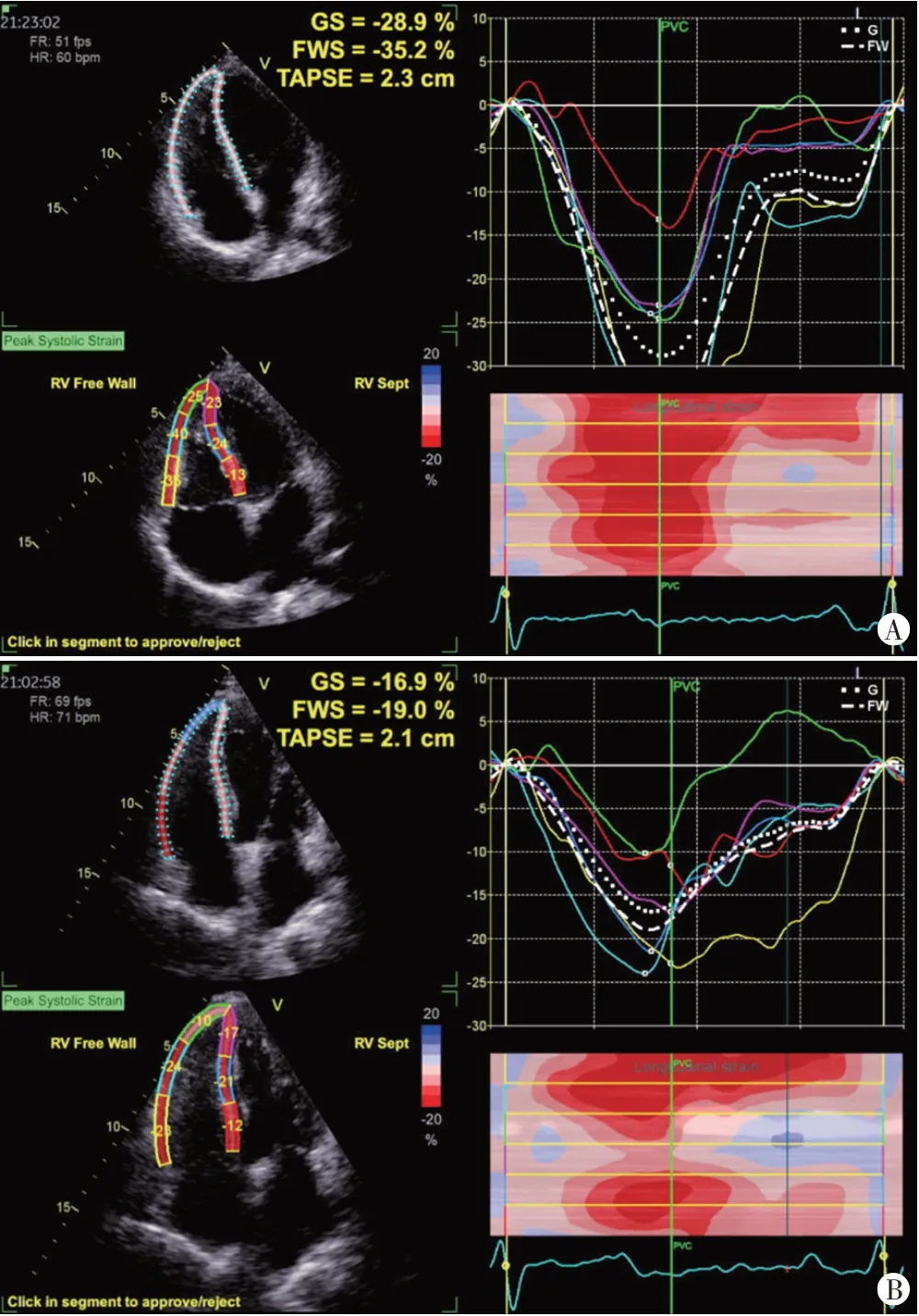
图2 两组2D-STI图
三、MS患者RVFWS与各代谢因素的相关性分析
MS 患者RVFWS 与EAT、年龄、收缩压、舒张压、BMI、WtHR、Glu、TG、LDL-C、TC均呈负相关,与HDL-C呈正相关(均P<0.05)。见表3。
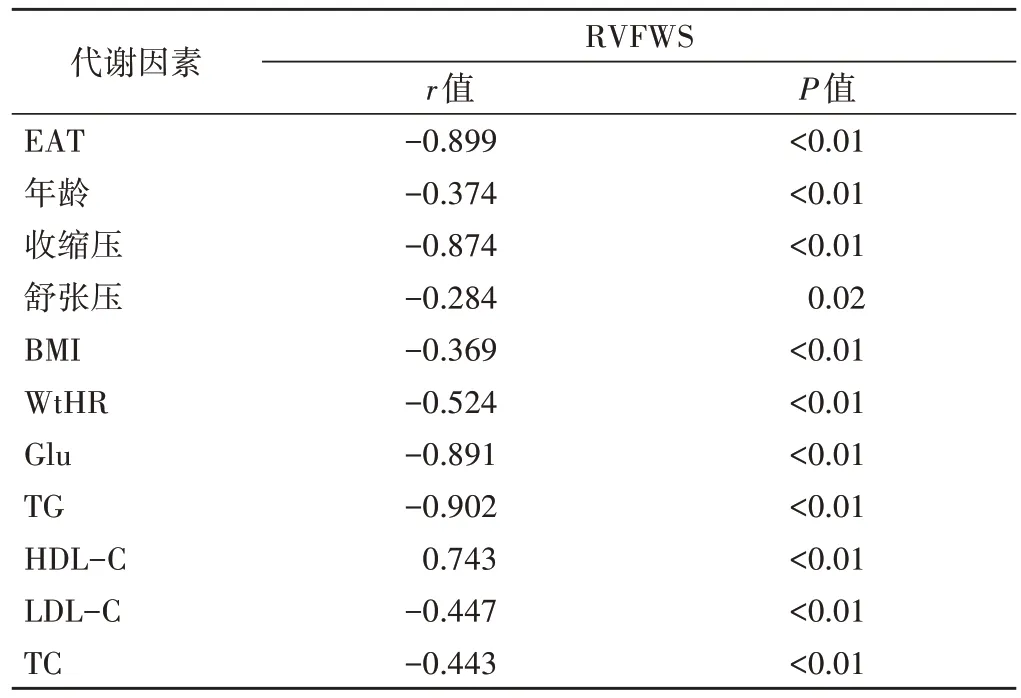
表3 MS患者RVFWS与各代谢因素的相关性分析
四、MS 患者RVFWS 与各代谢因素的多元线性回归分析
多元线性回归分析显示,EAT、收缩压、Glu、TG、HDL-C 均为RVFWS 的独立影响因素(β=-0.261、-0.185、-0.204、-0.204、0.133,均P<0.05)。见表4。
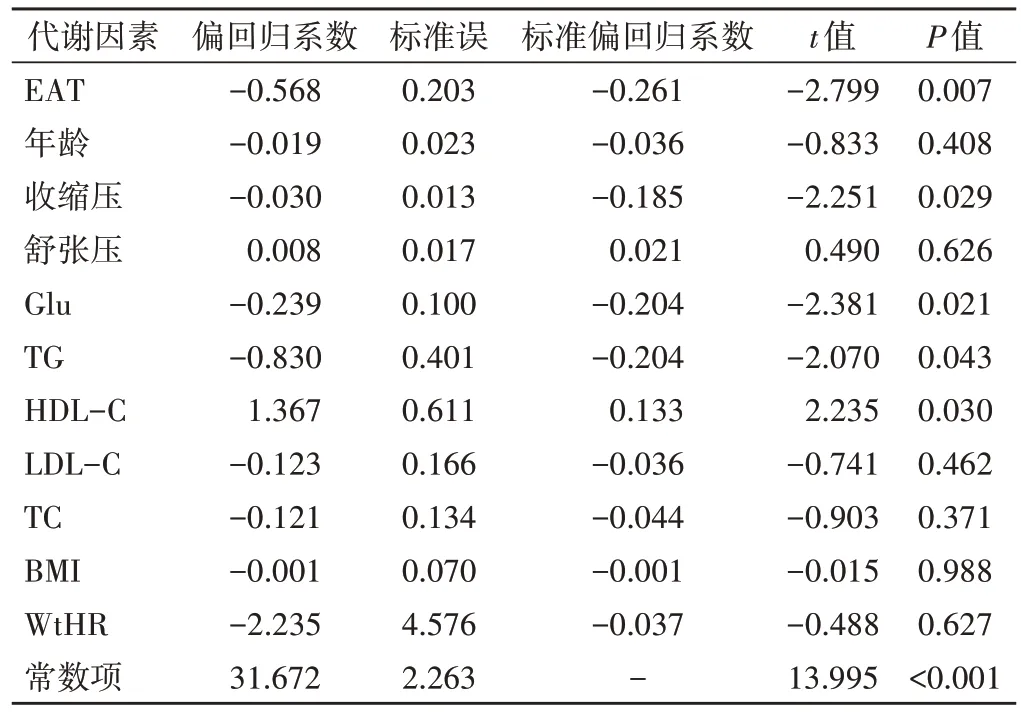
表4 MS患者RVFWS与各代谢因素的多元线性回归分析
五、MS患者RVFWS与EAT间中介效应分析
EAT 对RVFWS 有直接影响(β=-0.6095,95%可信区间:-0.9750~-0.2441),且收缩压、Glu、TG、HDL-C部分介导EAT对RVFWS的影响(β=-0.6176,95%可信区间:-0.7662~-0.4859),总效应值β1=-1.9524,中介效应占总效应的31.63%。见表5和图3。
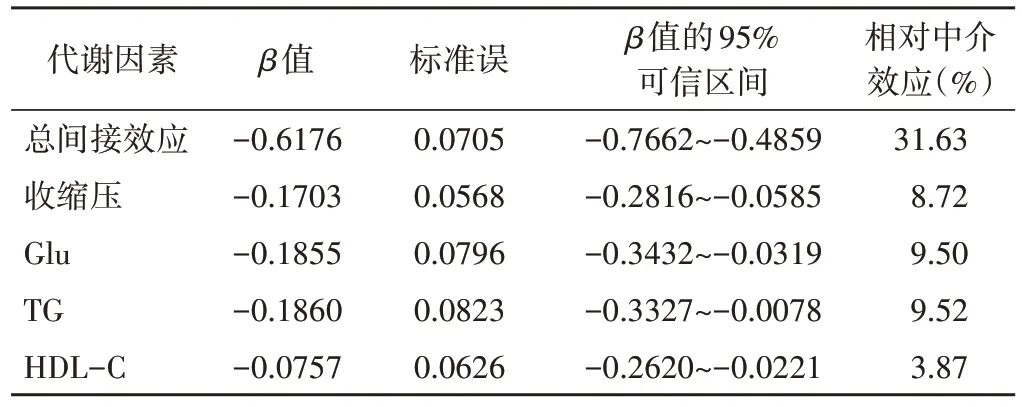
表5 RVFWS与EAT之间中介效应分析
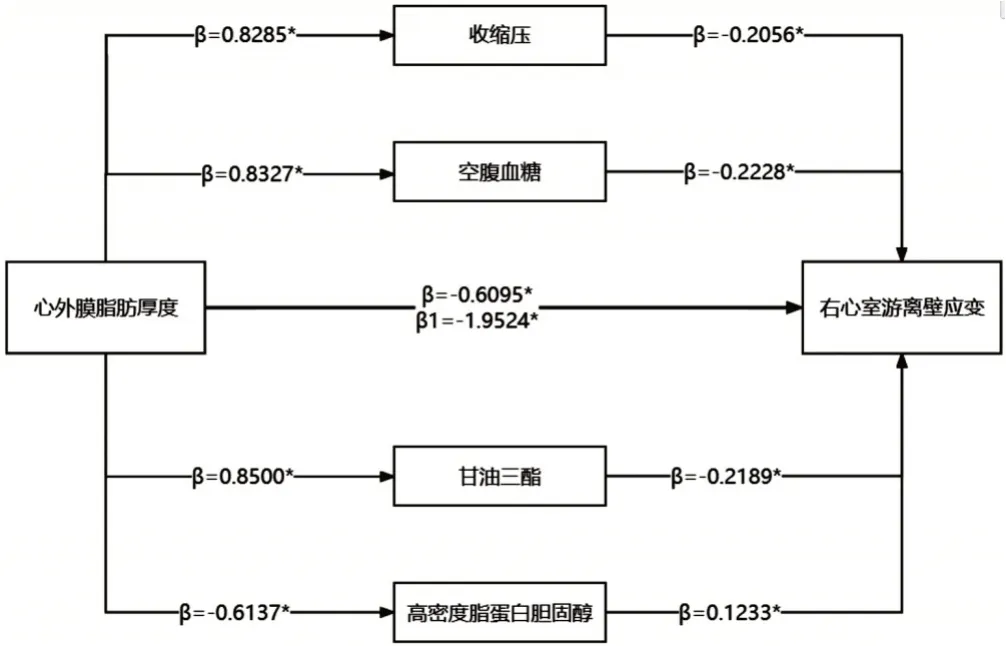
图3 RVFWS与EAT之间的中介效应分析图(β1为总效应,*示P<0.05)
六、2D-STI参数的一致性检验
RVGLS、RVFWS 两次测量一致性均良好(ICC=0.847、0.838,均P<0.05)。
讨论
MS 是一组以肥胖、高血糖(糖尿病或糖调节受损)、血脂异常(高TG 血症和/或低HDL-C 血症)及高血压等聚集发病、严重影响机体健康的临床症候群,是一组在代谢上相互关联的危险因素的组合。研究[8]表明,MS 会造成右室功能障碍,而右室功能障碍会增加不良心血管事件发生的风险。因此,及早识别MS患者右室功能改变对临床早期干预有重要意义。常规超声心动图是目前评价右室功能最常用的检查方法,临床常用的检测右室功能的参数有FAC、TAPSE、S’等,但当右室处于亚临床功能障碍时,这些参数并不敏感。本研究结果显示,两组常规超声心动图参数TAPSE、E/e’比较差异虽均有统计学意义(均P<0.05),但其仍均属正常范围,且常规超声心动图的角度依赖性会影响其对右室收缩及舒张功能评价的准确性。2D-STI无角度依赖性,较常规超声心动图能更准确评价右室收缩功能的改变。既往研究[9]表明,内脏脂肪的过度累积是造成心肌功能受损的重要因素,因此准确评价内脏脂肪累积程度对MS 患者的危险分层有重要意义。临床上常用的评价脂肪累积程度的指标包括BMI、WtHR 等,但是这些指标均无法区分皮下脂肪与内脏脂肪,亟需一种能直接反映内脏脂肪累积程度的指标,以期为MS 患者心血管损伤的风险预测提供指导。心外膜脂肪组织是一种围绕心脏表面的内脏脂肪组织,常规超声心动图可以便捷地获取EAT,量化内脏脂肪的累积程度。基于此,本研究应用2D-STI 评价MS 患者右室收缩功能,并分析其与EAT的关系,旨在为临床早期检测MS 患者亚临床右室收缩功能障碍,以及预测MS 患者右室收缩功能受损风险提供新的参考指标。
本研究结果显示,MS 组RVGLS、RVFWS 均较对照组减低,差异均有统计学意义(均P<0.05),提示MS患者右室收缩功能障碍。分析原因可能为:①MS患者交感神经系统、肾素-血管紧张素-醛固酮系统过度激活,诱发肺血管高反应性,从而导致右室血流动力学及功能改变[10];②双心室之间的相互机械作用也会影响右室收缩功能。既往研究[11-12]表明MS 患者室间隔增厚,而室间隔肌可协助右室射血,推测室间隔的机械变化可能会引发MS 患者右室收缩功能改变;③MS的病理生理基础为胰岛素抵抗,晚期糖基化终末产物和氧自由基生成的增加会使胶原蛋白在心肌中累积,造成心肌纤维化,进而导致心肌弹性丧失[13],最终表现为右室收缩功能障碍。另外,本研究RVGLS、RVFWS 两次测量一致性均良好(ICC=0.847、0.838,均P<0.05),表明两参数具有良好的可重复性,可用于临床开展应用。
既往研究[9]表明,内脏脂肪的过度累积是MS引发心血管系统损伤的关键环节,其可通过促进胰岛素抵抗增加MS 患者发生不良心血管事件的风险。因此,评价MS 内脏脂肪的累积程度可能对MS 的危险分层及预后有一定帮助。心外膜脂肪组织可通过内分泌、旁分泌作用刺激局部炎症因子释放,促进胰岛素抵抗,引发MS患者心肌功能受损[6]。常规超声心动图测量的EAT 不受皮下脂肪组织的影响,可用于评价内脏脂肪。本研究结果显示,MS 组EAT 高于对照组,差异有统计学意义(P<0.05),与Demir 等[14]研究结果一致,表明MS 患者心外膜脂肪含量增加,提示心外膜脂肪含量在诊断MS 中的重要性。为了进一步探讨反映内脏脂肪累积程度的EAT 与右室收缩功能的关系,本研究选取2D-STI 图像勾勒的感兴趣区仅包含右室游离壁,从而避免室间隔对右室收缩功能评估准确性的干扰,以RVFWS 作为因变量,探讨RVFWS 与EAT 的相关性,结果显示,MS 患者RVFWS 与EAT、年龄、收缩压、舒张压、BMI、WtHR、Glu、TG、LDL-C、TC 均呈负相关,与HDL-C 呈正相关(均P<0.05),表明右室收缩功能受损与EAT 的增加有关。多元线性回归分析结果显示,EAT、收缩压、Glu、TG、HDL-C 均为RVFWS 的独立影响因素(均P<0.05)。进一步证实,与BMI、WtHR等未区分脂肪性质的临床指标相比,EAT 能更好地反映MS 患者内脏脂肪累积对右室收缩功能的影响,凸显EAT在MS患者危险分层中的重要性。
目前,关于EAT 与RVFWS 之间独立相关的潜在机制尚未明确。本研究结果显示,EAT 对RVFWS有直接影响(β=-0.6095,95% 可信区间:-0.9750~-0.2441),且收缩压、Glu、TG、HDL-C 部分介导EAT 对RVFWS 的影响(β=-0.6176,95%可信区间:-0.7662~-0.4859),总效应值β1=-1.9524,中介效应占总效应的31.63%。表明Glu、TG、HDL-C、收缩压可能为EAT 与右室收缩功能相关的部分原因,这或许可为内脏脂肪累积与右室收缩功能受损的原因提供新的研究思路。分析原因可能为:①游离脂肪酸是TG 循环中产生心肌能量的来源,其过载或利用不足时会促使心肌内TG 异常积聚,造成心脏脂肪毒性[15],从而影响心室收缩功能;②收缩压增高不仅可以通过体液调节直接影响右室收缩功能,也可通过影响肺动脉舒张功能、左室结构及功能间接导致右室收缩功能障碍[3];③Glu 增高通过损伤自主神经、激活肾素-血管紧张素-醛固醇系统造成胶原蛋白在心肌中累积,致使心肌功能障碍[16];④HDL-C 可以抵抗氧化应激、逆转不平衡的脂质代谢从而保护心肌细胞[17]。本研究结果提示TG、Glu、收缩压、HDL-C有望作为标志物,通过其远程效应在心外膜脂肪组织调节右室收缩功能中发挥重要作用。
本研究的局限性:①样本量较小,且为回顾性、单中心研究,可能影响结果的可靠性和普适性;②心脏表面心外膜脂肪组织的分布存在差异,常规超声心动图测量会产生一定误差,今后需结合其他影像学检查、扩大样本量进一步研究。
综上所述,2D-STI能敏感、准确地评价MS患者早期右室收缩功能障碍。EAT 为RVFWS 的独立影响因素,可通过循环代谢部分介导其对右室功能产生影响。

