紫杉醇联合替吉奥化疗方案治疗进展期胃癌的临床效果
赵凯,李尚日
作者单位: 435000 湖北省黄石市第二医院消化内科
胃癌为常见的恶性肿瘤,具有很高的发病率,对患者身心健康和生命安全危害极大。在全部胃癌中进展期胃癌约占60%~80%,常合并腹膜、淋巴和血行转移,部分患者出现直接浸润扩散[1]。临床对早期胃癌患者主要采取手术治疗方式,多数患者治疗效果较好,预后也较好。进展期胃癌由于已扩展到胃浆膜层和壁肌层,若仍然采用手术治疗很难取得理想效果,这就需要针对患者展开全身化疗[2-3]。然而目前临床对于进展期胃癌的化疗方案尚无统一标准,实际的临床操作中多采用铂类化疗药物为基础的化疗方案,常用药物包括紫杉醇、替吉奥等[4]。本研究观察紫杉醇联合替吉奥化疗方案治疗进展期胃癌的临床效果。现报道如下。
1 资料与方法
1.1 临床资料 选择2019年1月—2021年3月华中科技大学同济医学院附属协和医院肿瘤中心收治的进展期胃癌患者82例,根据随机数字表法分为研究组和对照组,各41例。研究组中男25例,女16例;年龄35~79(47.63±9.25)岁;其中分化腺癌4例,中低分化腺癌34例,印戒细胞癌3例;胃底贲门和结合部癌15例,胃窦癌11例,胃体癌15例。对照组中男24例,女17例;年龄33~80(47.53±9.48)岁;其中分化腺癌3例,中低分化腺癌36例,印戒细胞癌2例;胃底贲门和结合部癌14例,胃窦癌10例,胃体癌17例。2组患者临床资料比较差异无统计学意义(P>0.05),具有可比性。本研究经医院医学伦理委员会审核批准。
1.2 病例选取标准 纳入标准:(1)符合进展期胃癌诊断标准[5];(2)入组前未接受过放疗或化疗等;(3)签署知情同意书。排除标准:(1)合并严重脏器功能不全;(2)合并其他恶性肿瘤;(3)合并出血倾向或贫血疾病;(4)发生脑转移;(5)中途退出研究。
1.3 治疗方法[6]对照组单纯采取替吉奥方案进行化疗,第1天给予奥沙利铂(浙江海正药业股份有限公司生产,规格:50 mg)130 mg/m2静脉滴注,第1~14天每天服用替吉奥胶囊(江苏恒瑞医药股份有限公司生产,规格:替加氟20 mg,吉美嘧啶5.8 mg,奥替拉西钾19.6 mg)80 mg/m2,分早晚2次服用[7-8]。研究组在对照组基础上给予注射用紫杉醇(白蛋白结合型)(江苏恒瑞医药股份有限公司生产,规格:100 mg),治疗第1天给予175 mg/m2[9]。2组均治疗2个周期。
1.4 观察指标 (1)治疗前后采集患者空腹静脉血,通过酶联免疫吸附法检测2组癌胚抗原(CEA)水平。(2)比较2组不良反应发生率,包括肝功能损害、肾功能损害、白细胞下降、恶心呕吐、腹泻等。(3)比较2组总生存时间和无进展生存时间。(4)比较2组患者1年生存率、复发率和转移率。
1.5 近期疗效判定标准 参照WTO实体瘤近期疗效评价标准(RECIST1.1)[10]。完全缓解:全部目标病灶在治疗后完全消失,无新病灶产生,且持续时间≥4周;部分缓解:全部目标病灶的最长径之和在治疗后减少幅度≥50%,且持续时间≥4周;稳定:全部目标病灶的最长径之和在治疗后减少幅度<50%,或增加幅度≤25%,且持续时间≥4周;进展:全部目标病灶的最长径之和在治疗后增加幅度>25%,或产生新病灶。客观缓解率=(完全缓解+部分缓解)/总例数×100%。

2 结 果
2.1 治疗效果比较 研究组客观缓解率为60.98%,高于对照组的39.02%,差异有统计学意义(χ2=3.951,P=0.047),见表1。
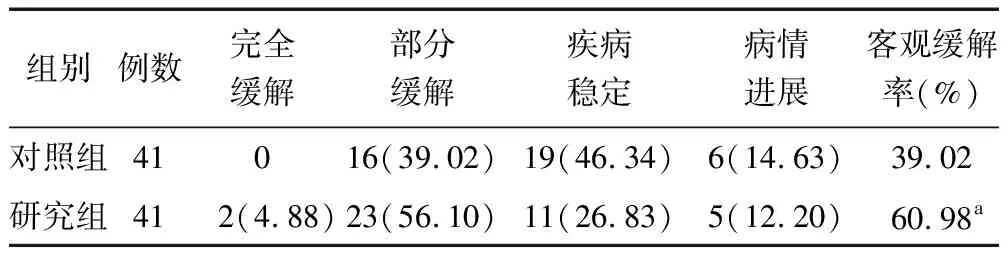
表1 对照组与研究组治疗效果比较 [例(%)]
2.2 CEA水平比较 治疗前,2组CEA水平比较差异无统计学意义(P>0.05)。治疗2个周期后,2组CEA水平均低于治疗前,且研究组低于对照组(P<0.01),见表2。

表2 对照组与研究组治疗前后CEA水平比较
2.3 不良反应比较 2组肝功能损害、肾功能损害、白细胞下降发生率与对照组比较差异无统计学意义(P>0.05);研究组恶心呕吐、腹泻发生率高于对照组(P<0.05),见表3。

表3 对照组与研究组不良反应比较 [例(%)]
2.4 总生存时间、无进展生存时间比较 2组总生存时间、无进展生存时间比较差异无统计学意义(P>0.05),见表4。

表4 对照组与研究组总生存时间、无进展生存时间比较
2.5 1年生存率、复发率、转移率比较 2组1年生存率比较差异无统计学意义(P>0.05);研究组复发率、转移率均低于对照组(P<0.05或P<0.01),见表5。
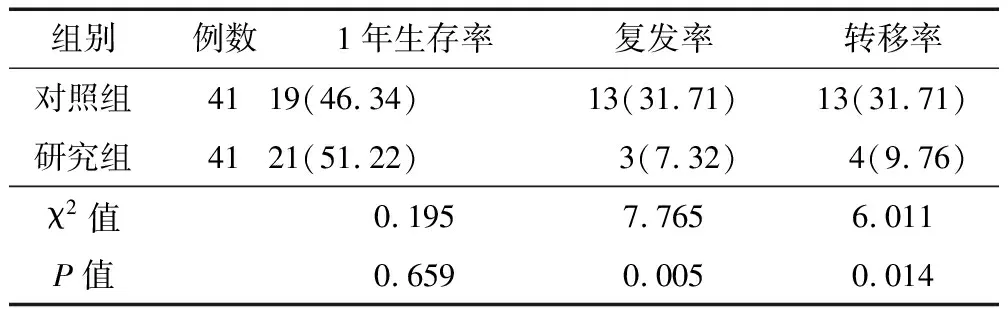
表5 对照组与研究组1年生存率、复发率、转移率比较 [例(%)]
3 讨 论
胃癌具有很高的发病率,年龄、饮食、吸烟、遗传及环境等因素都与胃癌的发病具有密切关系,此外,幽门螺杆菌感染也是非常重要的危险因素[11]。由于早期胃癌具有很强的隐匿性,很难被及时发现和确诊,大部分患者在确诊时病情已发展为进展期胃癌。进展期胃癌会出现体质量短时间明显下降、乏力、贫血等恶病质及恶心、呕吐等上腹部不适,一些患者还会由于肿瘤突破血管而出现黑便、呕血等症状[12]。患者一旦发展为进展期胃癌,不仅治疗难度更大,且预后效果较差。现阶段,对于进展期胃癌临床上主要通过外科手术辅助其他治疗方式的多学科综合治疗方案进行治疗,其中最常用的辅助治疗方法为化疗。通过规范科学的化疗方案,能使进展期胃癌患者的临床症状得到有效控制,延长其生存时间的同时还能进一步保证其生活质量[13]。但现阶段对于进展期胃癌的化疗方案临床上尚无统一标准,不同的治疗方案在效果方面存在着较大的差异,因此如何选择合适的化疗方案受到临床上的普遍重视。
目前临床治疗进展期胃癌的主要化疗药物为拓扑异构酶抑制剂、第三代铂类、紫杉醇、氟尿嘧啶等。紫杉醇为一种短叶紫衫树皮提取物,具有很强的肿瘤细胞毒性,能发挥微管稳定效果,在结合微管的基础上抑制微管解聚,从而进一步阻滞细胞的有丝分裂,促进肿瘤细胞的凋亡[14];能起到脂多糖样作用,即对脂多糖免疫细胞会表现为低应答,在此基础上通过免疫调节的方式对细胞凋亡产生诱导作用;此外,紫杉醇还能对Fas/Fas L通路产生作用,从而对核因子Kappa B的活性进行调节,进一步加快细胞凋亡。所以,紫杉醇能通过多种方式起到非常突出的抗肿瘤作用,且在治疗阿霉素耐药、顺铂耐药等肿瘤细胞时也具有非常明显的效果[15]。替吉奥为氟尿嘧啶类药物,是一种复方制剂,其中包括奥替拉西、吉美嘧啶及替加氟等,与5-氟尿嘧啶相比,替加氟具有双倍的化疗指数,而吉美嘧啶则能够增加5-氟尿嘧啶的血药浓度。相对于5-氟尿嘧啶而言,替吉奥的化疗毒性较其低1/7~1/4,而奥替拉西则能够对5-氟尿嘧啶的磷酸化产生阻断效果,进一步降低患者的胃肠道反应。替吉奥具有较长的半衰期,进入人体12 h后还能保持较高的血药浓度[16]。替吉奥的主要使用方法为口服,用药简单且不良反应少,患者耐受度较高,极大地保证了患者的治疗依从性。
本研究结果显示,研究组总有效率为60.98%,高于对照组的39.02%,说明紫杉醇联合替吉奥方案化疗治疗进展期胃癌具有很好的效果。2组总生存时间、无进展生存期比较差异无统计学意义,说明紫杉醇联合替吉奥方案化疗在延长患者生存时间方面没有突出的效果。本研究中,2组患者1年生存率比较差异无统计学意义,研究组复发率、转移率均低于对照组,证实了紫杉醇联合替吉奥方案化疗治疗能降低进展期胃癌的复发率和转移率。治疗2个周期后,2组CEA水平均低于治疗前,且研究组低于对照组,证明了紫杉醇联合替吉奥方案化疗治疗能有效抑制机体中的肿瘤标志物水平。最后,在不良反应方面,2组肝功能损害、肾功能损害、白细胞下降发生率与对照组比较差异无统计学意义;研究组恶心呕吐、腹泻发生率高于对照组,说明紫杉醇联合替吉奥方案化疗不良反应风险较大,特别是恶心呕吐和腹泻等。
综上所述,紫杉醇联合替吉奥化疗方案治疗进展期胃癌效果良好,可提高患者生存率,降低复发率和转移率,且能抑制CEA水平,但不良反应风险大。
利益冲突所有作者声明无利益冲突

