利奈唑胺致血红蛋白减少危险因素的Meta分析
自雪梅,张峻,柳汝明,何瑾
1 资料与方法
1.1 文献检索 通过计算机检索中国知网、PubMed、万方数据知识服务平台、Embase、Cochrane Library、中国生物医学文献数据库,文献检索时间为数据库成立至2021年9月。中文检索词包括“利奈唑胺”“血红蛋白减少”“贫血”“血液系统不良反应”“血液学毒性”“剂量调整”“治疗药物浓度监测”“危险因素”“影响因素”。英文检索词包括“Linezolid”“Hemoglobinopenia”“Anemia”“Adverse reactions of the blood system”“Hematological toxicity”“Dosagestrategy”“Therapeutic drug monitoring,TDM”“Risk factor”“Influencing factor”。
1.2 文献纳入与排除标准 纳入标准:(1)研究类型为对照研究;(2)研究对象为应用利奈唑胺治疗的患者,其中,血红蛋白减少者为HP组,未发生血红蛋白减少者为NHP组;(3)血红蛋白减少的发生确定与使用利奈唑胺有关;(4)结局指标为肾小球滤过率、用药疗程、利奈唑胺血药谷浓度、血肌酐、基础血红蛋白、总胆红素等。排除标准:(1)重复发表的文献;(2)会议摘要或仅发表摘要的文献;(3)文章中有效数据不全的文献。
1.3 文献筛选、资料提取与质量评价 两位研究者独立检索和阅读文献并摘录相关信息,按照纳入与排除标准独立筛选文献、提取资料和评价纳入研究的质量,若出现分歧,则进行讨论并征求第三方意见以达成一致。参考纽卡斯尔—渥太华质量评估量表(NOS)[5]进行文献质量评定,0~5分为研究质量较低,6~9分为研究质量较高。
1.4 统计学方法 运用RevMan 5.4软件对数据进行Meta分析。若异质性检验显示P>0.10,I2<50%,提示各研究之间无异质性,采用固定效应模型;若异质性检验显示P≤0.1和(或)I2≥50%,则采用随机效应模型。连续性变量采用标准均数差(SMD)为效应分析统计量,区间估计采用95%置信区间(CI)。P<0.05时差异有统计学意义。
2 结 果
2.1 检索结果与质量评价 初检出文献883项,阅读文题及摘要后,排除不符合纳入标准的文献,得到49项,通过进一步查阅全文、复筛,最终纳入研究8项,患者1 715例,均采用利奈唑胺600 mg口服或静脉滴注,每12小时1次,其中,HP组245例,NHP组1 470例,纳入文献基本特征见表1(已将各研究中四分位间距转换为均值±标准差[6-7])。

表1 纳入文献基本特征
2.2 Meta分析结果
2.2.1 肾小球滤过率:6项研究[8-11,13-14]报道患者肾小球滤过率,各研究间有统计学异质性(P=0.10,I2=46%),采用随机效应模型合并效应量进行分析。结果显示,HP组给药前肾小球滤过率低于NHP组[SMD=-26.72,95%CI(-35.18,-18.25),P<0.000 01],见图1。
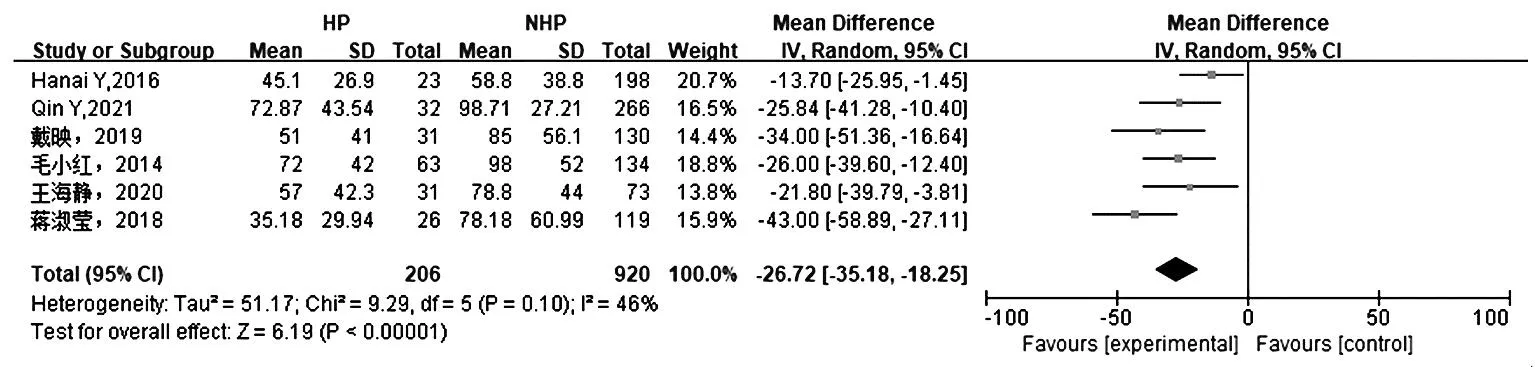
图1 HP组与NHP组肾小球滤过率与血红蛋白减少的Meta分析森林图
2.2.2 用药疗程:6项研究[8-11,13-14]报道应用利奈唑胺的用药疗程,各研究间具有同质性(P=0.31,I2=16%),采用固定效应模型。结果显示,HP组应用利奈唑胺用药疗程显著长于NHP组[SMD=2.09,95%CI(1.10,3.09),P<0.000 1],见图2。
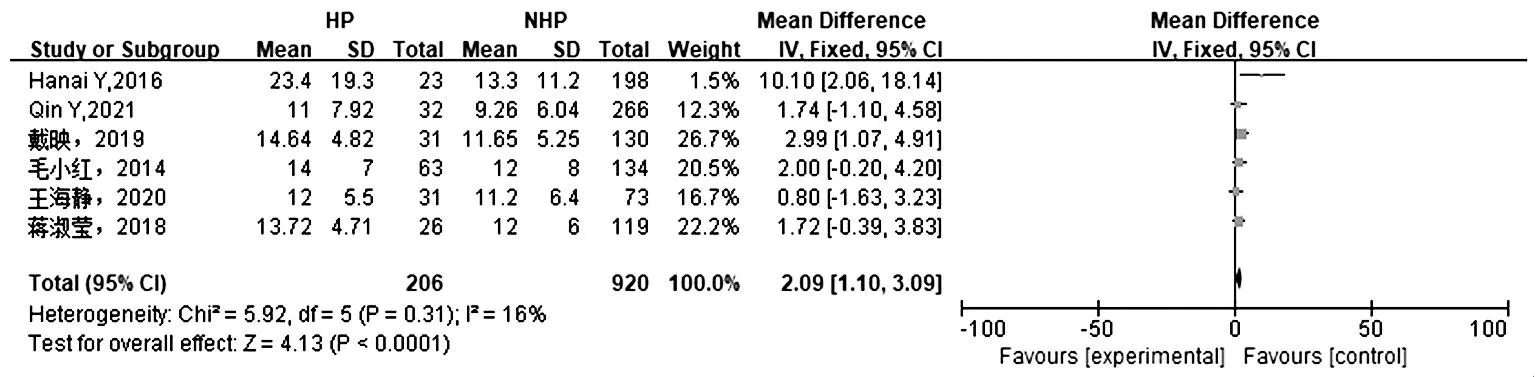
图2 HP组与NHP组用药疗程与血红蛋白减少的Meta分析森林图
2.2.3 利奈唑胺血药谷浓度:3项研究[8-10]报道利奈唑胺血药谷浓度,各研究间具有同质性(P=0.5,I2=0%),采用固定效应模型。结果显示,HP组利奈唑胺谷浓度显著高于NHP组[SMD=3.25,95%CI(1.67,4.84),P<0.000 1],见图3。
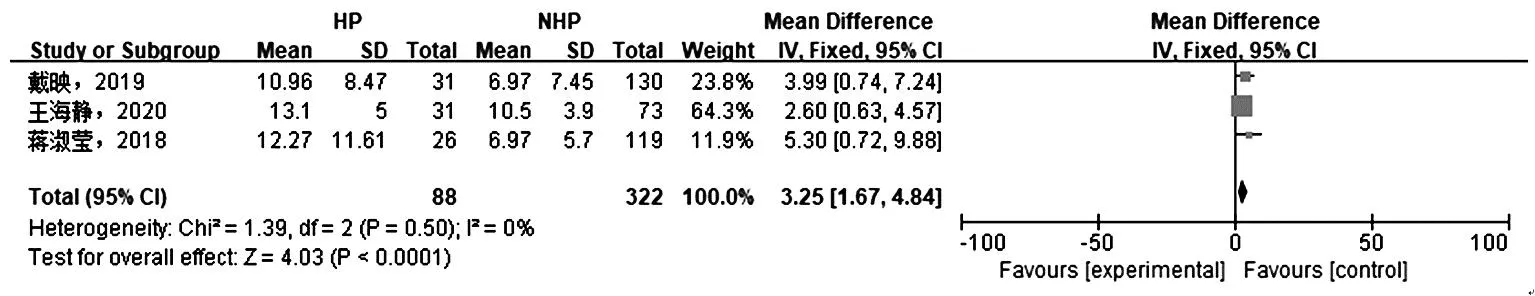
图3 HP组与NHP组利奈唑胺血药谷浓度与血红蛋白减少的Meta分析森林图
2.2.4 血肌酐:3项研究[9-10,14]报道血肌酐,各研究间具有同质性(P=0.14,I2=49%),采用固定效应模型。结果显示,HP组血肌酐水平高于NHP组[SMD=43.11,95%CI(21.35,64.86),P=0.000 1],见图4。
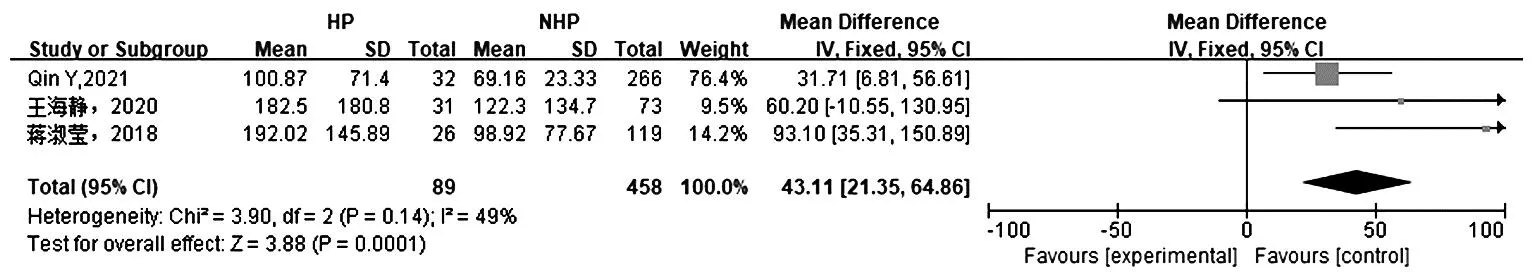
图4 HP组与NHP组血肌酐与血红蛋白减少的Meta分析森林图
2.2.5 基础血红蛋白:7项研究[8-14]报道基础血红蛋白,各研究间具有同质性(P=0.63,I2=0%),采用固定效应模型。Meta分析结果显示,HP组基础血红蛋白低于NHP组[SMD=3.43,95%CI(0.96,5.91),P=0.007],见图5。
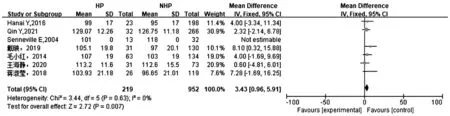
图5 HP组与NHP组基础血红蛋白与血红蛋白减少的Meta分析森林图
2.2.6 总胆红素:3项研究[11,13-14]报道总胆红素,各研究间具有同质性(P=0.34,I2=7%),采用固定效应模型。结果显示,HP组总胆红素高于NHP组[SMD=2.16,95%CI(0.74,3.58),P=0.003],见图6。
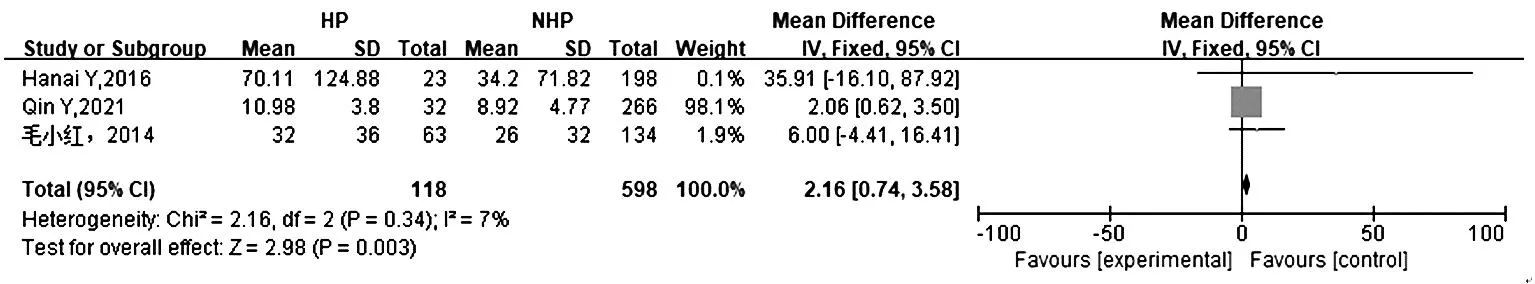
图6 HP组与NHP组总胆红素与血红蛋白减少的Meta分析森林图
3 讨 论
利奈唑胺在革兰阳性菌感染中广泛使用[16-17],其中利奈唑胺引起血红蛋白减少是较严重且发生率高的不良反应[14]。本研究对可能导致利奈唑胺相关血红蛋白减少的危险因素进行系统评价。
本研究结果显示,HP组肾小球滤过率低于NHP组,提示肾小球滤过率低的患者更容易发生利奈唑胺相关血红蛋白的减少,因此在肾功能不全的患者中,需密切关注血红蛋白的变化。Hiraki等[18]发现血红蛋白随着肾小球滤过率下降而降低,两者具有较强的线性相关(r2=0.54),患者肾小球滤过率越低,使用利奈唑胺发生血红蛋白减少的风险就越大。本研究结果表明,使用利奈唑胺的疗程长也是发生血红蛋白减少的危险因素,既往研究得出利奈唑胺引起血红蛋白减少的危险因素具体包括疗程≥14 d[19]或15 d[11]、年龄[20]、肾小球滤过率<60 ml/min[8-9]等。沈赟等[21]认为利奈唑胺的用药时间、总胆红素和肾小球滤过率是血红蛋白减少发生的独立危险因素,且利奈唑胺相关血红蛋白减少的发生率远高于说明书,在临床用药时,对于肾功能不全、总胆红素偏高的患者,应加强用药前后血常规监测,合理控制用药疗程。此外,利奈唑胺血药浓度过高也是引起血红蛋白减少的危险因素,对用药疗程长的患者进行血药浓度监测发现,利奈唑胺谷浓度越高越容易发生血红蛋白减少[3]。而谷浓度≥7 mg/L组较<7 mg/L组血红蛋白减少发生风险高1.87倍[8]。利奈唑胺说明书指出,在肝功能不全的患者中无需调整剂量,本研究结果显示,HP组总胆红素水平高于NHP组,提示肝功能异常是发生血红蛋白减少的危险因素。时薛丽等[22]认为,肝肾功能不全患者会导致利奈唑胺血药浓度波动,利奈唑胺血药浓度波动则可能增加药品不良反应。为了保证肝功能受损患者使用利奈唑胺的有效性与安全性,应对其进行血药浓度监测,且可根据患者的肝功能制定不同的给药方案[23]。当患者基础血红蛋白较低时,更应警惕血红蛋白减少症的发生,毛小红等[11]研究表明,基础血红蛋白<95 g/L是发生利奈唑胺相关血红蛋白减少的高危因素,因此骨髓储备能力较差的患者在使用利奈唑胺时更应警惕不良反应的发生。在临床使用利奈唑胺时,应监测患者的血红蛋白水平,对于基线较低的患者,应全面评估其发生血红蛋白减少的危险因素,个体化治疗。
综上所述,肾小球滤过率低、用药疗程长、谷浓度高、总胆红素低、血肌酐水平高、基础血红蛋白水平低是影响利奈唑胺诱发血红蛋白减少的重要因素。因此在临床用药中,对血红蛋白的变化不可忽视,应基于患者的基础血红蛋白水平、肾小球滤过率、用药疗程、总胆红素水平等指标,结合利奈唑胺药物监测的血药浓度结果制定用药方案,进行剂量调整,降低诱发血红蛋白减少发生的风险。本文纳入文献偏倚风险低,但尚存在部分文献样本量较小的缺点,可能会对分析结果造成干扰。文中纳入研究均为回顾性研究,且大部分为单中心研究,可能存在一定的临床异质性。纳入研究中的部分文献数据未采用均值±标准差表示,虽已根据公式进行估算,但可能与实际数值存在一定差异。因此,本文结论有待更多高质量、大样本、多中心前瞻性研究进一步证实。
利益冲突所有作者声明无利益冲突

