山核桃茶藨子葡萄座腔菌全基因组的分泌蛋白预测和功能分析
吴怡豪,诸葛君昊,张立华,周乐,杜盛楠,杜世平,苏秀
( 1. 浙江农林大学 林业与生物技术学院,浙江 杭州 311300;2. 泰顺县自然资源和规划局,浙江 温州 325500;3. 临海市河头镇农业综合服务中心,浙江 临海 317034 )
茶藨子葡萄座腔菌Botryosphaeriadothidea属子囊菌门Ascomycota、座囊菌纲Dothideomycete、葡萄座腔菌目Botryosphaeriales、葡萄座腔菌科Botryosphaeriaceae、葡萄座腔菌属Botryosphaeria真菌[1-2],其分布极为广泛,可以侵染多种经济林、用材林、园林绿化林木,如苹果Maluspumila、梨Pyrusp.、桃Prunuspersica、核桃Juglans regia、葡萄Vitisvinifera、杨Populussp.、桉Eucalyptussp.[3-10]等,导致严重的果实损失和生产减产。该菌可引起山核桃干腐病Macrophomacaryae,对山核桃Caryacathayensis的产量和品质产生了显著的负面影响[11]。因此,对于了解茶藨子葡萄座腔菌的致病机理以及筛选抗病品种的研究具有重要的实践意义,可以为山核桃生产提供有力的支持,减少果实损失,维护生产稳定性和生态平衡。
病原菌产生的分泌蛋白与寄主抗性基因的蛋白产物之间的分子互作是病原菌与寄主之间互作的核心[12-13],分泌蛋白在其中起着重要的作用。研究表明,黄曲霉Aspergillusflavus通过分泌一些细胞外酶和毒素来侵染寄主,这些酶可以破坏宿主细胞壁和木质素,可以诱导宿主细胞凋亡和坏死,从而使得该菌对宿主的感染更加容易发生[14];果树炭疽菌Colletotrichumgloeosporioides分泌的氧化还原酶可以降低植物的抗氧化能力,导致宿主细胞的损伤和死亡[15];稻瘟菌Magnaportheoryzae利用分泌外源蛋白,包括纤维素酶、蛋白酶和细胞壁水解酶等,破坏植物细胞壁和膜结构,从而增加了其侵染的能力。此外,该病原体还释放毒素,如稻瘟菌素和谷氨酰胺酰胺酶,导致植物细胞的死亡和坏死[16]。分泌蛋白不仅对真菌自身的生长和代谢有重要的调节作用,还能够通过对植物细胞的破坏、毒素的作用等方式,导致植物的损伤和病害发生。因此,研究茶藨子葡萄座腔菌分泌蛋白的功能和作用机制,对研究该病害的发病机理与防控具有重要意义和应用价值。
茶藨子葡萄座腔菌全基因组测序数据的公开,为开展该菌分泌蛋白的研究提供了坚实的基础。本研究以山核桃茶藨子葡萄座腔菌BDLA16-7 的全基因组蛋白序列为基础,以经典分泌蛋白特征为依据,结合Augustus、SignalP、Funannotate、WoLF PSORT、Ensembl Fungi、GenomeTools 等网站和软件,对BDLA16-7 的分泌蛋白组进行了预测和功能分析,为进一步深入研究该病原菌与寄主互作的分子机制提供了基础,并为挖掘病原菌关键致病基因提供依据。
1 材料和方法
1.1 材料
山核桃茶藨子葡萄座腔菌BDLA16-7 是从浙江省杭州市临安区的一棵患有溃疡病的山核桃树的树干上分离出的山核桃茶藨子葡萄座腔菌菌株。最初,该真菌在马铃薯葡萄糖琼脂培养基上的菌落呈淡白色,随后逐渐转变为黑色。子囊座pycnidia通常是单独存在的,呈灰黑色、球形,并被菌丝覆盖。该菌株的基因组DNA 和mRNA是从培养了10 天的菌丝体中提取而得。山核桃茶藨子葡萄座腔菌BDLA16-7 全基因组蛋白质氨基酸序列,来自中国生物信息中心(CNCB-NGDC 成员和合作伙伴2021)的基因组仓库(GWH)(https://ngdc.cncb.ac.cn/gwh/),注册号为GWHBEBO00000000,原始序列来自CNCBNGDC 的基因组序列档案(https://ngdc.cncb.ac.cn/gsa/)上公开访问,登录号为CRA004612(生物项目PRJCA005744)[17]。
1.2 预测方法
1.2.1 茶藨子葡萄座腔菌全基因组蛋白N-端信号肽预测 使用SignalP 5.0 在线工具(https://services.healthtech.dtu.dk/services/SignalP-5.0/)和Phobius (https://phobius.sbc.su.se/)来预测基因组编码的所有蛋白质是否带有N-端信号肽[18]。
1.2.2 茶藨子葡萄座腔菌蛋白的亚细胞定位 使用蛋白亚细胞定位在线预测软件Cell-PLoc 2.0[19](http://www.csbio.sjtu.edu.cn/bioinf/Cell-PLoc-2/)来确定带有N-端信号肽的蛋白质的亚细胞定位。
1.2.3 茶藨子葡萄座腔菌分泌型蛋白的跨膜结构预测 使用蛋白跨膜结构预测软件TMHMM[20](https://dtu.biolib.com/DeepTMHMM),对全蛋白序列中具有信号肽且主要定位于细胞外的蛋白进行是否含有跨膜结构预测。
1.2.4 茶藨子葡萄座腔菌分泌型蛋白的锚定位点预测 使用GPI 锚定位点预测软件GPI-SOM(http://gpi. unibe.ch)[21],对全蛋白序列中具有信号肽、主要定位于细胞外且不包含跨膜结构域的蛋白序列进行GPI 锚定位点的预测。
1.2.5 分泌蛋白中效应蛋白的预测和功能分析 使用EffectorP3.0(http://effectorp.csiro.au)[22]软件对全蛋白序列中具有信号肽、主要定位于细胞外、不包含跨膜结构域且不包含GPI 锚定位点的蛋白序列进行效应蛋白的预测。同时,通过eggnog-mapper[23]数据库和Pathogen Host Interactions[24]数据库对预测出的效应蛋白的组成和功能进行分析。
1.2.6 分泌蛋白中碳水化合物活性酶类预测和功能分析 使用CAZymes 在线预测工具dbcan[25](http://bcb.unl.edu/dbCAN2/)中的HMMER、DIAMOND 和HOTPEP 程序,对分泌蛋白中的碳水化合物活性酶进行预测和功能注释。
2 结果与分析
2.1 山核桃茶藨子葡萄座腔菌全基因组蛋白N-端信号肽预测
BDLA16-7 基因组编号为GWHPBEBO000001 到GWHPBEBO013130,总共编码了13 130 条蛋白质序列。通过使用SignalP 5.0 和Phobius 软件进行分析,结果表明其中含有N-端信号肽序列的有1 402 条蛋白质序列,占总蛋白质序列数量的10.67%。这些具有N-端信号肽序列的蛋白质全部属于标准的Sec/SPI 型分泌蛋白质,它们会在信号肽序列的引导下进入细胞的内质网腔中。
2.2 山核桃茶藨子葡萄座腔菌全基因组蛋白的亚细胞定位
在BDLA16-7 全基因蛋白序列中,将含有信号肽的1 402 条蛋白序列经Cell-PLoc 2.0 软件分析发现,其中有1 188 条蛋白序列属于胞外分泌型,而其余214 条序列虽然具有信号肽,但其并不分泌到细胞外,而是转运到了细胞中不同的细胞器或质膜上。
2.3 山核桃茶藨子葡萄座腔菌分泌型蛋白的跨膜结构预测
在BDLA16-7 全基因蛋白序列中,有一些蛋白具有信号肽序列,并且属于胞外分泌型。经过跨膜结构域预测软件TMHMM 分析,发现1 188 条胞外分泌型蛋白序列中,有97 条蛋白序列具有跨膜区。因此,这些序列有可能是离子通道蛋白、膜锚定蛋白或膜受体蛋白,而无法分泌到细胞膜外。除此之外的1 091 条蛋白序列没有跨膜结构域,具有典型的分泌蛋白特征。
2.4 山核桃茶藨子葡萄座腔菌分泌型蛋白的GPI 锚定位点预测
在BDLA16-7 全基因蛋白序列中,有一些蛋白具有信号肽序列,属于胞外分泌型蛋白,并且没有跨膜结构域。经过GPI-SOM 软件预测,发现1 091 条蛋白序列中有193 条含有GPI 锚定位点,不符合经典的分泌型蛋白特征,因此将其去除。除此之外,有898 条分泌型蛋白序列不含GPI 锚定位点,符合经典的分泌蛋白特征,因此将其认定为BDLA16-7 的分泌蛋白组(表1)。
2.5 山核桃茶藨子葡萄座腔菌分泌蛋白组特征分析
2.5.1 山核桃茶藨子葡萄座腔菌分泌蛋白组的氨基酸长度分析 对BDLA16-7 分泌蛋白组的序列长度进行分析,发现分泌蛋白的长度分布跨度较大。其中,存在长度小于100 个氨基酸的小分子蛋白,最短的为66 个氨基酸;同时也存在长度超过1 000 个氨基酸的大分子蛋白,最长的蛋白为2 028 个氨基酸。分泌蛋白的氨基酸长度主要分布在100~600 个氨基酸范围内,共有721 条序列,占分泌蛋白序列总数的80.29%(图1)。
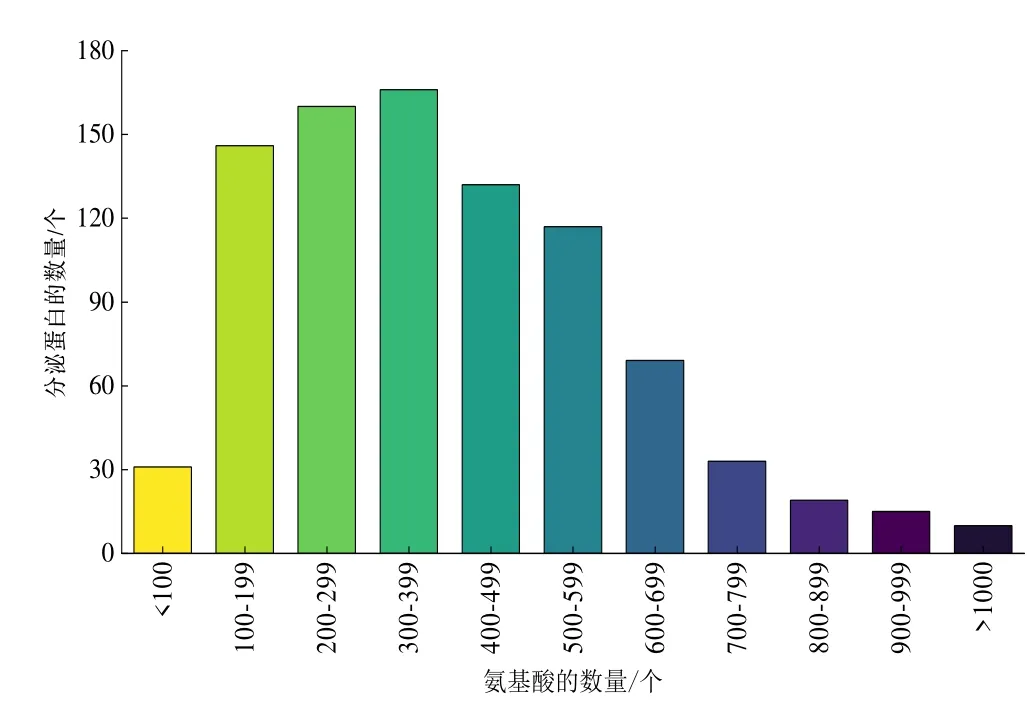
图1 山核桃茶 藨子葡萄座腔菌分泌蛋白质组的长度分布Fig. 1 Length distribution of secretory proteome of B. dothidea
2.5.2 山核桃茶藨子葡萄座腔菌分泌蛋白组的氨基酸组成分析 在BDLA16-7 分泌蛋白组的氨基酸组成分析中,发现不同的氨基酸含量有显著差异,按照含量从高到低的顺序排列如下:A 丙氨酸、G 甘氨酸、S 丝氨酸、L 亮氨酸、T 苏氨酸、V 缬氨酸、P 脯氨酸、D 天冬氨酸、N 天冬酰胺、E 谷氨酸、I 异亮氨酸、F 苯丙氨酸、Y 酪氨酸、Q 谷氨酰胺、R 精氨酸、K 赖氨酸、W 色氨酸、H 组氨酸、C 半胱氨酸、M 蛋氨酸,氨基酸可以被分为不同的类别。其中,非极性疏水氨基酸(A、G、L、V、P 和I)的含量最高,占总含量的43.6%,显示出明显的优势,亲水的极性氨基酸(S、T、N、Q、M 和C)的含量相对较低,为27.7%;酸性氨基酸(A 和E)的含量为14.8%,碱性氨基酸(K、R、H)的含量为8.7%,芳香族氨基酸(F、Y 和W)的含量为9.7%(图2)。

图2 山核桃茶藨子葡萄座腔菌分泌蛋白质组中氨基酸组成比例Fig. 2 Composition of amino acids of secretory proteome of B. dothidea
2.5.3 山核桃茶藨子葡萄座腔菌分泌蛋白组信号肽的氨基酸长度分析 BDLA16-7 分泌蛋白组中的信号肽序列具有不同的氨基酸长度,这个长度范围从14 到41 个氨基酸。在这些信号肽序列中,长度为16 到24 个氨基酸的序列最为常见,总共有806 个,占了分泌蛋白组总数的89.76%。其中,信号肽长度为19 个氨基酸的序列最多,共有169 个,占了分泌蛋白组总数的18.82%。其次,长度为18 个氨基酸的信号肽序列有132 个,占了分泌蛋白组总数的14.70%。相反,信号肽长度为31、35、39 和41 个氨基酸的序列最为罕见,每个长度仅有1 个序列(图3)。

图3 山核桃茶藨子葡萄座腔菌分泌蛋白质组信号肽长度分布Fig. 3 Length distribution of signal peptides of secretory proteome B. dothidea
2.5.4 山核桃茶藨子葡萄座腔菌分泌蛋白组信号肽的氨基酸组成分析 根据对BDLA16-7 分泌蛋白组信号肽的氨基酸组成进行的分析,发现20 种氨基酸在信号肽中的出现频率存在显著差异,按频率从高到低排列如下:A、L、S、V、T、M、F、I、G、P、R、K、Q、H、C、N、Y、W、D 和E。其中,非极性氨基酸丙氨酸(A)的出现频率最高,占总出现频率的22.40%,亮氨酸(L)的出现频率次之,为19.29%。相反地,天冬氨酸(D)和酸性氨基酸谷氨酸(E)的出现频率最低,分别仅为0.29%和0.27%(图4)。

图4 山核桃茶藨子葡萄座腔菌分泌蛋白质组信号肽中氨基酸组成比例Fig. 4 Composition of amino acids of signal peptides of secretory proteome in B. dothidea
2.5.5 山核桃茶藨子葡萄座腔菌分泌蛋白组信号肽切割位点分析 通过对BDLA16-7 分泌蛋白组信号肽的切割位点(-3 到+2 位点)进行统计分析,得到以下结果:在-3、-2、-1、+1 和+2 位点出现频率最高的氨基酸分别为A、S、A、A 和P,它们分别占据了50.56%、18.93%、81.74%、25.61%和37.08%的比例。具体来说:在-3 位点,除了A 之外,V(24.28%)和S(8.91%)也比较常见,而E、F、H、K、M、N、W 和Y 没有被使用。在-1 位点,除了A 之外,G(8.24%)和S(5.90%)也相对常见,而D、E、H、I、L、M、N、V、W 和Y 没有出现。在-2、+1 和+2 位点,所有的氨基酸都被使用。这些结果表明,在BDLA16-7 分泌蛋白组信号肽中,切割位点-3 和-1 位置上的氨基酸相对来说比较保守,可能在信号肽酶的识别过程中起到关键作用。其他位点则更加多样化,容纳了各种不同的氨基酸(表2)。
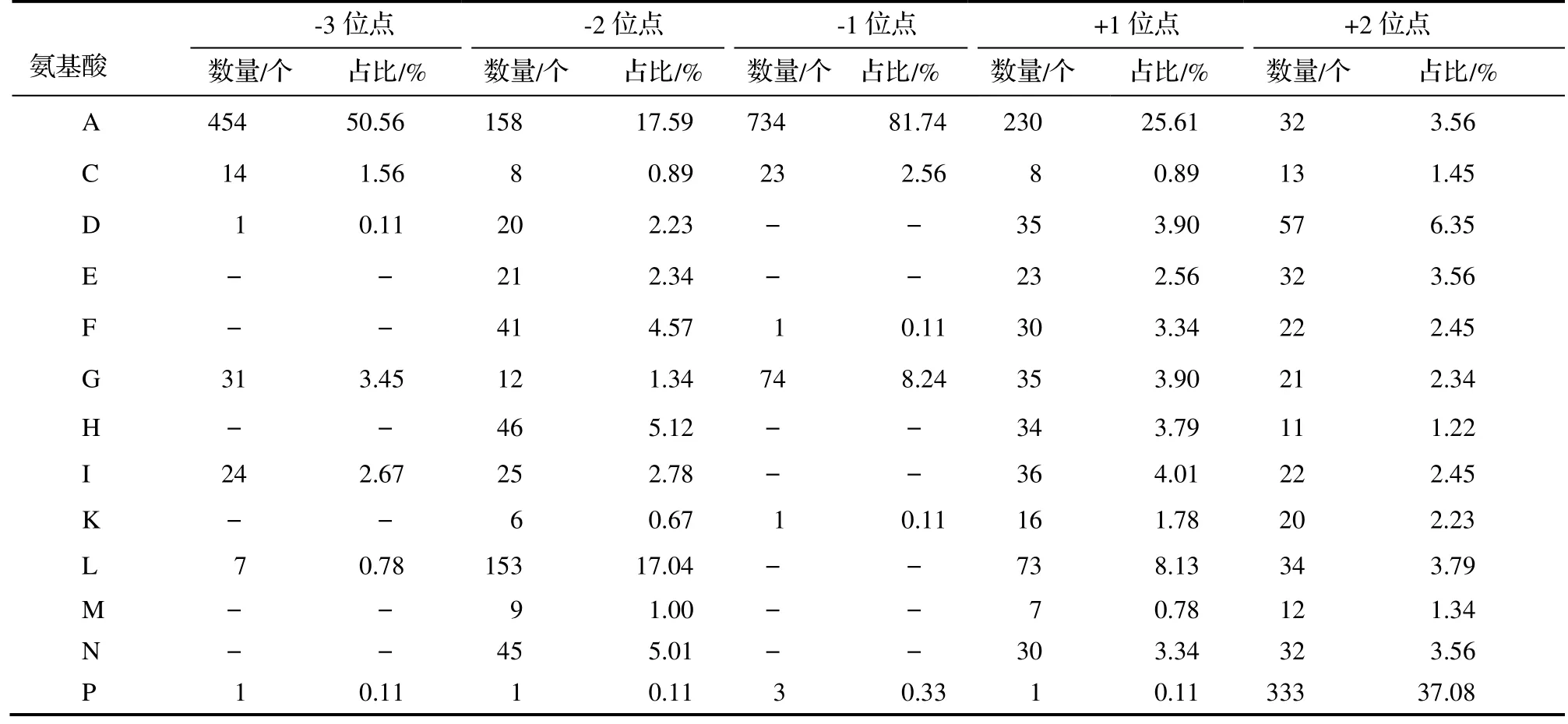
表2 信号肽酶切割位点周围20 个氨基酸残基的频率Tab. 2 The frequency of 20 amino acid residues around the signal peptidase cleavage sites
2.5.6 山核桃茶藨子葡萄座腔菌分泌蛋白组的功能注释
通过使用eggnog-mapper 数据库、PHI 数据库和Geneious Prim Trial 数据库对BDLA16-7 分泌蛋白组的898条序列进行功能分析。结果表明,共有600 条序列可以被注释到具有完整功能。通过COG(Clusters of Orthologous Genes)数据库对这些功能进行分类,发现最多的分泌蛋白被归类为G 类,即碳水化合物的运输和代谢(Carbohydrate transport and metabolism),总共有229 条序列归入这一类别。其次是S 类,即功能未知类(Function unknown),其中包括一些蛋白的结构域和功能未知的蛋白,如酪氨酸酶中心结构域(Comon central domain of tyrosinase)、泛素3 绑定蛋白But2 的C-端结构域(Ubiquitin 3 binding protein But2 C-terminal domain)、DUF3129和DUF3455 等,总共有152 条序列归入这一类别。其他类别:O 类蛋白翻译后修饰和分子伴侣(Post-translational modification, protein turnover, chaperones)86 条序列,E 类氨基酸运输和代谢相关(Amino acid transport and metabolism)44 条序列,C 类能量产生和转化相关(Energy production and conversion)24 条序列,以及Q 类次生代谢物的生物合成、转运和分解相关(Secondary metabolites biosynthesis transport and catabolism)23 条序列。其余的功能分类包含的分泌蛋白数目较少,没有超过10 个。这些分析结果揭示了BDLA16-7 分泌蛋白组的功能多样性,其中大部分分泌蛋白与碳水化合物代谢相关,但也包含一些功能未知的蛋白以及其他生物学功能。这种功能分类有助于理解这些蛋白在生物体内的作用和生物过程中的角色(图5)。

图5 山核桃茶 藨子葡萄座腔菌分泌蛋白质组的COG 目录Fig. 5 COG catalog of the secretory proteome of B. dothidea
2.6 山核桃茶藨子葡萄座腔菌分泌蛋白组中效应蛋白的预测和功能分析
BDLA16-7 分泌蛋白组经TargetP 2.0 Server 软件分析,再次确认898 条蛋白序列全部含有信号肽,并可以分泌到细胞外。继而通过效应蛋白预测软件EffectorP 3.0 对潜在的效应蛋白进行预测,结果发现271 条蛋白序列可被预测为效应蛋白,占分泌蛋白总数的30.18%。其中101 条序列可以被eggnog-map 数据库注释到具体的功能,其中42 条序列在COG 分类中属于S 类,主要包括蛋白结构域和功能未知的蛋白,如:IgE 绑定蛋白(Ig Ebinding protein)、Cupin 家族蛋白、成束蛋白结构域(Fasciclin-domain)、CFEM 结构域(CFEM-domain)等,41 条序列属G 类,14 条序列属于O 类,2 条序列属于C 类,1 条序列属于A 类RNA 加工和修饰相关(RNA processing and modification),1 条序列属于E 类(图6)。
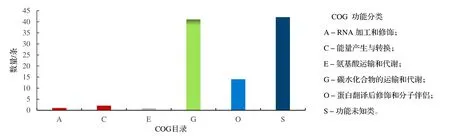
图6 山核桃茶藨子葡萄座腔菌的效应蛋白质组COG 目录Fig. 6 COG catalog of the effector proteome of B. dothidea
对预测为潜在效应蛋白的271 条序列,经PHI 数据库Blastp 比对,有14 条序列可以比对到相应的致病功能注释。其中 1 条序列(GWHPBEBO006248)可以比对到黄曲霉的致病效应蛋白序列,1 条蛋白序列(GWHPBEBO004805)可以比对到禾谷镰刀菌Fusariumgraminearum和黄单胞菌Xanthomonasaxonopodis的致病效应蛋白序列,1 条蛋白序列(GWHPBEBO011899 和GWHPBEBO003128)可以比对到寄生疫霉Phytophthora parasitica的致病效应蛋白序列,1 条蛋白序列(GWHPBEBO008334)可以比对到稻瘟菌的致病效应蛋白序列,2 条序列(GWHPBEBO008083 和GWHPBEBO000994)可以比对到禾谷镰刀菌的致病效应蛋白序列,2 条蛋白序列(GWHPBEBO006043 和GWHPBEBO006222)可以比对到扩展青霉Penicilliumexpansum的致病效应蛋白序列,5 条蛋白序列(GWHPBEBO010105、GWHPBEBO006002、GWHPBEBO003061、GWHPBEBO003727 和GWHPBEBO001912)与褐腐菌Moniliniafructicola致病性增强的效应蛋白序列有较高的相似性,其同时也与柑橘褐斑菌Alternariaalternata的致病效应蛋白序列存在较高的相似性。
2.7 山核桃茶藨子葡萄座腔菌分泌蛋白组中碳水化合物活性酶类(CAZymes)预测
碳水化合物活性酶类(CAZymes)是病原菌分泌蛋白组的重要组成部分,其主要参与对寄主细胞壁的降解作用,与病原菌的致病性有紧密的联系。利用HMMER、DIAMOND 和HOTPEP 三个软件,在BDLA16-7 分泌蛋白组898 条蛋白序列,共预测到293 个分泌蛋白属于CAZymes 酶类,分属于糖苷水解酶(Glycoside Hydrolases,GHs)、氧化还原酶(Auxiliary Activities, AAs)、糖酯酶(Carbohydrate Esterases, CEs)和多糖裂解酶(Polysaccharide Lyases, PLs)四个分类,占总分泌蛋白数的32.26%。其中基于序列相似性的HMMER 软件预测发现282 个分泌蛋白属于CAZymes,基于结构域的DIAMOND 和HOTPEP 软件分别预测到了188 个和275个分泌蛋白属于CAZymes。三个软件都预测到CAZymes 的数量为169 个(图7)。
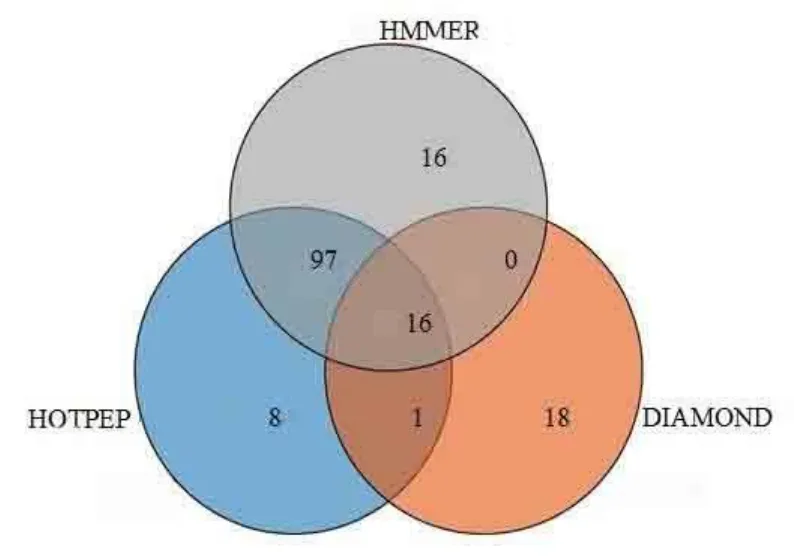
图7 Hmmer Diamond 和Hotpep 对山核桃茶藨子葡萄座腔菌分泌蛋白质组碳水化合物酶类预测结果Fig. 7 CAZymes prediction on secretory proteome of B. dothidea by Hmmer diamond and Hotpep
在预测到的169 个CAZymes 中,GHs 数量最多为99 个,主要包括GH3、GH28、GH92、GH1 和GH31 等多个亚家族;其次为AAs,有42 个,主要包括AA3_2、AA1_3、AA3 和AA9 等亚家族;CBMs 为12 个,主要包括CBM1、CBM35 和CBM18 等亚家族;PLs 为9 个,包括PL1_4、PL3_2 等亚家族;CEs 为6 个,包括CE0、CE1、CE16、CE4 和CE8 亚家族;CTs 的数量最少,为1 个,属于GT32 亚家族(图8)。
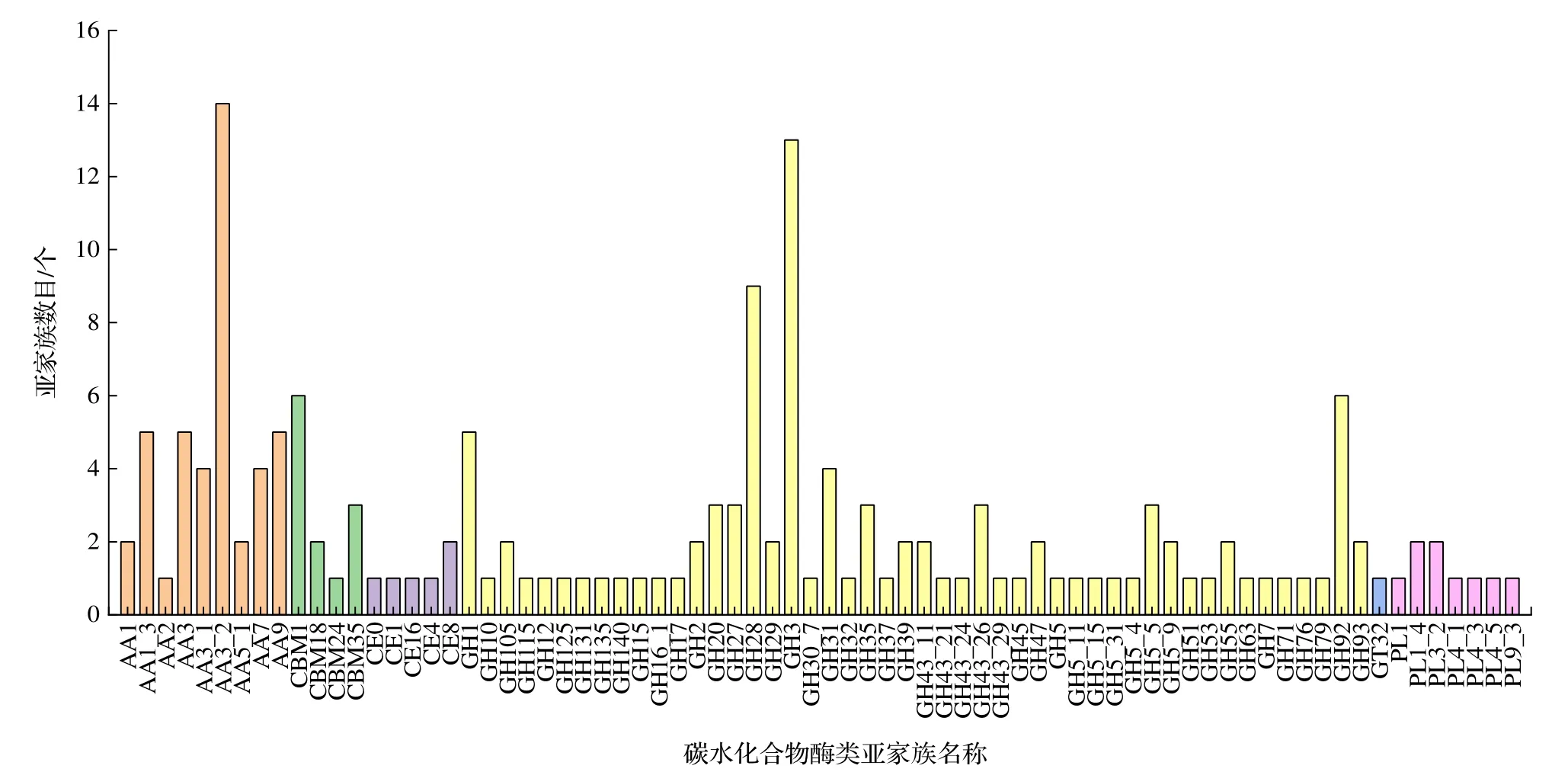
图8 山核桃茶藨子葡萄座腔菌分泌蛋白质组碳水化合物酶类亚家族分布预测Fig. 8 Prediction of distribution of carbohydrate enzyme subfamily in secretory proteome of B. dothidea
在BDLA16-7 分泌蛋白组的169 个CAZymes 中,参与寄主细胞壁纤维素、木聚糖和果胶降解的CAZymes数量有85 个,而在丝孢堆黑粉菌Sporisoriumreilianum、玉蜀黍黑粉菌Ustilagomaydis、水稻稻瘟病病菌Magnaporthegrisea、禾谷镰刀菌、灰葡萄孢Botrytiscinerea、大丽轮枝菌Verticilliumdahliae分别有26、30、128、127、87、165 个(表3)[32]。

表3 不同营养类型真菌参与寄主细胞壁纤维素、木聚糖和果胶降解的CAZymes 数量Tab. 3 The number of CAZymes involved in the degradation of host cell wall cellulose, xylan and pectin by different trophic fungi
3 讨论
病原真菌分泌蛋白的预测最为重要的是对信号肽进行预测。为了提高信号肽预测的准确性,本文通过SignalP 和Phobius 相结合的方法,排除了与信号肽具有相似结构导肽(transit peptide)的影响,保证了含有信号肽分泌蛋白预测的准确性。通过Cell-PLoc 2.0、TMHMM、GPI-SOM、EffectorP3.0、dbcan 等软件的分析,本文成功预测了山核桃茶藨子葡萄座腔菌BDLA16-7 分泌蛋白组898 条蛋白序列,占其蛋白序列总条数的6.84%;与尖孢镰刀菌Fusariumoxysporum(7.5%)[26]、假禾谷镰孢菌Fusariumpseudograminearum(5.5%)[27]、新月弯孢菌Curvularialunata(7.7%)[28]、禾谷炭疽菌Colletotrichumgraminicola(5.2%)[29]分泌蛋白在全基因组蛋白序列中所占的比例相似。
分析BDLA16-7 分泌蛋白组的氨基酸构成显示,非极性疏水氨基酸(包括A、G、L、V、P 和I)的含量为43.6%,明显高于亲水极性氨基酸(S、T、N、Q、M 和C)的含量(27.7%)。这表明,分泌蛋白通常需要在其折叠和稳定化过程中形成一个疏水核心结构。这个核心结构有助于保护蛋白质免受水分子和其他极性分子的干扰,同时有助于维持蛋白质的结构完整性,从而使其能够正确履行其功能。特别值得注意的是,信号肽长度为19 个氨基酸的分泌蛋白数量最多,这可能意味着这个长度的信号肽对于茶藨子葡萄座腔菌分泌蛋白质的正确转运和定位至关重要。这也可能是生物进化过程中的结果,即这个长度的信号肽的功能在生物进化中被保留下来并广泛应用。需要强调的是,这个结论是基于统计学推断的,不一定适用于所有分泌蛋白。此外,需要进一步的研究来验证这一结论,并探索不同长度信号肽的功能和进化意义。对于BDLA16-7 分泌蛋白组的信号肽氨基酸构成,发现20 种氨基酸在信号肽中的出现频率存在较大差异。前六位出现频率最高的氨基酸均为脂肪族氨基酸,这可能与信号肽需要穿越细胞质膜有关。此外,分泌蛋白组的信号肽切割位点在-3 和-1 位置的氨基酸相对保守,其氨基酸组成为A-S-A,属于A-X-A 型,这是真核生物中相对典型的信号肽切割位点,可被SpaseI 型信号肽酶所识别。
效应蛋白(effector)是一种在植物病原微生物中广泛存在的重要致病因子,它们通过干扰寄主植物的免疫反应来感染宿主[30]。因此,效应蛋白既是病原微生物致病的关键分子,也是用于筛选植物抗病性基因的重要工具[31]。研究表明,在对葡萄座腔菌效应蛋白预测中,预测为潜在效应蛋白的119 条序列,有11 条序列可以比对到相应的致病功能注释[32]。当在对BDLA16-7 分泌蛋白组效应蛋白的预测中,我们发现271 条序列(30.18%)符合效应蛋白的定义,其中101 条序列可以被eggnog-map 数据库注释到具体的功能,经PHI 数据库Blastp 比对,有14 条序列可以与黄曲霉、禾谷镰刀菌、黄单胞菌、寄生疫霉、稻瘟菌、扩展青霉、褐腐菌、柑橘褐斑菌比对到相应的致病功能注释,其中5 条蛋白序列与褐腐菌M.fructicola致病性增强的效应蛋白序列有较高的相似性,但其同时也与柑橘褐斑菌A.alternata致病性降低的致病效应蛋白序列存在较高的相似性。相比较而言,我们研究比对的潜在效应蛋白序列更多(271 条),这意味着它在研究潜在效应蛋白与致病菌之间的关系时有更多的数据支持,可以提供更全面的信息;比对到的致病菌种类更多,从细菌到真菌,从黄曲霉到寄生疫霉等,这增加了研究的多样性和广泛性。但目前尚不清楚这些潜在的效应蛋白如何具体影响茶藨子葡萄座腔菌的致病性,需要进一步通过实验手段来验证和研究其功能。
CAZymes(碳水化合物活性酶类)在真菌中指的是一组各种酶类,参与碳水化合物的分解和代谢,这些酶在生物质降解、病原菌感染宿主、形态变化、寄生植物侵染以及真菌与寄主的相互作用等方面发挥着作用[33]。为了准确预测BDLA16-7 中的CAZymes 数量,我们使用了三种不同的软件,包括Diamond、Hmmer 和Hotpep,通过对这三种软件的预测结果求交集的方法来进行预测。在众多CAZymes 中,特别是在直接参与植物细胞壁成分降解的GH、AA、PL 和CE 亚家族中,这些酶发挥着关键作用[34]。在三种软件都预测到的169 个CAZymes中,GHs 数量最多,共有99 个,这些亚家族主要负责果胶和纤维素的降解。此外,BDLA16-7 的CAZymes 中还包括大量的辅酶模块,其中AAs 有42 个,PLs 有9 个,CEs 有6 个,这进一步增强了茶藨子葡萄座腔菌对细胞壁的降解能力,有助于病原菌成功侵染寄主植物。许多研究表明,植物病原真菌分泌的CAZymes 与其寄生性之间存在一定的相关性[35]。通常认为,寄生性更强的植物病原真菌编码的胞外CAZymes 数量较少[36]。通过比较不同营养型真菌的CAZymes 数量,本研究发现,半活体营养型的茶藨子葡萄座腔菌中,参与寄主细胞壁纤维素、木聚糖和果胶降解的CAZymes 数量与活体营养型真菌相比显著增加,但与死体营养型真菌相比,CAZymes数量基本相同或更少。这一研究结果与对终极腐霉Pythiumultimum[37]、颖枯壳多孢Stagonosporanodorum[38]、大丽轮枝菌[39]等非活体营养型病原菌CAZymes 数量的研究结果相一致。
4 结论
本文以山核桃茶藨子葡萄座腔菌BDLA16-7 全基因组蛋白序列为基础,采用生物信息学的方法,对BDLA16-7 分泌蛋白组进行了预测,明确了BDLA16-7 分泌蛋白的长度分布特征,功能分类、信号肽切割位点的氨基酸组成、切割位点的类型和CAZymes 数目,以及CAZymes 中纤维素酶、果胶酶、木聚糖酶的亚家族组成,并筛选到14 个GWHPBEBO0(06248、04805、11899、03128、08334、08083、00994、06043、06222、10105、06002、03061、03727、01912)与致病性紧密联系的潜在效应蛋白,为从分子水平上解析茶藨子葡萄座腔菌的致病机理奠定了基础。

