大黄灵仙方调控胆管细胞炎症的作用及机制研究
陈伟棠 俞渊 庞浇安 李敏鹏 潘孟 陆世锋 杨文 滕金豪 叶桂源
原发性肝内胆管结石是指发生于左右肝管汇合部位以上的肝胆管结石,是我国常见的良性胆道疾病,具有发病隐匿、病变复杂、术后残石复发高等特点[1]。该病早期易继发胆管炎症、胆道出血、化脓性胆道炎、梗阻性黄疸等,病程晚期可并发胆汁性肝硬化、肝实质损坏甚至胆管癌等危重并发症,严重影响患者的生命安全[2]。流行病学显示:该病的好发年龄群体主要为35岁至75岁[3],男女之间发病率无明显差异,而在国家和种族人群之间存在差异,东亚地区发病率约占25%,欧美发病率约为1%[4]。中国是胆结石发病的重灾区国家之一,胆结石的发病率可占所有疾病的10%,而肝胆管结石的发病率约占胆石病的30%[2]。
相关研究证实:肝胆管结石的发病机制涉及多种因素和多个环节,常见的病因主要有胆道感染、胆管炎、胆汁淤积以及胆管解剖变异等因素[5],其中以感染致结石最为显著。本课题组前期已证实:大黄灵仙方可有效预防肝内胆管结石的形成及术后复发,改善胆管微环境,降低胆道感染发生几率,使胆管恢复到非炎性状态,其机制可能与调控Toll样受体4(Toll-like receptor 4,TLR4)/髓样分化因子88(myeloid differentiation factor 88,MyD88)信号通路和激活核转录因子κB(nuclear factor kappa-B,NF-κB)信号通路相关炎症因子的表达水平有关[6-7]。而白细胞介素-1受体相关激酶(interleukin-1 receptor-associated kinase,IRAK)-1、IRAK-4以及成纤维生长因子激活酶1MAP3KT结合蛋白2(TGF-3 activator 1 map3KT-binding protein 2,TAB2)作为上述信号轴的下游信号分子,在该通路中具有正向传导信号的作用,与骨关节炎、胃肠道炎症、癌症等疾病密切相关。但在胆管炎症中,通过调控IRAK-1、IRAK-4以及TAB2的异常表达,缓解和抑制胆管细胞炎症反应,预防肝胆管结石的形成及术后复发,尚无相关文献研究。为进一步完善大黄灵仙方修复胆管细胞炎症损伤的作用靶点,本课题通过内毒素脂多糖(lipopolysaccharide,LPS)构建胆管炎症大鼠模型,推测大黄灵仙方可能通过调控IRAK-1、IRAK-4和TAB2的异常表达,抑制胆管系统炎症损伤,进而防治肝胆管结石。
1 材料与方法
1.1 实验动物
SPF级健康雄性SD大鼠45只,平均鼠龄6周,体质量:160~200 g。购买于湖南斯莱克景达实验动物有限公司[许可证号SCXK(湘)2019-0004],饲养于广西中医药大学仙葫校区动物房,室温20~24℃,湿度45%~55%。实验方案经广西中医药大学实验动物伦理委员会同意通过,相关实验操作均按照动物伦理审查标准严格进行,批准号DW20191017-023。
1.2 动物分组
45只大鼠随机分为9组:空白组、模型组、大黄灵仙颗粒组、NF-κB阻断剂组、p38MAPK阻断剂组、NF-κB阻断剂+p38MAPK阻断剂组、NF-κB阻断剂+大黄灵仙颗粒组、p38MAPK阻断剂+大黄灵仙颗粒组、NF-κB阻断剂+ p38MAPK阻断剂+大黄灵仙颗粒组,每组大鼠5只。本课题均在广西中医药大学第一临床医学院7楼实验操作室进行操作。
1.3 主要药物与器材
大黄灵仙方:生大黄15 g、威灵仙30 g、金钱草30 g、黄芪30 g、芒硝10 g、泽兰15 g、柴胡12 g、郁金12 g、鸡内金12 g、枳壳12 g、磁石10 g、炙甘草5 g,经广西中医药大学第一附属医院药剂科按相当量换算配为颗粒剂,所有中药颗粒剂均由江阴天江药业有限公司提供,LPS、p38丝裂活化蛋白激酶(mitogen activated protein kinase,MAPK)信号通路阻断剂、p38MAPK信号通路阻断剂、NF-κB信号通路阻断剂(均购于美国Sigma公司,批号分别为L4391-1MG、IC50-17、5108-96-3),IRAK4 Antibody、TAB2(C88H10)Rabbit mAb(均购于美国CST公司,批号分别为:4363、3745)、Mouse Anti-βactin mAb(购于北京中杉金桥生物技术有限公司,批号:TA-09)、IRAK-1 Antibody(购于Santa Cruz公司,批号sc-5288),羊抗兔IgG、羊抗鼠IgG(均购于Proteintech公司,批号分别为SA00001-2、SA00001-1),PVDF膜浸润活化液、特超敏ECL化学发光试剂盒(均购于上海碧云天,批号分别为P0021S、P0018AS)。
1.4 造模与给药
大鼠胆管炎症模型参考文献进行,在胆总管一次注射5 mg/kg LPS以构建肝内胆管感染动物模型[8]。根据等效剂量系数折算法及前期研究基础,大鼠剂量=6.3×成人的临床剂量,最终确定大黄灵仙颗粒给药剂量320 mg/kg。具体造模如下:(1)空白组:第1~7天予蒸馏水灌胃(2次/天,灌胃量为2 mL/100 g)(2)模型组:第1~3天予蒸馏水灌胃(2次/天,灌胃量为2 mL/100 g),第4天在胆总管注射LPS以构建肝内胆管炎症大鼠模型,第5~7天继续予蒸馏水。(3)大黄灵仙颗粒组、NF-κB阻断剂组、p38MAPK阻断剂组、NF-κB阻断剂+p38MAPK阻断剂组:第1~3天予分别行320 mg/kg大黄灵仙颗粒、120 mg/kg NF-κB信号阻断剂、10 mg/kg p38MAPK信号阻断剂、120 mg/kg NF-κB信号阻断剂联合10 mg/kg p38MAPK信号阻断剂进行腹腔注射(1次/天,连续干预3天),第4天在胆总管注射LPS 以构建肝内胆管炎症大鼠模型,第5~7天继续予大黄灵仙方灌胃;(4)NF-κB阻断剂+大黄灵仙颗粒组、p38MAPK阻断剂+大黄灵仙颗粒组、NF-κB阻断剂+ p38MAPK阻断剂+大黄灵仙颗粒组:第1~3天予大黄灵仙方灌胃(2次/天,灌胃量为2 mL/100 g)并分别予120 mg/kg NF-κB信号阻断剂、10 mg/kg p38MAPK、120 mg/kg NF-κB信号阻断剂联合10 mg/kg p38MAPK信号阻断剂进行腹腔注射(1次/天,连续干预3天),第4天在胆总管注射LPS以构建肝内胆管炎症大鼠模型,第5~7天继续予大黄灵仙方灌胃;(5)第7天灌胃结束后禁食禁水12小时,随后无菌操作下取材,各组大鼠在造模和干预期间无死亡。
1.5 标本采集及方法
大鼠术前12小时禁食禁水,使用3%戊巴比妥钠4 mg/100 g腹腔注射麻醉大鼠,随后腹部去毛,置于无菌手术台上在剑突下作横行切口,经全身肝素化、灌注预热后,大鼠肝脏由红褐色变成土黄色,在显微镜下剔除多余的肝脏组织,保留完整的胆管树,进行实时荧光定量PCR(quantitative real-time PCR,RT-qPCR)、蛋白免疫印迹法(Western blot,WB)等相关指标检测。
1.6 观察指标及方法
1.6.1 RT-qPCR技术检测 IRAK-4、IRAK-1、TAB2 mRNA表达情况 (1)引物合成。各基因及内参基因β-actin引物采用Primer 5.0软件设计,见表1。(2)检测方法。采用Trizol法从胆管树中提取总RNA,于超微量紫外线光度仪分析RNA浓度、纯度及完整性,提取质量:OD260/OD280应在1.8~2.0之间;按照逆转录试剂盒将RNA进行逆转录从而获得 cDNA;依据荧光定量PCR反应条件进行扩增反应,检测 IRAK-4、IRAK-1、TAB2 mRNA表达量,最终采用2-△△ct计算。
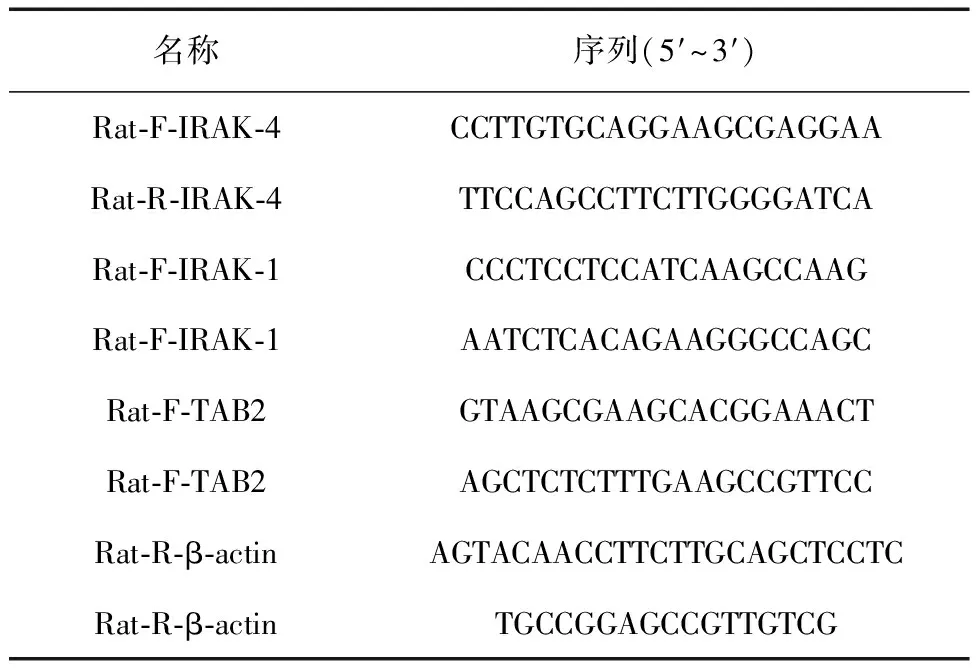
表1 目的基因荧光定量PCR引物序列
1.6.2 WB技术检测IRAK-1、IRAK-4、TAB2蛋白表达水平 剪取等体积胆管树研磨,用移液枪吸取1 mL细胞裂解液加入研磨管后置于冰上充分研磨,待组织完全裂解后转移至EP管中4℃离心取上清液,采用BCA法测定蛋白含量。制备SDS-PAGE凝胶,电泳分离蛋白湿转模式下将蛋白转印至PVDF膜上,5%脱脂奶粉封PVDF膜然后加入相应一抗:β-actin(1∶2 000)、IRAK-4(1∶1 500)、IRAK-1(1∶1 500)、TAB2(1∶1 500),4℃冰箱中孵育过夜。回收一抗,TBST洗PVDF膜,加入二抗(1∶10 000),室温孵育1小时后用TBST 洗涤3次。超敏ECL化学发光底物在凝胶成像系统中进行检测,Image J软件计算各组蛋白条带与β-actin的灰度值比值。
1.7 统计学分析
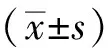
2 结果
2.1 大黄灵仙方对IRAK-4、IRAK-1、TAB2蛋白表达的影响
与空白组比较,模型组的IRAK-1、IRAK-4、TAB2的蛋白表达量升高,差异具有统计学意义(P<0.05)。与模型组比较,大黄灵仙颗粒组、p38MAPK阻断剂组、NF-κB阻断剂组、NF-κB阻断剂+p38MAPK阻断剂组、NF-κB阻断剂+大黄灵仙颗粒组、NF-κB阻断剂+ p38MAPK阻断剂+大黄灵仙颗粒组的IRAK-1、IRAK-4、TAB2的蛋白表达量降低,差异具有统计学意义(P<0.05)。与大黄灵仙颗粒组比较,NF-κB阻断剂+大黄灵仙颗粒组、NF-κB阻断剂+ p38MAPK阻断剂+大黄灵仙颗粒组的IRAK-1、IRAK-4、TAB2的蛋白表达量下降,差异有统计学意义(P<0.05)。见图1,表2。

注:A为空白组;B为模型组;C为大黄灵仙颗粒组;D为p38MAPK阻断剂组;E为NF-κB阻断剂组;F为NF-κB阻断剂+p38MAPK阻断剂组;G为p38MAPK阻断剂+大黄灵仙颗粒组;H为NF-κB阻断剂+大黄灵仙颗粒组;I为NF-κB阻断剂+ p38MAPK阻断剂+大黄灵仙颗粒组。

表2 IRAK4、IRAK1、TAB2蛋白表达情况鼠只=5)
2.2 大黄灵仙方对IRAK-4、IRAK-1、TAB2 mRNA表达的影响
与空白组比较,模型组的IRAK-1、IRAK-4、TAB2 mRNA表达量升高,差异具有统计学意义(P<0.05)。与模型组比较,大黄灵仙颗粒组、p38MAPK阻断剂组、NF-κB阻断剂组、NF-κB阻断剂+p38MAPK阻断剂组、NF-κB阻断剂+大黄灵仙颗粒组的IRAK-1、IRAK-4、TAB2 mRNA表达量下降(P<0.05),NF-κB阻断剂+p38MAPK阻断剂+大黄灵仙颗粒组的TAB2 mRNA表达量下降(P<0.05);与大黄灵仙颗粒组比较,NF-κB阻断剂+p38MAPK阻断剂组的IRAK-1、IRAK-4、TAB2 mRNA表达量下降,差异具有统计学意义(P<0.05)。见表3,图2、3、4。
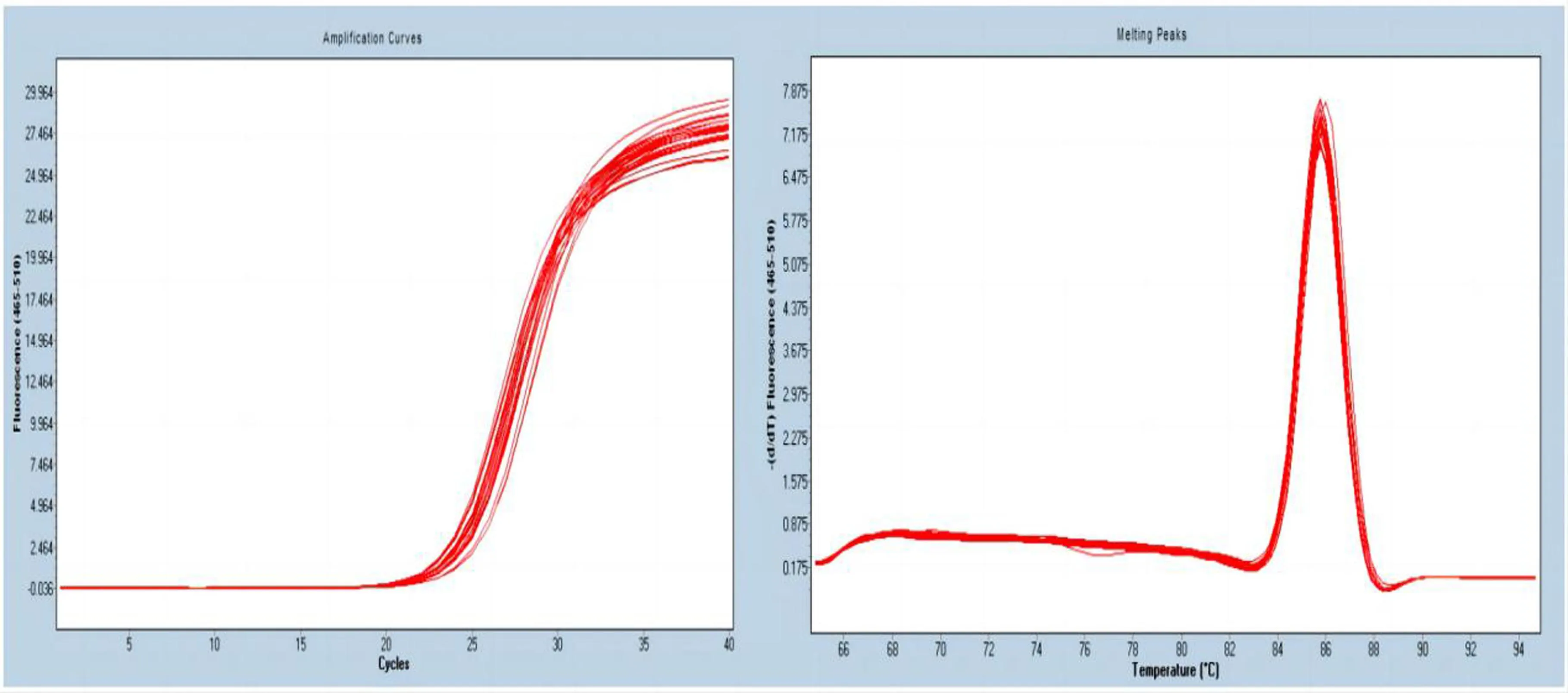
图2 IRAK-1的扩增曲线与溶解曲线

图4 TAB2的扩增曲线与溶解曲线

表3 IRAK4、IRAK1、TAB2 mRNA表达情况鼠只=5)
3 讨论
肝脏是人体最大的实质器官,具有分解代谢、清除毒素、抗氧化等功能,然而肝脏容易受到体内外各种致病因素的侵扰而损伤,原发性肝内胆管结石作为常见的难治性良性胆道疾病,一直是肝脏疾病中的研究热点。因此,探索针对其机制的有效防治措施是现今亟需解决的难题。而中医药对胆石症的治疗由来已久,许多临床实践及实验也证实了其在缓解患者临床症状、溶石排石及改善血清学指标等方面具有确切的疗效。大黄灵仙方是唐乾利根据十多年临床经验创制的中药复方,该方以疏肝利胆、攻下排石为立方原则,全方由生大黄、威灵仙、芒硝、金钱草、枳壳、鸡内金、泽兰、柴胡、郁金、磁石、黄芪、炙甘草组成,临床上常用于肝内胆管结石的治疗。现代药理学证明:大黄、威灵仙可作用于肝脏的酶和蛋白,调节胆汁酸与肝脏脂质的平衡,增强胆囊收缩,减少胆汁淤积,从而降低结石的形成几率[9]。而柴胡中蕴含的皂苷、有机酸、挥发油等化学成分,可促进胆汁、胆固醇的分泌与排泄,枳实中的黄酮类,甘草中的甘草酸、甘草苷,金钱草中的酚性成分、黄酮类等均有疏肝、利胆、排石等功效[10-11]。由此可见,大黄灵仙方中的组方药物具有缓解胆道炎症、增强胆道收缩功能、抑制结石形成等功效。
目前已经证实,肝胆管结石的形成与感染互为因果[12]。2015年,Peers C等[13]发现,胆管感染以革兰氏阴性菌感染为主,LPS是革兰阴性菌细胞壁的重要组成部分,经肝脏排入胆汁中的内毒素大部分仍保留LPS完整的分子结构,具有内毒素的生物特性,当LPS作用于细胞膜受体,通过细胞内信号传递级联使基因表达发生变化,介导内皮细胞、平滑肌细胞以及单核巨噬细胞的激活,诱导炎症细胞因子合成和释放,从而引发胆道内慢性炎症。
炎症的发生与信号通路的调控失常及关键基因的异常表达存在关联,而药物治疗胆石症常从削弱炎症信号通路出发,通过减轻炎症反应减少结石形成。2015年,Skevaki等[14]研究发现,IRAK1和IRAK-4是IRAK激酶家族成员,在免疫系统中发挥重要作用,参与调控Toll样受体(Toll-like receptors,TLRs)和肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)的表达。当IRAK-1发生磷酸化反应时,亦会活化TRAF6并与由TABs(TAB2)组成的蛋白激酶复合物结合,引起NF-κB信号通路产生促炎细胞因子[15]。2019年,Yin D等[16]也证实了,IRAK-1能通过驱动单核细胞/巨噬细胞浸润,促进炎性细胞的分泌,通过对慢性压迫性损伤大鼠模型注射IRAK1的siRNA可降低IRAK-1的表达,逆转脊髓中该信号通路下游分子p-NF-κB表达的上调,抑制神经炎症的进展。IRAK-4过度表达可增强LPS诱导的NADPH氧化酶活性,激活MAPK信号通路并启动炎症应答[17]。相关研究也证实了:在溃疡性肠炎的炎症产生机制中,TLR/MyD88炎症信号通路的异常表达起着关键作用,TLRs能够通过与病原识别模式分子结合的方式,介导其下游的信号传递分子MyD88进行胞内信号转导,而大量募集的MyD88可诱导IRAK4发挥激酶活性,产生磷酸化反应,最终释放TNF-α、IL-1β等细胞炎症因子,引发炎症级联反应[18]。动物实验证实了:当LPS与TLR4结合后通过MyD88招募并活化信号蛋白IRAK(特别是IRAK-1和IRAK-4),可激活下游NF-κB和MAPK信号通路并交互放大炎性反应[19],通过抑制IRAK-1、IRAK-4以及TAB2的异常表达可下调TLR4/NF-κB/MAPK信号通路的炎症应激反应。可见,IRAK-1、IRAK-4和TAB2作为TLR4/NF-κB/MAPK信号通路的下游因子,在炎症反应过程中扮演着重要角色。但通过调控IRAK-1、IRAK-4和TAB2的异常表达,缓解和抑制胆管细胞炎症反应,进而预防肝胆管结石的形成及术后复发,尚无相关报道。故本课题采取大黄灵仙方干预胆管炎症大鼠模型,探究其抑制胆管细胞炎症反应的作用机制。
结合胆管炎性反应是导致肝内胆管结石形成的关键因素的论点,IRAK-1、IRAK-4、TAB2作为TLR4/NF-κB/MAPK信号通路的下游信号分子,在该通路中具有正向传导信号的作用。为进一步验证IRAK-1、IRAK-4和TAB2与胆管炎症之间的关系,笔者运用WB和RT-qPCR对其进行检测。研究结果显示:与空白组对比,模型组的IRAK-1、IRAK-4、TAB2蛋白及mRNA表达显著增加,提示经LPS诱导后模型组大鼠的信号通路被激活并呈现出高表达状态,大鼠胆管细胞炎症反应增强,分别给予大黄灵仙方、p38MAPK信号通路阻断剂以及NF-κB信号通路阻断剂干预后,IRAK-1、IRAK-4、TAB2的蛋白及mRNA表达量均有不同程度下调,表明大黄灵仙方可阻碍其所介导的TLR4/NF-κB/MAPK信号通路进行信号传导,降低大鼠胆管组织炎症反应。当p38MAPK信号通路阻断剂与NF-κB信号通路阻断联合使用后,其抑制胆管炎症反应的效果明显优于单一使用信号通路阻断的大鼠,说明同时下调IRAK-1、IRAK-4和TAB2三者的炎症表达水平,能进一步抑制TLR4/NF-κB/MAPK信号通路介导的炎症瀑布反应,使得大鼠胆管炎症损伤进一步缓解。而大黄灵仙颗粒和P38MAPK信号通路阻断剂、NF-κB信号通路阻断剂三者联合使用后,上述通路指标的表达量进一步降低的同时,胆管组织炎症损伤也进一步缓解,表明大黄灵仙颗粒联合信号阻断剂可进一步促进大黄灵仙方抑制炎症信号通路的活化作用,可能是防治肝胆管结石的机制之一。但在与模型组对比中,p38MAPK阻断剂+大黄灵仙颗粒组中的IRAK-4的蛋白及mRNA表达量和p38MAPK阻断剂+大黄灵仙颗粒组中的IRAK-1的蛋白表达量异常增加,引起的炎症反应的结果与其它研究不一致[20],推测其原因可能是存在其它炎症因子与IRAK-1或IRAK-4发生竞争性结合,使TLR4/NF-κB/MAPK信号通路表达异常上升,具体作用机制仍需进行下一步验证。
综上所述,初步推测大黄灵仙方可缓解LPS诱导的大鼠胆管炎症反应,促进胆管细胞的修复,从而达到减少肝胆管结石发生及术后复发的目的,其作用机制可能与抑制TLR4/NF-κB/MAPK信号通路下游IRAK-1、IRAK-4、TAB2炎症因子的活化有关。但该方是复方中药,具有多靶点、多途径的特征,其确切的抗胆管炎症的作用机制尚未完全阐明,后续对于具体分子机制以及相关信号通路之间的联系仍需进行基因靶点敲除或网络药理学等研究。

