DTaP-IPV-Hib-HepB六联疫苗安全性及免疫原性的Meta分析
刘静文,贾征,罗兴献,傅书勇,杨悦,邢花
1.沈阳药科大学工商管理学院,辽宁沈阳 110016;
2.唐山职业技术学院,河北唐山 063000;
3.清华大学药学院药品监管科学研究院,北京 100000
随着疫苗可预防疾病种类越来越多,儿童预防接种剂次也越来越多。《国家免疫规划疫苗儿童免疫程序及说明》(2021版)中,纳入儿童免疫规划的疫苗13种,可预防12种疾病,共需接种22 ~25剂次[1]。联合疫苗是指含有2 个或多个活的、灭活的微生物或提纯的抗原,用于预防多种疾病或由同一微生物的不同种或不同血清型引起的疾病[2]。联合疫苗不仅减少了预防接种工作量,也减少了预防接种异常反应发生概率,提高了疫苗覆盖率[3]。
无细胞百白破-灭活脊髓灰质炎-b 型流感嗜血杆菌(结合)-重组乙型肝炎(DTaP-IPV-Hib-HepB)六联疫苗是目前全球已上市疫苗产品中联合程度最高的疫苗,可同时保护受试者免受百日咳、白喉、破伤风、脊髓灰质炎、乙型肝炎和b 型流感嗜血杆菌引起的侵袭性感染。2000 年,第1 支六联疫苗(Hexavac)在欧洲上市使用。截至目前,全球范围内已上市4款六联疫苗,分别为葛兰素史克公司的Infanrix hexa、赛诺菲巴斯德的Hexaxim(Hexavac 改进后的产品)和Vaxelis 以及印度Panacea 公司的EasySix。六联疫苗已经在100 多个国家和地区上市,累计使用超过1亿剂,但我国市场尚未引进。本研究采用Meta分析对DTaP-IPV-Hib-HepB 六联疫苗的安全性及免疫原性进行评价,为该疫苗在我国的实际应用提供科学依据。
1 材料与方法
1.1检索策略以吸附无细胞百白破疫苗、灭活脊髓灰质炎疫苗、b型流感嗜血杆菌疫苗、乙肝疫苗、六联疫苗、免疫原性、安全性为中文检索词,检索中国知网(China National Knowledge Infrastructure,CNKI)、中文科技期刊数据库(China Science and Technology Journal Database)、万方和中国生物医学文献数据库(China Biology Medicine,CBM)。以DTaP-IPV-Hib-HepB、DTaP/IPV/HepB/PRP-T、immunogenicity、safety为英文检索词,检索Pubmed、the Cochrane Library、Clinical Trail、Web of Science、Medline、Scopus 等外文电子数据库。检索时间均为建库至2022 年4 月1 日。检索采用主题词和自由词相结合的方式进行。
1.2文献纳入及排除标准
1.2.1文献纳入标准 ①随机对照临床试验(randomized controlled trial,RCT),无论是否采用盲法均纳入;②试验组采用DTaP-IPV-Hib-HepB 六联疫苗,对照组采用DTaP-IPV-Hib + HepB 疫苗或DTaP-IPVHepB+Hib 疫苗;③纳入文献采用的评价标准如下:安全性指标为发热、嗜睡、易怒、厌食、注射部位红斑和注射部位肿胀等,免疫原性指标为血清保护性抗体水平;④报道中的数据为原始数据或可被相关软件分析。
1.2.2文献排除标准 ①综述、系统评价等二次文献;②动物实验;③非病例对照研究;④重复发表的论文;⑤无法获得Meta分析所需的信息或相关信息不清楚的研究;⑥联合使用其他的疫苗。
1.3文献质量评价及提取 根据纳入和排除标准,由2 名研究者独立筛选文献、提取资料并交叉核对。如对纳入及排除文献存在分歧意见,则由第3 名研究者介入进行裁决。文献筛选时,首先阅读文献题目,排除明显不相关文献后,再进一步阅读摘要和全文以确定是否纳入。资料提取内容包括:①一般资料。题目、第一作者姓名、试验地点、文章发表时间、样本量等;②研究特征。研究对象年龄、疫苗接种程序、疫苗名称、疫苗制造商等;③结局测量指标。白喉、百日咳、破伤风、脊髓灰质炎、b 型流感嗜血杆菌和乙肝的血清保护性抗体水平、注射部位不良反应以及全身不良反应。采用《Cochrane系统评价员手册(6.3版)》中的Cochrane 风险偏倚评估工具(RoB 2)对纳入文献进行方法学质量评价[4],从随机化过程偏倚、偏离既定干预偏倚、缺失结果数据偏倚、结果测量偏倚和结果选择性报告偏倚5 个部分进行评分,每部分低风险计1分,总分5分为最高。
1.4统计学分析 采用Revman 5.4.1 软件对纳入文献[5-11]进行Meta分析。根据异质性情况,采用固定效应模型(fixed effects model,FE,P≥0.05)或随机效应模型(random effects models,RE,P<0.05),以相对危险度(relative risk,RR)及其95%置信区间(confidence interval,CI)为效应分析统计量,检验水准为α=0.05。首先采用χ²检验分析各研究结果间的异质性,检验水平为α=0.1,同时结合I²判断异质性大小。如P≥0.1 且I²≤50%,表明各研究间同质性较好,采用FE进行Meta分析;如P<0.1 且I² >50%,表明各研究结果间存在统计学异质性,采用RE进行Meta分析。
2 结果
2.1文献分析
2.1.1文献筛选流程及结果 对各数据库按照相应的检索模式进行初检后,共获得555 篇文献,均为英文文献。2 名研究者独立对文献进行筛选、阅读后,去除不符合纳入标准的文献,最终剩余7 篇文献,共8个RCT研究。见图1。

图1 文献筛查流程图Fig.1 Flow chart of literature screening
2.1.2纳入文献的基本特征 纳入的7篇英文文献均为RCT,共纳入研究对象3 429 人,其中试验组1 614人,对照组1 815 人。纳入文献分布于亚洲、欧洲和美洲。免疫程序分为3类,分别为2-4-6、2-3-4和3-5-11月龄。见表1。
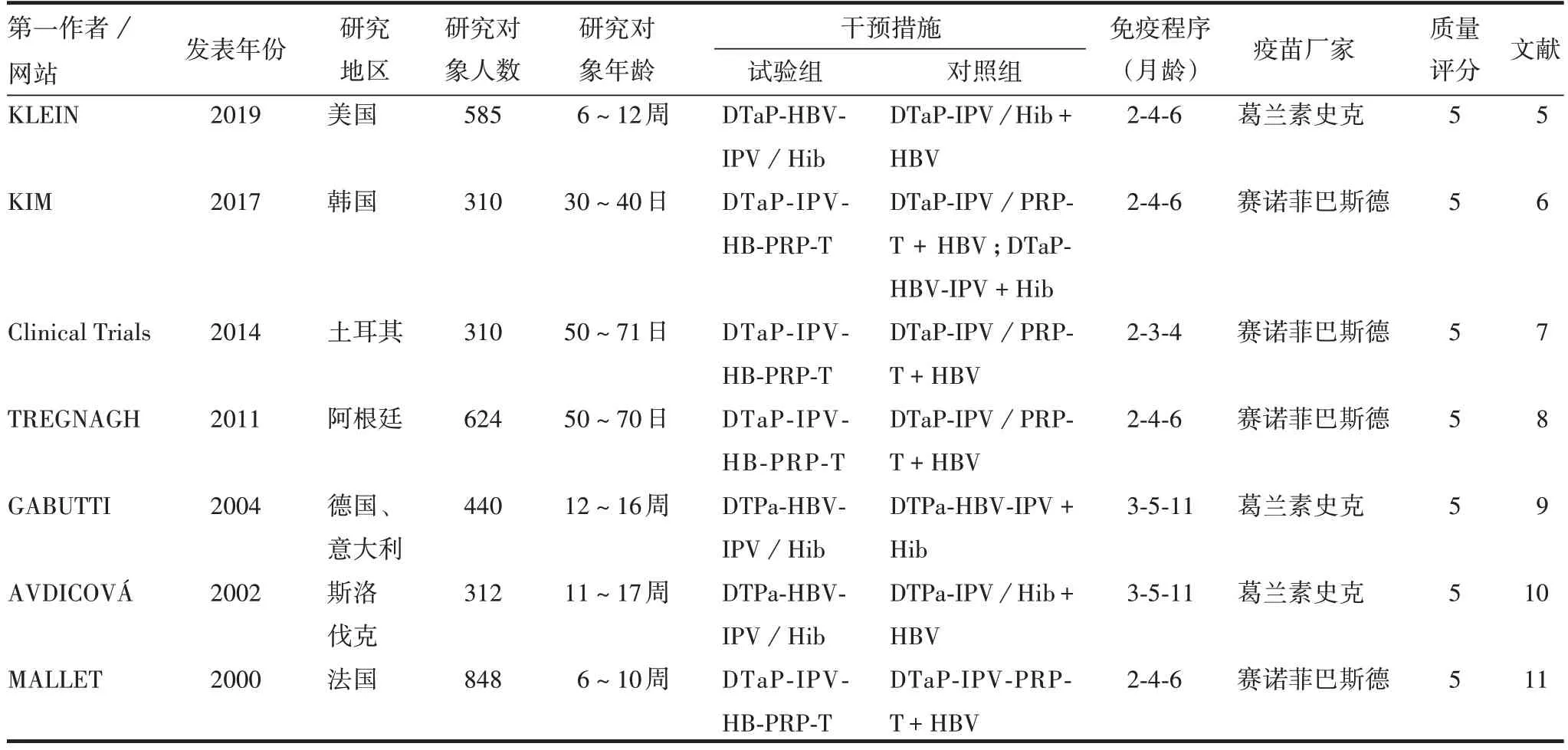
表1 符合纳入标准文献的基本特征Tab.1 Basic characteristics of literatures meeting inclusion criteria
2.1.3纳入文献的方法学质量评价 纳入的7 篇英文文献中,1 篇文献随机方法为区组随机化,6 篇文献未明确描述具体的随机方法;7 篇文献对分配隐藏、是否选择性报告研究结果均未提及;7 篇文献均未采用盲法且结果数据完整,无其他偏倚来源。见表2。
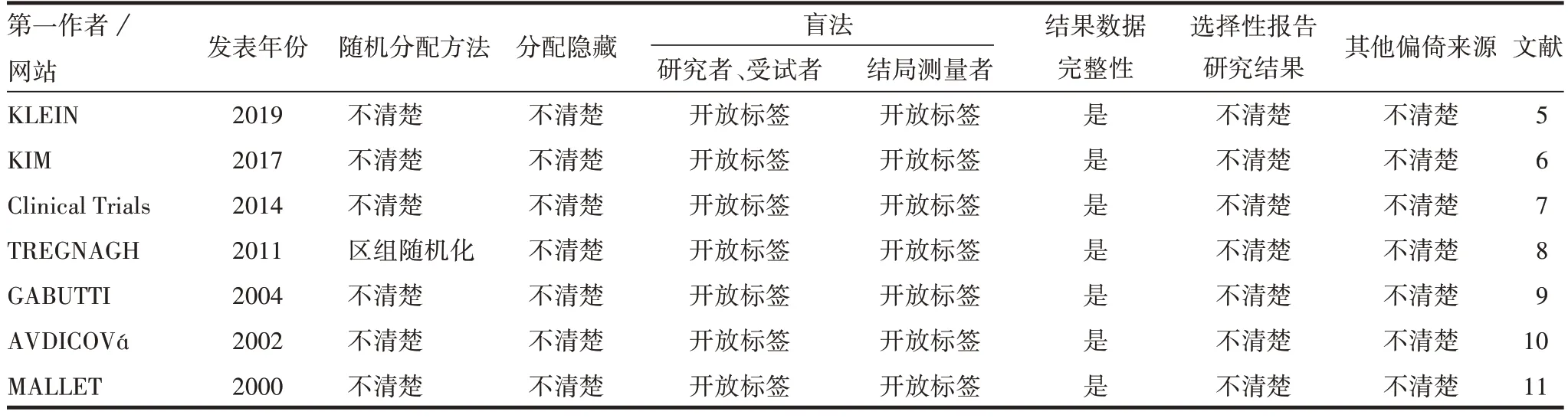
表2 纳入文献的方法学质量评价Tab.2 Methodological quality evaluation of included literatures
2.2统计分析
2.2.1DTaP-IPV-Hib-HepB 六联疫苗安全性的Meta分析 纳入英文文献经Meta分析,六联疫苗除注射部位硬结外(RR= 0.75,95%CI:0.64 ~0.88,P=0.000 3),其他注射部位不良反应发生率差异无统计学意义(P>0.05);接种六联疫苗儿童哭闹发生率更高(RR= 1.30,95%CI:1.09 ~1.55,P= 0.004),其他全身不良反应发生率差异无统计学意义(P>0.05)。见表3。
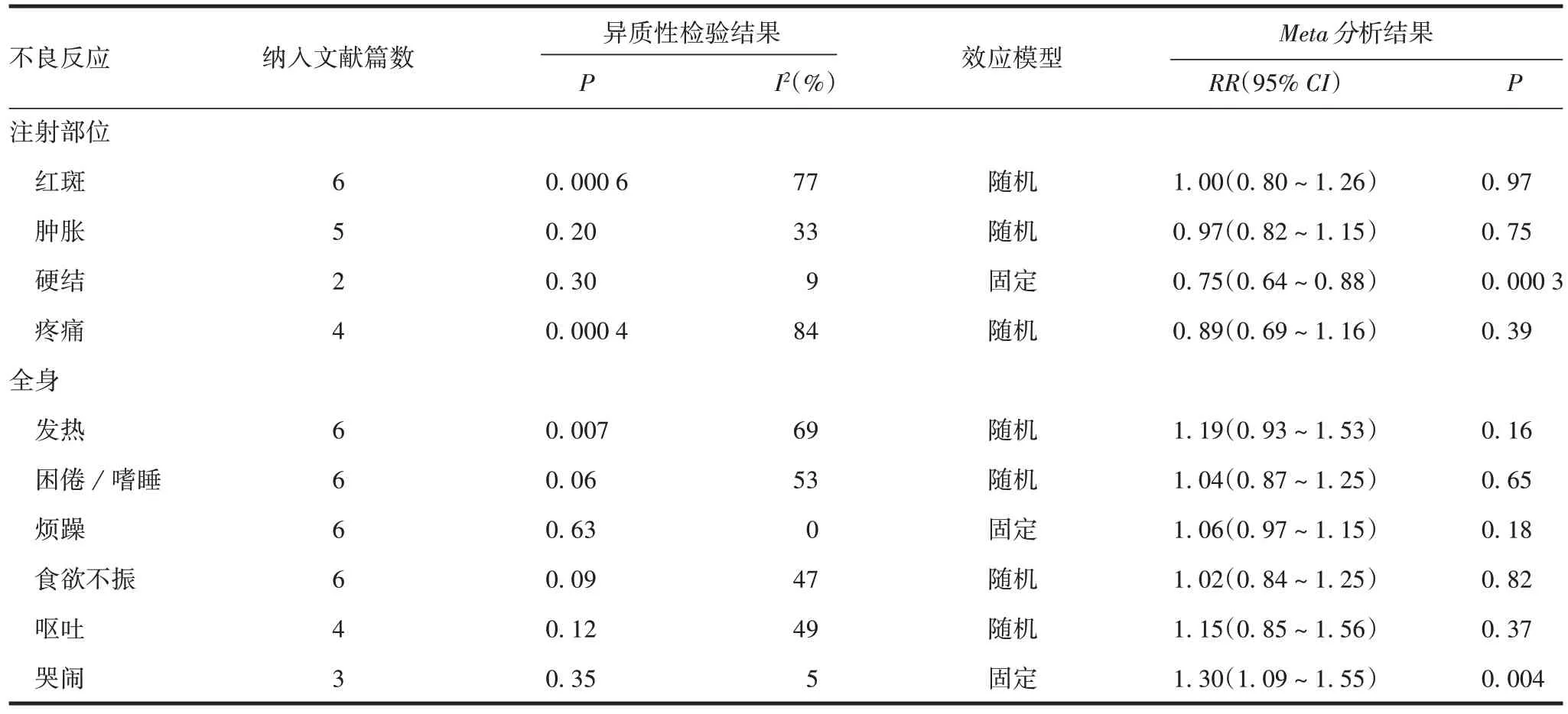
表3 六联疫苗注射部位及全身不良反应发生率的Meta分析Tab.3 Meta-analysis of incidence of injection site and systemic adverse reactions of hexavaccine
2.2.2DTaP-IPV-Hib-HepB 六联疫苗免疫原性的Meta分析 纳入的7 篇英文文献经Meta分析,六联疫苗的各项抗体指标与五联疫苗差异无统计学意义(P>0.05),见表4。37 篇文献均对乙肝表面抗体(hepatitis B surface antibody,anti-HepB)进行了分析,结果显示,接种六联疫苗与同时接种HepB 单苗后产生的血清保护性抗体水平差异无统计学意义(RR=0.99,95%CI:0.98 ~1.00,P=0.11),见图2。
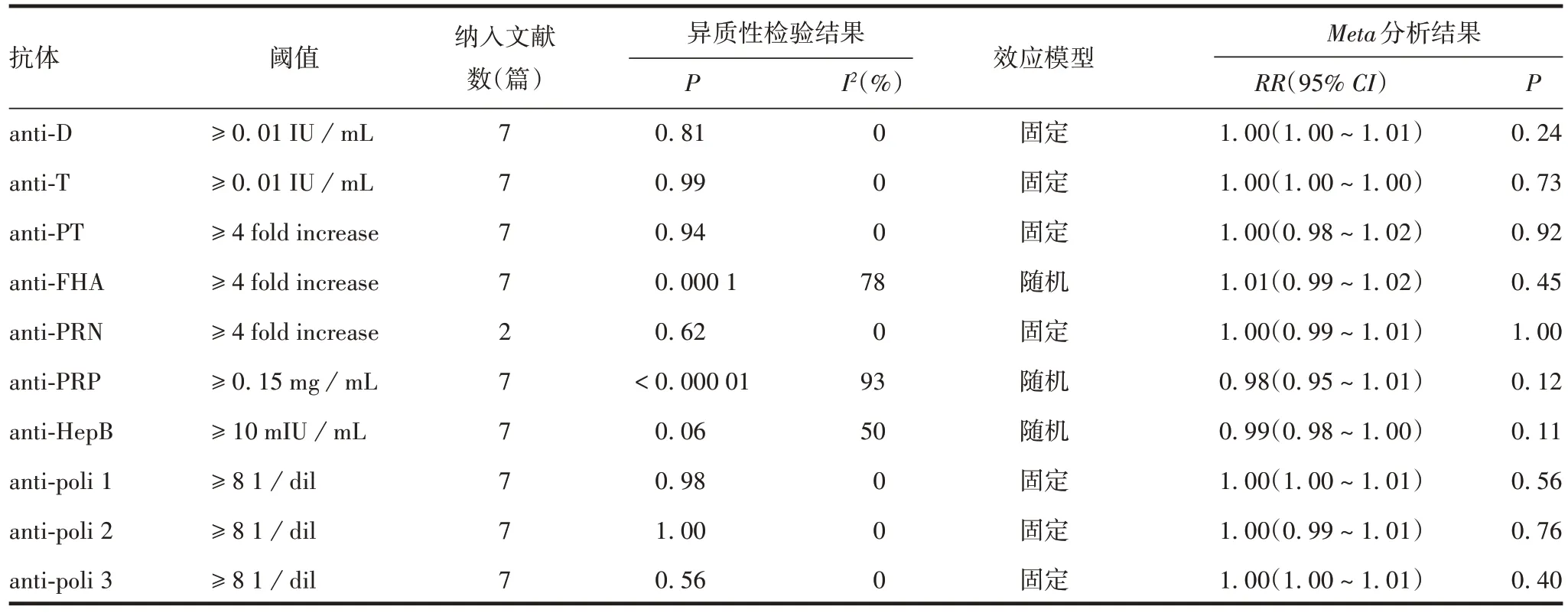
表4 血清学保护性抗体水平的Meta分析Tab.4 Meta-analysis of serum protective antibody level
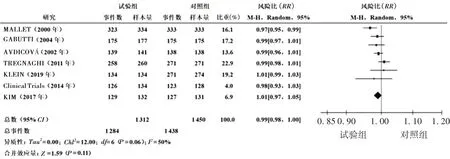
图2 anti-HepB的Meta分析Fig.2 Meta-analysis of anti-HepB
2.2.3DTaP-IPV-Hib-HepB 六联疫苗接种地区及免疫程序分层分析 在血清保护性抗体水平中,Meta分析结果均无明显改变,见表5和表6。
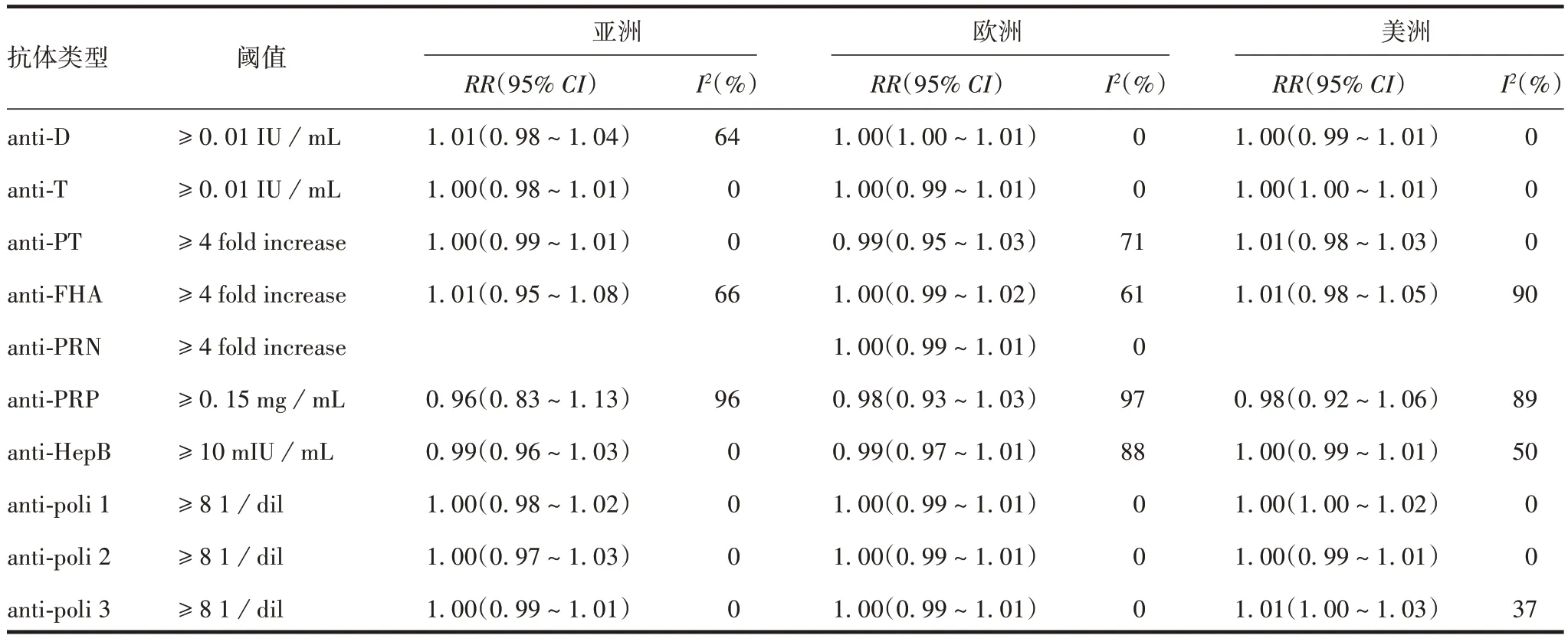
表5 血清保护性抗体水平地区分层分析Tab.5 Regional stratification analysis of serum protective antibody level
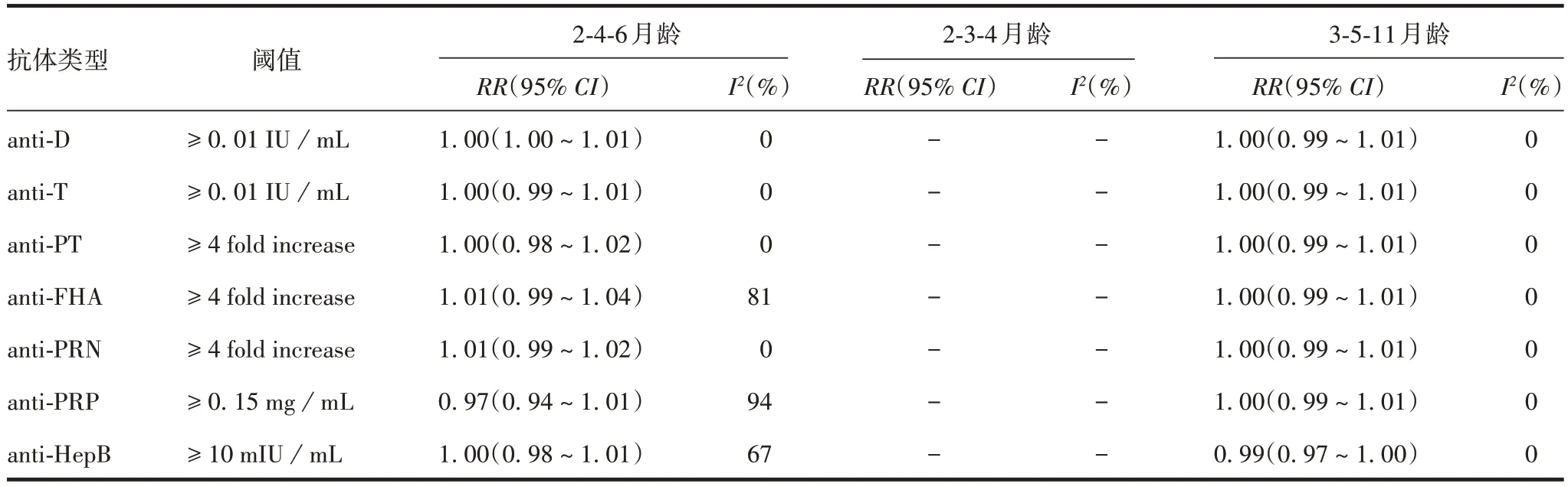
表6 血清保护性抗体水平免疫程序分层分析Tab.6 Stratified analysis of inoculation procedure for serum protective antibody level
3 讨论
联合疫苗能够在保证疫苗免疫原性和安全性的前提下,减少就诊次数,使接种疫苗更便捷,经济负担有所减轻,接种工作效率提高[12]。此外,联合疫苗的使用还与更高的疫苗接种依从性有关[13]。截至目前,DTaP-IPV-Hib-HepB 六联疫苗已在全球100 多个国家和地区被用于儿童免疫接种,但尚未在我国上市,主要问题是接种程序与我国现行HepB 疫苗免疫程序存在冲突。我国作为乙肝高发国家,新生儿应在出生24 h内接种HepB 疫苗,实现母婴阻断。国内推荐的HepB 疫苗接种程序为0-1-6 月,而六联疫苗需按照2-3-4 或2-4-6 或3-5-11 月龄的程序接种3剂才能完成基础免疫,第2 剂接种推迟对HepB 疫苗免疫原性的影响以及多剂次接种的安全性等是未来六联疫苗在我国应用面临的最主要挑战[14]。本研究通过对DTaP-IPV-Hib-HepB 六联疫苗不同接种程序的分地区分析发现,与同时接种的对照疫苗在不同接种程序下对乙肝表现出相似的血清保护性抗体水平[15]。以往研究表明,受试者3-4-5 月龄时接种3 剂六联疫苗,乙肝血清保护性抗体水平与2-4-6 月龄相似,本研究同样验证了该结论[16]。
疫苗安全性是影响预防接种依从性的重要因素[17]。已有研究表明,在使用不同免疫策略接种DTPa-HepB-IPV-Hib六联疫苗时,受种者均显示出良好的耐受性,且具有与单苗相当的安全性[18]。本研究对六联疫苗的安全性进行系统评价,结果表明,在纳入研究的5 个RCT 中,六联疫苗注射部位硬结发生率较高(P= 0.000 3)。以DTaP 为基础的联合疫苗含有的氢氧化铝佐剂有提高免疫效果的作用[19],但由于其沉淀颗粒较大且局部组织吸收困难,因此,人体注射后极易出现注射部位硬结等相关不良反应[20]。六联疫苗引起的注射部位硬结虽然具有较高的发生率,但消退较快。注射部位硬结不是六联疫苗特有的症状,而是所有灭活疫苗均常见的不良反应之一,绝大多数情况下不用进行特殊处理。
联合疫苗不良反应的总发生率小于单独接种时每种单苗不良反应发生率的总和[21],这是联合疫苗的潜在优势之一[22]。按照现有的国家免疫规划程序,在2岁以前,每个儿童需接种12剂次才能完成相关疫苗的预防接种,但DTaP-IPV-Hib-HepB 六联疫苗在2岁以前仅需接种3剂,明显减少了预防接种不良反应发生率[23]。DTaP-IPV-Hib五联疫苗已在我国上市使用10 余年,临床试验数据证明其在中国儿童中具有良好的免疫原性和安全性[24-25]。六联疫苗在五联疫苗的基础上再联合HepB 疫苗,可有效简化免疫接种程序,提高疫苗覆盖率,降低服务成本,减少疫苗储存空间需求。此外,六联疫苗已在全球多个国家或地区上市使用,接种程序超过30 种,证明不同的接种策略均安全有效[26]。
本研究的局限性在于纳入研究数量少、样本量小,可能会产生一定偏倚;研究地区大多地处欧美等发达国家,仅新加坡为亚洲国家,缺乏我国人群的数据,影响研究结果的外推行;免疫原性由于缺乏数据,无法进行抗体滴度分析。综上所述,DTaP-IPV-Hib-HepB 六联疫苗可应用于婴幼儿群体预防相关疾病。但受纳入研究数量和质量限制,尚有待进一步开展更大样本、多中心、高质量的RCT加以验证。

