MSCT 后处理技术诊断耳硬化症
关 荣,张 宏,邬小平,杨 静,杨想春,张增增,马鸣岳*
(1.西安交通大学附属西安市中心医院放射科,陕西 西安 710003;2.西安中医脑病医院医学影像中心,陕西 西安 710032)
耳硬化症指原发于骨迷路、以耳囊骨代谢异常为特征的特发性听力障碍性疾病,以双耳渐进性听力减退为主要临床症状,目前主要依靠临床表现、听力学测试及高分辨率多层螺旋CT(multi-slice spiral CT,MSCT)进行诊断。耳硬化症发病部位主要为前庭窗前区、镫骨底板及耳蜗周围骨质[1-3],因病灶微小,极易漏诊,常规MSCT 诊断敏感度为53.7%~91%[3-4]。MSCT 后处理技术可对耳硬化症发病部位行多平面重 组(multi-planar reformation,MPR)及曲面重组(curved planar reformation,CPR),能更加直观、清晰显示耳硬化症病灶,进行诊断和鉴别诊断。本研究旨在对比原始MSCT 轴位图像与采用MSCT 后处理技术对耳硬化症的诊断效能,评估MSCT 后处理技术对耳硬化症的诊断价值。
1 资料与方法
1.1 研究对象 回顾性收集2012 年12 月—2023 年3月西安交通大学附属西安市中心医院经手术证实或临床综合诊断的47 例(92 耳)耳硬化症患者(耳硬化症组)资料,其中男18 例(35 耳)、女29 例(57 耳),年龄16~63岁,中位年龄31.4 岁;收集同期经手术确诊的65 例(79耳)非耳硬化症听力障碍患者(对照组),男28 例(33耳)、女37例(46耳),年龄14~65岁,中位年龄32.3 岁。2 组患者发病前无其他耳部相关病史,均呈进行性听力下降,鼓膜完整;术前均接受颞骨MSCT 检查。本研究经医院伦理委员会批准(LW-2023-31);检查前患者均知情同意。
1.2 听力测试 纯音测听结果显示,耳硬化症组双侧听力障碍45 例、单侧2 例,包括传导性耳聋64 耳、感音神经性耳聋8 耳、混合性耳聋20 耳,均存在气骨导差,听力图呈现Carhart 切迹22 例(37耳);对照组单侧听力障碍51 例、双侧14 例,其中传导性耳聋44耳、感音神经性耳聋17 耳、混合性耳聋18 耳。
1.3 MSCT 及后处理 采用Philips Brilliance iCT 256 层螺旋CT 仪行颞骨轴位扫描。嘱患者仰卧,以下眶耳线为扫描基线,自颞骨上缘至乳突尖端行各向同性扫描,扫描参数:管电压120 kV,300 mAs,准直0.5 mm,螺距0.25,层厚0.67 mm,矩阵512×512;以骨算法重建图像,矩阵1 024×1 024,间隔0.3 mm,窗宽3 000 HU,窗位400 HU。
将MSCT 原始图像上传至Philips EBW 工作站并行镫骨、耳蜗MPR 及听骨链CPR 等后处理[5]:于颞骨轴位MSCT 显示镫骨层面中将“十字”交叉置于镫骨头,旋转斜冠状面,使之与前庭窗龛平行,调整斜矢状面以显示镫骨全貌(图1A);于MSCT 显示耳蜗底周层面将“十字”交叉置于耳蜗底周并旋转斜冠状面至与之平行,调整斜矢状面以显示耳蜗全貌(图1B);于MSCT 显示锤砧关节层面将“十字”交叉置于锤砧关节处,旋转斜冠状面使之与锤砧关节面平行,依次沿前庭窗、镫骨、砧镫关节、砧骨、锤砧关节及锤骨进行连线,并适当切换轴位图像以清晰显示上述各结构,将线条置于其中心位置以显示听骨链全貌(图1C、1D)。
由2 名具有10 年以上头颈部诊断经验的影像科副主任医师分别于盲态下依次读取全部颞骨轴位MSCT 及后处理图像并进行诊断,意见不一致时经讨论达成共识。

图1 对颞骨轴位MSCT 行镫骨MPR(A)、耳蜗MPR(B),听骨链CPR(C、D)后处理方法示意图
1.4 统计学分析 采用SPSS 22.0 统计分析软件。以描述正态分布计量资料,组间行t检验;以中位数(上下四分位数)描述偏态分布计量资料,组间行Mann-WhitneyU检验。计数资料以例/耳(%)表示,组间行χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 基本资料 2 组患者性别及年龄差异均无统计学意义(P均>0.05)。
2.2 颞骨轴位MSCT 耳硬化症组耳硬化症相关异常表现包括前庭窗前区低密度病灶伴或不伴镫骨底板增厚50 耳、单纯耳蜗周围低密度病灶4 耳、前庭窗前区低密度病灶伴或不伴镫骨底板增厚合并耳蜗周围低密度病变12 耳;对照组6 耳(先天性胆脂瘤2 耳、成骨不全4 耳)前庭窗前区见低密度病灶。根据原始MSCT图像于耳硬化症组正确诊断66 耳、对照组误诊6 耳为耳硬化症,诊断耳硬化症的敏感度71.74%、特异度为92.41%。见表1。

表1 颞骨轴位MSCT 及其联合图像后处理技术诊断耳硬化症的效能[%(耳)]
2.3 MSCT 联合后处理技术 MSCT 联合后处理技术于耳硬化症组正确诊断89 耳、对照组误诊3 耳耳硬化症,其敏感度96.74%、特异度96.20%,见表1。正确诊断的89 耳耳硬化症中,67 耳前庭窗型耳硬化症表现为前庭窗前区低密度病灶伴/或不伴镫骨底板增厚(图2),4 耳耳蜗型耳硬化症表现为耳蜗周围低密度病灶(图3),18 耳混合型耳硬化症表现为耳蜗周围、前庭窗前区同时见低密度病灶伴或不伴镫骨底板增厚(图4)。误诊3 耳中,1 耳先天性胆脂瘤表现为中耳腔内镫骨旁软组织密度影伴前庭窗前区低密度骨质破坏病灶,2 耳(1 例双耳)成骨不全表现为双侧前庭窗、耳蜗、半规管及面神经管周围骨质呈对称性、广泛低密度改变。
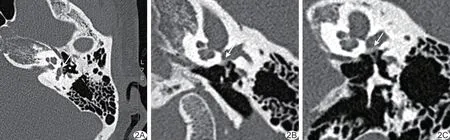
图2 患者女,36 岁,前庭窗型耳硬化症 A.颞骨轴位MSCT 图;B.镫骨MPR 图;C.听骨链CPR 图(箭示病灶)
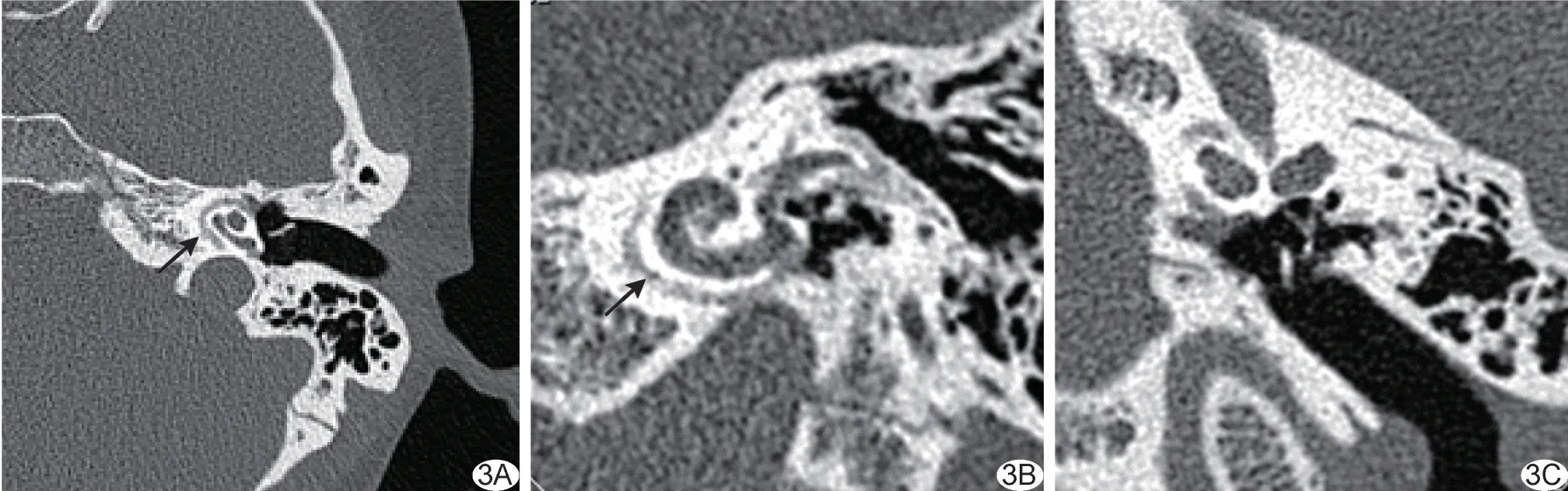
图3 患者女,30 岁,耳蜗型耳硬化症 A.颞骨轴位MSCT 图;B.耳蜗MPR 图;C.镫骨MPR 图示前庭窗前区及镫骨底板未见病变(箭示病灶)
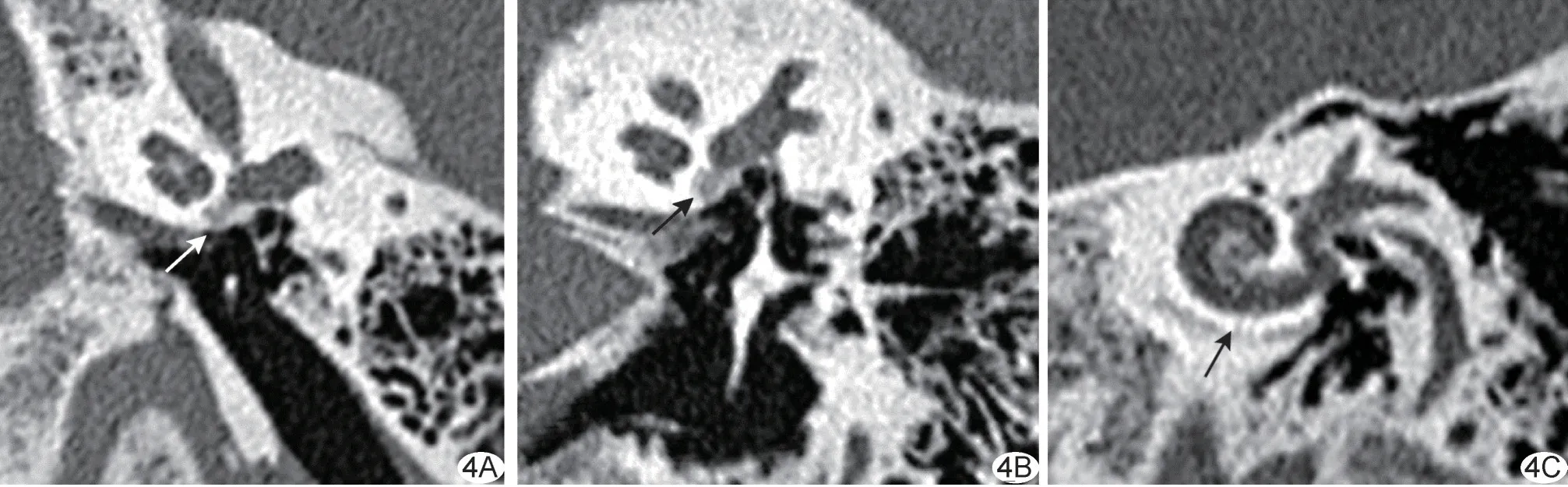
图4 患者男,26 岁,混合型耳硬化症 A.镫骨MPR 图;B.听骨链CPR 图;C.耳蜗MPR 图(箭示病灶)
2.4 诊断效能比较 相比仅根据颞骨轴位原始MSCT,MSCT 联合后处理技术诊断耳硬化症的敏感度、阴性预测值及准确率均升高(P均<0.05),而二者特异度及阳性预测值差异均无统计学意义(P均>0.05)。见表1。
3 讨论
耳硬化症是成人听力障碍常见病因之一,目前对其发病机制尚不完全清楚,可能与遗传、自身免疫、炎性细胞因子、麻疹病毒感染、激素及环境因素有关[6-7];20~50 岁为发病高峰,男女比例接近1∶2,多为双侧发病[6]。前庭窗型耳硬化症临床最常见[8-9],以渐进性听力减退而鼓膜完整为特征:发病早期因前庭窗区病变使镫骨底板与前庭窗连接固定、镫骨失去传音功能而出现进行性听力下降,表现为传导性耳聋;病变累及耳蜗则可表现为感音神经性耳聋或混合性耳聋,可伴耳鸣、幻听及眩晕。本组耳硬化症以双侧多见(95.74%,45/47),以传导性耳聋为主,混合性耳聋次之,单纯感音神经性耳聋较少。
随着MSCT 的广泛应用,近年耳硬化症检出率有所增加。耳硬化症可分为海绵化期及硬化期。海绵化期病变始于骨迷路内生软骨层,之后波及外层及内层,以海绵化骨形成为特征,病理改变包括骨迷路致密骨局限性骨质吸收脱钙、髓腔扩大,血管增多,致密骨逐渐被海绵状新生骨替代;CT 表现为前庭窗前区、耳蜗周围局灶性骨密度减低,呈裂隙状及片状,前庭窗窗龛扩大,耳蜗周围病变典型者可呈“双环”征。随着病程进展,进入硬化期后,骨质破坏与成骨可同时存在,部分海绵化骨逐渐发生骨质沉着、硬化并产生致密板层骨,部分或全部封盖前庭窗,致镫骨环状韧带固定镫骨、镫骨底板增厚及前庭窗狭小;此时骨内致密板层骨与周围正常骨质密度接近,无法依据CT 所示密度差识别骨迷路内病灶,可致漏诊,因此,发现镫骨底板增厚及前庭窗狭小,结合渐进性听力下降病史及听力学测试结果亦可考虑硬化期耳硬化症。伊景如等[10]认为骨密度CT 值差用于诊断前庭窗型耳硬化症具有一定客观性且敏感度尚可;CHEN 等[11]发现耳硬化症患者听力改变与CT 值变化相关,但仍需更多前瞻性、多中心大样本研究进一步观察。
有学者[12]认为MPR 有助于提高高分辨率CT 诊断耳硬化症的敏感性。本研究对比仅依靠颞骨轴位原始MSCT 与其联合MPR 及CPR 等后处理技术,发现后者可显著提高诊断效能;原因可能在于颞骨轴位MSCT 显示耳硬化症前庭窗前区小病灶易存在遗漏,联合镫骨、耳蜗MPR 及听骨链CPR 可更为直观地显示耳硬化症所致骨迷路骨质结构改变而提高诊断准确率。镫骨MPR 可通过局部放大及调整而将前庭窗前区骨质、镫骨底板、前庭窗及镫骨前后脚等结构清晰地显示于1 幅图像中,以直观显示前庭窗型耳硬化症病灶及其累及周围结构情况,耳蜗MPR 能在1 幅图像上直观显示耳蜗“两圈半”结构、周围病灶及“双环征”改变;听骨链CPR 则可将前庭窗前区骨质、镫骨底板、前庭窗及完整的听骨链结构同时显示于1 幅图像上,清晰显示前庭窗前区是否存在耳硬化症病灶及听骨链结构有无异常,有利于正确诊断前庭窗型和混合型耳硬化症,并与其他疾病鉴别。
综上,联合后处理技术有助于提高MSCT 诊断耳硬化症的敏感度和准确率。
利益冲突:全体作者声明无利益冲突。
作者贡献:关荣研究设计和实施、撰写文章;张宏和邬小平图像分析、修改文章;杨静研究实施、图像处理;杨想春图像分析;张增增统计分析;马鸣岳研究设计、指导、修改和审阅文章、经费支持。

