宫腔镜冷刀刨削系统在子宫内膜息肉切除术中的应用效果
侯进琳 刘美玲 李梦琦
子宫内膜息肉是一种常见的妇科疾病,子宫内膜在子宫腔内突出形成的良性肿块,会导致患者出现月经不调、不孕和不规则出血等症状[1]。有资料显示,有5%~35%的育龄女性患有子宫内膜息肉,需要进行及时治疗,以控制疾病的发展和并发症的发生[2]。宫腔镜下电切术是治疗子宫内膜息肉常用的手术方法,可避免传统开腹手术的创伤,减少患者的疼痛和术后恢复时间;同时,术野清晰,保证切除的精准、彻底,但是易导致术后并发症的发生[3]。宫腔镜冷刀刨削系统是一种在妇科手术中常用的技术,通过冷刀头直接刨削,避免了电凝带来的热损伤,减少术后疼痛和热损伤的可能性。此外,切削方式相对温和,较少引起出血,有效减少术中出血量;同时降低穿孔、术后黏连等并发症的风险,术后恢复期较短[4]。本研究对宫腔镜冷刀刨削系统在降低子宫内膜息肉术后粘连中的应用效果进行探究,报道如下。
1 资料与方法
1.1 一般资料
选择2021 年12 月—2023 年6 月于厦门弘爱妇产医院接受治疗的子宫内膜息肉拟行手术治疗患者80 例,采用随机数字表法分为对照组与观察组,各40 例。两组患者一般资料对比,差异无统计学意义(P>0.05),具有可比性,见表1。本研究通过厦门弘爱妇产医院医学伦理委员会审批(批件号:HAFC20230702-004-01)。
表1 观察组与对照组一般资料对比 (±s)
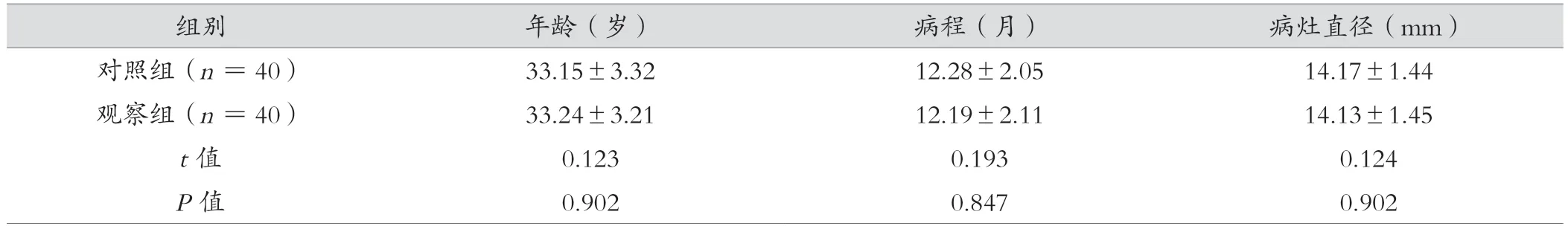
表1 观察组与对照组一般资料对比 (±s)
组别年龄(岁)病程(月)病灶直径(mm)对照组(n =40)33.15±3.3212.28±2.0514.17±1.44观察组(n =40)33.24±3.2112.19±2.1114.13±1.45 t 值0.1230.1930.124 P 值0.9020.8470.902
纳入标准:(1)子宫内膜息肉的诊断符合《子宫内膜息肉诊治中国专家共识(2022 年版)》[5]中的相关标准。(2)经临床以及超声诊断确诊。(3)具有手术治疗指征。(4)患者知晓研究内容并签署同意书。排除标准:(1)心、肺功能不全。(2)凝血功能障碍。(3)生殖系统感染。(4)具有麻醉禁忌证。(5)精神障碍。
1.2 方法
于月经结束后3 ~7 d 接受宫腔镜手术治疗。术前准备:手术前按照医生的指示进行禁食和禁水,使用米索前列醇片(华润紫竹药业有限公司,国药准字H20000668,规格:0.2 mg)0.6 mg/次,阴道上药或间苯三酚[南京恒生制药有限公司,国药准字H20046766,规格:4 mL:40 mg(按C6H6O3·2H2O 计)]40 mg 静脉推注软化宫颈。患者处于膀胱截石位,盆腔稍微抬高,使用扩张器将宫颈扩张至9.5号,通过宫腔镜观察宫腔的形态,确定病灶的位置、息肉尺寸、形态以及数目。
对照组应用德国KARL STORZ 公司生产的宫腔镜电切系统:将带有电流的细小电切环[史托斯(德国,国械注进20173010132,型号:26050G]放置在息肉基底处,通过电流的作用将息肉切除。在切除过程中确保完全切除息肉,避免损伤周围组织,完成后电凝技术止血。
观察组应用德国 KARL STORZ 公司生产的冷刀刨削系统(intergrated BIGATTI shaver,IBS)治疗:医生将冷刀刨削器头直接紧贴息肉表面,冷刀刨削系统通过旋转刀片的方式将息肉表面层层切削,直至完全切除,刨削转速1 200 ~2 100 r/min,吸引泵流量 250 mL/min。刨削过程中,使用吸引管的出水口包裹纱布,以过滤和收集刨削的标本组织。手术过程中医生需要尽可能刨削掉整个息肉,以减少残留组织的存在。
两组将术中清除的息肉组织送病理科检查。
1.3 观察指标
手术相关指标:记录两组手术时间、术中出血量并进行组间对比。
子宫内膜厚度、月经失血图评分:术前和术后3 个月(月经第15 天)通过超声测定子宫内膜厚度,使用月经失血图(menstrual blood loss chart,PBAC)[6]评估月经量。将一片日用卫生巾上血染面积与整个卫生巾面积进行对比,并给予相应的评分:血染面积占整个卫生巾面积的1/3 或以下,计1 分;血染面积占整个卫生巾面积的1/3 ~3/5,计5 分;整个卫生巾都被血染色,计20 分。评分达到100 分或以上,则表示月经量较多。
并发症和复发率:记录患者术后宫腔粘连、感染等并发症的发生率;并对患者进行为期3 个月的随访,记录息肉的复发率并对比。
1.4 统计学方法
应用SPSS 26.0 统计学软件对数据进行统计学处理。符合正态分布的计量资料采用(±s)表示,应用t检验;计数资料采用n(%)表示,应用χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 观察组与对照组手术相关指标对比
观察组手术时间、术中出血量均低于对照组(P<0.05),见表2。
表2 观察组与对照组手术相关指标对比 (±s)

表2 观察组与对照组手术相关指标对比 (±s)
组别手术时间(min)术中出血量(mL)对照组(n =40)30.46±5.119.87±1.22观察组(n =40)26.71±4.896.03±1.05 t 值3.35315.088 P 值0.001<0.001
2.2 观察组与对照组子宫内膜厚度、月经失血图评分对比
术前,两组子宫内膜厚度、月经失血图对比,差异无统计学意义(P>0.05);术后3 个月,两组子宫内膜厚度以及月经失血图评分下降,观察组低于对照组(P<0.05),见表3。
表3 观察组与对照组子宫内膜厚度、月经失血图评分对比(±s)
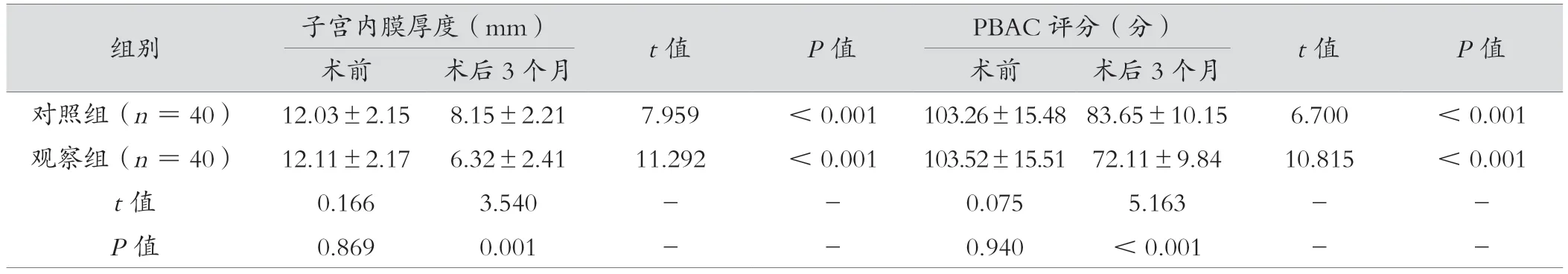
表3 观察组与对照组子宫内膜厚度、月经失血图评分对比(±s)
组别子宫内膜厚度(mm)t 值P 值PBAC 评分(分)t 值P 值术前术后3 个月术前术后3 个月对照组(n =40)12.03±2.15 8.15±2.217.959<0.001103.26±15.48 83.65±10.156.700<0.001观察组(n =40)12.11±2.17 6.32±2.4111.292<0.001103.52±15.51 72.11±9.8410.815<0.001 t 值0.1663.540--0.0755.163--P 值0.8690.001--0.940<0.001--
2.3 观察组与对照组并发症和复发率对比
观察组术后宫腔粘连、感染等并发症的发生率以及息肉复发率均低于对照组(P<0.05),见表4。

表4 观察组与对照组并发症和复发率对比[例(%)]
3 讨论
子宫内膜息肉是育龄期女性常见的宫腔病变之一,当雌孕激素比例失衡时,长期的雌激素刺激会导致周围组织发生息肉样增生,从而在子宫腔内形成多个光滑肿块[7]。因此常引起不孕、异常子宫出血、下腹不适、白带异常等症状,降低子宫内膜对受精卵的容受性等而影响女性的生育能力,治疗的首选方法是宫腔镜手术[8]。目前,宫腔镜下电切术是常用的治疗方法。近年来,随着宫腔镜冷刀技术的不断发展,宫腔刨削系统在治疗息肉方面显示出较多的优势,尤其是对于多发性息肉患者,不仅降低子宫内膜息肉的复发率,同时能降低术后宫腔黏连的发生率[9]。
3.1 宫腔镜冷刀刨削系统对子宫内膜息肉切除术手术时间和术中出血量的影响
本研究显示,观察组手术时间、术中出血量低于对照组(P<0.05)。这说明宫腔镜冷刀刨削系统在子宫内膜息肉切除术中能够提供更精确的切除和止血效果,相比传统手术方法可以减少手术时间和出血量。另外,宫腔镜冷刀刨削系统采用直接刨削的方式进行手术,相比电切术其切除息肉的过程更为迅速。刨削刀头直接贴近息肉表面进行刨削,无需额外操作,可以减少手术时间的消耗。 刨削刀头直接切削息肉,切除的过程中可以较好地控制出血情况,从而降低术中出血量[10]。宫腔镜冷刀刨削系统的使用有助于提高手术的效率和安全性、减少手术时间、缩短患者在手术台上的时间、减轻患者术中的不适感,同时也减少手术的风险和不良反应的可能性[11]。
3.2 宫腔镜冷刀刨削系统对子宫内膜厚度、月经失血图评分的影响
本研究显示,术前两组子宫内膜厚度、月经失血图对比,差异无统计学意义(P>0.05);术后3 个月,观察组子宫内膜厚度高于对照组,月经失血图评分下降,观察组低于对照组(P<0.05);这与王静璇等[12]的研究结果吻合。这说明使用该系统进行切除后,可以减少子宫内膜厚度,并改善月经失血量,从而缓解患者的症状。另外,宫腔镜冷刀刨削系统能够去除异常的组织,为子宫内膜提供更好的生长环境,促进创面的愈合和子宫内膜的再生,有助于子宫内膜恢复正常的结构和功能[13]。
3.3 宫腔镜冷刀刨削系统对降低子宫内膜息肉术后并发症和复发率的影响
本研究显示,观察组术后宫腔粘连、感染等并发症的发生率以及息肉复发率均低于对照组(P<0.05),与李小娟等[14]的研究结果具有相似性。这说明该系统的切割技术和止血措施能够减少手术中的出血风险,减少感染和其他术后并发症的发生。另外,宫腔镜冷刀刨削系统的切削方式较为温和,减少对正常组织的创伤,因此减少了宫腔粘连的风险[15]。同时在手术过程中提供了清晰的视野和放大效果,使医生能够准确观察和清除息肉组织,减少残留组织的可能性;对于感染起到预防效果,能有效降低术后感染的风险。宫腔镜冷刀刨削系统可以彻底去除病灶组织,减少了复发的可能性[16]。
本研究具有一定局限,如随访时间相对较短,长期效果和复发率的评估可能不充分。长期随访数据能够更全面地评估宫腔镜冷刀刨削系统在术后并发症和复发率方面的影响,将在临床的治疗以及后续研究中增加随访时间以更全面地评估宫腔镜冷刀刨削系统的效果和安全性。
综上所述,在子宫内膜息肉切除术中采用宫腔镜冷刀刨削系统能缩短手术时间、降低术中出血量以及膨宫液用量,改善子宫内膜厚度降低术后粘连发生率和疾病复发率。本研究结果还为子宫内膜息肉诊断标准的更新制定提供了借鉴内容。

