Cu基甲醇合成催化剂在两种模拟工业合成气中反应的结构变化及稳定性研究
邱正璞,邢爱华,张 凡,徐晓颖
(北京低碳清洁能源研究院,北京 102211)
甲醇是一种重要的化工产品和中间体,近年来在碳中和、碳达峰的背景下,甲醇汽油、甲醇燃料电池和甲醇储氢等清洁能源技术也越来越受到广泛关注[1-3]。通过合成气一步转化制备甲醇的方法已有近百年的历史,工业上甲醇合成反应的合成气一般通过煤气化、焦炉煤气和天然气转化得到,这3种原料转化后的合成气中的CO2含量存在明显差异,其中煤制气转化后CO2含量(体积分数,下同)为1%~3%,焦炉煤气为6%~8%,天然气为8%~12%。
CO2的存在对于甲醇合成反应的贡献不可忽视,有很多研究者进行了相关研究并尝试解释合成气中CO2含量的变化对催化剂微观性质及其合成甲醇的性能的影响。LAUDENSCHLEGER 等[4]研究发现,CO2含量对于实现Cu-Znδ+界面位的最佳氧化状态至关重要,如没有CO2,界面位的活性较低,金属含量较高;加入少量的CO2,会大大提高甲醇产率,而随着CO2含量的增加,甲醇的产率进一步提高,还发现CO2比CO氢化成甲醇的速率快得多,较高的CO2含量导致生成的含氧吸附物(甲酸盐)的覆盖范围增加,这些吸附物可产生更多的Cu-Znδ+界面位。蔡俊修等[5]认为CO2对CO 加氢制甲醇有着很大的影响,CO2含量在3%以下时,可促进CO加氢,CO2含量超过3%就起到阻碍作用。KLⅠER等[6]发现CO2含量较低时,能够抑制原料气中CO、H2对催化剂的活性中心Cu物种的过度还原,维持氧化态铜物种活性中心的存在,进而提高CO加氢合成甲醇的反应速率,而高含量的CO2会和原料气在催化剂活性中心上产生竞争吸附,不利于CO的加氢反应,降低反应速率。但多数研究来自于理想化的实验设计并且主要集中在催化剂催化反应过程的机理方面,对实际工业应用下的真实气体组成之间CO2的差异对原颗粒催化剂本身及其稳定性的影响规律鲜有讨论。
本文在排除气体中杂质的影响下,采用原颗粒工业甲醇催化剂在模拟工业煤和天然气制得的合成气条件下进行甲醇合成反应,探究合成气中CO2含量对Cu 系甲醇合成催化剂结构变化以及稳定性的影响,为工业生产过程中催化剂寿命的判断验证提供数据参考和指导。
1 实验部分
1.1 实验材料与试剂
选用5种不同厂家的原颗粒工业甲醇合成催化剂A、B、C、D 和E(下文统称催化剂A、B、C、D 和E),其主要成分均为CuO、ZnO 和Al2O3,部分含有少量MgO。以Al2O3为基准,催化剂中主要组分质量比如表1所示。实验过程中所用气体均从液化空气集团采购,纯度为99.99%,未经其他特殊处理直接使用。
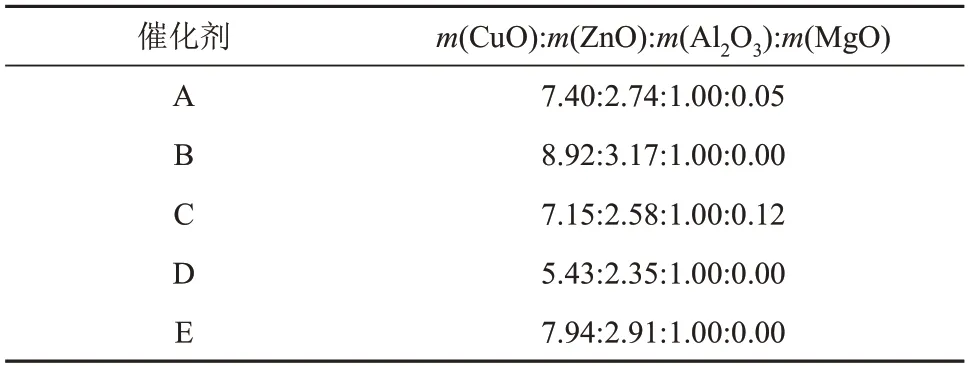
表1 催化剂的主要组分质量比Table 1 Mass ratio of main components of catalysts
1.2 实验装置与方法
1.2.1 实验装置
实验设备由上海迈瑞尔公司定制,模拟工业水冷塔单管尺寸,反应器内径40 mm,原颗粒催化剂藏量0~500 mL。反应工艺流程如图1所示,气体通过各路气体质量流量计计量后在混合罐中充分混合,此时气体定义为新鲜气,再经过预热器进行预热后进入反应器进行还原或者甲醇合成反应。产物进入冷高分,生成的甲醇或水蒸汽经过冷凝变为液体滞留在冷高分底部,适时放入冷高分取样罐。不凝气一部分经过循环系统升压并计量后,重新进入预热气前端,与新鲜气气体进行混合,再次预热后进入反应器;另一部分通过背压阀后,系统压力降至常压,经尾气表计量后排空。
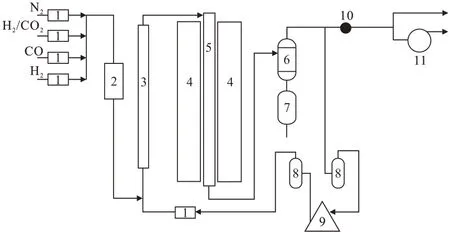
图1 反应工艺流程示意图Fig.1 Schematic diagram of reaction process flow
1.2.2 实验方法
催化剂的还原与钝化:采用定制的内径为40 mm的列管式夹套反应器(工业单管),将5种催化剂A、B、C、D 和E 分别装填于自制的316L 材质的小框中(小框高度约5 mm,直径略小于反应器内径),按照自上到下的顺序依次装填入反应器内,两个小框之间还需加入一定量5 mm 瓷球进行分隔,装填完毕气密合格后,按照还原程序(室温下以1.00 ℃/min的升温速率升至110 ℃,保持30 min,再以0.13 ℃/min的升温速率升至230 ℃,5%H2/95%N2,还原气新鲜气空速1000 h-1)进行统一还原。
还原结束后,在惰性气体氛围下待反应器降至室温,将空速为1000 h-1的钝化气新鲜气通入含有1%O2/99%N2的钝化气约20 h,结束后加大空速,反应器内部催化剂床层温度不上升视为钝化完成,保证整个钝化过程中催化剂床层温度不超过40 ℃。拆卸反应器得到催化剂样品Red-p(Reduction-passivation)。
催化剂活性测试与钝化:装填100 mL催化剂至内径为40 mm的列管式夹套反应器(工业单管)中,重复催化剂还原程序,将催化剂进行还原,在合成气气氛下,以反应温度225~230 ℃和反应压力5 MPa为基准,在相应的合成气条件下(表2)进行甲醇合成反应(Feed Ⅰ为模拟工业煤制合成气组成的气源,Feed ⅠⅠ为模拟天然气转化制合成气组成的气源),反应结束后在惰性气体氛围下待反应器冷却至室温,并重复钝化操作。拆卸反应器得到催化剂样品Rea-p(Reaction-passivation)。5 种催化剂需要通过单独实验来完成。
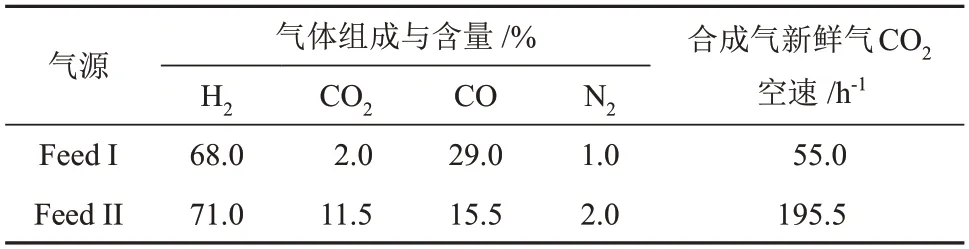
表2 两种模拟工业气源的反应条件Table 2 Reaction conditions of two simulated industrial gas sources
1.3 催化剂表征方法
采用Bruker D8X射线衍射系统对催化剂样品进行 X 射线衍射分析,管电压和管电流分别为40 kV和40 mA,采用Cu Kα射线(0.15406 nm),扫描速率为2 (°)/min。
采用Rigaku ZSX Primus ⅠⅠX-Ray荧光光谱仪(XRF)分析催化剂实际元素组成。
2 结果与讨论
2.1 催化剂稳定性对比
将催化剂B分别在Feed Ⅰ和Feed ⅠⅠ的条件下进行了催化剂的稳定性测试,结果如图2 所示。在稳定的工艺条件下,选取实验过程中约0~600 h 的数据进行催化剂稳定性的对比,由图2可知,在两种条件下,催化剂B转化CO和CO2的能力均出现了明显的下降的趋势:在Feed Ⅰ条件下运行600 h后,CO转化率从97.67%降至95.91%,降低了1.76%,在Feed ⅠⅠ条件下运行600 h 后,CO 转化率减小更为明显,降低了5.53%;同样,Feed Ⅰ条件下运行600 h,CO2转化率从63.59% 降至49.53%,降低了14.06%,在Feed ⅠⅠ条件下降低了6.68%。以上数据显示反应气中高CO2含量会明显抑制催化剂CO转化能力的稳定,却提高了其部分保持CO2转化稳定性的能力,这可能是由于CO2含量不同导致催化剂的活性位产生了变化。因此,催化剂转化CO 和CO2能力的衰减情况与CO2含量有关。王东升等[7]在260 ℃、5 MPa和4000 h-1条件下的浆态床甲醇合成过程中发现,较高的CO2含量会使催化剂加快失活。栾友顺等[8]发现添加少量的CO2改变了Cu 基催化剂的失活机理和路径,催化剂失活的活化能不随CO2含量的变化而改变,CO2在反应中不是C 源,而是弱氧化剂。
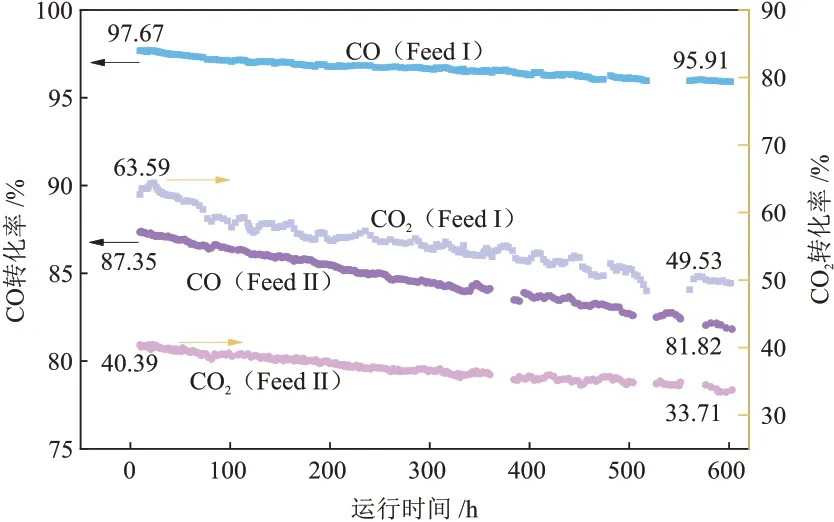
图2 催化剂B在Feed I和Feed II条件下的稳定性Fig.2 Stability of type B catalysts under Feed I and Feed II conditions
2.2 催化剂使用前后晶粒尺寸对比
传统铜系甲醇合成催化剂的主要成份是CuO、ZnO 和Al2O3,催化剂在使用前需经还原活化处理,将惰性的CuO 还原为具有催化活性的单质Cu。目前较为统一的观点为Cu晶粒尺寸增大是Cu基甲醇催化剂失活的主要原因之一。FⅠCHTL 等[9]发现CuO/ZnO/Al2O3甲醇合成催化剂的失活不仅与Cu 表面积的减小有关,同时也观察到烧结过程中ZnO 晶粒尺寸的增大,因此分析使用前后ZnO晶粒的尺寸大小对于分析催化剂的失活机理也很关键。
对5 种催化剂还原、钝化后的样品进行了XRD表征,结果如图3所示。由图3可知,所有样品均存在明显单质Cu的特征峰,说明钝化效果好。
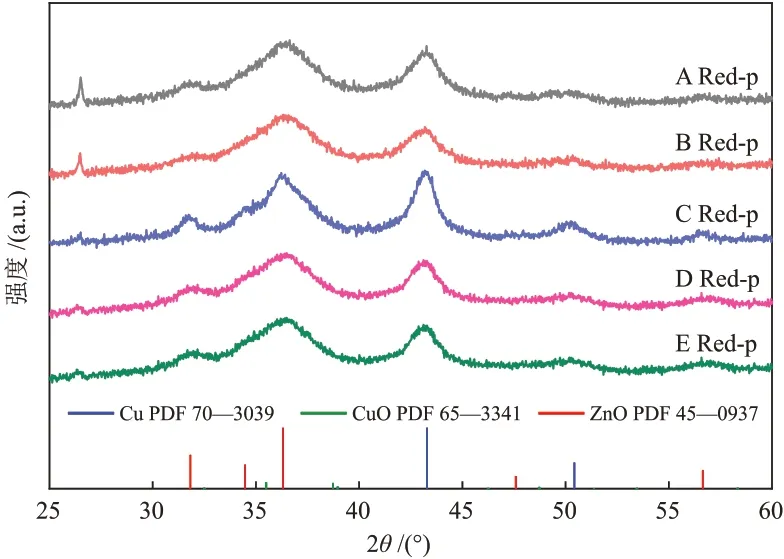
图3 5种催化剂还原、钝化后样品的XRD谱图Fig.3 XRD patterns of samples after reduction and passivation of five catalysts
选取2θ=43.3°单质Cu 的衍射峰计算Cu 晶粒尺寸,选取2θ=36.2°处ZnO的衍射峰计算ZnO晶粒尺寸,相对球形度选择0.89,得到的结果汇总于表3。催化剂A、B 和D 还原后的初始Cu 晶粒尺寸均为5~6 nm,催化剂C和E的Cu晶粒尺寸偏大,为7~8 nm,因此不同催化剂在相同还原条件下得到的初始Cu晶粒已经存在明显差异;ZnO 晶粒整体差别不大,但对比Cu晶粒看,ZnO晶粒尺寸更小,且Cu晶粒尺寸较小的催化剂对应的ZnO 晶粒尺寸也偏小。BALTES 等[10]认为催化剂前驱体Zn/Cu 孔雀石具有Cu和Zn的同构结构,易于交换位置,使两种金属之间的相互作用比纯相中更强,因该结构形成了更小的粒子,从而提高了催化剂性能。王琼[11]认为催化剂中Cu-ZnO 界面是反应的活性中心,Cu 与ZnO 晶粒尺寸越小说明分散的越均匀,越有利于两组分的相互接触,增加组分间的协同作用,提供了更大的比表面积,能够为后续反应提供更多的活性中心,催化剂的活性越高。

表3 5种催化剂还原、钝化后的初始Cu晶粒尺寸对比Table 3 Comparison of initial Cu particle sizes after reduction and passivation of five catalysts
其中催化剂C和D常见于工厂在Feed Ⅰ条件下使用,催化剂B 和E 常见于工厂在Feed ⅠⅠ条件下使用,催化剂A 在两种条件下均可使用。将3 种催化剂分别置于Feed Ⅰ和Feed ⅠⅠ条件下进行反应,运行不同时长后进行钝化,钝化后得到不同反应气体条件下不同反应时间后的样品(图4)。由图4 可知,5种催化剂在参与一定时间的反应后,Cu和ZnO的衍射峰均增强,表明Cu和ZnO晶粒尺寸均增大,说明在反应过程中Cu和ZnO都直接或者间接作为活性物种参与了反应。
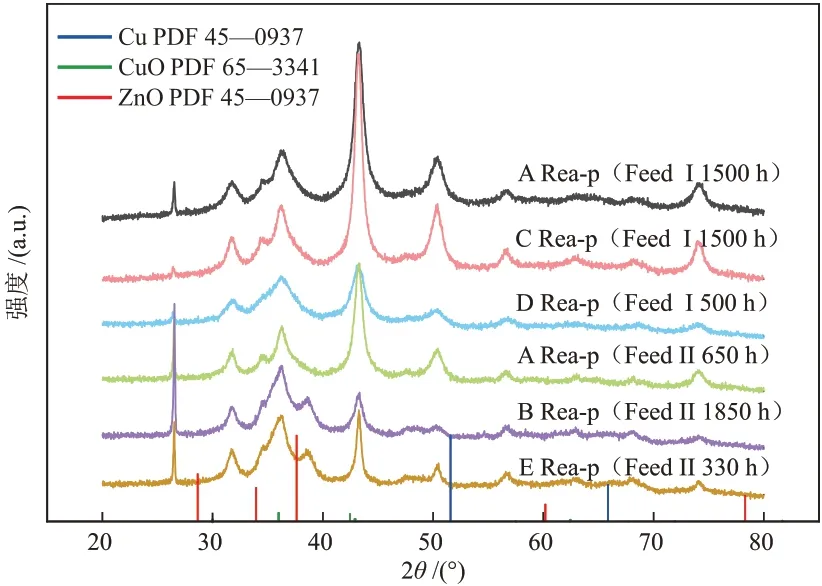
图4 不同条件下不同催化剂反应不同时间后钝化样品的XRD谱图Fig.4 XRD patterns of passivated samples of different catalysts with different reaction time under different conditions
选取2θ=43.3°的单质Cu 的衍射峰计算Cu 晶粒尺寸,2θ=36.2°ZnO 的衍射峰计算ZnO 晶粒尺寸,结果汇总于表4和表5。
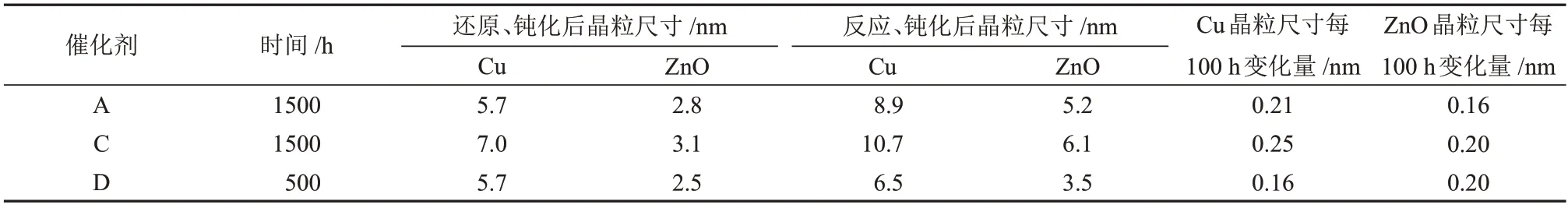
表4 Feed I条件下3种催化剂在反应不同时间后Cu与ZnO晶粒尺寸变化Table 4 Changes in particle sizes of Cu and ZnO of three catalysts with different reaction time under Feed I
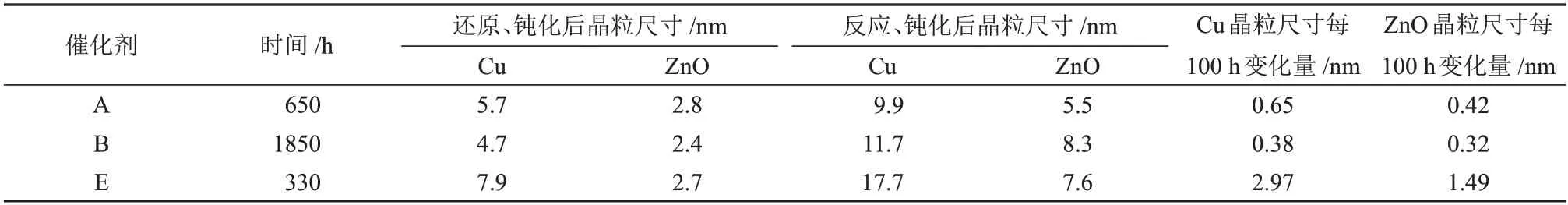
表5 Feed II条件下3种催化剂在反应不同时间后Cu与ZnO晶粒尺寸变化Table 5 Changes in particle sizes of Cu and ZnO of three catalysts with different reaction time under Feed II
由表4 可知,在Feed Ⅰ条件下,催化剂A 和C的测试是分别在两套装置上同时进行的,通过反应时间为1500 h 的数据对比,催化剂A 和C 的Cu晶粒尺寸分别增大了3.2 nm 和3.7nm;催化剂A 和C 的ZnO 晶粒尺寸分别增大了2.4 nm 和3.0 nm。结合图2 的稳定性测试结果,催化剂C 出现了比A 更明显的CO 转化能力减小的趋势,结合活性数据分析,由于催化剂C 的Cu 和ZnO 晶粒尺寸绝对值增加较快,导致Cu-ZnO 有效界面减少更为明显,带来了更明显的活性衰减。TOPSOE 等[12]研究认为,在研究Cu/ZnO 基催化剂体系的催化作用时,需考虑表面合金位点的存在。表面合金物种将随着气体环境氧化电位的增加而逐渐被破坏,这可能会导致ZnO 物种的形成,这些物种最初可能会以小簇的形式装饰Cu 表面,也可能发生偏析形成较大的ZnO 晶体或与原始ZnO 载体结合。催化剂D 和A 具有相同的初始Cu 晶粒尺寸,但催化剂D 反应时间更短,Cu 晶粒尺寸每100 h变化量为催化剂C >A >D,催化剂会随着在某一温度下的持续使用而逐渐烧结;而ZnO 晶粒尺寸每100 h 变化量为催化剂D=C >A,说明不同催化剂受同一反应气体的影响不同,这可能是催化剂配方与其合成工艺的差别造成的。陈海波[13]发现焙烧时间对 CuO 和 ZnO 平均晶粒尺寸以及催化性能有影响。
同样在Feed ⅠⅠ条件下,3 种催化剂A、C 和D 在反应一定时间后晶粒尺寸也出现明显增大的现象。由表5 可知,催化剂A 的Cu 晶粒尺寸在反应650 h后增加了4.2 nm;催化剂B 的Cu 晶粒尺寸在反应1850 h后增加了7.0 nm,对比催化剂E来看,仅仅反应了330 h,Cu 晶粒尺寸增至17.7 nm,结合图5 发现,反应100 h后,催化剂E的Cu晶粒尺寸增幅达到了2.97 nm,明显高于催化剂A 和B 的增幅,ZnO 也有完全相同的规律。催化剂B与E具有更显著的对比,催化剂B与E同期运行,催化剂B又在E的运行条件的基础上又延长了约1500 h,而催化剂B 的增长速率仍然比E 更低,同样说明了不同催化剂的稳定性有一定差别。
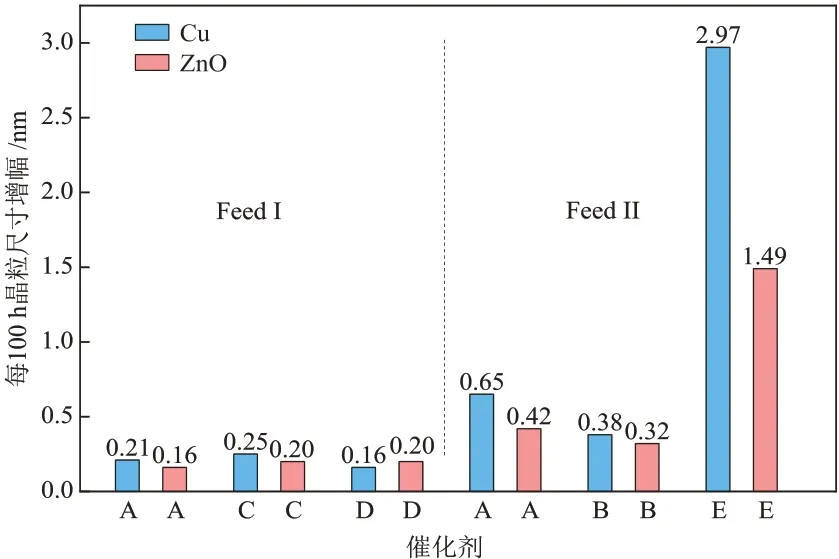
图5 不同催化剂的Cu、ZnO晶粒尺寸增幅对比Fig.5 Comparison of particle size increase of Cu and ZnO of different catalysts
由图5可知,相同运行时间内,在Feed Ⅰ条件下反应的催化剂的Cu 晶粒尺寸增幅远小于在Feed ⅠⅠ条件下的Cu 晶粒尺寸增幅,也就是说,高CO2含量会促使Cu和ZnO晶粒尺寸的增大。
与此同时,在研究过程中发现煤制气和天然气制甲醇过程中,煤制气产生的粗甲醇中水含量一般在5%左右,天然气为18%,这是由于CO2转化为甲醇必定生成同物质的量的水,因此,CO2含量高必然会产生更多的水,不同的CO2含量会造成催化剂活性组分晶粒的不同程度长大。
2.4 催化剂失活机理分析
从催化剂反应后晶粒尺寸增大情况看,晶粒尺寸与反应时间成正相关,并且都经历了缓慢累积长大的变化过程,催化剂一旦开始使用,所有Cu 与ZnO的晶粒尺寸便开始缓慢增大,符合迁移与团聚以及Ostwald 熟化的猜想。
研究认为甲醇合成过程中,同时存在CO和CO2作为碳源的反应,当界面主要被Cu+物种覆盖时,CO是主要的碳源;当金属Cu覆盖表面时,CO2是主要的碳源,碳源取决于催化剂表面Cu+和Cu0的数量比例,因此存在Cu+与Cu0之间的相互转化[14-15]。结合前期催化剂性能稳定性的变化,在高CO2含量下,Cu表面Cu+和Cu0数量比例降低,更多Cu0覆盖Cu表面,使得Cu 晶粒尺寸加速增大,同时导致CO 转化能力的稳定性下降,反而CO2转化能力的稳定性有所提升。
ZnO 可能在富CO2环境中生成ZnCO3,会破坏Cu 与ZnO 之间的协同作用。通过分析所有反应后样品的XRD,未能找到ZnCO3对应的特征衍射峰,代表了ZnO 变性的可能性较小。CHOⅠ等[16]发现通过物理混合的Cu/SiO2和ZnO/SiO2在甲醇反应过程中,ZnO 未改变Cu 的形貌,但Zn 从ZnO 迁移到Cu/SiO2上,形成了Cu-Zn活性位点。KANAⅠ等[17]在600 K 以上高温还原Cu/ZnO 催化剂时,观察到ZnO 部分迁移到Cu 表面并溶解到Cu 晶粒中形成Cu-Zn合金,Cu晶粒上的ZnOx被还原为Zn,而Zn在之后CO2加氢反应条件下被CO2再氧化。同样AMANN 等[18]通过X 射线光电子能谱进行分析,认为CO2加氢时,ZnO以团簇或纳米晶粒的形式出现,而纯CO中,表面Zn-Cu合金更为突出,甲醇合成中ZnO 同样存在与Zn 相互转化的过程。合成气中较高的CO2含量,促使Zn 物种转化过程中更多的以ZnO团簇或纳米晶粒的形式出现,也导致ZnO晶粒尺寸快速增大。除此以外,KULD等[19]研究表明,来自ZnO的Zn在Cu表面的覆盖率是催化剂活性丧失的主要原因,且具有更小晶粒尺寸的纳米级ZnO或高比表面的催化剂的甲醇合成活性更高。
由图6可知,催化剂还原结束后,会提供一个初始界面上的Cu+和Cu0数量比例,n(CO2)/n(CO)增加的同时,表面覆盖物种的Cu+和Cu0数量比例降低。在反应过程中,Cu+在迁移过程中更多的被Cu 表面捕获,对CO 转化的稳定性产生明显影响。越来越多的Cu覆盖了活性表面,使得CO2作为碳源的能力得到提升,催化剂开始呈现一定的CO2的转化稳定性。与此同时,Cu-Zn(O)表面动态迁移中的Zn有更高的几率迁移至ZnO表面,脱离界面束缚重新变化为ZnO,最后Cu 和ZnO 并在各自表面逐渐富集,使得Cu和ZnO晶粒尺寸同时加速增大。
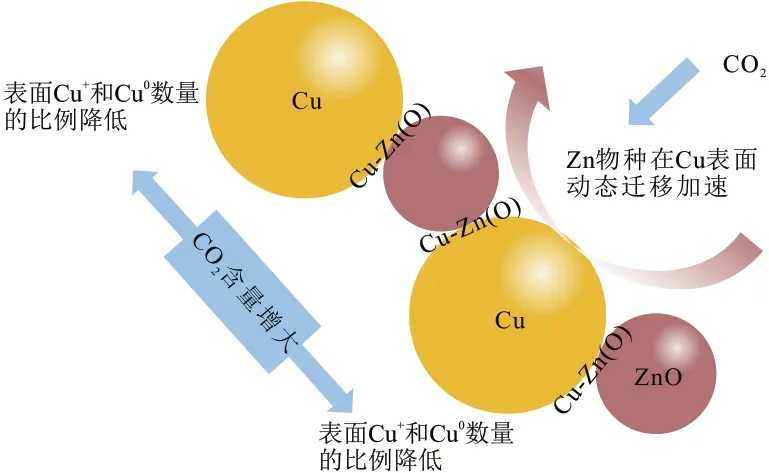
图6 CO2含量变化导致Cu与ZnO晶粒尺寸变化的机理Fig.6 Mechanism of particle size variation of Cu and ZnO due to CO2 content variation
3 结论
本文选用5种原颗粒工业催化剂,在模拟的两种工业合成气组成的条件下,于40 mm的列管式夹套(工业单管)反应器上进行了催化剂性能和稳定性测试,并对反应前后催化剂结构进行了分析,得到如下结论。
(1)催化剂在两种条件下反应后均出现了Cu和ZnO晶粒尺寸增大的情况,不同催化剂之间的晶粒尺寸变化存在差异。催化剂A 在模拟天然气制合成气条件下每100 h Cu 和ZnO 晶粒的尺寸增大速率约是模拟煤制合成气条件下的3 倍;在天然气制合成气条件下催化剂A、B和E的Cu和ZnO晶粒尺寸增大速率均明显超过煤制合成气,高CO2含量更容易促使Cu和ZnO晶粒尺寸增大。
(2)采用催化剂B 在模拟的两种工业合成气中分别反应600 h,其在模拟煤制合成气条件下的CO转化率降低1.76%,CO2转化率降低14.06%,而在天然气制合成气条件下CO转化率降低5.53%,CO2转化率降低6.68%,不同合成气明显影响催化剂性能的稳定性,高CO2含量加速破坏催化剂对CO 转化能力的稳定性,提升了CO2转化能力的稳定性。
(3)不同合成气的n(CO2)/n(CO)影响催化剂表面的Cu+和Cu0的数量比例,Cu+和Cu0的数量比例随n(CO2)/n(CO)的增加而降低,这导致Cu+在Cu表面覆盖度降低,并转化为Cu。同时高含量的CO2也加速了Zn物种在Cu表面的迁移,使其更多的以ZnO团簇和纳米晶粒的形式出现,造成了催化剂在不同合成气条件下催化剂活性晶粒尺寸的变化,影响了催化剂的稳定性。

