天然虾青素提取和纯化的研究进展
◆作者:郝孔利 张策
◆单位:山东金城生物药业有限公司
虾青素(3,3'-二羟基-b,b'- 胡萝卜素-4,4'- 二酮)是一种氧化类胡萝卜素,虾青素(AXN)最初发现于1938 年,并首次用作水产养殖的色素。自1991 年以来,虾青素已被批准作为食品补充剂的色素(Nouchi等,2020)。虾青素的抗氧化活性是玉米黄质、叶黄素、角黄素、β- 胡萝卜素的10 倍,是α-生育酚的100 倍,其抗氧化活性比辅酶Q10 或维生素E 高约100~1000 倍(Zhang 等,2020)。虾青素对癌症、高血压、糖尿病、心血管疾病、胃肠疾病、肝脏疾病、神经退行性疾病和皮肤病在内的多种疾病具有潜在作用,经常被用来对抗病变细胞的氧化损伤(Aneesh 等,2022)。
虾青素有两个对称的手性中心,有3 种异构体(3R,3'R)、(3R,3'S)和(3S,3'S)。合成虾青素含有三种异构体的混合物,比例为25∶50∶25。天然虾青素也含有三种异构体,但比例与合成虾青素不同。藻类产生的虾青素,例如淡水雨生红球藻,产生90%以上的3S,3'S 异构体,酵母黄叶菌产生90% 以上的3R,3'R 异构体(Rezanka 等,2020)。合成虾青素的抗氧化能力低于天然虾青素,这可能是因为合成虾青素是外消旋混合物,含有三种异构体。此外由于合成中间体和副产物的潜在残留,合成虾青素用于人类存在安全问题(Shah 等,2016)。迄今为止,合成虾青素尚未被批准用于人类(Koller 等,2014)。目前,市场上95%以上的虾青素是人工合成的(Nouchi 等,2020)。
在动物饲料的应用中,全微生物细胞可以配制成饲料成分,而不需要提取色素。然而,对于更多的定制应用,如化妆品和食品配料,色素的提取和纯化尤为重要(Harith 等,2020)。虾青素是微生物细胞内的产物,有效的工艺应该使提取的色素保持其稳定性、颜色和生物活性。提取虾青素的纯度决定了它的市场价格,可能在2500~7000 美元/kg之间(Shah 等,2016)。鉴于虾青素对健康的潜在益处,其在食品工业、医药、化妆品和动物饲料(如鲑鱼和大虾)中的需求正在迅速增加。到2025 年,其全球市场预计将达到25.7 亿美元(Nouchi 等,2020)。文章拟介绍雨生红球藻和红法夫酵母虾青素下游工艺提取纯化的方法,旨在为推动天然虾青素的规模化生产提供理论依据。
1 细胞回收
AXN 通过生物技术工艺生产,下游工艺的第一步就是细胞回收。通过这种方式生产的虾青素,必须选择一种合适的细胞回收方法,以确保得到最多的细胞,并减少与细胞脱水的相关成本。微生物细胞主要通过重力沉降、絮凝、浮选、膜过滤和离心来回收,表1 列举了这几种回收方法的优缺点。

表1 微生物细胞回收常用的方法
2 细胞破碎和天然虾青素的提取
2.1 细胞破碎
AXN 的提取过程中,细胞破碎和提取是相关的,提取AXN的量取决于所选细胞破碎方法的效率。细胞破碎技术主要有珠磨、超声波、渗透冲击、高压匀浆、冻融、酶裂解和化学裂解,这些技术可以单独应用或组合应用。珠磨和高压均质等机械方法可以保证AXN 的高破碎率。然而,这些技术的能耗很高,同时这些方法会产生较多的细胞碎片,局部的过度加热可能会破坏AXN。据报道,珠磨和高压匀浆主要用于破坏大规模雨生红球藻细胞的(Panis 等,2016)。有研究表明,β-1,3- 葡聚糖酶、蛋白酶、纤维素酶和果胶酶可对雨生红球藻和红酵母有很高的细胞破碎率和AXN 提取率(Harith等,2019;Ye 等,2020)。离子液体(IL)是由相对较大的不对称有机阳离子与较小的无机或有机阴离子组成的盐。具有高水解活性、对各种有机和无机化合物显著的增溶能力、高导电性、低挥发性、低粘度以及高热和化学稳定性等多种特性。Choi 等(2018)评估了10 种基于1- 乙基-3- 甲基咪唑(Emim)的离子液体、果胶酶/纤维素酶(1∶1)和4 mol/L 的HCl 破坏雨生红球藻细胞,结果表明AXN 的提取率分别为86.71%、71.0%和80.52%。IL 被认为是机械细胞破碎方法的真正替代品(Choi 等,2018;Liu 等,2019)。
2.2 天然虾青素的提取
2.2.1 传统溶剂萃取方法
在AXN 提取过程中,大量的AXN 是通过两步获得的。第一步涉及细胞破碎,第二步涉及有机溶剂提取。在AXN 提取的过程中,乙醇、丙酮、己烷、异丙醇、二氯甲烷和二甲基亚砜(DMSO)是最常用的,美国食品药品监督管理局(FDA)将它们归类为对人类健康低风险物质,这些溶剂在一定限度内被批准用于制药(L 等,2021)。
2.2.2 新型萃取方法
加压液体萃取(PLE)是一种在高温和高压下应用常规溶剂对固体或半固体样品进行萃取的技术。该技术使用的溶剂为液态,更容易渗透到细胞基质中,从而能够提高AXN 的溶解度和萃取率,但高温可能会影响不耐热类胡萝卜素的稳定性,因此应用该方法时必须把控好温度(Gallego 等,2019)。
超临界流体萃取(SFE)具有萃取和分离的双重作用,超临界流体具有高渗透性、扩散性,能够迅速渗透到复杂基质的孔隙中。SC-CO2(超临界CO2)是大规模生产用最多的技术(Panis 等,2016;X 等,2020)。SC-CO2比传统有机溶剂更易扩散到细胞内,在温度为40~60℃下运行,避免了化合物的降解,最终产品无溶剂,在减压过程中易与AXN 分离,通常使用乙醇作为助溶剂来提高萃取效率(Antonio 等,2018)。影响SFE 萃取率的主要条件是温度、压力、助溶剂的类型和浓度、溶剂流速和提取时间。SFE 的主要限制是设备成本高(X 等,2020;Musmarra 等,2020)。
脉冲电场(PEF)辅助提取技术的原理是应用重复的短高压脉冲来诱导生物材料(植物、动物或微生物细胞)的透化(电穿孔)。这种技术具有低能耗、易于扩展和非热能的优势,并且可以最大限度减少细胞碎片的释放,因此还能够进一步提高提取物的纯度(熊强等,2022)。PEF 会随着样品的电导率和质地的变化而变化,因此脉冲持续时间和电场强度应随样品的不同进行优化(Aguilar-Machado等,2020)。表2 列举了不同破壁和提取方法对AXN 回收率的影响。
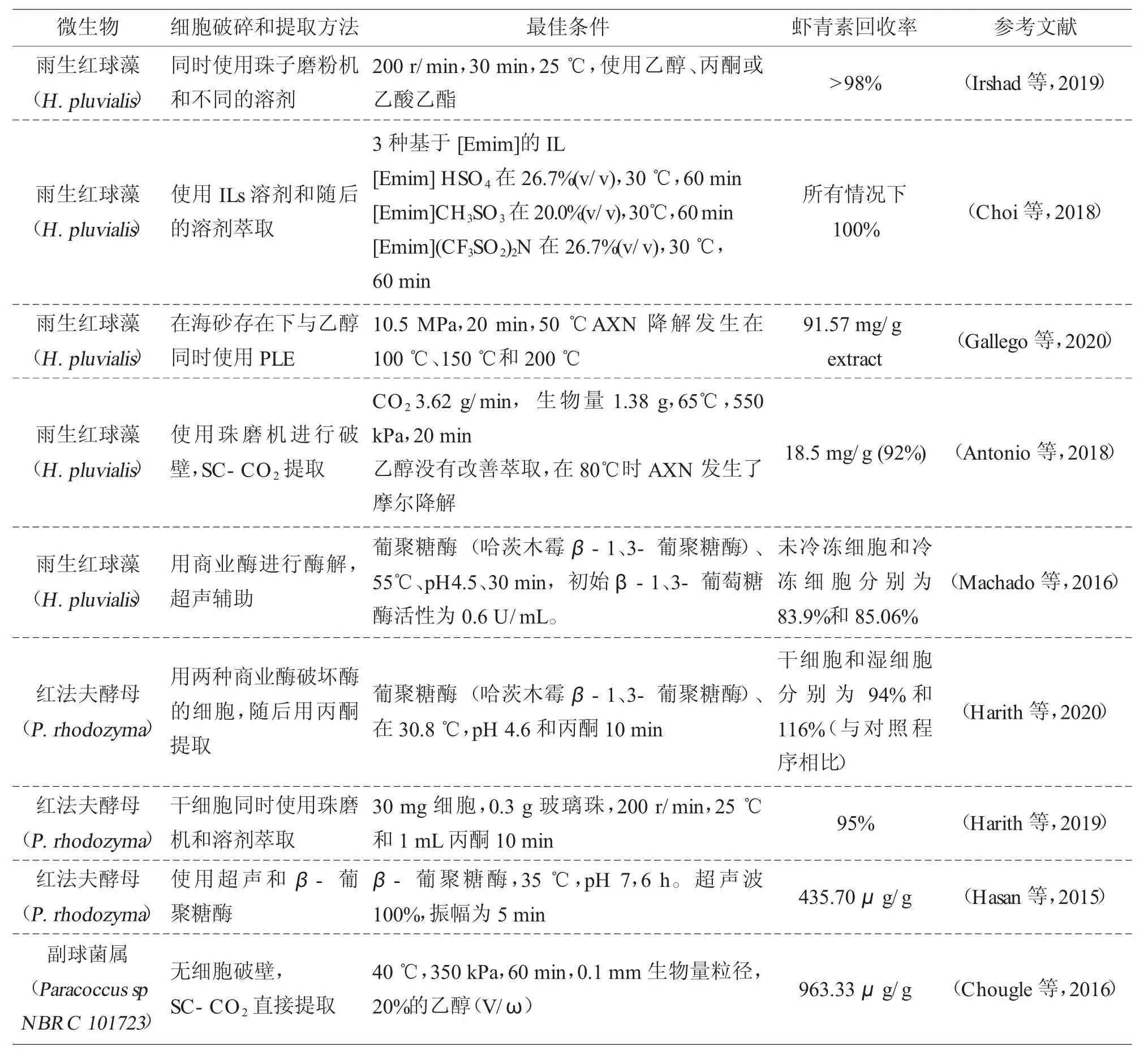
表2 AXN 细胞破壁和提取方法
Praveenkumar 等(2015)报道了使用金纳米手术刀在雨生红球藻细胞中切开并提取AXN,随后该细胞治愈了伤口并重新萌发,释放出含有AXN 的游动孢子。Bauer 和Minceva(2019)使用乙酸乙酯直接从含有雨生红球藻细胞的培养基中提取AXN。
3 天然虾青素的纯化
AXN 的生物活性已在临床试验中得到广泛测试,其有效性使其成为具有巨大潜力的化合物,可用作营养品或医药产品,制备这类产品时,必须保证化合物的纯度(L 等,2021)。AXN 提取完成后,由于其他类胡萝卜素、蛋白质、盐、酯、细胞碎片、消泡剂、溶剂和其他污染物等杂质,需要进行纯化。表3 是有关AXN 纯化过程的最新研究结果。
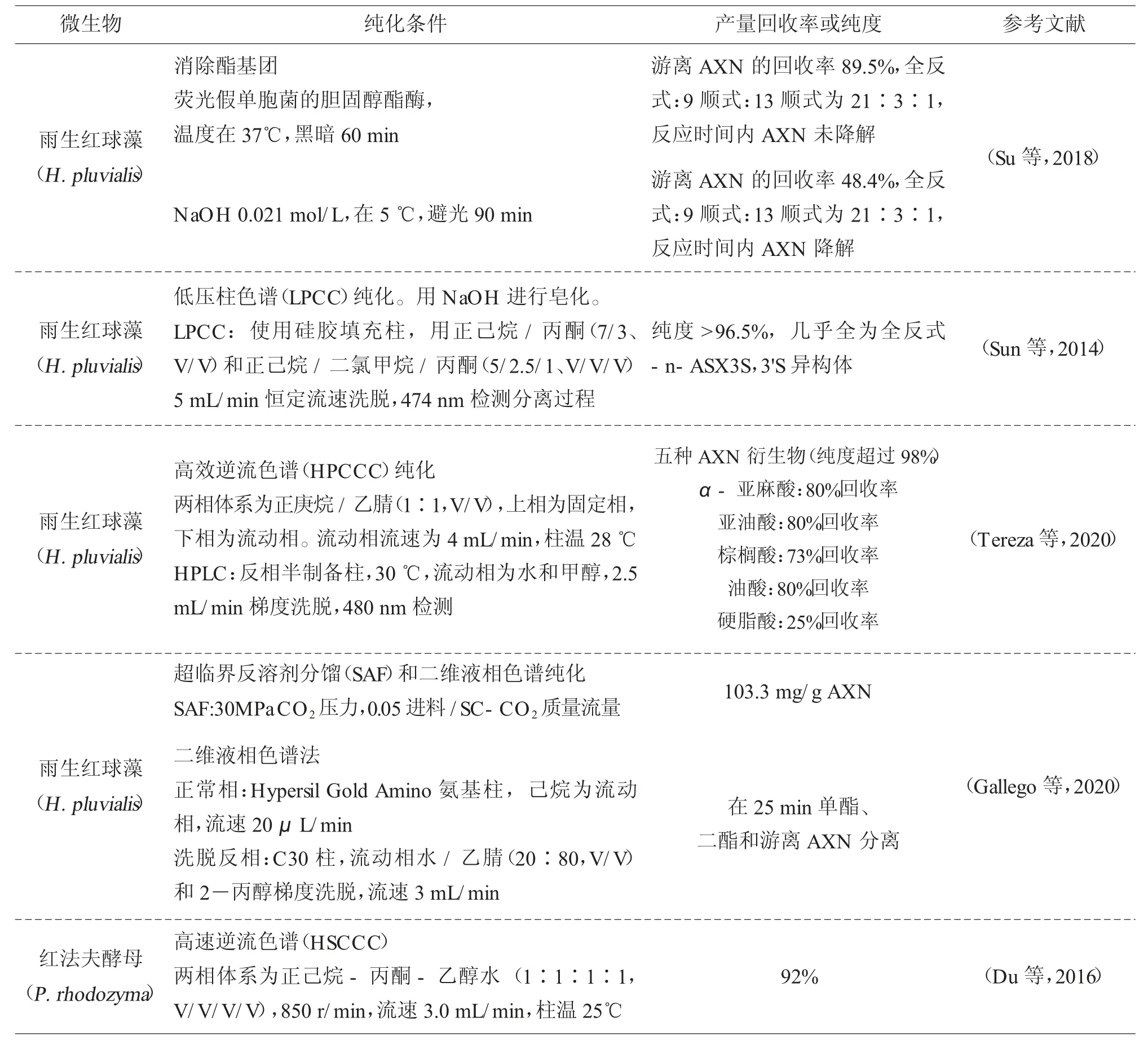
表3 AXN 纯化方法
4 结论
天然虾青素比合成的虾青素具有更好的生物相容性,但天然虾青素的生产成本较高。近年来,破壁技术和提取技术取得了很大的进展,为天然虾青素的高效提取提供了新的思路和方法,如脉冲电场法、离子液体法、DES(低共溶剂)法、双水相法等破壁提取技术,但这些研究还处于初步阶段,没有进一步运用到生产过程中。SC-CO2技术因其提取效率高且分子没有降解(温和的操作条件),而被广泛用于大规模AXN 提取过程。在制药应用中,需要高纯度产品。目前已通过液- 液色谱结合液- 固色谱的方法得到99%的高纯度虾青素。然而在AXN 生产工艺中未呈现。
天然虾青素下游工艺占虾青素生产成本的80%,天然虾青素生产成本的改进主要是下游工艺,这些阶段的任何改进都可能对整个工艺的可行性产生相当大的影响。因此对下游工艺的改进仍然是重中之重。
参考文献:(略)

