玉米赤霉烯酮和脱氧雪腐镰刀菌烯醇双特异性抗体的制备及检测方法构建
王云云, 石广革, 孙嘉笛, 陆 欣, 纪 剑, 孙秀兰*,
(1.江南大学 食品学院,江苏 无锡 214122;2.菏泽市食品药品检验检测研究院,山东 菏泽 274000)
真菌毒素是一类由曲霉菌、镰刀菌、青霉菌等丝状真菌产生的次生代谢产物。 常见的真菌毒素如赭曲霉毒素、玉米赤霉烯酮(ZEN)、黄曲霉毒素、脱氧雪腐镰刀菌烯醇(DON)和伏马菌素,可通过日常饮食被生物体摄入并在体内累积,对生物体的肝肾功能、生殖系统、免疫功能等造成不可逆的伤害[1-2]。2013—2014 年,Han 等对麦麸在内的357 个饲料样本的真菌毒素污染情况调查显示,DON 是中国饲料中最常见的真菌毒素,其次是ZEN 和AFB1[3]。 2019年,Yang 等对国内市场上的576 个玉米制品中的真菌毒素污染水平进行评估,结果表明78%的样品至少存在一种真菌毒素污染, 其中DON 和ZEN 的发生率分别为63%和46%[4]。 可见,DON 和ZEN 广泛存在于粮食以及饲料中, 对粮食中ZEN 和DON 开展同步快速检测对保障粮食安全具有重要意义。
目前针对DON 和ZEN 的检测手段主要包括仪器检测分析法和免疫检测法两大类[5-7]。 气相色谱、液相色谱、气相色谱质谱联用等大型仪器法可以实现高精确度检测,但同时复杂的样品处理流程使其无法实现现场检测[8]。 免疫检测方法是一种基于抗原抗体特异性结合的检测手段。 相对于色谱和质谱方法, 免疫检测方法对操作人员和场地要求低,且能够实现低成本、快速灵敏检测污染物[9]。 目前,通过动物免疫获得的多克隆或单克隆抗体是免疫检测中使用的主要识别元件。 其中多克隆抗体特异性差,检测背景信号值高,不适于真菌毒素的精准定量;单克隆抗体的特异性强,批间差异小,但技术要求高、制备周期长、成本高且只能检测一类具有类似结构的真菌毒素。 因此,特异性抗体的高效制备是免疫检测方法开发的关键因素。
近年来,基因重组抗体技术发展迅速。 该技术将含有抗体基因的载体导入到原核或真核生物中,在一定条件下培养可诱导产生具有生物活性的蛋白质。 重组抗体克服了传统抗体生产的局限性,无须经过复杂的细胞融合筛选过程, 具有生产周期短、重复性好的优点。 相比传统的杂交-杂交瘤融合技术,重组表达的双特异性抗体无须经过多次细胞融合筛选的过程,且不易发生由染色体丢失造成的生产能力丧失的情况。 目前双特异性抗体类型有区内交换抗原结合片段、抗原结合片段-单链抗体、单链抗体-单链抗体(scFv)2等[10]。 其中(scFv)2形式可以通过多肽连接臂连接2 种scFv, 具有结构简单、相对分子质量低且不存在错误组装、表达效率高等优势[11]。 因此,作者首先在哺乳动物细胞Expi293F中表达了ZEN 单链抗体(ZEN-scFv)和DON单链抗体(DON-scFv),进一步设计和制备可识别ZEN 和DON 的双特异性抗体(Bis-scFv)并建立酶联免疫检测方法。 表达抗体Bis-scFv 制备周期短、重现性好和可定向改造,有助于提高抗体制备效率,实现多种物质同时检测,具有良好的应用前景。
1 材料与方法
1.1 材料与设备
1.1.1 菌株与细胞大肠杆菌(E.coli DH5α)感受态:天根生化科技有限公司(北京);Expi293F 细胞:赛默飞世尔科技有限公司(美国);表达质粒构建、引物合成和基因测序由安升达生物科技有限公司(苏州)完成。
1.1.2 主要试剂玉米赤霉烯酮(ZEN)、脱氧雪腐镰刀菌烯醇(DON)、黄曲霉毒素B1(AFB1)、赭曲霉毒素A(OTA)和T-2 毒素等标准品:Sigma-Aldrich公 司;ExpiFectamine293 转 染 试 剂 盒、Opti-MEM I无血清培养基、Expi293F 表达培养基、Gene Ruler DNA Ladder Mix: 赛默飞世尔科技有限公司 (美国);卵清蛋白(ovalbumin,OVA)、无缝克隆试剂盒、氨苄青霉素(Amp):生工生物工程有限公司(上海);PCR Master Mix 高保真酶: 翌圣生物科技股份有限公司(上海);辣根过氧化物酶标记抗His 标签单克隆抗体:ImmunoWay 生物技术公司;His 标签蛋白纯化试剂盒、预染蛋白质Marker:碧云天生物技术公司(南通);牛血清蛋白(bovine albumin,BSA):国药集团化学试剂有限公司(上海)。
1.1.3 实验仪器T-100 链式反应核酸扩增仪、Mini-PROTEAN Tetra1658033 蛋白质电泳系统:Biorad 公司(上海);Thermo3111 恒温培养箱:赛默飞世尔科技有限公司(美国);VS-1300L-U 超净工作台:安泰空气技术有限公司(苏州)。
1.2 实验方法
1.2.1 质粒设计抗体由两组轻链(VL、CL)和重链(VH、CH1、CH2和CH3)组成,结构呈现“Y”型,见图1(a)。 抗体的可变区负责识别结合抗原,可变区的VH 和VL 可通过长度通常为10~25 个氨基酸残基的多肽接头连接形成scFv,见图1(b)。 其作为小相对分子质量的单个多肽更容易被改造和表达,并且能够保留原始抗体的性质[12]。作者首先构建了ZENscFv 和DON-scFv 重组质粒, 并在哺乳动物细胞Expi293F 中表达。 通过柔性连接子 (Gly4Ser)3将ZEN-scFv 和DON-scFv 基因序列连接用于融合表达,获得双特异性抗体Bis-scFv,见图1(c),以期可以同时结合ZEN 和DON 这2 种不同的表位。 为促进重组抗体通过Expi293F 细胞进行高表达分泌,在DON-scFv、ZEN-scFv、Bis-scFv 前添加信号肽(SP),信号肽序列为:MGWSCIILFLVATATGVHS[13-14]。DON-scFv 和ZEN-scFv 基因序列来自NCBI 数据库,DON-scFv NCBI:AY151141.1,AY151140.1;ZENscFv NCBI:U74672.1,U74671.1。
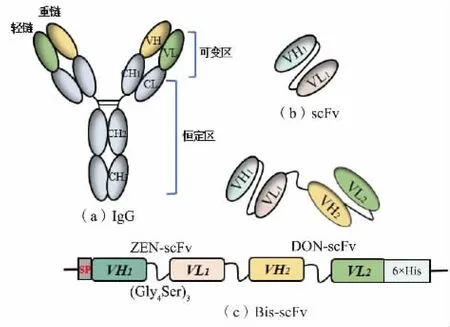
图1 重组抗体质粒设计Fig.1 Design of recombinant antibody plasmid
1.2.2 重组载体构建双特异性抗体表达载体构建采用无缝克隆技术,构建流程见图2,构建过程使用的引物见表1。 CH-Linker-DON-scFv-pTT5 载体由金斯瑞生物科技股份有限公司构建,保存于作者所在实验室。 Bis-scFv-pTT5 重组载体的构建采用无缝克隆技术, 将CH-Linker-DON-scFv-pTT5 载体中的CH 基因替换成ZEN-scFv。 以ZEN-scFvpCMV 为模板, 以BIS-SCFV-F1/F2 为引物, 经过PCR 扩增获得ZEN-scFv 片段 (802 bp)。 以CHLinker-DON-scFv-pTT5 载体作为模板, 以BISSCFV-V1/V2 为引物对经PCR 扩增获得Linker-DON-scFv-pTT5 载体片段(5 227 bp)。 利用无缝克隆酶连接上述的PCR 纯化产物, 取100 ng Linker-DON-scFv-pTT5 的PCR 产物和40 ng ZEN-scFv 扩增片段,两者之间的摩尔比保持在1∶2~1∶3,加入10 μL 的2×无缝克隆酶混合液, 用无菌水补足体系至20 μL。 混合物置于50 ℃水浴下反应40 min,立即冰浴冷却2 min 后进行热激转化(42 ℃、90 s)。转化后的E.coli DH5α 进行菌落PCR 验证,经琼脂糖凝胶电泳验证,将长度正确的菌株接种到含有氨苄的LB 培养基中培养6 h, 用于测序。 相同操作进行DON-scFv-pCMV 重组载体构建。

表1 质粒构建所用引物Table 1 Primers used in plasmid construction
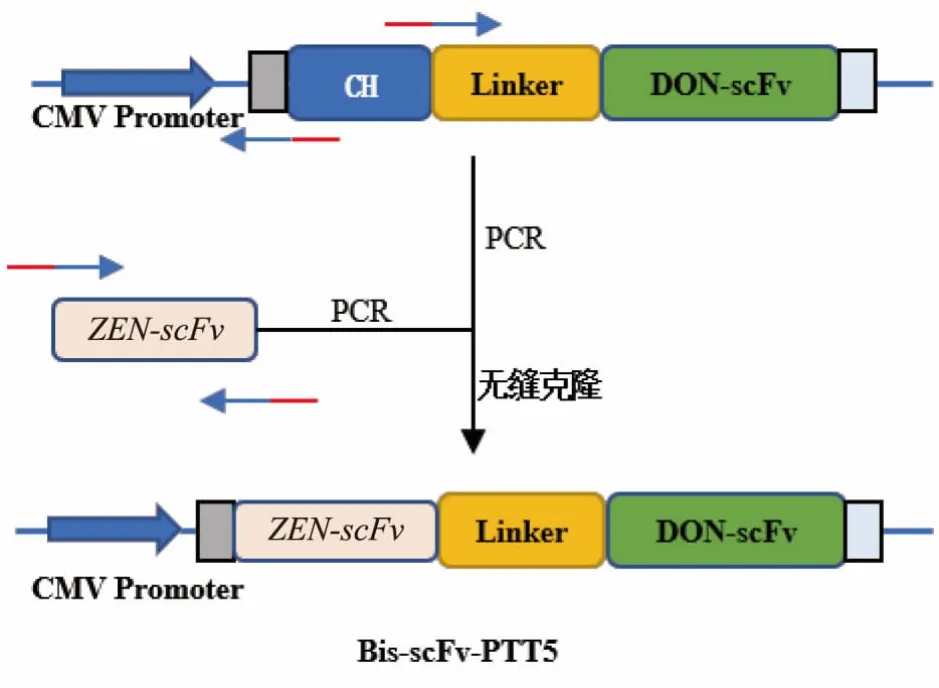
图2 Bis-scFv-pTT5 构建流程Fig.2 Construction process of Bis-scFv-pTT5
1.2.3 哺乳动物细胞表达重组抗体Expi293F 细胞的培养和转染遵循Vazquez-Lombardi 的实验方案[14]。 首先将液氮保存的1×107个Expi293F 细胞加入25 mL 培养基中, 在37 ℃含体积分数8.0%的CO2条件下培养并传代3~4 代。取7.5×107个细胞置于25.5 mL 培养基中, 并向其中加入表达抗体质粒和阳离子脂质体转染试剂继续培养,18 h 后再加入增强剂Ⅰ和增强剂Ⅱ以维持细胞活性, 继续培养7 d,将培养物以3 200 r/min 离心20 min,上清液用于纯化。
1.2.4 表达产物纯化以及聚丙烯酰胺蛋白质电泳验证 向3 mL 柱体积的层析亲和柱中加入1 mL 的Ni-TAN 凝胶, 加入1mL 的非变性裂解液平衡2~3次。 将待纯化的上清液加入亲和柱中,富集分离目的蛋白质。加入1 mL 的洗涤液(含20 mmol/L 咪唑)洗涤3 次,去除多余的杂蛋白质。 加入1 mL 的洗脱液(含250 mmol/L 咪唑),重复洗脱6 次,收集洗脱液。纯化产物用12.5 g/dL 的十二烷基硫酸钠聚丙烯酰胺凝胶电泳(SDS-PAGE) 验证相对分子质量大小。 为保护抗体的活性, 对上述的洗脱产物用PBS缓冲溶液(0.01 mol/L,pH 7.4)透析3 d,去除杂质离子。
1.2.5 抗体亲和性验证抗体亲和性采用ELISA法测定。 步骤如下:
1)包板 向96 孔板加入100 μL 质量浓度为1 μg/mL 的DON 或ZEN 抗原,37 ℃孵育2 h,然后用PBST (含有体积分数0.05%吐温-20 的PBS 溶液)洗涤5 次。
2)封闭 PBST 洗涤后,每孔加入250 μL 含有5 g/dL 脱脂奶粉PBS 缓冲液,37 ℃封闭2 h,结束后再将96 孔板用PBST 洗涤5 次并干燥。
3)加样 取100 μL 纯化抗体、50 μL 纯化抗体与50 μL 不同质量浓度的毒素标准品的混合液,37 ℃孵育1 h,PBST 洗涤5 次。
4)加二抗 将100 μL 辣根过氧化物酶标记的抗His 标签二抗加入孔中,并在37 ℃下孵育30 min,PBST 洗涤5 次。
5)显色读数 向每个样品孔中加入100 μL 的3,3’,5,5’-四甲基联苯胺溶液,15 min 后加入50 μL 浓度为2 mol/L 的H2SO4溶液终止显色反应,测定OD450。 添加体积分数10%甲醇的PBS 溶液到对照孔, 其OD450为B0, 添加DON 和ZEN 标准品的OD450为B。 以毒素质量浓度为横坐标,B/B0为纵坐标,用origin 2018 软件通过非线性拟合得到标准曲线,并确定B/B0为50%时所对应的真菌毒素的质量浓度,即半抑制质量浓度(IC50)。 此外,通过对比相同质量浓度下的ZEN、DON、OTA、AFB1、T-2 毒素对于抗体与抗原结合的抑制效果, 验证抗体的特异性。 对各组抑制率采用graphpad prism8.0.1 单因素方差(ANOVA)分析,不同字母标记(a/b)表示2 组差异显著性(P<0.05)。
1.2.6 实际样品检测取5 g 玉米粉, 分别添加质量分数为40、80 μg/kg 的ZEN 标准品充分混匀,用20 mL 甲醇-水(体积比86∶14)超声提取30 min。 将提取物于12 000 r/min 离心15 min, 并用0.22 μm微孔滤膜过滤后用氮气干燥。将其重新溶解于1 mL体积分数10%的甲醇PBS 中, 提取物用体积分数10%的甲醇PBS 稀释20 倍用于ELISA 检测。 相同步骤对玉米进行DON 加标分析, 加标的质量分数分别为80 μg/kg 和240 μg/kg。
式中:CV 为加标回收率,%;m1为玉米粉中ZEN 质量分数的测定值,μg/kg;m2为玉米粉中实际ZEN 加标的质量分数,μg/kg;RSD 为相对标准偏差,%;SD为玉米粉中ZEN 质量分数测定值的标准偏差,μg/kg;m3为玉米粉中ZEN 质量分数测定值的平均值,μg/kg。
2 结果与分析
2.1 重组载体的构建
重组载体Bis-scFv-pTT5 和DON-scFv-pCMV的琼脂糖凝胶电泳验证结果见图3。 Bis-scFv-pTT5其扩增片段大小位于2 000 bp 附近,见图3(a),符合理论值1 904 bp。 DON-scFv-pCMV 其扩增片段大小位于1 000~1 200 bp,见图3(b),符合理论值1 075 bp。 对菌落PCR 长度验证正确的菌株进行碱基测序显示,重组载体片段正确组装,且碱基序列正确, 未发生基因突变, 表明Bis-scFv-pTT5 和DON-scFv-pCMV 重组载体构建成功。
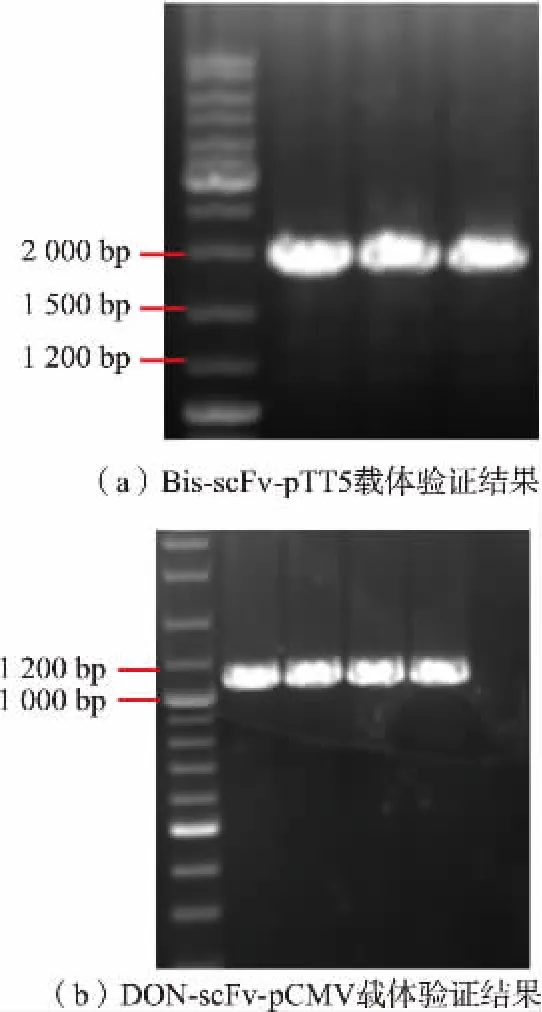
图3 重组载体琼脂糖凝胶电泳验证图Fig.3 Agarose gel electrophoresis of recombinant antibody plasmids
2.2 ZEN-scFv 和DON-scFv 的SDS-PAGE 分析
Expi293F 细胞采用了30 mL 的体系,诱导表达后离心去除细胞, 对上清液进行纯化, 分别收获1.55 mg ZEN-scFv 和253 μg 的DON-scFv,SDSPAGE 验证结果见图4。 ZEN-scFv 含有251 个氨基酸, 通过SnapGene 软件计算蛋白质理论相对分子质量为26 700,在26 000~34 000 条带单一,见图4(a),符合ZEN-scFv 理论相对分子质量。 DON-scFv含有257 个氨基酸,其蛋白质理论相对分子质量为27 400,在26 000~34 000 条带单一,见图4(b),符合DON-scFv 理论相对分子质量。

图4 Expi293F 细胞表达的单链抗体的SDS-PAGE 图Fig.4 SDS-PAGE analysis of the expression of single chain antibodies expressed by Expi293F cells
2.3 ZEN-scFv 和DON-scFv 亲和性验证
透析纯化后获得质量浓度为188 μg/mL 的ZEN-scFv。 将ZEN-scFv 稀释为0.5 μg/mL,测定其对1.0 μg/mL 的ZEN-BSA 和1.0 μg/mL 的BSA 亲和性, 定义ZEN-BSA 的吸光度OD450为P,BSA 的吸光度OD450为阴性对照N。当P/N≥2.1 时,则判定亲和性为阳性[15]。 如图5 所示,ZEN-scFv 对应的P值为2.57,N 值为0.07,两者比值为36.71,显著大于2.1,表明ZEN-scFv 能够识别并结合抗原上偶联的ZEN 分子,亲和性为阳性。 DON-scFv 经过纯化、二喹啉甲酸法蛋白质质量浓度测定后, 获得的最大DON-scFv 质量浓度为38 μg/mL。 将DON-scFv 稀释至质量浓度为1 μg/mL 进行验证,对1 μg/mL 的DON-OVA 和1 μg/mL 的OVA 测定亲和性。 DONscFv 对应的P 值为0.89,N 值为0.10, 两者比值为8.9,表明DON-scFv 能够识别并结合抗原上偶联的DON 分子,亲和性为阳性。
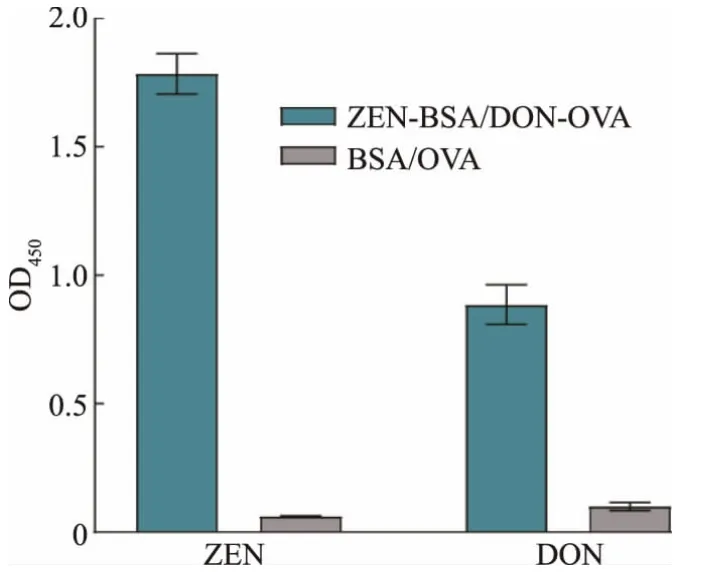
图5 ZEN-scFv 和DON-scFv 结合活性ELISA 验证Fig.5 ELISA validation of the binding activity of ZENscFv and DON-scFv
2.4 ZEN-scFv 和DON-scFv 灵敏度的测定
采用间接竞争ELISA 法对ZEN-scFv 和DONscFv 识别的灵敏性进行分析。首先利用ELISA 棋盘优化确定当ZEN-BSA 包被质量浓度为0.125 μg/mL、ZEN-scFv 包被质量浓度为0.125 μg/mL 时,OD450约为1.0。 在此条件下, 建立了0~1 000 ng/mL 的ZEN 标准抑制曲线,结果见图6(a)。 ZEN-scFv 的IC50值为8.66 ng/mL, 灵敏度较报道的该序列单特异性ZEN-scFv(IC50为11.20~14.00 ng/mL)高[16-17]。此外,DON-OVA 包被质量浓度为1.0 μg/mL,DONscFv 的质量浓度为1.0 μg/mL。在该条件下,在DON质量浓度为0~10 000 ng/mL 建立标准曲线,结果见图6(b)。 DON-scFv 的IC50为69.01 ng/mL,表明对DON 具有较高的敏感性,能够满足国内对于粮食中DON 限量(1 000 μg/kg)的检测要求。
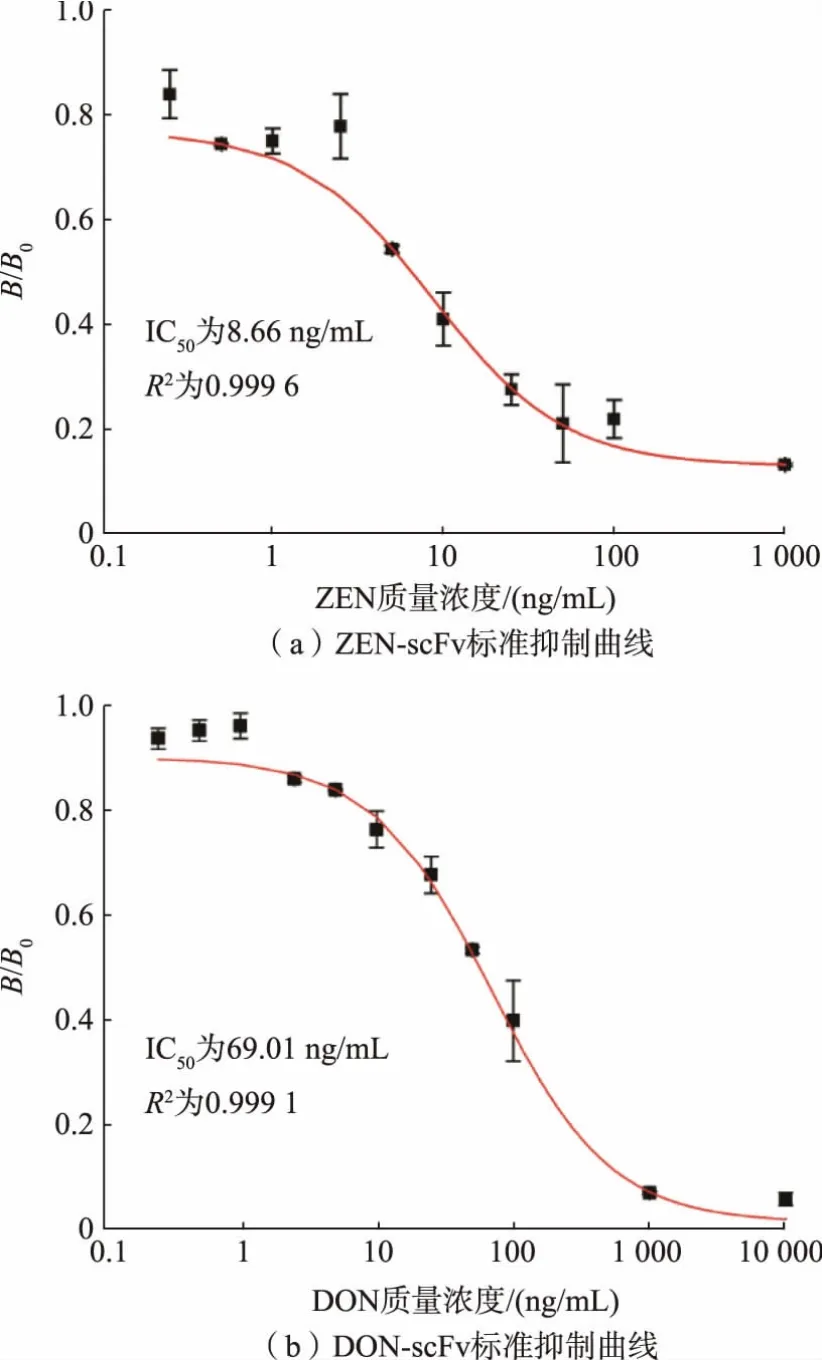
图6 单链抗体标准抑制曲线Fig.6 Standard inhibition curves for single chain antibodies
2.5 双特异性抗体验证
6×His、 标签DON-scFv 由515 个氨基酸组成,理论相对分子质量为54 100。图7(a)显示在相对分子质量55 000~72 000 存在清晰的单一蛋白质条带,电泳条带与理论相对分子质量略微偏大,可能是由于磷酸化或糖基化修饰使得蛋白质电荷发生改变从而影响了蛋白质在凝胶上的转移速度。 进一步对DON-OVA(1 μg/mL)和ZEN-BSA(1 μg/mL)结合能力进行ELISA 验证,结果见图7(b)。 表达抗体Bis-scFv 对2 种抗原的OD450与对照组OVA/BSA 存在明显差异,P/N 远大于2.1。 可见, 通过(Gly4Ser)3 Linker 连接ZEN-scFv 和DON-scFv 组成的双特异抗体Bis-scFv 保留了DON-scFv 和ZEN-scFv 的亲和识别功能。 同时,在相同抗原和抗体质量浓度下,Bis-scFv 对ZEN 的OD450比DON强,表明Bis-scFv 对ZEN 具有更强的亲和力。
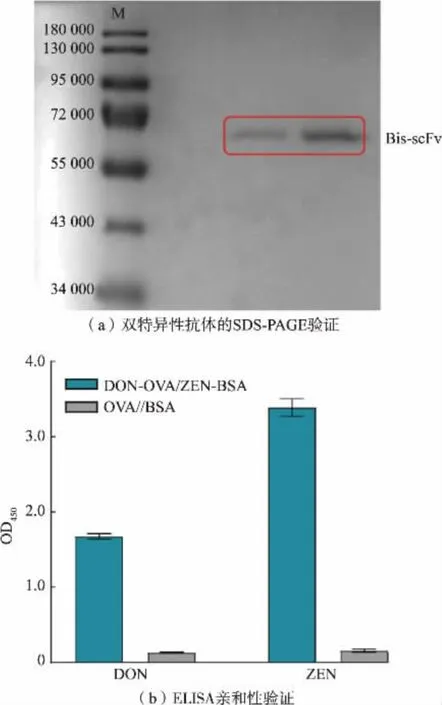
图7 双特异性抗体的SDS-PAGE 和ELISA 亲和性验证Fig.7 SDS-PAGE and ELISA validation of the affinity of bispecific antibody
2.6 抗体灵敏度测定
ELISA 棋盘优化确定ZEN-BSA 包被质量浓度为1.0 μg/mL,Bis-scFv 的质量浓度为5 μg/mL。 将ZEN 溶于体积分数10%的甲醇PBS 中,配制成质量浓度为0.25~10 000 ng/mL 的标准品,Bis-scFv 对ZEN 的非线性抑制曲线见图8(a)。Bis-scFv 对ZEN表现良好的灵敏度, 其IC50为20.64 ng/mL。 同样,ELISA 棋盘优化确定8 μg/mL 的Bis-scFv 和2 μg/mL的DON-OVA 时,OD450值约为1.0。 在此条件下,在DON 为0~10 000 ng/mL 建立非线性抑制曲线,测得其IC50为132.29 ng/mL,见图8(b)。 将Expi293F表达的重组抗体与目前报道的单克隆抗体(mAb)进行比较,结果见表2。 Expi293F 表达的Bis-scFv 与ZEN-scFv 灵敏度相近, 且与目前报道的部分抗ZEN mAb 灵敏度相近。 目前,欧盟和我国对于粮食中ZEN 的最大限量分别为100、60 μg/kg,ZEN-scFv和Bis-scFv 能够满足ZEN 的检测要求。 与DONscFv 比较,Bis-scFv 对DON 的灵敏度显著下降,但仍显著优于部分报道的抗DON mAb。 研究表明,scFv 连接肽的长度以及VH 和VL 排列取向会导致不同结合活性和寡聚状态[18-19]。Bis-scFv 融合抗体的形式对DON 敏感性的干扰大于ZEN, 这可能是由ZEN-scFv 和DON-scFv 排列取向差异导致。
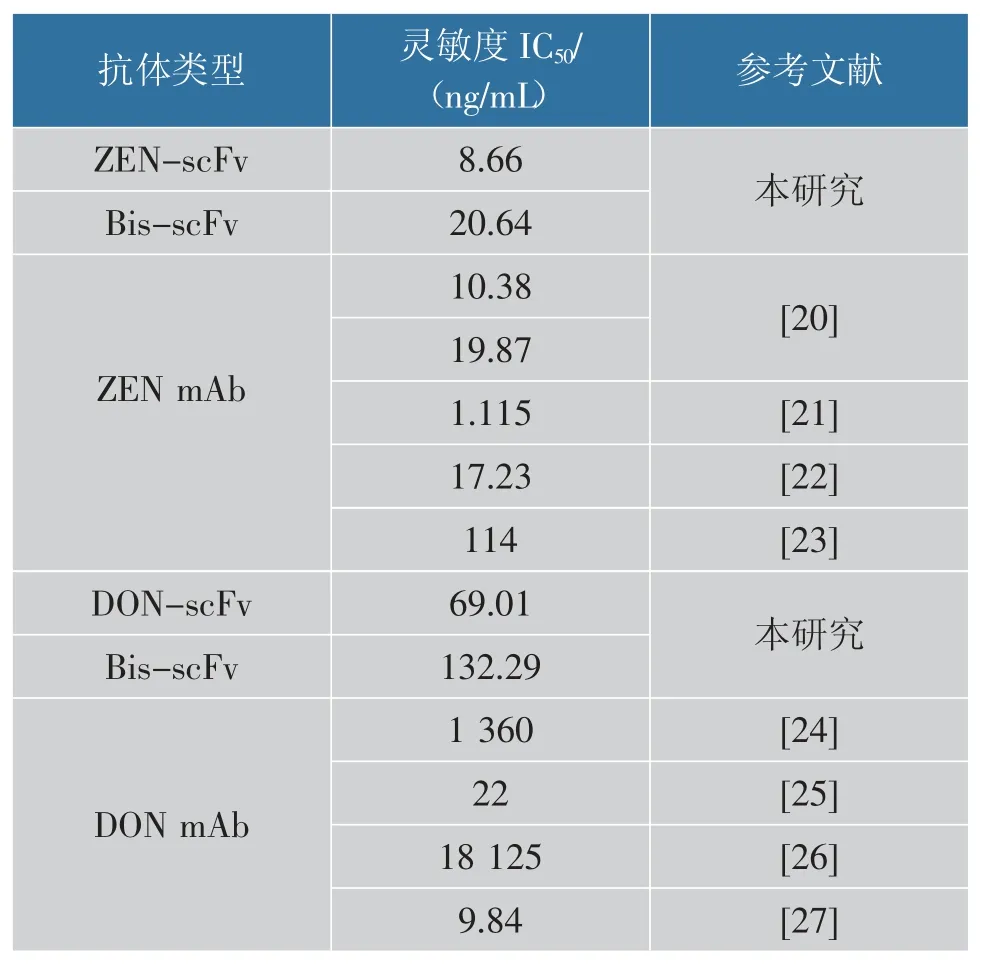
表2 重组表达抗体与传统抗体灵敏度比较Table 2 Sensitivity comparison between the recombinant antibodies and the traditional antibodies
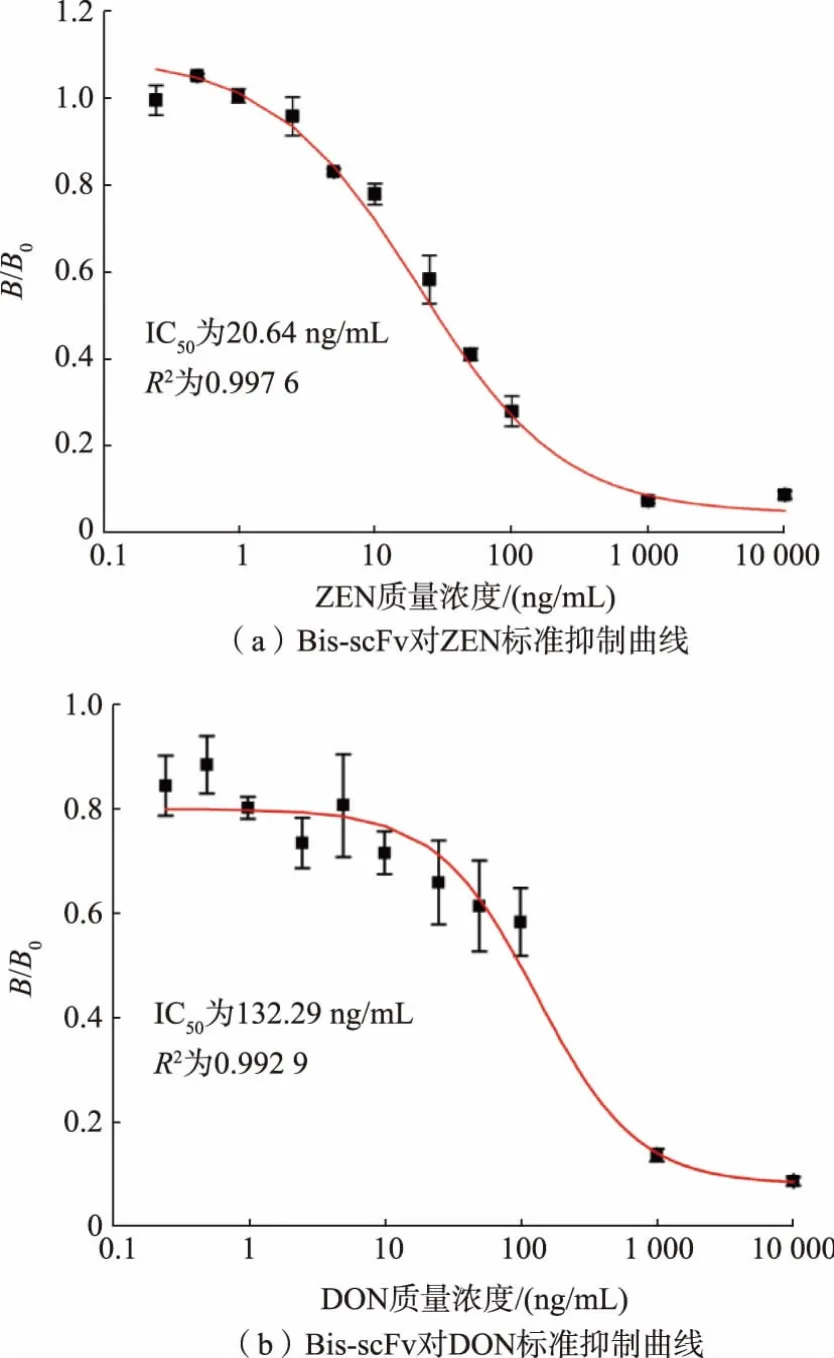
图8 双特异性抗体标准抑制曲线Fig.8 Standard inhibition curves of bispecific antibody
2.7 抗体特异性验证
为验证Bis-scFv 对ZEN 和DON 识别的特异性,考察了OTA、AFB1、T-2 毒素与Bis-scFv 的结合能力,结果见图9。在相同质量浓度的抗体和包被抗原的情况下, 当ZEN 和DON 质量浓度达到10 000 ng/mL 时, 游离的Bis-scFv 与游离的ZEN 和DON结 合,Bis-scFv 与ZEN-BSA 和DON-OVA 的 结 合受到抑制,此时抑制率接近100%。 当向体系加入质量 浓 度 为10 000 ng/mL 的OTA、AFB1、T-2 毒 素时, 对抗体与包被抗原结合的抑制效果显著小于DON 和ZEN,抑制率小于10%,这表明OTA、AFB1、T-2 无法与Bis-scFv 结合,Bis-scFv 与OTA、AFB1、T-2 之间不存在明显的交叉反应。
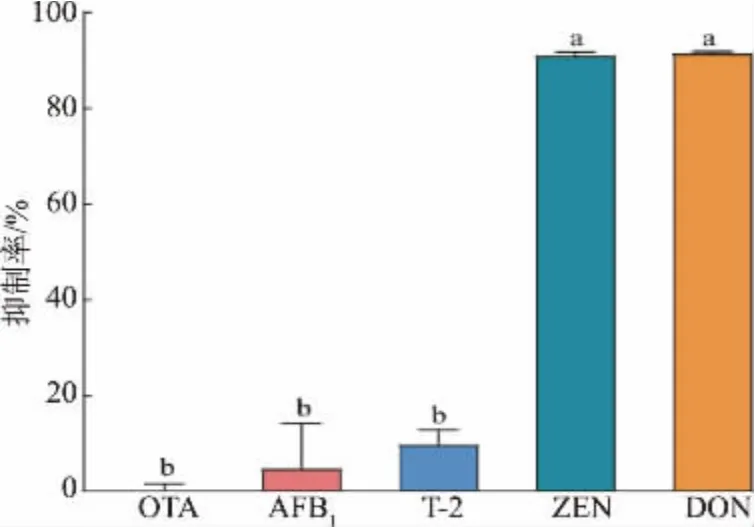
图9 表达抗体Bis-scFv 特异性Fig.9 Specificity of antibody Bis-scFv
2.8 基于双特异性抗体的ELISA 检测方法构建
基于Bis-scFv 建立ELISA 检测方法, 当ZEN质量浓度在1~100 ng/mL 时,B/B0与ZEN 质量浓度对数值呈线型关系,见图10(a)。 线性关系为Y=-0.402 8lg X+0.961 4, 线性拟合优度R2=0.946 7,IC50为13.98 ng/mL。 当DON 质量浓度在10~500 ng/mL 时,DON 质量浓度的对数与B/B0线型关系为Y=-0.527 5lg X+1.585,线性拟合优度R2=0.968 1,IC50为113.99 ng/mL,见图10(b)。 用BisscFv-ELISA 检测ZEN 和DON 加标的玉米样品,结果见表3。 玉米粉中ZEN 加标量为40 μg/kg 和80 μg/kg,Bis-scFv-ELISA 测定的平均值为34.45 μg/kg 和86.52 μg/kg, 平 均 回 收 率 为86.13%~108.14%;玉米粉中DON 加标量为80 μg/kg 和240 μg/kg,Bis-scFv-ELISA 测 定 的 平 均 值 为75.08 μg/kg 和206.44 μg/kg, 平 均 回 收 率 为86.02%~93.85%。 玉米样品加标回收检测结果表明,BisscFv-ELISA 具有良好的准确性,能够用于实际样品检测。将Bis-scFv-ELISA 同步检测与基于单克隆抗体的同步检测方法进行比较,Bis-scFv-ELISA 具有更广定量检测范围,见表4。
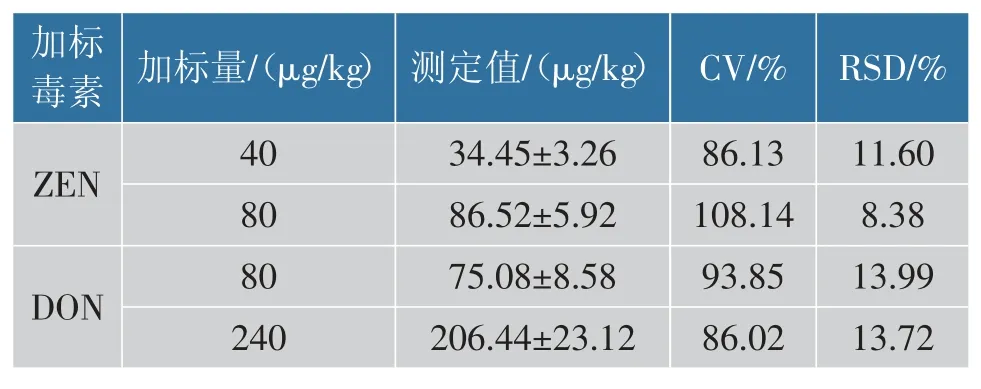
表3 玉米粉的DON 和ZEN 加标检测结果(n=3)Table 3 Detection results of DON and ZEN in spiked corn flour samples(n=3)
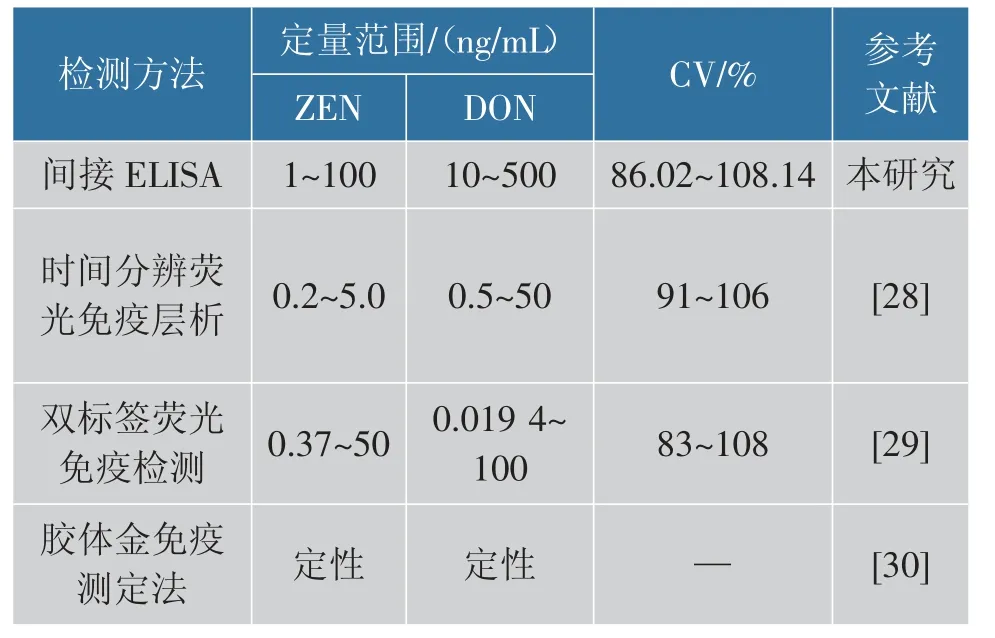
表4 DON 和ZEN 检测方法比较Table 4 Comparison of DON and ZEN detection methods
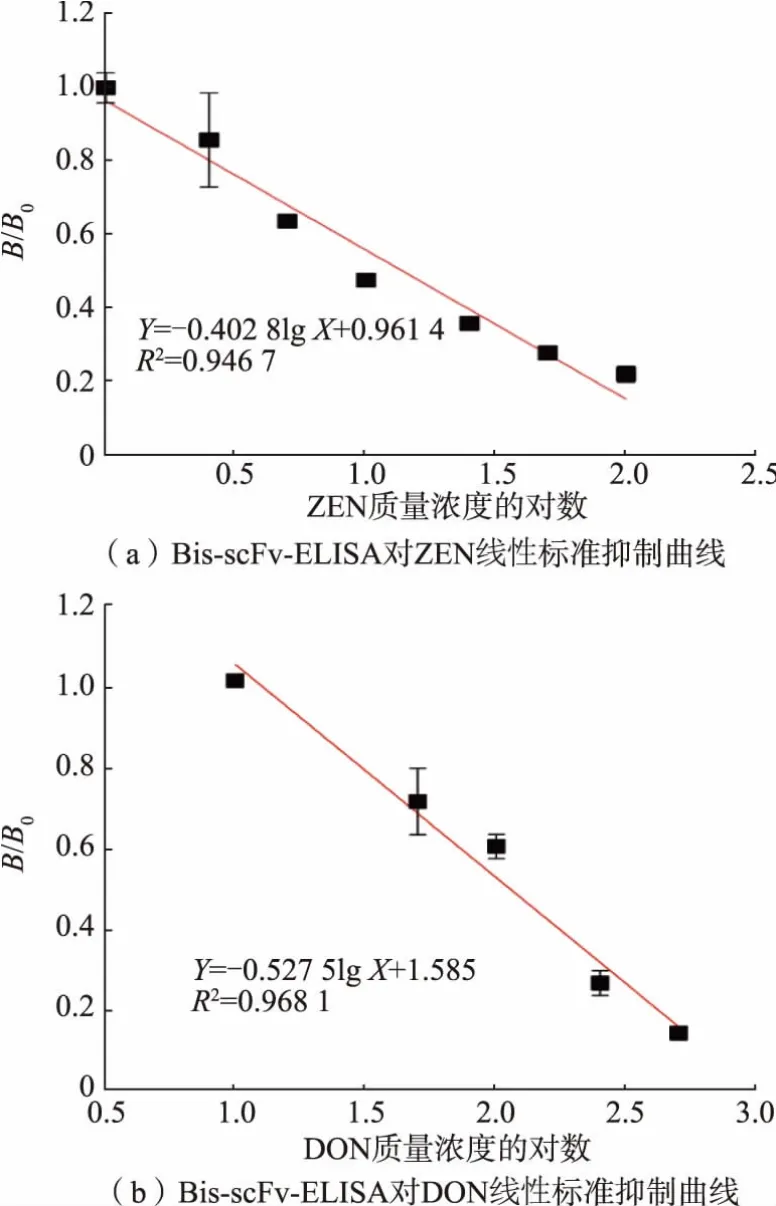
图10 Bis-scFv-ELISA 线性标准抑制曲线Fig.10 Linear standard inhibition curves of Bis-scFv-ELISA
3 结 语
结合重组抗体表达技术,在Expi293F 表达系统中成功表达了能够用于免疫检测的ZEN-scFv 和DON-scFv,IC50分别为8.66 ng/mL 和69.01 ng/mL。基于性质良好的单特异性抗体片段进行基因改造,获得了具有ZEN 和DON 结合位点的Bis-scFv。 经ELISA 验 证,Bis-scFv 对ZEN-BSA 和DON-OVA存在亲和性。 Bis-scFv 对ZEN 灵敏度接近ZENscFv,IC-ELISA 的IC50为20.64 ng/mL, 而对DON敏感性显著下降,IC-ELISA 的IC50为132.29 ng/mL。Bis-scFv 对OTA、AFB1、T-2 毒素无显著的交叉反应, 具有良好的特异性。 基于Bis-scFv 建立的ELISA 检测方法, 其对ZEN 检测的线性范围为1~100 ng/mL,DON 的检测线性范围为10~500 ng/mL。Bis-scFv-ELSIA 对玉米粉中ZEN 和DON 的加标回收率分别为86.13%~108.14%和86.02%~93.85%,相对标准偏差小于15%, 检测稳定性高, 表明BisscFv-ELISA 能够满足粮食中ZEN 和DON 检测要求。

