微生态制剂联合美沙拉嗪对溃疡性结肠炎患者肠道菌群及炎性因子水平的影响
贾音 邓大一
溃疡性结肠炎(ulcerative colitis, UC)作为一类慢性非特异炎症病, 具有病程长、易反复发作的特点, 以20~30 岁人群较为多见, 患病者最初多以血性腹泻为典型表现, 并伴有不同程度的腹痛、便血、呕吐等, 部分暴发性患者因起病急骤、病情进展迅速甚至会诱发全身中毒症状, 引起中毒性结肠扩张, 增加患者的病死风险[1]。目前, 临床对于UC 的病因和具体的发病机制尚未有准确定论, 因此始终缺乏特效的治疗方式, 其中免疫抑制剂、激素、氨基水杨酸等药物虽对病情的控制有力, 但这些药物的稳定性不佳, 易出现一系列的不良反应, 并导致疾病的复发[2]。现如今, 随着临床对UC 研究的深入, 逐渐发现在UC 发生、发展的过程中菌群失调和氧自由基损伤起着关键作用, 因此做好肠道内部的微生态环境调节对减轻临床症状, 促进患者康复有重要意义[3]。美沙拉嗪长期以来一直是UC 患者治疗的首选药物, 其抗炎、改善肠道功能的功效已经被临床普遍认可;但调节肠道菌群、抑制内毒素和病原菌的产生也是UC 患者治疗的原则之一[4]。对此,本研究为进一步提高UC 患者的临床治疗效果, 前瞻性选取64 例UC 患者进行分组研究, 分析在美沙拉嗪治疗基础上联合微生态制剂的效果和安全性, 现报告如下。
1 资料与方法
1.1 一般资料 选取本院2019 年10 月~2021 年10 月收治的64 例UC 患者作为研究对象。纳入标准:①符合《炎症性肠病诊断与治疗的共识意见》诊断标准[5];②均为初次发病患者;③发病时长≥3 个月;④患者年龄≥18 岁;⑤参与本项研究前3 个月未接受过免疫抑制剂、氨基水杨酸类和微生态制剂等相关药物进行治疗;⑥配合度及依从性较高者;⑦对本研究知情同意。排除标准:①自身免疫性疾病患者;②对治疗用药存在过敏;③合并其他胃肠道疾病;④合并其他全身性的炎症疾病;⑤高度疑似恶性病变;⑥心肺、肝肾等脏器存在功能异常;⑦精神异常;⑧资料存在缺失;⑨研究期间退出研究。经伦理委员会通过后, 选择随机排列法将患者分为对照组、研究组, 每组32 例。两组患者一般资料比较差异无统计学意义(P>0.05), 具有可比性。见表1。
表1 两组一般资料比较(n, ±s)
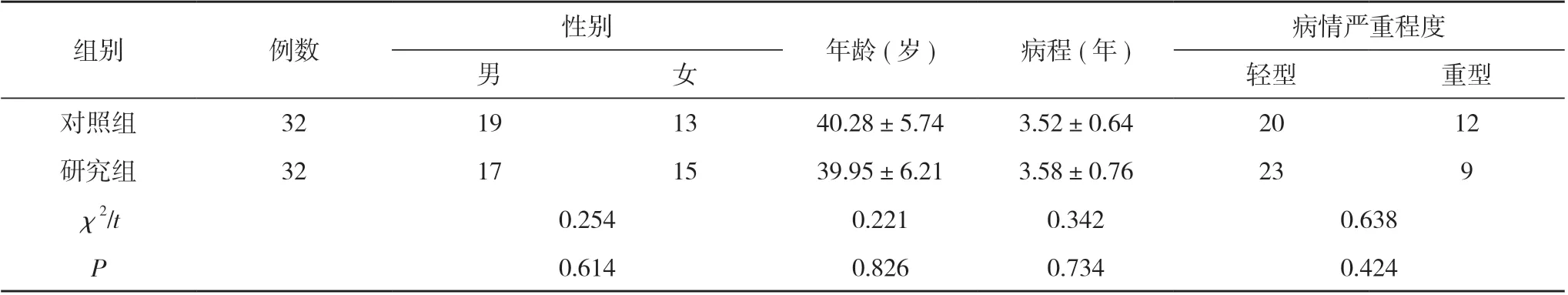
表1 两组一般资料比较(n, ±s)
注:两组比较, P>0.05
组别例数性别年龄(岁)病程(年)病情严重程度男女轻型重型对照组32191340.28±5.743.52±0.642012研究组32171539.95±6.213.58±0.76239 χ2/t0.2540.2210.3420.638 P 0.6140.8260.7340.424
1.2 方法 两组患者治疗前均先给予肠镜检查。对照组给予美沙拉嗪肠溶片(葵花药业集团佳木斯鹿灵制药有限公司, 国药准字H19980148, 规格:0.25 g)治疗, 3 次/d, 1 g/次, 于三餐前温水口服。研究组在对照组基础上给予微生态制剂口服治疗, 选用双歧杆菌三联活菌胶囊(上海信谊药厂有限公司, 国药准字S10950032, 规格:0.21 g)口服, 3 次/d, 0.42 g/次。两组用药治疗2 个月。
1.3 观察指标及疗效判定标准
1.3.1 肠道菌群 治疗开始前和结束后收集大便0.5 g, 先对粪便标本以1∶1000 稀释法进行稀释, 随后将其放置在密封的培养基中进行培养, 48 h 后统计每克样品中存在的菌落数量, 比较两组双歧杆菌、乳杆菌、大肠埃希菌以及双歧杆菌和大肠埃希菌比值。
1.3.2 炎性因子 治疗开始前和结束后采集空腹静脉血5 ml, 离心处理分离出血清标本后经酶联免疫法对IL-6、IL-8、TNF-α 展开测定, 采用免疫比浊法测定hs-CRP 水平, 比较两组治疗前后炎性因子水平。
1.3.3 疗效判定标准 以患者治疗2 个月后内镜检查无颗粒感, 溃疡面愈合, 血管分布正常, 便血、腹痛等一系列临床症状全部消失为治愈;以内镜检查溃疡面较治疗前相比愈合≥75%, 便血、腹痛等临床症状明显改善为显效;以内镜检查溃疡面较治疗前相比愈合50%~74%, 便血、腹痛等临床症状有改善为有效;和上述情况均不吻合为无效。总有效率=(治愈+显效+有效)/总例数×100%[6]。
1.3.4 不良反应 包括头晕头痛、恶心呕吐和胃部不适等。
1.4 统计学方法 采用SPSS23.0 统计学软件对研究数据进行统计分析。计量资料以均数±标准差( x-±s)表示, 采用t 检验;计数资料以率(%)表示, 采用χ2检验。P<0.05 表示差异具有统计学意义。
2 结果
2.1 两组治疗前后肠道菌群比较 治疗前, 两组双歧杆菌、乳杆菌、大肠埃希菌数量以及双歧杆菌和大肠埃希菌比值比较差异无统计学意义(P>0.05);治疗后,两组双歧杆菌、乳杆菌数量以及双歧杆菌和大肠埃希菌比值高于本组治疗前, 大肠埃希菌数量低于本组治疗前, 且研究组双歧杆菌、乳杆菌数量以及双歧杆菌和大肠埃希菌比值高于对照组, 大肠埃希菌数量低于对照组, 差异具有统计学意义(P<0.05)。见表2。
表2 两组治疗前后肠道菌群比较( ±s)
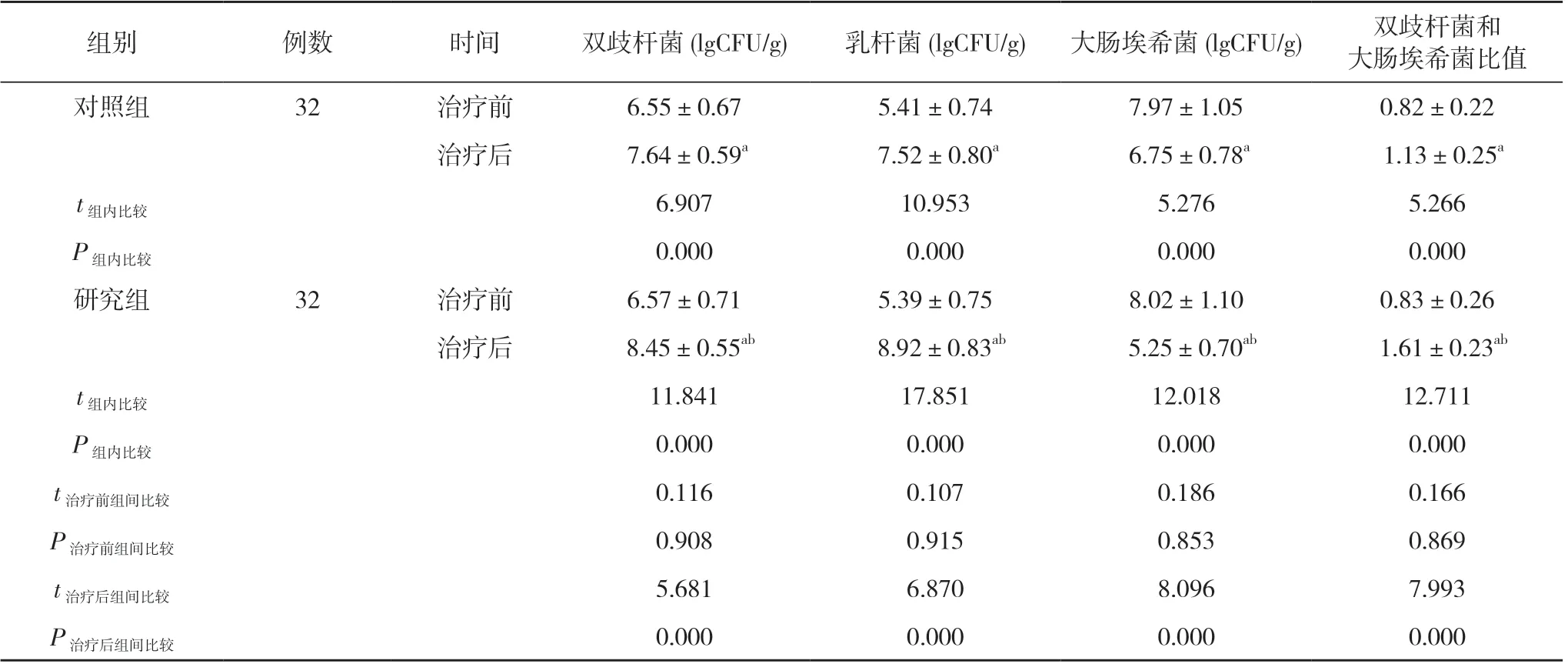
表2 两组治疗前后肠道菌群比较( ±s)
注:与本组治疗前比较, aP<0.05;与对照组治疗后比较, bP<0.05
组别例数时间双歧杆菌(lgCFU/g)乳杆菌(lgCFU/g)大肠埃希菌(lgCFU/g)双歧杆菌和大肠埃希菌比值对照组32治疗前6.55±0.675.41±0.747.97±1.050.82±0.22治疗后 7.64±0.59a 7.52±0.80a 6.75±0.78a 1.13±0.25a t组内比较6.90710.9535.2765.266 P组内比较0.0000.0000.0000.000研究组32治疗前6.57±0.715.39±0.758.02±1.100.83±0.26治疗后 8.45±0.55ab 8.92±0.83ab 5.25±0.70ab 1.61±0.23ab t组内比较11.84117.85112.01812.711 P组内比较0.0000.0000.0000.000 t治疗前组间比较0.1160.1070.1860.166 P治疗前组间比较0.9080.9150.8530.869 t治疗后组间比较5.6816.8708.0967.993 P治疗后组间比较0.0000.0000.0000.000
2.2 两组治疗前后炎性因子水平比较 治疗前, 两组IL-6、IL-8、TNF-α、hs-CRP 水平比较差异无统计学意义(P>0.05);治疗后, 两组IL-6、IL-8、TNF-α、hs-CRP 水平均低于本组治疗前, 且研究组低于对照组,差异具有统计学意义(P<0.05)。见表3。
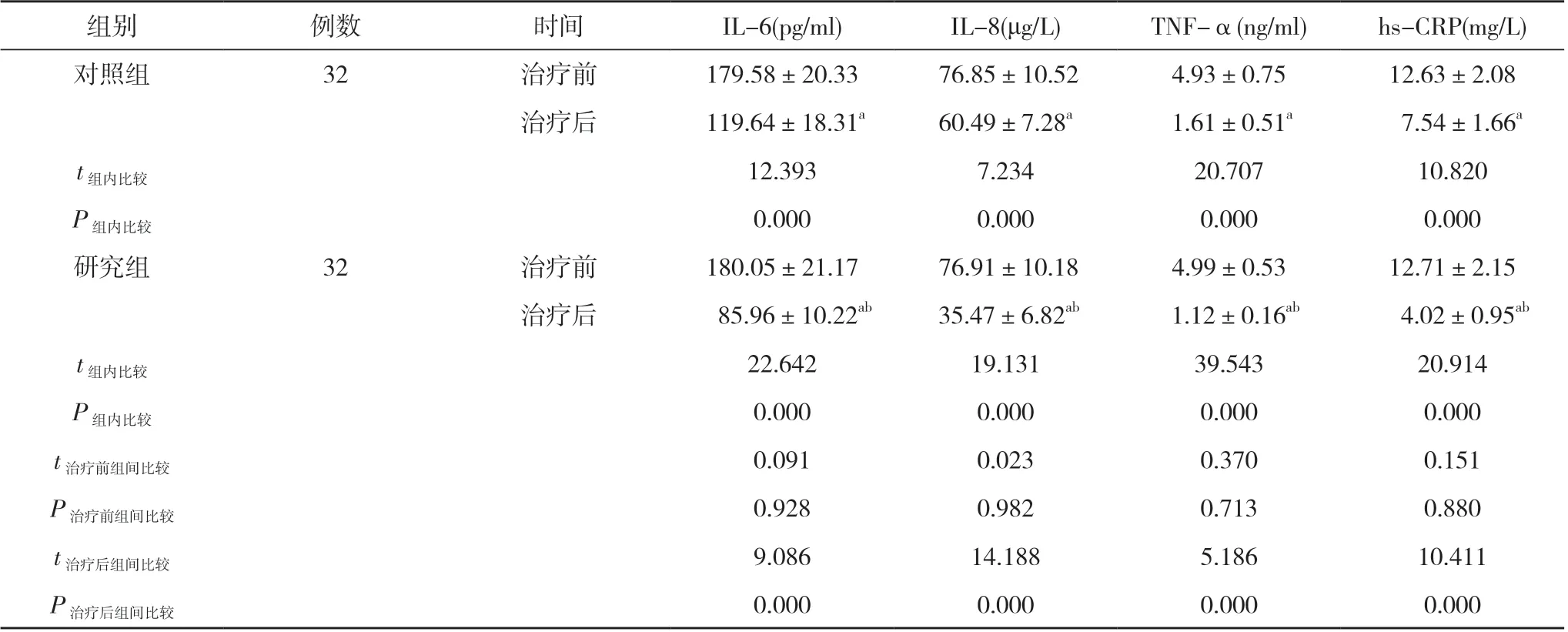
表3 两组治疗前后炎性因子水平比较( x-±s)
2.3 两组治疗效果比较 研究组治疗总有效率为90.63%, 高于对照组的68.75%, 差异具有统计学意义(P<0.05)。见表4。

表4 两组治疗效果比较[n, n(%)]
2.4 两组不良反应发生情况比较 两组不良反应发生率比较差异无统计学意义(P>0.05)。见表5。

表5 两组不良反应发生情况比较[n, n(%)]
3 讨论
目前, 临床对于UC 的发病机制尚未完全阐明, 对于该疾病的治疗也始终缺乏标准化的方案。美沙拉嗪属于当前UC 治疗中使用较多的一类药物, 是新出现的氨基水杨酸有关药物, 它可以有效抑制机体白三烯、前列腺素等一系列炎症介质生成, 将活性氧等众多的损伤因子充分清除, 使肠道黏膜通透度明显下降, 减轻黏膜水肿现象。但经研究证实, 美沙拉嗪不宜长期使用,容易引发不良反应, 影响患者的治疗效果[7-10]。因此还需积极探索更加安全有效的治疗方案。
随着临床研究的深入, 临床逐渐认可UC 发生期间免疫系统紊乱也有着重要影响, 而免疫紊乱的主要原因与肠道菌群紊乱有着密切的联系, 受肠道菌群失调的影响, 患者肠道黏膜发生损伤, 进而促进UC 的发生和发展, 因此改善消化道内环境对于控制UC 患者病情进展有重要意义[11-14]。经本研究发现, 治疗后, 两组双歧杆菌、乳杆菌数量以及双歧杆菌和大肠埃希菌比值高于本组治疗前, 大肠埃希菌数量低于本组治疗前, 且研究组双歧杆菌、乳杆菌数量以及双歧杆菌和大肠埃希菌比值高于对照组, 大肠埃希菌数量低于对照组, 差异具有统计学意义(P<0.05)。反映出联合用药可以有效调节UC 患者的肠道菌群。分析其原因可以发现, 双歧杆菌三联活菌胶囊属于一种微生态制剂,不仅可以对消化道内的正常的生理菌群进行有效的补充, 还可以抑制有害菌和肠源性毒素的产生, 有效调节肠道菌群失衡的情况[9]。另外, 经研究证实[15-18],双歧杆菌三联活菌胶囊作用于UC 患者时可以生成不同类型的维生素, 加快矿物质、蛋白质以及维生素吸收以及利用速度;同时可以借助与致病菌之间竞争作用, 使得有害菌生成大大减少;能够分泌出较多的抗生素, 使得肠道中的pH 下降, 最终减少致病菌繁殖。与此同时, 本研究还发现, 治疗后, 两组IL-6、IL-8、TNF-α、hs-CRP 水平均低于本组治疗前, 且研究组低于对照组, 差异具有统计学意义(P<0.05)。这和张华等[19]研究结果有着较高一致性, 反映出美沙拉嗪联合双歧杆菌三联活菌胶囊治疗还可以降低UC 患者机体的炎性因子水平。究其原因可以发现, 美沙拉嗪的有效成分是5-氨基水杨酸, 可以减少巨噬细胞及中性粒细胞释放IL-6、IL-8, 减少TNF-α 的产生, 从而降低炎性因子水平, 减轻其对肠道黏膜的损害作用;而双歧杆菌三联活菌胶囊则可以直接通过诱导T 细胞凋亡, 调节机体的免疫功能, 使炎性因子分泌减少;同时使用二者能起到协同治疗作用, 使疗效得到明显提高。本文结果显示:研究组治疗总有效率为90.63%, 高于对照组的68.75%, 差异具有统计学意义(P<0.05)。两组不良反应发生率比较差异无统计学意义(P>0.05)。与魏来等[20]研究结果一致, 充分表明二者联合治疗不会增加不良反应, 具有较高的安全性。
综上所述, 微生态制剂联合美沙拉嗪治疗UC 患者可以有效调节肠道菌群, 降低炎性因子水平, 提升疗效, 且不会使不良反应增多, 值得推广应用。但是本研究还有不足, 如纳入样本数少, 样本全部是一家医院收入, 且未开展远期随访, 获得的结果有局限性, 这些还需日后继续完善。

