金纳米花结构的制备及其催化性能研究
王灵娟, 欧全宏, 严 昊, 汤俊琪
云南师范大学物理与电子信息学院, 云南 昆明 650500
引 言
纳米金颗粒具有优异的化学稳定性、 良好的生物相容性和独特的光学性质, 在催化、 生物医学工程、 电子和光电子学、 传感以及信息存储等领域有着广泛的应用[1-2]。 通过化学还原法, 可以制备出多种不同形貌的金纳米颗粒, 如各向同性的球形纳米金颗粒、 以及各向异性的金纳米棒、 金纳米立方体、 金纳米八面体、 金纳米片、 树枝状金纳米结构和金纳米花等结构[3]。 其中金纳米花结构由于具有多分枝的形貌、 很高的表面积-体积比, 增强的电磁场效应而更加受到人们的关注, 在生物标签、 化学传感、 表面增强拉曼散射(SERS)和催化等领域进行了持续的研究[4-5]。
考虑到在纳米花状结构的分枝处可很好地实现局域电磁场增强, 从而可拓展纳米金在SERS和催化方面的应用, 开发出不同的方法制备金纳米花结构并探讨其应用是当前研究的重点。 由于金纳米花结构表面形貌的特殊性, 有时也被称为金纳米星、 星状金纳米结构或者海胆状金纳米结构等。 最常用的方法是采用是种子生长法制备不同大小和形貌的金纳米花状结构。 采用25 nm大小的球形纳米金颗粒为种子, 在氯金酸和盐酸羟胺的混合液中, 可以快速实现金纳米花结构的制备。 研究还发现, pH值不仅影响表面分枝的长度, 还可以改进金纳米花的长期稳定性[6]。 随后还有研究指出, 当pH值在12~12.5之间时, 不需要种子即可在氯金酸和盐酸羟胺溶液中实现金纳米花结构的制备[7]。 另外, 抗坏血酸也是一种最常用的还原剂来制备金纳米花结构, 不管是对金纳米花形成机理[8], 还是不同形貌或者光学特性的金纳米花的分析, 均有比较系统性的研究[9]。 通过引入适量的十六烷基三甲基溴化铵等表面活性剂, 也可实现金纳米花结构的制备[10], 但是表面活性剂会限制金纳米花结构的进一步表面修饰、 生物医学或者催化应用。 由于植物提取物体现了良好的“绿色化学”的原则, 一些植物提取物也常常被用作表面包覆剂和还原剂来制备金纳米花结构[11]。 除了探索不同的方法制备金纳米花结构外, 在开发金纳米花结构应用方面也有各种各样的研究[12]。 例如在催化领域, 金纳米花结构可作为一种纳米催化剂, 在加氢反应, 羰基化反应, 对硝基苯酚还原和一氧化碳还原等催化反应中可表现出良好的催化性能。 例如, Yu等报道了在胰蛋白酶为模板, 抗坏血酸为还原剂的情况下, 可制备出良好稳定性的金纳米花胶体。 该金纳米花结构可对氯胺T-四甲基联苯胺的反应产物具有很好的SERS增强, 间接发挥催化增强的效果[13]。 Mao等研究了一种无需表面活性剂和种子的方法制备金纳米花结构, 可对芳香族硝基化合物农药进行有效降解[14]。 以磁铁矿(Fe3O4)为载体, 制备出负载型的Au/Fe3O4纳米花微球[15-16], 在催化还原4-硝基苯酚的反应中表现良好。 采用其他物质如石墨烯[17]、 聚合物[18]等作为载体, 也可以实现金纳米花结构的制备和催化应用。
因此, 基于金纳米花形貌结构的特殊性以及可广泛应用的多功能性特征, 拓展不同方法制备金纳米花结构和探讨其催化性能仍具有重要的意义。 本文采用抗坏血酸溶解的左旋多巴混合溶液制备出了一种微米级的金纳米花结构, 通过不同方法对制备的金纳米花结构进行了表征分析。 同时研究了该金纳米花结构的催化性能, 基于对4-硝基苯酚(4-NP)的催化还原反应分析, 显示了这种方法制备的金纳米花结构具有良好的催化活性。
1 实验部分
1.1 试剂与仪器
左旋多巴(C9H11NO4, Levodopa缩写为L-DOPA)、 抗坏血酸(C6H8O6)、 氯金酸(HAUCl4)、 对硝基苯酚(4-NP)、 硼氢化钠(NaBH4)购于上海麦克林生化科技有限公司; 所有试剂均为分析纯, 未再进一步纯化而直接用于反应; 实验用水为超纯水(18·25 MΩ·cm)。
UV2600紫外可见分光光度计(日本岛津公司), FEI Quanta 250扫描电子显微镜(美国FEI公司), X射线粉末衍射仪(XRD, UltimaIV, 日本理学), JEM-2100透射电子显微镜(日本电子)。
1.2 方法
1.2.1 金纳米花结构的合成
左旋多巴是儿茶酚胺类物质多巴胺的前体, 因其具有两个邻位的酚羟基而具有一定的还原性[19]。 但左旋多巴在常温下是一种微溶于超纯水的物质, 本研究将左旋多巴溶于1 mmol·L-1的抗坏血酸中得左旋多巴的抗坏血酸混合溶液备用。 室温下, 将2 mL的10 mmol·L-1HAuCl4加入到7 mL超纯水中, 在600 r·min-1磁力搅拌条件下加入1 mL的左旋多巴的抗坏血酸混合溶液, 获得的混合反应溶液总体积为10 mL。 继续在600 r·min-1磁力搅拌条件搅拌20 min, 溶液逐渐由黄色变为浅褐色, 保持溶液在室温下过夜后即可获得金纳米花状胶体结构。 改变超纯水和左旋多巴的抗坏血酸混合溶液的添加量, 但混合溶液总体积仍维持10 mL, 可获得不同形貌的金纳米结构。 取5 mL纳米金胶体于离心管中在5 000 r·min-1转速下离心5 min, 去上清液后加入等量超纯水溶解, 重复该过程后使纳米金胶体均匀分散在离心管中并静置备用。
1.2.2 金纳米花结构的表征
对金纳米花结构的光谱特性、 大小和形貌等表征分别按照如下过程进行。 首先取2.5 mL制备的金纳米花胶体放入10 mm石英比色皿中, 在UV-2600紫外可见光谱仪上进行紫外可见光谱测试(300~900 nm); 其次, 取少量金纳米花沉淀置于铜片上自然干燥后进行扫描电子显微镜(Scanning Electron Microscope, SEM, FEI 250)表征样品的形貌(20 kV); 取2 μL金纳米花胶体在200目铜网上自然干燥后进行透射电子显微镜(TEM)观察样品的大小和形貌; 取大量金纳米花沉淀在石英片上自然干燥后进行XRD测试, X射线衍射(X-ray diffraction, XRD)使用Cu Kα射线(λ=0.154 06 nm)在5°~90°(2θ)的范围扫描, 管电压为40 kV, 管电流为40 mA。
1.2.3 金纳米花结构的催化性能
取40 μL的10 mmol·L-1的4-NP溶液在1 cm的比色皿中稀释至2 mL, 然后加入800 μL的0.1 mol·L-1的NaBH4溶液, 再加入适量的金纳米花结构作为纳米催化剂进行催化还原反应。 可肉眼观察到当加入过量硼氢化钠时, 溶液颜色变为亮黄色。 但加入催化剂后, 溶液颜色逐步转变为无色, 表明该纳米催化剂具有良好的催化效果。 整个反应过程以紫外可见光谱仪下测定不同时刻(间隔2 min左右)的光谱图。 最后, 再根据最大吸收峰值的变化情况对金纳米花催化剂的催化效果进行评价分析。
2 结果与讨论
2.1 紫外可见光谱、 粒径大小及形成机制分析
图1(a)为金纳米花胶体溶液的紫外-可见吸收光谱。 可以看到, 金纳米花胶体溶液在650 nm左右存在一个明显的表面等离子体共振峰(surface plasmon resonance, SPR)。 根据相关研究报道表明, 基于不同方法所制备的金纳米花结构通常在560~730 nm范围内存在一个明显的表面等离子体共振宽峰[4, 15, 20-22]。 因此, 图1(a)的紫外可见光谱初步表明, 所制备的金纳米颗粒是金纳米花结构。 通过扫描电子显微镜(SEM)的观察表明, 所制备的金纳米颗粒确实是花状结构, 而且表面存在很多尖锐的纳米片, 展现了纳米花结构比较高的表面积-体积比构型[图1(b)]。 基于200个纳米颗粒的统计分析, 图1(c)显示制备的金纳米花结构其大小为(1.10±0.14) μm。 根据所加的试剂及反应条件, 我们推测金纳米花结构的可能形成机制如图1(d)所示。 当加入抗坏血酸溶解的左旋多巴溶液后, 由于抗坏血酸的强还原性, 在溶液中立即形成小的纳米金种子颗粒, 随后在相对弱还原性的左旋多巴的诱导下, 金种子会进一步的增长为各向异性的金纳米花结构。
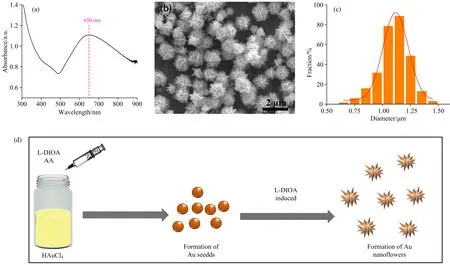
图1 (a)金纳米花溶液的紫外可见光谱图; (b)金纳米花结构的扫描电子显微镜(SEM)图; (c)金纳米花结构的粒径统计分布图; (d)金纳米花结构的形成机制图Fig.1 (a) UV-Vis spectum of gold nanoflowers(AuNFs). The surface plasmon resonance (SPR) peak is at 650 nm; (b) Scanning electron microscope (SEM) of fabricated gold nanoflowers; (c) Size distributions of AuNFs; (d) Illustration of possible mechanism for the formation of AuNFs
2.2 XRD分析
图2为金纳米花结构的XRD图和纳米金标准X射线衍射图。 从图中可知, 位于2θ=38.40°、 44.62°、 64.76°、 77.80°和81.82°的衍射峰分别与金的(111)、 (200)、 (220)、 (311)和(222)晶面衍射峰相对应。 在38.40°时衍射峰强度最大, (200)/(111)的比值为0.38, 参照纳米金的标准衍射图(JCPDS No.04-0784), 可知金纳米花结构晶形较好, 结晶程度高, 为面心立方(face-center cubic, FCC)结构。
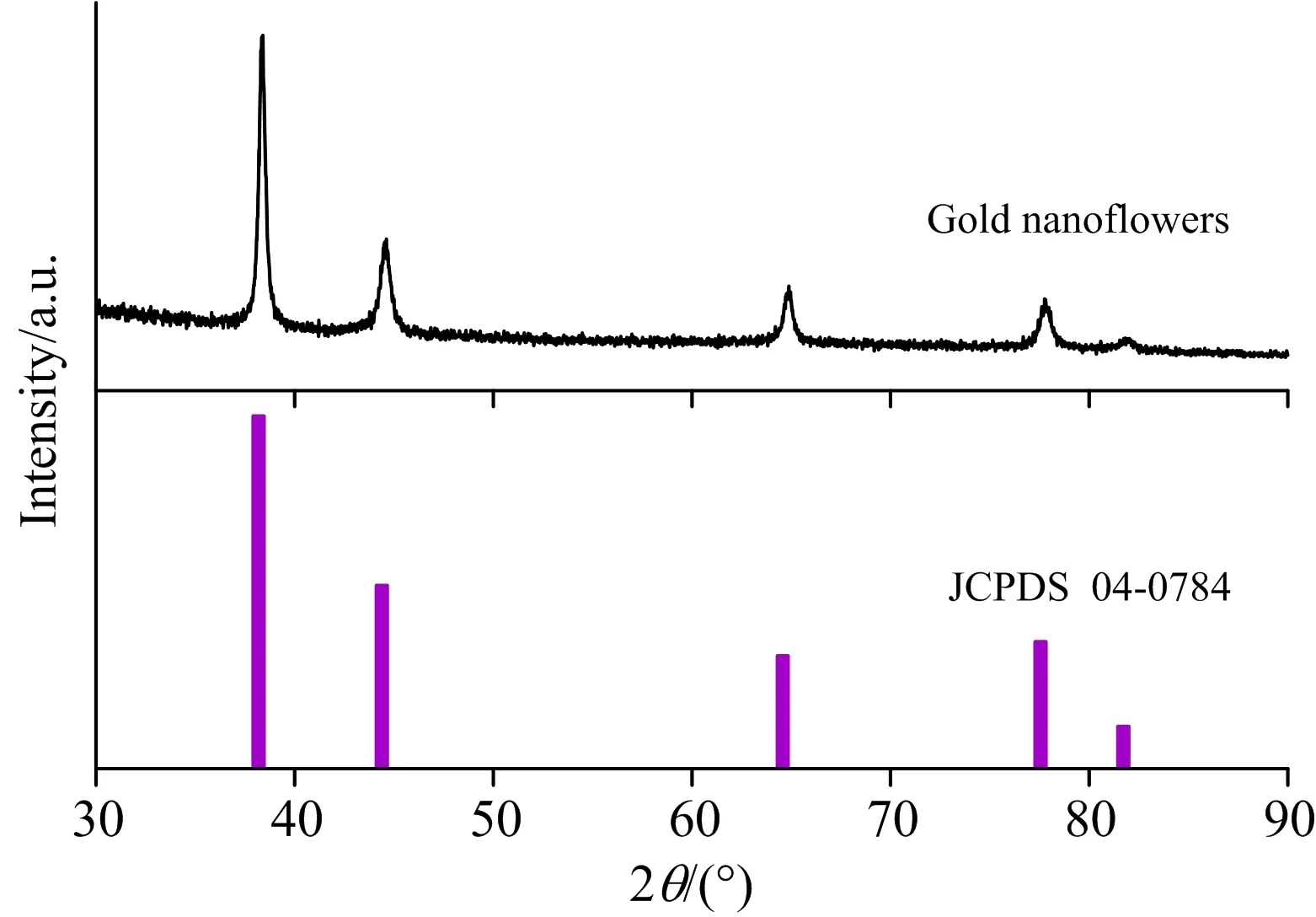
图2 金纳米花结构的XRD图和金的标准PDF卡片Fig.2 XRD patterns of gold nanoflowers (AuNFs) and the corresponding standard PDF card (JCPDS No.04-0784)
2.3 结构与形貌分析
通过对金纳米花结构合成条件的考察, 发现金纳米花结构的合成主要受到参与反应物量的影响。 通过改变不同量的左旋多巴的抗坏血酸混合溶液, 可以看到金纳米花结构的形貌变化明显。 图3(a)的SEM图显示了在加入较多的左旋多巴的抗坏血酸混合溶液时, 可以形成金纳米花结构, 但是由于左旋多巴和抗坏血酸的过量包覆作用, 导致形成的金纳米结构主要为菜花状纳米金结构。 通过TEM图[图3(b), (c)]更加清晰地看出, 在该条件下主要形成了表面较粗糙的菜花状纳米金结构。 随着降低左旋多巴的抗坏血酸混合溶液的添加量, 形成了表面具有非常尖锐的片状的金纳米花结构[图3(d)-(f)], 且该纳米花的大小明显变大。 再降低左旋多巴的抗坏血酸混合溶液的量, 通过SEM和TEM证实形成的主要形成的是球形纳米金颗粒[图3(g)-(i)]。 这些电镜图片说明反应物的量对最终产物金纳米结构的影响明显。

图3 添加不同量的左旋多巴的抗坏血酸混合溶液制备的金纳米结构的SEM和TEM图片(a)-(c): 2 mL; (d)-(f): 1 mL; (g)-(i): 0.25 mLFig.3 SEM and TEM images of the varying amount of levodopa dissolved in ascorbic acid solutions for preparation of gold nanoflowers (AuNFs)(a)-(c): 2 mL; (d)-(f): 1 mL; (g)-(i): 0.25 mL
2.4 催化性能分析
由于金纳米花结构的优异形状特征, 很多研究证实了金纳米花结构在近场光学增强中的优异表现, 比如在SERS应用中[23-24], 表现出其他各向异性纳米金结构达不到的高增强因子。 在催化领域, 同样可展现优秀的催化效能。 在本研究中, 基于过量的硼氢化钠, 将对硝基苯酚催化还原成对氨基苯酚的模式反应, 讨论了所制备的金纳米花结构的催化性能。 如图4(a)所示, 对硝基苯酚(4-NP)的最大的吸收峰在317 nm左右(左边的黑色曲线)。 在加入过量的NaBH4后, 4-NP转变为4-硝基苯酚钠, 溶液由浅黄色变为亮黄色(右边的黄色曲线), 最大吸收峰红移到400 nm。 然后加入一定量的金纳米花结构作为纳米催化剂[图4(b)], 可以看到, 400 nm处的吸收峰强度逐渐减小至消失(右边的黄色曲线), 而在300 nm处新出现一个吸收峰(左边的灰色曲线), 该位置是对氨基苯酚(4-AP)的特征峰, 并且强度会随反应的进行而逐渐增大。 图4(c)-(f)显示了添加不同量的金纳米花结构作为催化剂, 在十分钟左右的时间内, 反应体系中的4-NP均可被完全还原成4-AP, 表明金纳米花结构的优良的催化活性。 基于该反应的拟一级动力学特征, 计算出反应速率常数(k)分别为3.53×10-3、 5.27×10-3和5.4×10-3s-1。 对比文献中报道, 如Liang等采用柠檬酸根包裹的58 nm的球形纳米金为纳米催化剂, 其反应速率常数分别为1.67×10-3s-1[25]。 而Du等以13 nm的球形纳米金颗粒分别还原邻硝基苯酚, 间硝基苯酚和对硝基苯酚, 其速率常数为1.65×10-3、 3.75×10-3和2.18×10-3s-1[26]。 Guo等报道的中空多孔球形纳米金颗粒, 催化反应的速率常数为7.42×10-3s-1[27]。 Chiu等报道了立方体, 八面体和菱形十二面体等不同形状的纳米金颗粒, 其催化能力分别为1.843×10-2、 3.99×10-3和7.575×10-2s-1[28]。 总的来说, 以各向异性的纳米金作为催化剂, 催化活性表现较高。 同时, 本方法制备的金纳米花结构具有尖锐的片状结构特征和较高的比表面积, 因此也展现了很好的催化活性。
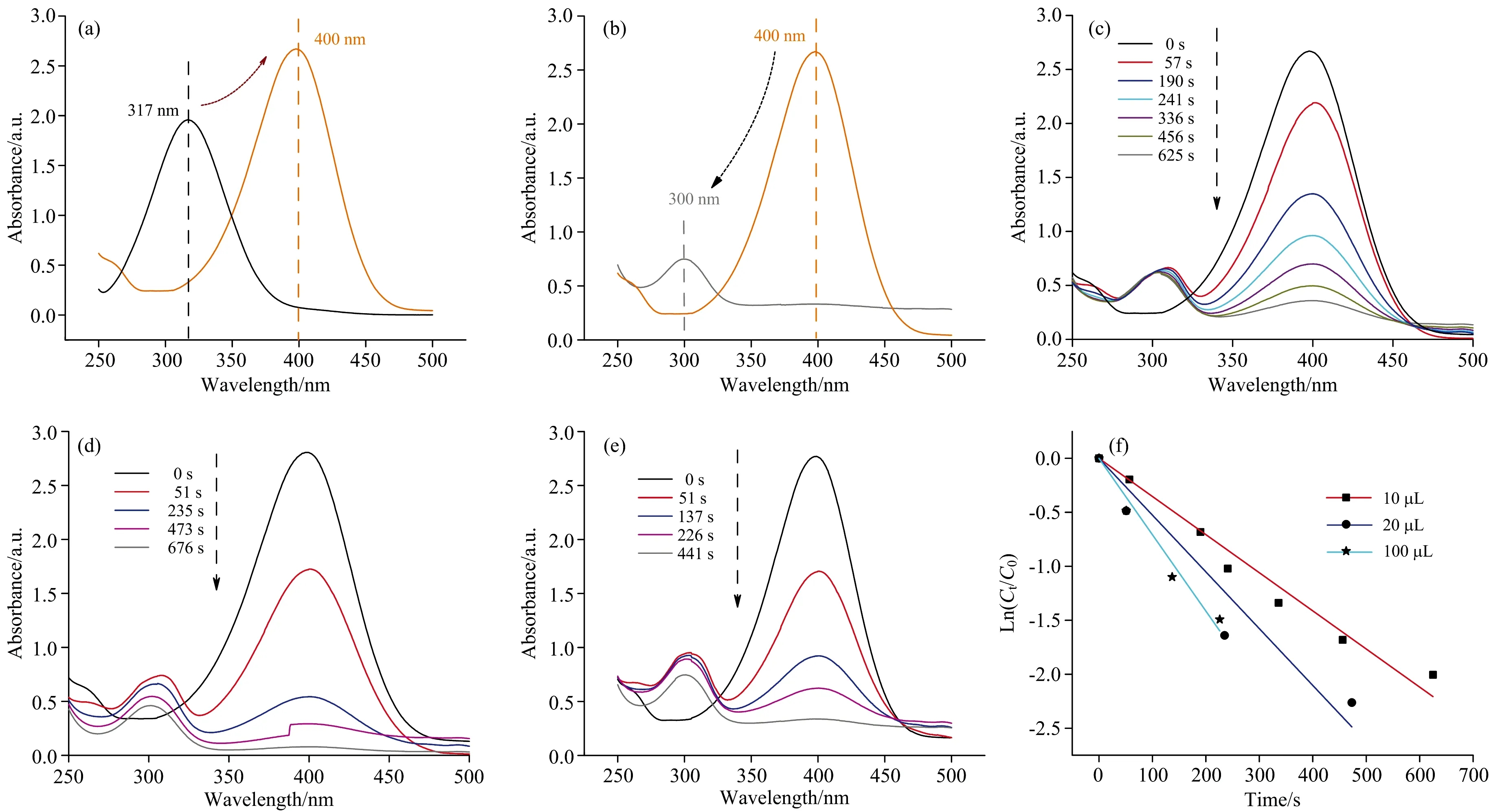
图4 不同量的金纳米花结构催化对硝基苯酚还原成对氨基苯酚(a): 在加入硼氢化钠后, 对硝基苯酚转变为对硝基苯酚钠; (b): 在加入适量催化剂后, 对硝基苯酚钠转变为对氨基苯酚; (c)-(e): 分别加入10、 20和100 μL的金纳米花结构作为催化剂; (f)不同量的金纳米花结构催化还原对硝基苯酚的ln(ct/c0)与时间t的关系图Fig.4 The catalytic reduction of 4-nitrophenol (4-NP) to 4-aminophenol (4-AP) with different amount of gold nanoflowers (AuNFs)(a): The generation of sodium p-nitrophenolate after addition of NaBH4; (b): Sodium p-nitrophenolate shift to 4-aminophenol after adding adequate catalyst; (c)-(e): Time-dependent UV-Vis adsorption spectra of the catalytic reduction reaction with 10, 20 and 100 μL of gold nanoflowers (AuNFs); (f): The linear relationship of ln(ct/c0) versus reaction time for the reduction of 4-NP with different amount of gold nanoflowers (AuNFs)
3 结 论
采用化学还原法, 以抗坏血酸溶解左旋多巴形成混合溶液为还原性溶液, 在常温下还原氯金酸实现了金纳米花结构的制备。 对该金纳米花结构进行了光谱特征、 晶体结构、 形貌和大小等方面的表征分析, 证明该金纳米花结构的独特形貌。 该金纳米花结构的表面等离子体共振峰位于650 nm附近, 粒径达到了(1.10±0.14) μm大小, 表面具有明显的尖锐的片状结构特征。 应用金纳米花结构催化还原对硝基苯酚并计算该反应的速率常数, 在添加金纳米花结构10、 20和 100 μL体积情况下, 获得了速率常数(k)分别为3.53×10-3、 5.27×10-3和5.4×10-3s-1, 证明了该金纳米花结构具有优良的催化活性。 为促进该金纳米花结构的在表面等离激元纳米光子学、 光催化、 光学和生物医学光子学等领域的应用打下了基础。

