黄芩苷-甘草酸纳米晶的制备工艺优化及体外释放考察Δ
谢 龙 ,赵雨芯 ,刘 凯 ,古 环 ,李小芳 #(1.成都中医药大学西南特色中药资源国家重点实验室,成都 611137;2.成都中医药大学药学院,成都 611137)
黄芩苷(baicalin,BCN)是从黄芩干燥根中提取的主要有效成分,具有解热抗炎、抗病毒及免疫调节等多种药理活性,但其水溶性及脂溶性较差,体内生物利用度较低,严重限制了黄芩苷的临床应用[1]。甘草酸(glycyrrhizic acid,GA)是从甘草干燥根及根茎中提取的主要有效成分,具有抗炎、抗肿瘤、抗病毒等多种药理活性,难溶于冷水,但可与其他天然产物形成复合物[2]。相关研究发现,黄芩-甘草药对中BCN 的溶出与两者配伍比例有关,且GA可能会增加BCN的溶解度[3]。
纳米晶是近年一种增加难溶性药物溶解度的新型载药技术,以少量表面活性剂或高分子材料作为稳定剂,可降低原料药的粒径至纳米级以增加难溶性药物的溶出度,进而提高药物的生物利用度[4―5]。基于此,本研究根据经典药对“黄芩-甘草”配伍比例,采用沉淀法结合高压均质法制备BCN-GA 纳米晶(BCN-GA solid nanocrystals,BCN-GA-SN),对其理化性质进行表征,并考察其体外释放性能,以期为BCN-GA-SN 制剂的研发提供参考。
1 材料
1.1 主要仪器
本研究所用的主要仪器有MS-280-H型磁力搅拌器(杭州旌斐仪器科技有限公司)、FA224 型电子天平(上海舜宇恒平科学仪器有限公司)、AH-100型高压均质机(加拿大ATS公司)、Nicomp 380ZLS型激光粒度分析仪(美国PSS公司)、SJIA-10N-50型冷冻干燥机(宁波市双嘉仪器有限公司)、ZRS-8G 型智能溶出试验仪(天津市天大天发科技有限公司)、Agilent 1200型高效液相色谱仪(美国Agilent 公司)、DSC3 型差示扫描量热仪(瑞士Mettler Toledo 公司)、SU8010 型扫描电子显微镜(日本Hitachi公司)等。
1.2 主要药品与试剂
BCN原料药(批号GB-20191023,纯度92%)、GA原料药(批号GB-201905021,纯度98%)均购自西安小草植物科技有限公司;BCN 对照品(批号MUST-19081012,纯度98%)、GA 对照品(批号MUST-1908080,纯度98.89%)均购自成都曼斯特生物科技有限公司;十二烷基硫酸钠(sodium dedecyl sulfate,SDS)、聚乙二醇400[Poly(ethylene glycol)-400,PEG-400]、泊洛沙姆188(poloxamer 188,P188)、吐温-80、聚乙烯吡咯烷酮K30(polyvinylpyrrolidone-K30,PVP-K30)、甘露醇、壳聚糖、乳糖、山梨醇、葡萄糖、无水乙醇均购自成都市科龙化工试剂厂;甲醇、乙腈为色谱纯,水为超纯水。
2 方法与结果
2.1 BCN-GA配伍比例的确定
黄芩-甘草为中医经典药对,在中药复方中具有解表清里、清热解毒功效时的配伍比例为3∶2(m/m);再根据2020年版《中国药典》(一部)对BCN 和GA 含量的要求[6―7],本研究最终确定BCN和GA的配伍比例为6∶1。
2.2 BCN-GA纳米混悬液的制备及其工艺优化
2.2.1 BCN-GA纳米混悬液的制备
采用沉淀法结合高压均质法进行制备。称取BCN原料药1.2 g,加无水乙醇适量,超声(功率480 W,频率40 kHz)使其完全溶解;然后通过匀速泵注入至含GA原料药0.2 g 和适量稳定剂的水(100 mL)中,以相应转速搅拌一定时间,挥去乙醇至无醇味,即得粗混悬液。采用高压均质机,在一定压力下均质数次,即得BCN-GA纳米混悬液。
2.2.2 BCN-GA 纳米混悬液平均粒径及多分散性指数的测定
取“2.2.1”项下BCN-GA纳米混悬液适量,用水稀释3 倍后,采用激光粒度仪测定其粒径及多分散性指数(polydispersity index,PDI),PDI 越小,表明粒子的大小分布均匀。重复测定3次,取平均值。
2.2.3 BCN-GA纳米混悬液制备工艺的单因素考察
以平均粒径、PDI 为评价指标,分别对BCN-GA 纳米混悬液稳定剂的种类及用量、搅拌转速和时间、高压均质压力和次数6个工艺因素进行单因素考察。
(1)稳定剂种类的考察:按“2.2.1”项下方法制备粗混悬液,稳定剂用量为BCN原料药的10%,以1 000 r/min搅拌15 min,进而考察不同种类稳定剂(SDS、P188、PEG-400、吐温-80、PVP-K30)对BCN-GA纳米混悬液制备的影响。由表1 可知,当以SDS 为稳定剂时,所得BCN-GA 纳米混悬液的粒径较小,且体系较为稳定,优于其他稳定剂,故后续对稳定剂SDS的用量进行考察。
表1 不同种类的稳定剂对BCN-GA 纳米混悬液平均粒径、PDI及稳定性的影响(±s,n=3)
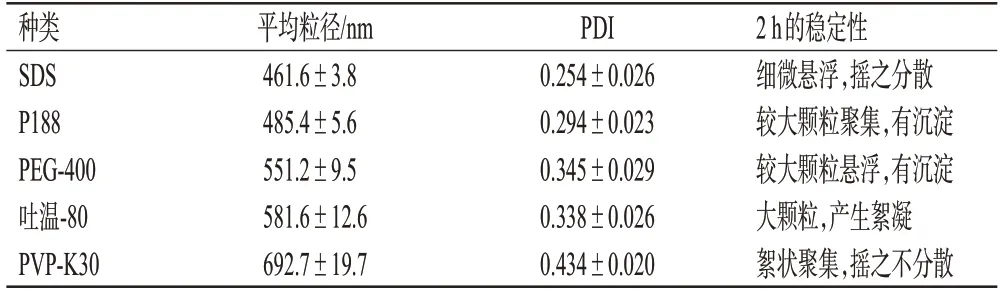
表1 不同种类的稳定剂对BCN-GA 纳米混悬液平均粒径、PDI及稳定性的影响(±s,n=3)
种类SDS P188 PEG-400吐温-80 PVP-K30平均粒径/nm 461.6±3.8 485.4±5.6 551.2±9.5 581.6±12.6 692.7±19.7 PDI 0.254±0.026 0.294±0.023 0.345±0.029 0.338±0.026 0.434±0.020 2 h的稳定性细微悬浮,摇之分散较大颗粒聚集,有沉淀较大颗粒悬浮,有沉淀大颗粒,产生絮凝絮状聚集,摇之不分散
(2)稳定剂SDS 用量的考察:按“2.2.1”项下方法制备粗混悬液,水中加入不同体积分数(相对于BCN的用量,下同)的SDS(分别为BCN用量的5%、10%、15%、20%、25%、30%),以1 000 r/min搅拌15 min,进而考察SDS的用量对BCN-GA 纳米混悬液制备的影响。由图1A 可知,随着SDS用量的增加,所得纳米混悬液的平均粒径、PDI 均先减小后增大,原因可能是SDS 使用过量,超过了其临界胶束浓度,使SDS 形成胶束与纳米粒竞争吸附,从而使纳米混悬液的稳定性降低,导致体系中粒子聚集和沉降。综合考虑,最终确定SDS的用量为15%。

图1 BCN-GA纳米混悬液制备工艺的单因素考察结果
(3)搅拌转速的考察:按“2.2.1”项下方法制备粗混悬液,SDS用量为15%,以不同转速(200、400、600、800、1 000、1 200 r/min)搅拌15 min,进而考察搅拌转速对BCN-GA 纳米混悬液制备的影响。由图1B 可知,当转速低于1 000 r/min 时,随着转速的增加,体系中粒子间的碰撞机会和强度增加,使得纳米混悬液的平均粒径和PDI均减小;当转速超过1 000 r/min时,搅拌过程中可能会产生气泡,阻碍了体系中粒子间的碰撞,导致沉降,从而使得纳米混悬液的平均粒径及PDI 均增大。综合考虑,最终确定搅拌速度为1 000 r/min。
(4)搅拌时间的考察:按“2.2.1”项下方法制备粗混悬液,SDS 用量为15%,以1 000 r/min 搅拌不同时间(5、10、15、20、25、30 min),进而考察搅拌时间对BCN-GA纳米混悬液制备的影响。由图1C 可知,随着搅拌时间的增加,所得纳米混悬液的平均粒径和PDI均先减小后趋于稳定而后增加,且当搅拌时间为15 min 时,纳米混悬液的平均粒径和PDI均较小。综合考虑,最终确定搅拌时间为15 min。
(5)均质次数的考察:按“2.2.1”项下方法制备粗混悬液,SDS 用量为15%,以1 000 r/min 搅拌15 min;将制得的粗混悬液先置于30 MPa压力下均质5次(由于低压环境有利于样品中大颗粒粒径的减小,高压环境可加速稳定剂的扩散使样品的粒径和PDI减小,故本实验采用高、低压相结合的形式进行优化),再于100 MPa压力下均质不同次数(5、10、15、20、25、30次),进而考察均质次数对BCN-GA 纳米混悬液制备的影响。由图1D 可知,随着均质次数的增加,所得纳米混悬液的平均粒径及PDI 均逐渐减小;当均质次数大于20 次时,其对纳米混悬液的平均粒径和PDI影响较小。综合考虑,最终确定均质次数为20次。
(6)均质压力的考察:按“2.2.1”项下方法制备粗混悬液,SDS 用量为15%,以1 000 r/min 搅拌15 min;将制得的粗混悬液先置于30 MPa压力下均质5次,再于不同压力(40、60、80、100、120、150 MPa)下均质20 次,进而考察均质压力对BCN-GA 纳米混悬液制备的影响。由图1E可知,随着均质压力的升高,所得纳米混悬液的平均粒径及PDI 均先逐渐减小;当均质压力达到120 MPa时,平均粒径和PDI 显著增大,这可能是由于均质过程中压力过大导致混悬剂的保护层被破坏,导致粒子发生聚集。综合考虑,最终确定高压时的均质压力为100 MPa。
(7)验证实验:采用经上述单因素实验考察得出的最优处方、制备工艺条件,重复制备3 批BCN-GA 纳米混悬液,并测定其粒径及PDI。结果显示,BCN-GA纳米混悬液的平均粒径为(394.7±4.6)nm,PDI 为0.195±0.011,RSD 值均小于5%。于室温条件下放置2 h 后,测定其平均粒径为(395.1±1.39)nm,PDI 为0.201±0.004,RSD 值均小于5%。这表明该制备工艺所制得的BCN-GA 纳米混悬液粒径大小均一,具有良好的稳定性。
2.3 BCN-GA-SN的制备及冻干固化工艺优化
2.3.1 BCN-GA-SN的制备
取按“2.2”项下最优工艺所制的BCN-GA 纳米混悬液10 mL,置于称量瓶中;加入冻干保护剂适量,于-50 ℃条件下预冻12 h,再减压冷冻干燥36 h,即得BCN-GA-SN。
2.3.2 BCN-GA-SN的再分散性评价
再分散系数(redispersibility index,RDI)是评价固化后纳米制剂分散性的指标,具体计算公式为RDI=冻干后再分散的制剂粒径/初始制剂粒径;其值越趋近于1,表明其固化损伤程度越低[6]。取“2.3.1”项下所得BCNGA-SN适量,加水10 mL,轻轻振荡使其复溶,采用激光粒度仪测定复溶后的平均粒径和PDI,并计算RDI。
2.3.3 BCN-GA-SN冻干固化工艺的优化及验证
以冻干固化后纳米晶的外观以及再分散后的平均粒径、PDI、RDI 为评价指标,对冻干保护剂种类及用量进行考察。
(1)冻干保护剂种类的考察:取按“2.2”项下最优工艺所制的纳米混悬液5份,分别加入常用的冻干保护剂甘露醇、壳聚糖、乳糖、山梨醇、葡萄糖(用量均为BCN的5%),各组平行3 份样品,按“2.3.1”项下方法制备BCN-GA-SN,以不加入冻干保护剂的样品为空白对照,考察冻干保护剂种类对BCN-GA-SN冻干固化工艺的影响。由表2 可知,未添加冻干保护剂的BCN-GA-SN 质地粗糙,且再分散后粒径增加最大;经甘露醇制备的BCN-GA-SN 冻干粉外观形状较为良好,复溶后粒径最小,且RDI最接近1。综合考虑,最终确定甘露醇为冻干保护剂。
表2 不同冻干保护剂对BCN-GA-SN 冻干固化工艺的影响(±s,n=3)
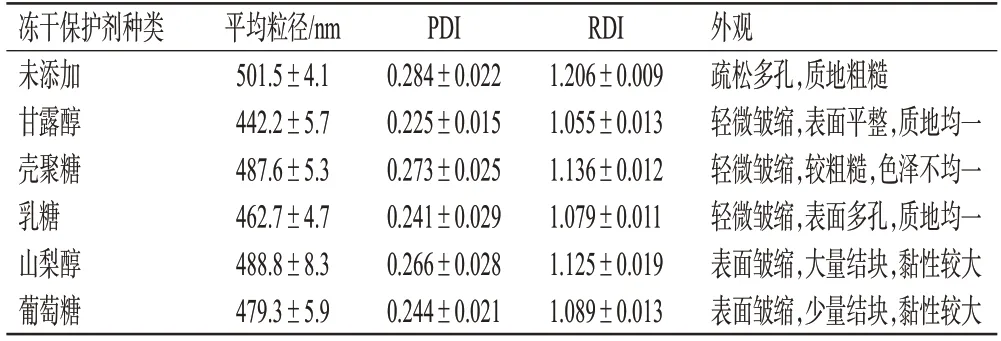
表2 不同冻干保护剂对BCN-GA-SN 冻干固化工艺的影响(±s,n=3)
冻干保护剂种类未添加甘露醇壳聚糖乳糖山梨醇葡萄糖平均粒径/nm 501.5±4.1 442.2±5.7 487.6±5.3 462.7±4.7 488.8±8.3 479.3±5.9 PDI 0.284±0.022 0.225±0.015 0.273±0.025 0.241±0.029 0.266±0.028 0.244±0.021 RDI 1.206±0.009 1.055±0.013 1.136±0.012 1.079±0.011 1.125±0.019 1.089±0.013外观疏松多孔,质地粗糙轻微皱缩,表面平整,质地均一轻微皱缩,较粗糙,色泽不均一轻微皱缩,表面多孔,质地均一表面皱缩,大量结块,黏性较大表面皱缩,少量结块,黏性较大
(2)冻干保护剂的用量考察:取按“2.2”项下最优工艺所制的纳米混悬液6 份,分别加入不同用量(0、1%、3%、5%、7%、10%,相对于BCN 的用量)的甘露醇,各组平行3 份样品,再按“2.3.1”项下方法制备BCN-GA-SN,考察冻干保护剂的用量对BCN-GA-SN冻干固化工艺的影响。由表3 可知,随着甘露醇用量的增加,BCN-GASN冻干粉表面逐渐平整光滑,RDI呈现先降低后增加的趋势;当甘露醇用量为5%时,冻干粉表面较为平整,无塌陷且质地均一,复溶后平均粒径为(442.2±5.7)nm,PDI 为0.225±0.015,RDI 为1.055±0.013,表明其再分散后仍能保持纳米混悬状态。综合考虑,最终确定甘露醇用量为BCN用量的5%。
表3 冻干保护剂用量对BCN-GA-SN 冻干固化工艺的影响(±s,n=3)

表3 冻干保护剂用量对BCN-GA-SN 冻干固化工艺的影响(±s,n=3)
甘露醇用量/%0 1 3 5 7 10平均粒径/nm 501.5±4.1 510.8±8.4 468.5±6.7 442.2±5.7 476.3±5.2 505.2±4.9 PDI 0.284±0.022 0.277±0.025 0.248±0.023 0.225±0.015 0.233±0.015 0.249±0.028 RDI 1.206±0.009 1.166±0.019 1.115±0.015 1.055±0.013 1.087±0.012 1.153±0.011外观疏松多孔,质地粗糙表面多孔,质地较粗糙表面较平整,质地较均一表面较平整,质地均一表面平整,质地均一表面平整
(3)验证实验:按上述筛选的最优保护剂及用量进行平行3次验证实验,结果显示,BCN-GA-SN的平均粒径为(443.1±3.8)nm,PDI 为0.221±0.011,RDI 为1.063±0.016,RSD值均小于5%,表明所制得的BCN-GA-SN粒径大小均一,且具有良好的重现性。
2.4 BCN-GA-SN的表征
2.4.1 BCN-GA纳米混悬液的外观形态
取BCN-GA 纳米混悬液在自然光下和激光下进行观察。由图2可知,BCN-GA纳米混悬液呈现淡黄色,颜色均一,流动性好;在自然光下透明澄清,在激光下出现丁达尔现象,属于混悬态液体。

图2 BCN-GA混悬液的外观形态观察结果
2.4.2 BCN-GA-SN平均粒径、PDI、RDI的测定
取适量以最优工艺制备的BCN-GA-SN 样品,用纯水稀释至一定浓度,待均匀分散后,于激光粒度仪中测定其平均粒径和PDI 并计算RDI。由图3 可知,BCNGA-SN 的平均粒径为(442.2±5.7)nm,PDI 为0.225±0.015,RDI 为1.055±0.013,表明本研究所制备的BCNGA-SN粒径大小均一、分布均匀。

图3 BCN-GA-SN的粒径分布
2.4.3 BCN-GA-SN的显微形态观察
取适量BCN、GA原料药和以最优工艺制备的BCNGA-SN 适量,对其表层作减压喷金处理后,采用扫描电子显微镜进行观察,并拍照。由图4可知,BCN和GA原料药为大小不均一的块状,且表面粗糙;BCN-GA-SN呈现不规则的球棒状,大小较为均一。

图4 BCN、GA原料药和BCN-GA-SN的显微图
2.4.4 差示扫描量热分析
取BCN-GA-SN、空白辅料SDS 和适量BCN、GA 原料药以及两者的物理混合物进行差示扫描量热分析,检测条件为温度25~350 ℃,升温速率为10 ℃/min,气体为氮气。由图5 可知,BCN 原料药在234 ℃有一吸收峰,GA 原料药在216 ℃有一吸收峰,空白辅料SDS 在188 ℃有一吸收峰;BCN-GA 物理混合物在216、234 ℃均有吸收峰,而BCN-GA-SN在这两处的吸收峰均消失,表明BCN、GA在该纳米晶体系中呈现无定形状态。
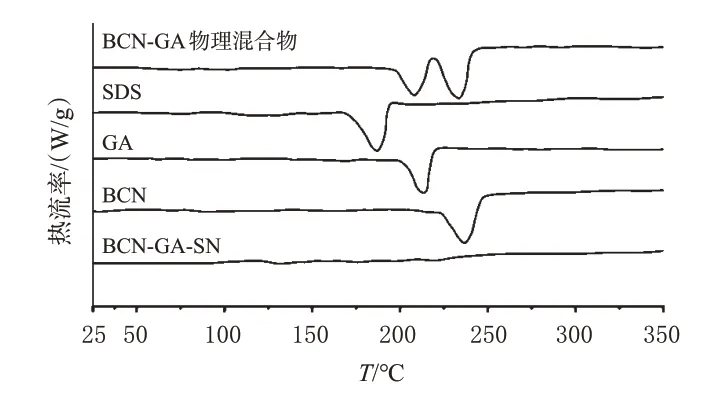
图5 差示扫描量热分析结果
2.5 体外溶出的评价
2.5.1 色谱条件
采用高效液相色谱法测定BCN-GA-SN 中BCN 和GA 的含量。色谱柱为Agilent EP-C18(250 mm×4.6 mm,5 μm),流动相为乙腈-0.2%磷酸溶液(37∶63,V/V),检测波长为277 nm,柱温为30 ℃,流速为0.8 mL/min,进样量为10 μL。
2.5.2 对照品溶液的制备
分别精密称取BCN、GA对照品各10 mg,置于同一50 mL容量瓶中,加入甲醇适量,超声使其充分溶解并定容,即得BCN、GA 质量浓度均为0.20 mg/mL 的混合对照品溶液。
2.5.3 供试品溶液的制备
精密称取按“2.3”最优工艺制备的BCN-GA-SN 适量,装入空心胶囊壳中,按照2020年版《中国药典》(四部)通则(桨法)进行实验。以水900 mL为溶出介质,温度为(37.0±0.5)℃,转速为100 r/min,于60 min 时取样5 mL,经0.45 μm微孔滤膜滤过,即得供试品溶液。
2.5.4 专属性考察
取混合对照品溶液、供试品溶液及空白辅料SDS样品溶液(以甲醇溶解)适量,按“2.5.1”项下色谱条件进样分析。由图6 可知,空白辅料对样品的测定无影响,且BCN与GA的分离度良好,表明本实验专属性良好。
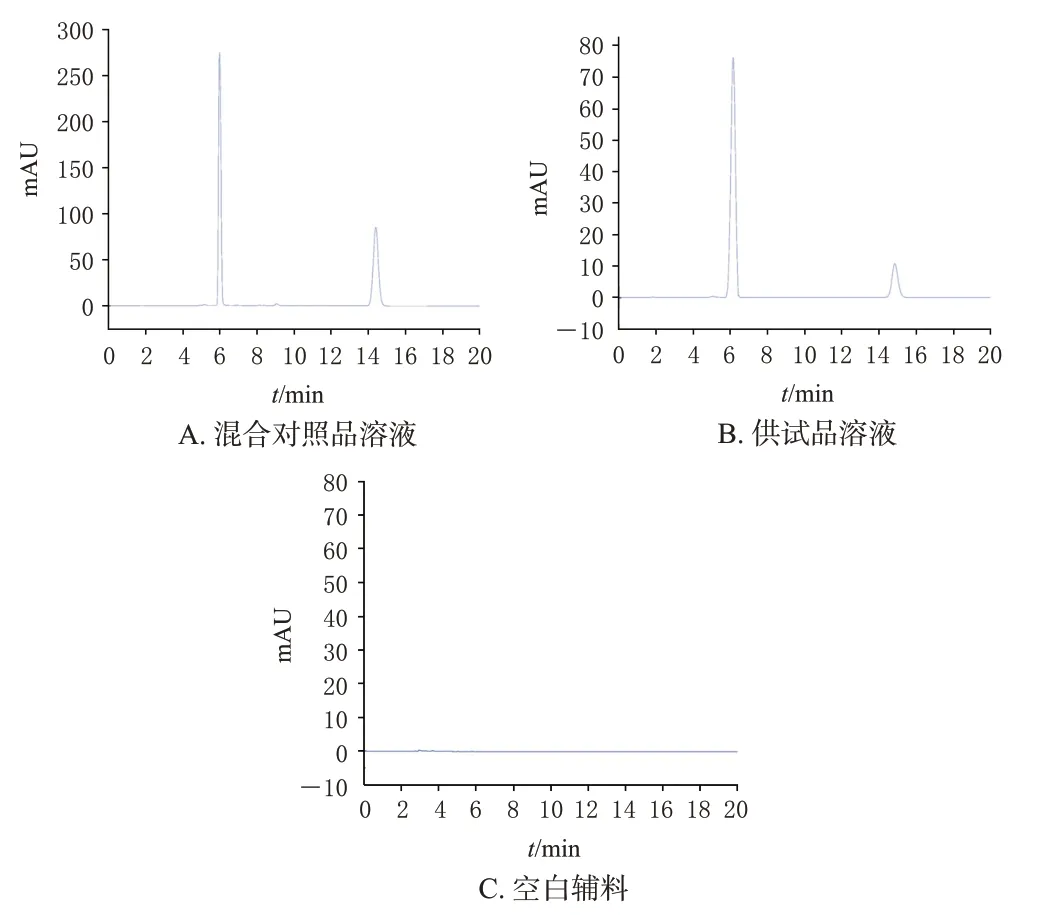
图6 专属性考察结果
2.5.5 线性范围考察
精密吸取混合对照品溶液适量,以甲醇稀释成不同质量浓度的系列溶液,然后按“2.5.1”项下色谱条件进样分析,记录峰面积。以待测成分峰面积为纵坐标(Y)、质量浓度为横坐标(X)绘制标准曲线。结果显示,BCN的回归方程为Y=39.263X-9.493(R2=0.999 8),线性范围为12.5~125.0 μg/mL;GA 回归方程为Y=42.751X+48.056(R2=0.999 8),线性范围为12.5~125.0 μg/mL,表明BCN和GA的含量测定方法线性关系良好。
2.5.6 载药量的测定
称取按“2.3”最优工艺制备的BCN-GA-SN适量(质量记为W),加入一定体积的甲醇(记为V),超声使其完全溶解,经0.45 μm微孔滤膜滤过;取滤液按“2.5.1”项下色谱条件进样分析,记录峰面积并代入回归方程分别计算BCN和GA的质量浓度(C),再计算载药量(载药量=CV/W)。结果显示,BCN 的载药量为(62.5±0.7)%,GA的载药量为(9.4±0.2)%,由此可知,两药的载药比例基本符合实验设计比例。
2.5.7 BCN-GA-SN的体外释放考察
按照2020年版《中国药典》(四部)通则(桨法)进行体外溶出度的测定,以考察BCN-GA-SN 的体外释放性能。精密称取以最优工艺制备的BCN-GA-SN 以及BCN-GA物理混合物适量,以水900 mL为溶出介质,温度为(37.0±0.5)℃,转速为100 r/min,分别于5、10、20、30、40、50、60 min取样5 mL,并同时补足等温等量介质。取样液体经0.45 μm 微孔滤膜滤过后,按“2.5.1”项下色谱条件进样分析,记录峰面积并代入回归方程,分别计算BCN 和GA 的质量浓度,再计算两者的累积溶出度,具体公式为累积溶出度(Xn)=(Cn×V0+C1×V1+C2×V1+…+Cn-1×V1)/M×100%(式中,Xn为第n个时间点的累积溶出度,Cn为BCN 或GA 的质量浓度,V0为溶出介质总体积,V1为每次取样后所补充的介质体积,M为样品中BCN 或GA 的含量)。同时,绘制BCN 和GA 的累积溶出度-时间曲线。由图7可知,在60 min时,BCN-GA-SN中BCN 的累积溶出度达91.1%,GA 的累积溶出度为98.5%;而物理混合物中BCN 的累积溶出度不超过50%,GA的累积溶出度为98.3%。这表明将BCN和GA制成BCN-GA-SN能够有效提高BCN的体外溶出度。
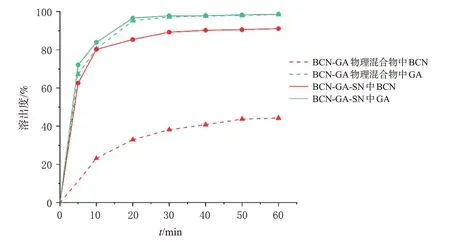
图7 BCN-GA-SN和BCN-GA物理混合物的溶出曲线
3 讨论
传统中药复方遵从“君臣佐使”配伍用药,相同药物也会根据患者的不同证候或不同疾病按照不同配伍比例进行组方[8―9]。黄芩和甘草的配伍比例决定了其主治和功效有所差别,根本原因在于其有效成分的比例发生了变化,因此制备符合药对配伍比例的纳米晶,为经典药对的中药新型制剂研究提供了新思路。
本实验基于经典药对黄芩-甘草用于“清热解毒”时的配伍比例,成功制备了BCN-GA 纳米混悬液,进一步将其固化为BCN-GA-SN。通过外观、显微形态观察发现,该纳米晶的粒径分布均匀,且以5%甘露醇为冻干保护剂固化后,该纳米晶粒径更小、更均一,且再分散性良好,最终载药比例也基本符合实验设计配伍比例。进一步进行体外释放考察发现,该纳米晶改善了BCN 单体药物的溶解性和体外释放特性,使药物释放加快、释放率提高,这也提示传统复方的配伍比例转化为有效成分比例制备中药新剂型的合理性。
综上所述,本研究成功制备了BCN-GA-SN,其粒径大小均一、分布均匀,可有效提高BCN的体外溶出度。

