不同频次MECT联合第二代抗精神药物治疗精神分裂症住院患者的效果
艾腾峰
精神分裂症系患病率较高的精神科疾病,有起病缓慢、病情反复等特点,目前其发病机制尚未完全明确,临床上常用的疗法有药物疗法、物理疗法、心理疗法[1]。其中,以奥氮平为代表的第二代抗精神病药物因其疗效较佳、不良反应较少而在临床上应用广泛,但因患者存在个体差异,药物治疗仍存在不足[2]。改良电抽搐治疗(MECT)为新型物理疗法,将传统电抽搐治疗与肌松剂、麻醉剂、疾病发作动态监测等改良措施相结合,治疗精神分裂症具有较好的效果[3]。目前,MECT 联合第二代抗精神药物是治疗精神分裂症的常用疗法,但MECT 治疗频次仍未明确,不同频次MECT 联合第二代抗精神药物治疗精神分裂症住院患者的效果的相关研究仍较少。基于此,上饶市第三人民医院老年科选取精神分裂症住院患者80 例,开展下述研究。
1 资料与方法
1.1 一般资料
选取本院老年科2019 年1 月—2022 年1 月收治的精神分裂症住院患者80 例,纳入标准:(1)符合文献[4]《安徽省精神分裂症分级诊疗指南(2016 版)》中精神分裂症的诊断标准;(2)符合文献[5]中MECT 的治疗指征;(3)急性发病后入院治疗。排除标准:(1)伴有相关药物过敏史;(2)近期接受过抗精神病治疗;(3)伴有其他精神疾病。按照随机数字表法将患者分为药物组(26 例)、高频组(27 例)、低频组(27 例)。所有患者均已签署知情同意书。本研究符合《赫尔辛基宣言》的相关医学研究要求,已获得本院医学伦理委员会的批准。
1.2 方法
药物组予以单纯第二代抗精神病药物治疗。口服奥氮平(生产厂家:齐鲁制药有限公司,批准文号:国药准字H20183501,规格:10 mg),初始剂量为5 mg/d,维持剂量为10~15 mg/d,根据患者临床状况适当调整用药剂量,用药剂量范围为5~20 mg/d,治疗时间为2 个月。高频组在药物组的基础上予以3 次/周的MECT 治疗。治疗前静脉注射0.5 mg 阿托品(生产厂家:成都第一制药有限公司;批准文号:国药准字H51022767,规格:1 mL︰0.5 mg)、1 mL/kg 丙泊酚(生产厂家:广东嘉博制药有限公司,批准文号:国药准字H20084457,规格:20 mL︰200 mg),观察到患者眼球固定、睫毛反射消失后,注射1.0 mg/kg 氯化琥珀酰胆碱(生产厂家:北京双鹤药业股份有限公司;批准文号:国药准字H11021581,规格:1 mL︰50 mg),待肌颤结束后启动MECT 治疗仪(生产厂家:美国美可达,型号:spECTrum5000Q),将电极放置在患者额头两侧,通电时间根据患者状态适当调整,治疗过程中随时检测患者的心率、血压等基础生命指标。MECT 治疗频次为3 次/周,治疗时间为2 个月。低频组在药物组的基础上予以1 次/周的MECT 治疗。MECT治疗方法同高频组,治疗频次为1 次/周,治疗时间为2 个月。
1.3 观察指标与评价标准
观察三组临床疗效、认知功能、神经递质水平。(1)临床疗效。临床疗效评估标准:于治疗2 个月后经阳性和阴性症状量表(PANSS)评估患者临床疗效,PANSS 量表包括30 个条目,各条目采用7 级评分法,评分与患者症状严重程度呈正相关。痊愈:治疗后PANSS 评分下降幅度超过75%;显效:治疗后PANSS 评分下降幅度为50%~75%;有效:治疗后PANSS 评分下降幅度为25%~49%;无效:治疗后PANSS 评分下降幅度低于25%[6]。临床总有效率=(总例数-无效例数)/总例数×100%。(2)认知功能。分别于治疗前、治疗2 个月后经MATRICS认知成套测验(MCCB)从处理速度(包括符号编码、连线测试、语义流畅性,满分150 分,取均值50 分)、注意/警觉、工作记忆(数字序列、空间广度,满分100 分,取均值50 分)、言语学习和记忆(满分50 分)、视觉学习和记忆(满分50 分)、推理与问题解决能力(满分50 分)、社会认知(满分50 分)等7 个维度10 个项目评估患者的认知功能,各维度分值均为50 分,评估与患者认知功能呈正相关[7]。(3)神经递质水平。分别于治疗前、治疗2 个月后采集患者空腹静脉血4 mL 离心后,经ELISA 检测患者血清中5-羟色胺(5-HT)、多巴胺(DA)、去甲肾上腺素(NE)的含量[8]。
1.4 统计学处理
使用SPSS 20.0 分析数据。计数资料用率(%)表示,用χ2检验;计量资料用(±s)表示,多组间比较用单因素方差分析,两组间比较用LSD-t 检验,组内比较用配对样本t 检验。以P<0.05 表示差异有统计学意义。
2 结果
2.1 两组一般资料对比
药物组男14 例,女12 例;年龄39~50 岁,平均(45.38±3.24)岁;病程15~34 个月,平均(23.14±4.26)个月;疾病分型:偏执型21 例,其他型5 例。高频组男16 例,女11 例;年龄36~49 岁,平均(45.69±3.51)岁;病程13~38 个月,平均(23.02±4.35)个月;疾病分型:偏执型20 例,其他型7 例。低频组男15 例,女12 例;年龄35~50 岁,平均(45.35±3.64)岁;病程12~35 个月,平均(23.29±4.53)个月;疾病分型:偏执型19 例,其他型8 例。三组的一般资料比较,差异均无统计学意义(P>0.05),具有可比性。
2.2 两组临床疗效对比
治疗前,三组的PANSS 评分比较,差异无统计学意义(P>0.05);治疗后,三组的PANSS 评分均降低(P<0.05),且低频组、高频组的PANSS 评分均低于药物组(P<0.05),低频组的PANSS 评分低于高频组(P<0.05)。低频组、高频组的临床总有效率均高于药物组(P<0.05);低频组、高频组的临床总有效率比较,差异无统计学意义(P>0.05)。见表1。

表1 两组临床疗效对比
2.3 两组认知功能对比
治疗前,三组的各项MCCB 评分比较,差异无统计学意义(P>0.05);治疗后,三组的各项MCCB 评分均升高(P<0.05),且低频组、高频组的各项MCCB 评分均高于药物组(P<0.05),低频组的各项MCCB 评分均高于高频组(P<0.05)。见表2。
表2 两组认知功能对比[分,(±s)]

表2 两组认知功能对比[分,(±s)]
*与本组治疗前比较,P<0.05;#与药物组比较,P<0.05;△与高频组比较,P<0.05。
组别 处理速度注意/警觉治疗前 治疗后 治疗前 治疗后药物组(n=26) 25.31±3.27 31.54±4.62* 27.45±3.84 31.85±4.52*高频组(n=27) 24.89±3.43 36.73±4.95*# 27.31±3.57 35.79±4.86*#低频组(n=27) 25.46±3.85 41.87±5.01*#△ 27.08±3.96 38.61±4.63*#△F 值 0.433 6.453 0.137 4.057 P 值 0.896 0.001 0.891 0.001组别 工作记忆言语学习和记忆治疗前 治疗后 治疗前 治疗后药物组(n=26) 23.65±3.34 31.63±4.29* 23.57±3.68 31.46±4.25*高频组(n=27) 24.16±3.07 37.39±4.15*# 24.06±3.79 35.21±4.32*#低频组(n=27) 24.78±3.46 42.28±4.36*#△ 23.92±3.54 39.83±4.39*#△F 值 0.397 6.315 0.478 5.185 P 值 0.921 0.001 0.635 0.001组别 视觉学习和记忆推理与问题解决能力社会认知治疗前 治疗后 治疗前 治疗后 治疗前 治疗后药物组(n=26) 24.26±3.53 30.56±4.21* 22.46±3.24 30.29±4.13* 24.32±3.51 31.45±4.26*高频组(n=27) 23.95±3.27 34.49±4.18*# 23.13±3.57 34.81±4.46*# 24.89±3.64 34.95±4.68*#低频组(n=27) 24.18±3.08 38.26±4.37*#△ 23.36±3.42 37.75±4.58*#△ 24.92±3.76 38.93±5.14*#△F 值 0.331 5.409 0.442 5.146 0.431 5.169 P 值 0.742 0.001 0.681 0.001 0.714 0.001
2.4 两组神经递质水平对比
治疗前,三组的5-HT、DA、NE 水平,差异无统计学意义(P>0.05);治疗后,三组的5-HT、DA、NE 水平较治疗前均升高(P<0.05);且低频组、高频组的5-HT、DA、NE 水平均高于药物组(P<0.05);低频组的5-HT、DA、NE 水平均高于高频组(P<0.05)。见表3。
表3 两组神经递质水平对比(±s)
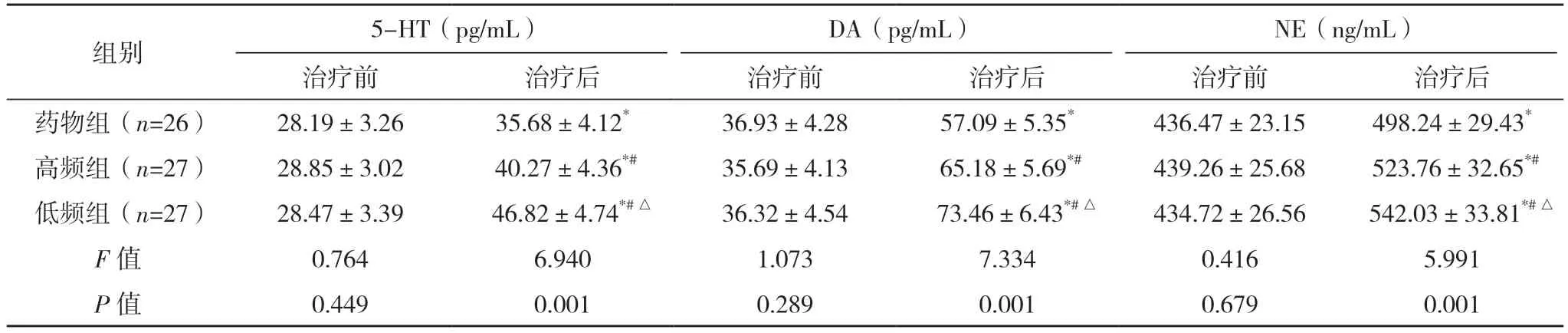
表3 两组神经递质水平对比(±s)
*与本组治疗前比较,P<0.05;#与药物组比较,P<0.05;△与高频组比较,P<0.05。
组别 5-HT(pg/mL)DA(pg/mL)NE(ng/mL)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后药物组(n=26) 28.19±3.26 35.68±4.12* 36.93±4.28 57.09±5.35* 436.47±23.15 498.24±29.43*高频组(n=27) 28.85±3.02 40.27±4.36*# 35.69±4.13 65.18±5.69*# 439.26±25.68 523.76±32.65*#低频组(n=27) 28.47±3.39 46.82±4.74*#△ 36.32±4.54 73.46±6.43*#△ 434.72±26.56 542.03±33.81*#△F 值 0.764 6.940 1.073 7.334 0.416 5.991 P 值 0.449 0.001 0.289 0.001 0.679 0.001
3 讨论
精神分裂症是一种严重、致残的慢性神经系统疾病,具有高度遗传性和神经生物学特性,其发病机制并不十分明确,目前主流观点认为其发生发展可受神经递质功能、心理因素、环境因素的多重影响,其临床症状变化迅速,具体可细分为阳性症状、阴性症状、认知症状[9]。阳性症状表现为妄想、幻觉、行为和语言紊乱,阴性症状表现为语言贫乏、情绪低落、兴趣丧失,认知症状表现为抽象能力、组织能力的缺陷[10]。目前临床上,对精神分裂症患者多采用第二代抗精神病药物治疗,但长期疗效欠佳。
MECT 是一种效果突出、安全性较高的改良物理疗法,通过以适量的电流刺激患者大脑皮质,诱发大脑放电,诱导脑细胞发生相应的电生理反应,促使脑部神经递质的分泌达到平衡,从而缓解相应症状[11]。目前MECT 治疗精神分裂症的频次尚未形成共识,有研究表明,高频MECT 治疗可导致患者短期认知功能损害,导致患者出现不同程度的记忆力丧失[12]。MECT 治疗需通电操作,若未合理控制治疗频次,可能会对患者机体产生一定的创伤,加剧患者的认知功能障碍,不利于患者的恢复。
本研究中,治疗后低频组、高频组的PANSS 评分均低于药物组(P<0.05),且低频组的PANSS 评分低于高频组(P<0.05);低频组、高频组的临床总有效率均高于药物组(P<0.05),但低频组、高频组的临床总有效率无统计学差异(P>0.05),提示低频次治疗与高频次治疗效果相当。这与赵永华等[13]的研究结果基本相符。
本研究中,治疗后低频组、高频组的各项MCCB 评分均高于药物组(P<0.05),且低频组的各项MCCB 评分均高于高频组(P<0.05),提示与高频次MECT 联合第二代抗精神药物治疗相比,低频次MECT 联合第二代抗精神药物可显著改善患者认知功能。究其原因:科学合理的MECT 治疗与可最大限度调节患者的神经电生理参数,促进受损神经元修复,同时可减轻高频次治疗过程中麻醉剂、肌松剂等药物对神经系统的损伤,改善患者认知功能[14]。
MECT 通过刺激患者脑部,诱发大脑内神经递质释放和传递,从而改善大脑功能,发挥抗精神病作用。5-HT、DA、NE 为与精神分裂症相关的神经递质,其中5-HT 为氧化还原活性单胺神经递质,在中枢神经系统中含量丰富,主要分布在下丘脑和松果体,可参与调节睡眠、情绪、食欲等生理过程[15];DA 是大脑中含量最丰富的儿茶酚胺类神经递质,其分泌和传递障碍可导致患者出现一系列精神分裂症症状[16];NE 是由交感节后神经元和脑内去甲肾上腺素能神经元合成和分泌的神经递质,在精神分裂症的病理生理过程中发挥着重要作用[17]。本研究中,治疗后低频组、高频组的5-HT、DA、NE水平均高于药物组(P<0.05),且低频组的5-HT、DA、NE 水平均高于高频组(P<0.05),提示与高频次MECT 联合第二代抗精神药物治疗相比,低频次MECT 联合第二代抗精神药物可有效调节神经递质水平。究其原因:高频次MECT 治疗通过借助脉冲电流刺激患者大脑皮层,可激活患者的下丘脑、松果体、多巴胺能通路、去甲肾上腺素能通路,刺激5-HT、DA、NE 的合成和分泌[18-19];同时,高频次MECT 的持续频繁的脉冲电流刺激可能损伤患者神经元结构,进而抑制5-HT、DA、NE 的合成和分泌,故高频次MECT 联合第二代抗精神药物治疗后患者体内的神经递质含量低于低频次MECT 联合第二代抗精神药物治疗[20]。
综上所述,与高频次MECT 联合第二代抗精神药物治疗精神分裂症住院患者相比,低频次MECT联合第二代抗精神药物治疗可显著改善患者认知功能,有效调节神经递质水平。但因为本研究存在一定局限,如纳入研究的样本量偏小,研究期间较短,导致两者的临床总有效率无统计学差异,今后拟扩大样本量、延长研究期间,进一步完善研究设计。

