吲哚布芬联合替格瑞洛治疗NSTE-ACS的临床观察*
邓婷婷 华永平 张垚 吴岸彪 席罡 王雁南
非ST 段抬高型急性冠状动脉综合征(NSTEACS)是因冠状动脉粥样硬化斑块破裂引起的不伴ST 段抬高的心肌缺血性梗死,流行病学资料显示,我国NSTE-ACS 的发病率逐渐升高,现已成为致残和致死的主要疾病之一[1-2]。目前,临床对于NSTE-ACS 以药物为基础治疗,必要时行经皮冠状动脉介入(PCI)、冠状动脉旁路移植(CABG)等介入或手术治疗。积极的血运重建虽能开通患者的梗死冠状动脉,但相关冠状动脉微循环被破坏,仍可能发生再梗死、恶性心律失常等心血管不良事件。近期,双联抗血小板治疗(DAPT)被证实可显著降低NSTE-ACS 患者心血管事件发生率和病死率[3]。临床最常用的DAPT 药物为阿司匹林联合替格瑞洛(P2Y12 受体拮抗剂),其中阿司匹林是最常用的冠心病二级预防药物,但部分患者尤其是老年患者用药后会出现严重的胃肠道反应、出血等现象[4]。吲哚布芬属于新型抗血小板药物,对胃肠道黏膜前列腺素的影响较小,考虑可对无法耐受阿司匹林的患者应用该药进行替代治疗[5]。但目前关于吲哚布芬联合P2Y12 受体拮抗剂治疗NSTE-ACS 患者的系统循证研究较缺乏,因此本研究探讨吲哚布芬联合替格瑞洛对NSTE-ACS 的治疗效果及安全性,现报道如下。
1 资料与方法
1.1 一般资料
选取2021 年5 月—2022 年12 月就诊于景德镇市第三人民医院的NSTE-ACS 患者60 例。(1)纳入标准:①符合美国心脏病学会(ACC)/美国心脏病协会(AHA)NSTE-ACS 管理指南中的相关诊断标准[6];②近2 周内未服用过其他抗血小板药物治疗,如阿司匹林、氯吡格雷等;③心功能Ⅱ、Ⅲ级。(2)排除标准:①有严重出血倾向、出血性疾病或近期出血史、重大创伤史;②其他原因导致的胸痛;③合并其他血栓性疾病;④合并血液性、感染性疾病;⑤有恶性肿瘤、严重肝肾疾病;⑥对研究药物有过敏史;⑦接受心脏急诊介入术。入选病例按随机数字表法分为两组,各30 例。患者或家属均签订知情同意书。本研究获医院医学伦理委员会批准。
1.2 方法
对照组发病首次服用阿司匹林(生产厂家:河南永和制药有限公司,批准文号:国药准字H41024127,规格:0.1 g)300 mg,替格瑞洛(生产厂家:石药集团欧意药业有限公司,批准文号:国药准字H20205031,规格:60 mg)180 mg;后维持阿司匹林100 mg/次,1 次/d,替格瑞洛90 mg/次,2 次/d。观察组发病首次给予吲哚布芬(生产厂家:杭州中美华东制药有限公司,批准文号:国药准字H20194067,规格:0.1 g)200 mg,替格瑞洛180 mg;后维持吲哚布芬100 mg,2 次/d,替格瑞洛90 mg,2 次/d。两组疗程均为4 周。
1.3 观察指标与评价标准
(1)心血管不良事件:统计用药4 周内,患者发生心绞痛复发、急性心肌梗死等情况。(2)血小板功能及参数:用药前、用药7 d 后,分别采集患者晨起血3 mL,置于抗凝试管中,待检;以二磷酸腺苷(ADP)做诱导,检测血小板聚集率。另采集2 mL 血液标本,检测血小板计数(PLT)、血小板压积(PCT)、平均血小板体积(MPV)、血小板分布宽度(PDW)。(3)肝肾功能指标:用药前、用药7 d 后,检测患者丙氨酸氨基转氨酶(ALT)、血尿素氮(BUN)、肌酐(Cr),取样及检测方法同上述步骤。(4)药物不良反应:统计患者用药期间出血、胃肠道反应发生情况。
1.4 统计学处理
2 结果
2.1 两组一般资料对比
对照组男18 例,女12 例;年龄54~77 岁,平均(65.23±4.21)岁;不稳定型心绞痛(UA)23 例,非ST 段抬高型心肌梗死(NSTEMI)7 例。观察组男15 例,女15 例;年龄52~80 岁,平均(66.17±5.43)岁;UA 20 例,NSTEMI 10 例。两组一般资料对比,差异均无统计学意义(P>0.05),具有可比性。
2.2 两组心血管不良事件对比
两组心血管不良事件发生率比较,差异无统计学意义(χ2=0.000,P=1.000),见表1。

表1 两组心血管不良事件对比[例(%)]
2.3 两组血小板功能及参数对比
用药前、用药7 d 后,两组组间血小板聚集率、PLT、PCT、MPV、PDW 对比,差异均无统计学意义(P>0.05);用药7 d 后,两组血小板聚集率均较用药前降低,差异均有统计学意义(P<0.05)。见表2。
表2 两组血小板功能及参数对比(±s)
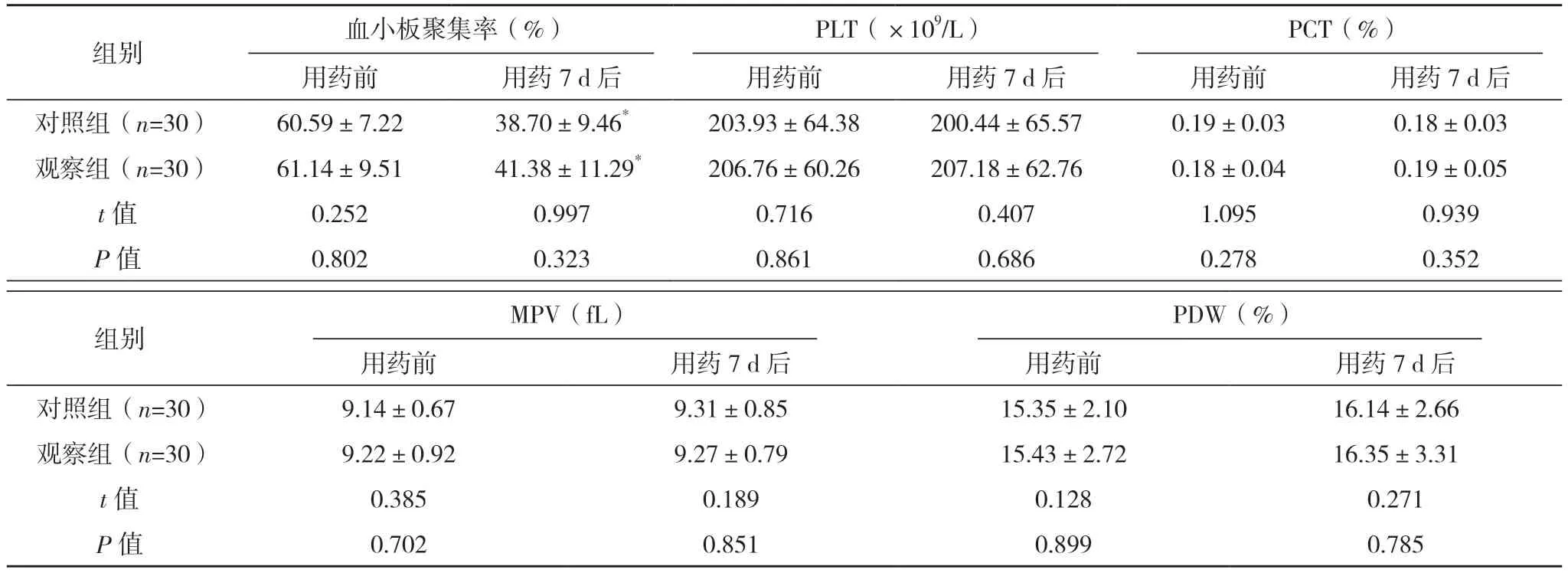
表2 两组血小板功能及参数对比(±s)
*与本组用药前对比,P<0.05。
组别 血小板聚集率(%)PLT(×109/L)PCT(%)用药前 用药7 d 后 用药前 用药7 d 后 用药前 用药7 d 后对照组(n=30) 60.59±7.22 38.70±9.46* 203.93±64.38 200.44±65.57 0.19±0.03 0.18±0.03观察组(n=30) 61.14±9.51 41.38±11.29* 206.76±60.26 207.18±62.76 0.18±0.04 0.19±0.05 t 值 0.252 0.997 0.716 0.407 1.095 0.939 P 值 0.802 0.323 0.861 0.686 0.278 0.352组别 MPV(fL)PDW(%)用药前 用药7 d 后 用药前 用药7 d 后对照组(n=30) 9.14±0.67 9.31±0.85 15.35±2.10 16.14±2.66观察组(n=30) 9.22±0.92 9.27±0.79 15.43±2.72 16.35±3.31 t 值 0.385 0.189 0.128 0.271 P 值 0.702 0.851 0.899 0.785
2.4 两组肝肾功能指标对比
用药前、用药7 d 后,两组组间、组内ALT、BUN、Cr 比较,差异均无统计学意义(P>0.05),见表3。
表3 两组肝肾功能指标对比(±s)

表3 两组肝肾功能指标对比(±s)
组别 ALT(U/L)BUN(mmol/L)Cr(μmol/L)用药前 用药7 d 后 用药前 用药7 d 后 用药前 用药7 d 后对照组(n=30) 26.54±6.93 25.35±7.65 4.72±1.17 4.55±1.25 74.98±10.34 73.09±10.76观察组(n=30) 25.97±8.02 25.18±8.34 4.68±1.30 4.26±1.38 76.40±11.59 72.96±13.81 t 值 0.115 0.082 0.125 0.853 0.501 0.041 P 值 0.909 0.935 0.901 0.397 0.618 0.968
2.5 两组药物不良反应发生情况对比
观察组药物不良反应总发生率为10.00%,低于对照组的33.33%,差异有统计学意义(χ2=4.812,P=0.028),见表4。

表4 两组药物不良反应发生情况对比[例(%)]
3 讨论
近年来,NSTE-ACS 发病率不断攀升,病死率居高不下,成为临床常见急危重症[7-8]。血小板活化、黏附、聚集在NSTE-ACS 的发生及发展中发挥着重要作用,故抗血小板是该病治疗的基石[9-10]。经典DAPT 方案中阿司匹林存在“阿司匹林抵抗”、胃肠道反应、血栓性事件复发率高等问题,因此选择更安全有效的DAPT 方案是临床亟待解决的问题[11-13]。
吲哚布芬是于1970 年研制而出的新型抗血小板药物,其化学本质是苯丁酸衍生物,对心血管疾病的治疗效果越来越受到重视[14-16]。本研究结果显示,两组心血管不良事件发生率和用药前、用药7 d后血小板聚集率、PLT、PCT、MPV、PDW 及两组组间、组内ALT、BUN、Cr 对比,差异均无统计学意义(P>0.05);用药7 d 后,两组血小板聚集率均较用药前降低,差异均有统计学意义(P<0.05);观察组药物不良反应总发生率较对照组低,差异有统计学意义(P<0.05)。说明吲哚布芬联合替格瑞洛治疗NSTE-ACS 可达到与阿司匹林联合替格瑞洛相当的抗血小板聚集效果,且不良反应更少。分析原因,阿司匹林是通过抑制环加氧酶达到抗血栓作用,其对抑制环氧化酶1 的作用是不可逆的,同时会影响胃肠道黏膜前列腺素的合成,增加胃肠道反应及出血事件发生风险[17-18]。而吲哚布芬可多靶点抑制抗血栓形成的过程,其治疗NSTE-ACS 的作用机制在于:一是减少血栓烷A2、血小板聚集;二是影响二磷酸腺苷受体P2Y12-ADP 的释放,抑制血小板的凝聚反应;三是拮抗血小板活化因子途径,减缓血小板的激活。吲哚布芬还具有一定抗凝血作用,主要通过影响凝血酶原时间、凝血酶时间和活化部分凝血活酶时间,延长凝血时间,并影响血小板因子3、4 和凝血因子Ⅱ、Ⅹ,从而发挥抗凝血、抗血小板的双重作用[19]。因此,吲哚布芬对心脑血管疾病的防治效果显著,在治疗血栓性疾病及减轻出血性事件方面安全性更优。此外,该药物对环氧化酶1的作用是可逆的,在NSTE-ACS 患者中给药后可在2 h 起效,24 h 后药效基本消退,环氧化酶1 的活性也可恢复,对胃肠道功能影响较小,可大大降低不良反应发生率[20]。
综上所述,吲哚布芬联合替格瑞洛治疗NSTEACS 能有效抗血小板聚集,不会增加心血管不良事件发生,且药物不良反应发生率更低。

