锰/锆-双金属有机骨架纳米酶比色法检测水中痕量氟
牟芝梅,邓治臣,赵静銮,柳敬鱼,丁芯茹,彭文洪,贺锦灿
(广东药科大学 公共卫生学院,广东 广州 510310)
氟是人体必需的微量元素之一,人体内的氟主要来源于饮水[1]。流行病学研究发现,适量的氟有促进生长发育、预防龋齿等作用[2],但过量摄入则可导致氟斑牙、氟骨症[3],还会影响中枢神经系统、肌肉、心血管系统以及血液系统。因此需对存在于饮用水中的氟含量进行严格限制。采用地表水或地下水为生活饮用水水源时,氟离子(F-)的最大允许浓度为1.0 mg/L[4]。中国是地方性饮用水氟中毒流行最广、危害最严重的国家之一,地方性氟中毒危及我国超过30个省(自治区)。据不完全统计,我国有此病的县总数已超过一千个,受影响群众达上亿人[5]。因此,检测和监管饮用水中氟离子含量,是保障人民饮用水安全的重要前提。
目前F-的检测方法主要有离子选择电极法、离子色谱法、荧光法、气相色谱法等[6-7]。其中,比色法是通过比较或测量有色物质溶液颜色深度来确定待测组分含量的方法。与其他分析方法相比,比色法不需要复杂的仪器,待测物预处理简便、检测成本低、方便快捷、操作简单、不依赖专业人员,符合现场快速检测的要求[8]。
金属有机框架(Metal-organic frameworks,MOF)是一类由金属中心和有机配体组装而成的纳米材料,具有比表面积与孔隙率高及孔隙结构可控的特点[9],在储气、分离、传感器、催化等方面[10-12]具有重要的应用。某些MOF 中含有的顺磁性金属,如铁、铜、钴、锰、锆等,赋予了MOF 类过氧化物酶(纳米酶)活性,与天然酶相比,MOF纳米酶具有性质稳定、易于保存、成本低等优点。MOF纳米酶可催化氧化无色的显色底物(如3,3',5,5'-四甲基联苯胺等)显色,在比色检测应用方面日益受到关注。例如,笔者所在课题组[13]设计了一种能选择性识别磷酸根离子的钴基MOF纳米酶,并将其成功用于食品中磷酸盐的比色检测。Wu 等[14]发现锆-氨基酸MOF 具有类过氧化物酶活性,但锆基MOF 的类过氧化物酶活性较弱,通常需与其他金属如铁[15]、铜[16]、铈[17]等协同以提高其纳米酶活性。锆基MOF除具有类过氧化物酶活性外,还具有选择性吸附氟的能力。Zhao 等[18]发现,相较于MIL-53(Fe,Cr,Al)、MIL-68(Al)、CAU-1、CAU-6,UiO-66(Zr)展现出更强的氟离子吸附能力 ;Zhu 等[19]发现MOF-801(Zr)对水中的氟化物具有较强的选择吸附作用。目前,锆基MOF 大多用于氟化物的吸附研究,在氟的比色定量检测方面鲜见报道。在各种过渡金属中,锰因其低毒性、多用性、多价性而备受关注[20]。有研究者发现,通过掺杂金属锰制备双金属催化剂,可以提高材料的催化活性[21]。因此,以锆盐和锰盐为金属前驱体,有望制备出一种对氟离子同时具有识别功能和比色检测功能的双金属MOF。
基于以上考虑,本研究通过共沉淀法合成了新型Mn/Zr-MOF 材料,同时基于锰离子、锆离子赋予该材料的类过氧化物酶活性及锆离子对F-的选择性识别作用,建立了一种灵敏、快速、高选择性检测F-的比色法,并应用于实际水样中F-的测定。
1 实验部分
1.1 仪器设备
xMark 酶标仪(美国 Bio-Rad 公司);Hitachi S4800 扫描电子显微镜(SEM,日本 Hitachi 公司);EscaLab 250Xi X 射线衍射仪(XRD,美国Thermo Fisher Scientific 公司);Axis Ultra DLD Kratos AXIS SUPRA X 射线光电子能谱仪(XPS,日本岛津公司);Nicolet iS10 傅里叶红外光谱仪(FTIR,美国Thermo Fisher Scientific 公司);Bruker E580 顺磁共振波谱仪(ESR,德国Bruker 公司);UV-3010 紫外-可见分光光度计(日本日立公司);FA 1204 B 电子分析天平(上海佑科仪器仪表有限公司);H3-18K 高速离心机(湖南可成仪器有限公司);DF-101S磁力搅拌器(河南巩义予华仪器有限责任公司);YC-S30恒温水浴锅(天津市泰斯特仪器有限公司);LGJ-10C冷冻干燥机(北京四环科学仪器厂有限公司)。
1.2 试剂与耗材
3,3',5,5'-四甲基联苯胺(TMB)、2,2'-联氮-双-3-乙基苯并噻唑啉-6-磺酸(ABTS)、邻苯二胺(OPD)、均苯三甲酸、氟化钠、氯化锆、无水乙醇均购自阿拉丁试剂有限公司;一水合硫酸锰、醋酸和无水醋酸钠购自广州化学试剂厂;过氧化氢(H2O2)购自江西健宝医药科技有限公司。所有化学试剂至少为分析纯,使用时无需进一步纯化。实验用水为超纯水(>18.2 MΩ•cm)。醋酸-醋酸钠缓冲溶液(HAc-NaAc,pH 4.8)由醋酸和无水醋酸钠按照一定比例配制。
1.3 实验方法
1.3.1 Mn/Zr-MOF的制备与表征 采用一锅共沉淀法制备Mn/Zr-MOF:配制20 mmol/L 均苯三甲酸溶液、系列不同浓度的氯化锆溶液(15、20、30、40、45、50 mmol/L)和一水合硫酸锰溶液(10、15、20、30、40、45 mmol/L)。向500 mL 三颈烧瓶中分别加入100 mL 的20 mmol/L 均苯三甲酸、100 mL 氯化锆溶液、100 mL一水合硫酸锰溶液(控制金属盐溶液总浓度为60 mmol/L,依次调整锆盐/锰盐的加入浓度比为1∶1、1∶2、1∶3、3∶1、2∶1、5∶1)。将混合溶液于25 ℃下磁力搅拌反应1 h,待溶液颜色由澄清转变成乳白色,将所获得的乳白色浊液于8 000 r/min 离心10 min,弃上清液,用超纯水洗涤两次,冷冻干燥12 h,得到6种不同锰、锆掺杂比的白色Mn/Zr-MOF材料。
通过 SEM、XPS、FTIR、XRD 等技术对Mn/Zr-MOF的形貌、元素、官能团、晶体结构进行表征。
1.3.2 分析方法将1 mL pH 4.8的HAc-NaAc缓冲溶液、1 mL 1.3 mg/L的Mn/Zr-MOF材料、一系列浓度梯度的氟化钠标准溶液、0.8 mL 2.0 mmol/L的TMB溶液和0.04 mL 0.997 mol/L的H2O2溶液依次加入5 mL 比色管中,使用HAc-NaAc 缓冲溶液定容至刻度,30 ℃孵育15 min。用紫外-可见分光光度计采集体系的吸收光谱图,并记录652 nm处的吸光度值。以不加Mn/Zr-MOF材料的体系作为对照组,实验组和对照组均平行测定3次,其吸光度平均值分别作为A和A0,计算二者差值ΔA(A0-A)。
1.3.3 样品处理取广州市龙潭涌河流水和当地超市所购买的纯净水各15 mL,经0.22 μm 微孔滤膜过滤及阳离子交换树脂后按照“1.3.2”进行分析。
1.4 数据处理
采用Origin 2022进行数据处理与分析。
2 结果与讨论
2.1 分析原理
方法的分析原理如图1 所示,Mn/Zr-MOF 具有类过氧化物酶活性,能够促进H2O2的降解反应并产生高活性的羟基自由基(•OH),这些具有强氧化性的•OH 能进一步氧化TMB 生成oxTMB,使体系呈蓝绿色。当反应体系中存在F-时,Mn/Zr-MOF 与F-特异性结合,占据了Mn/Zr-MOF 部分活性位点,使得Mn/Zr-MOF 的催化活性受到抑制,体系产生的•OH 较少,颜色变浅。颜色的深浅与F-的浓度相关,基于此原理可建立检测氟的Mn/Zr-MOF 纳米酶比色分析方法。
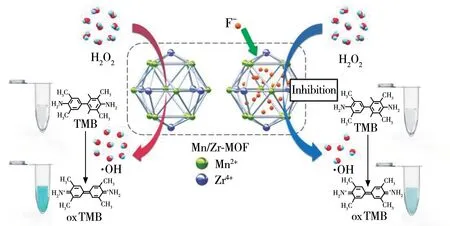
图1 锰/锆-双金属有机骨架纳米酶比色法检测氟的原理示意图Fig.1 Schematic diagram for the principle of colorimetric detection of fluoride based on Mn/Zr-MOF nanoenzyme
2.2 Mn/Zr-MOF的制备与表征
通过一锅共沉淀法制备了6 种不同锆盐/锰盐掺杂浓度比(1∶1、1∶2、1∶3、3∶1、2∶1、5∶1)的Mn/Zr-MOF 材料,比较这些材料催化过氧化氢氧化TMB 的效果,结果如图2 所示。结果显示,锆盐和锰盐掺杂比为3∶1 的Mn/Zr-MOF 材料催化活性最强,因此采用锆盐/锰盐掺杂浓度比为3∶1合成的Mn/Zr-MOF 材料进行后续表征和分析应用。

图2 不同锆盐/锰盐掺杂比合成的Mn/Zr-MOF材料用于催化H2O2-TMB反应所获得的652 nm处的吸光度Fig.2 The absorbance at 652 nm obtained from the system of H2O2-TMB catalyzed by Mn/Zr-MOF with different doping ratios of zirconium/manganese salts
SEM 图(图3A)显示Mn/Zr-MOF 为不规则的块状结构。用XPS 验证Mn/Zr-MOF 的组成,结果如图3B 所示。Mn/Zr-MOF 中存在 Zr 3d、C 1s、N 1s、O 1s、Mn 2p 的峰,插图显示,材料中同时存在 Mn2+、Mn3+。通过FITR 分析材料的官能团(图3C),3 472、1 652 、1 367、471 cm-1处分别归属于—OH、C=O、C—O—C、Ar—H 的伸缩振动;660 cm-1处的峰可归属为Zr—O、Mn—O 的伸缩振动[22]。采用XRD 表征Mn/Zr-MOF 的晶型结构(图3D),发现Mn/Zr-MOF 的结晶度较差,在40.46°、45.1°和51.4°处的衍射峰分别与模拟Mn-MOF 的(200)、(202)和(108)晶面对应;在8.3°和8.6°处的衍射峰分别与模拟MOF-808(Zr)的(311)和(222)晶面一致。上述结果表明,Mn-Zr/MOF成功合成。

图3 Mn/Zr-MOF的SEM图(A),XPS图(B),FTIR图(C)以及Mn/Zr-MOF的XRD谱图与Mn-MOF、MOF-808(Zr)的XRD模拟谱图(D)Fig.3 SEM image(A),XPS curve(B),FTIR spectrum(C) of Mn/Zr-MOF,and XRD spectrum of Mn/Zr-MOF,and simulation spectra of Mn-MOF and MOF-808(Zr)(D)
2.3 反应条件优化
酶的活性受pH 值和温度的影响最大,因此考察了pH 值(3.5、4.0、4.5、4.8、5.0、5.3)和温度(20、30、40、50、60、70 ℃)对吸光度的影响。结果显示,随着pH 值的升高,Mn/Zr-MOF 的催化活性先升高后降低,在pH 4.8时催化活性达到最高;而随着反应温度的升高,Mn/Zr-MOF 的催化活性先增加后降低,在30 ℃时达到峰值,过高或过低的温度均会影响Mn/Zr-MOF活性进而影响催化活性。此外,为了发挥反应体系的最大检测效能,本研究还对MOF 材料浓度、TMB 浓度、过氧化氢浓度、孵育时间进行了优化。
最终确定的最优反应条件为:1 mL 1.3 mg/L的MOF 材料、0.8 mL 2.0 mmol/L 的TMB、0.04 mL 0.997 mol/L 的过氧化氢、pH 4.8、温度30 ℃、反应时间15 min。
2.4 Mn/Zr-MOF的类过氧化物酶活性研究
以TMB、ABTS、OPD 为底物,研究Mn/Zr-MOF 的类过氧化物酶活性。如图4 所示,TMB、ABTS、OPD 溶液均无明显特征吸收峰,而在含有TMB和H2O2的NaAc-HAc缓冲溶液中加Mn/Zr-MOF,溶液由无色变成蓝色,且TMB-H2O2-Mn/Zr-MOF 体系在652 nm 处有较强的吸收峰。此外,Mn/Zr-MOF 也能催化ABTS 和OPD 显色。该结果说明Mn/Zr-MOF具有类过氧化物酶活性。
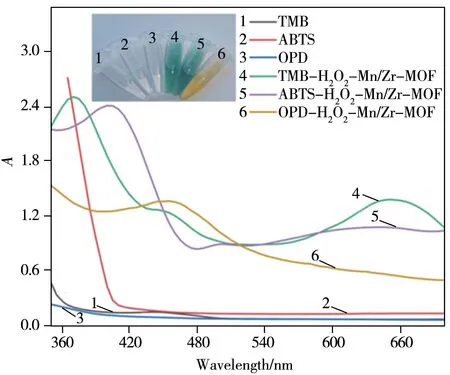
图4 3种底物(TMB、ABTS、OPD)被Mn/Zr-MOF催化氧化前后的吸收光谱图Fig.4 The absorption spectra of three substrates(TMB,ABTS,OPD) before and after catalytic oxidation by Mn/Zr-MOF insert:the chart of color change
以TMB和H2O2为底物,进一步研究Mn/Zr-MOF的类过氧化物酶活性,进行稳态动力学评价:在反应体系最适的pH 值和温度下,改变其中一种底物浓度,在652 nm 波长下进行40 min稳态动力学扫描,得到典型的Michaelis-Menten 曲线(图5),根据Michaelis 方程计算出米氏常数(Km)和最大反应速度(Vmax)。Mn/Zr-MOF以TMB和H2O2为底物的Km分别为0.75、4.23 mmol/L,Vmax分别为186.92×10-8、85×10-8mol/(L•s);在相同的实验条件下,测得辣根过氧化物酶(HRP)以TMB 和H2O2为底物的Km分别为0.74、0.65 mmol/L,Vmax分别为10.60×10-8、3.40×10-8mol/(L•s)。Mn/Zr-MOF 以H2O2为底物的Km值大约是HRP的6倍,说明Mn/Zr-MOF需要较高的H2O2浓度才能获得最大活性。以TMB为底物时,Mn/Zr-MOF 具有与HRP 相当的TMB 亲和力。此外,Mn/Zr-MOF 的Vmax大于HRP。Mn/Zr-MOF 以TMB 为底物的Km值稍低于MoS2@MgFe2O4[23]和Fe-Ag2S[24],Vmax是MoS2@MgFe2O4的2倍,Fe-Ag2S的12倍。上述数据表明,与其他纳米酶相比,Mn/Zr-MOF的反应速率较快,表现出较好的催化活性。
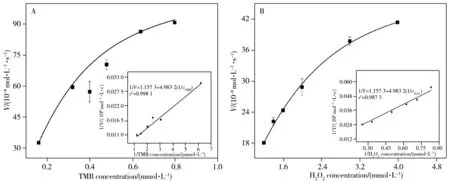
图5 底物TMB浓度(A)和H2O2 浓度(B)对Mn/Zr-MOF催化反应速率的影响Fig.5 Effect of TMB concentrations(A) and H2O2 concentrations(B) on the rate of catalytic reaction of Mn/Zr-MOF insert:double reciprocal plot
2.5 氟离子对Mn/Zr-MOF类过氧化物酶活性的影响
通过比较Mn/Zr-MOF 在F-存在/不存在以及不同存在浓度时反应体系光谱的变化,考察F-对Mn/Zr-MOF 类过氧化物酶活性的影响。如图6A 所示,TMB 溶液无特征吸收峰;TMB-H2O2-Mn/Zr-MOF 体系在652 nm 处有较强吸收峰,说明Mn/Zr-MOF 具有类过氧化物酶活性;当加入F-后,反应体系的吸光度明显降低;随着F-质量浓度的增加,反应体系的吸光度逐渐降低,说明F-抑制了Mn/Zr-MOF的类过氧化物酶活性。以5,5-二甲基-1-吡咯啉-N-氧化物(DMPO)为•OH 的捕获剂,通过ESR 表征考察F-对Mn/Zr-MOF 催化活性的影响(图6B)。当体系中不存在F-时,可以观察到显著的•OH 特征信号,表明Mn/Zr-MOF 能够催化H2O2,并产生高活性的•OH;当体系中存在F-时,ESR 峰值显著降低,说明生成的•OH减少。这一结果证明F-的吸附引起•OH的生成量减少,导致Mn/Zr-MOF的类过氧化物酶活性降低。通过对比加入F-前后O 1s(图6C)和Zr 3d(图6D)的XPS 图,发现F-存在时,Zr-OH 峰面积所占的百分比降低,Zr 3d 向较低结合能区域轻微移动。表明F-吸附在Mn/Zr-MOF 上时,与Zr-OH 发生离子交换,说明Zr与F-存在特异性识别作用。
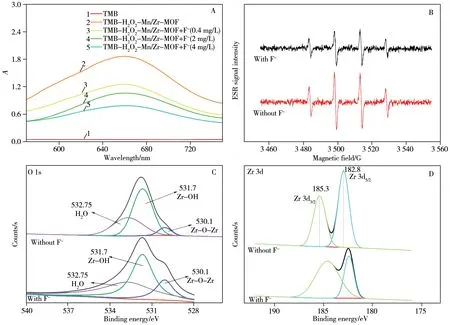
图6 不同体系的吸收光谱图(A),F- 加入Mn/Zr-MOF催化体系前后的ESR图谱(B)及Mn/Zr-MOF的O 1s(C)、Zr 3d(D)XPS光谱图Fig.6 The absorption spectra of different systems(A),the ESR curves of Mn/Zr-MOF-involved catalytic system before and after the addition of fluoride ions(B),the XPS spectra of O 1s(C) and Zr 3d(D) of Mn/Zr-MOF
2.6 方法建立
在上述优化的催化反应条件下进行实验,发现随着F-浓度的增大体系的颜色逐渐变浅,652 nm 处的吸光度逐渐降低,以F-质量浓度(ρ)为横坐标,ΔA为纵坐标进行线性拟合。结果显示,在0.40~5.0 mg/L范围内,F-质量浓度与ΔA线性相关,线性方程为ΔA=0.065 12ρ+0.751 17,相关系数(r)为0.999 6,以信噪比(S/N)为3计算得到检出限(LOD)为0.16 mg/L,低于国标饮用水中F-的准则值(1.0 mg/L)。与NH2-UiO-66 荧光法[25]、镍-吡咯苯并咪唑络合物比色法[26]和季胺型荧光探针法[27]相比(表1),本方法的检出限更低;尽管Ni-POCOP 探针比色法[28]比本方法的检出限更具优势,但Ni-POCOP 探针合成需要8 h,且使用有毒有机溶剂乙腈,而本方法中Mn/Zr-MOF 材料的合成只需1 h,溶剂为水,避免了有毒有害有机溶剂的使用。

表1 不同F- 检测方法的比较Table 1 Comparison of different methods for detection of F-
2.7 选择性分析
考察了18种水样中可能存在的阴、阳离子对体系检测2.0 mg/L F-的影响,结果如表2所示。大多数无机阴离子、无机阳离子对F-检测的影响较小,相对误差小于±7.0%。部分金属离子(如Tb3+、Ag+)的耐受倍数低,说明可能存在一定的干扰,可在样品检测前通过阳离子交换树脂去除。总体来说,该方法对F-具有较好的选择性。

表2 不同共存离子对检测体系的影响(n= 3)Table 2 The effect of different coexisting ions on detection system(n=3)
2.8 实际样品分析
将所建立的方法应用于河流水、纯净水实际样品中F-的测定,结果在河流水中检出0.86 mg/L 的F-,纯净水中未检出。将本方法与国家标准方法(氟离子选择电极法)[29]进行比对,T检验显示两种方法的检测结果无显著性差异(P> 0.05)。对样品进行3 个水平的加标回收实验,得到加标回收率为97.6%~106%,相对标准偏差(RSD)为0.27%~5.2%(n=3),见表3。上述结果说明本方法具有较好的准确性及精密度,满足实际水样中氟的检测要求。
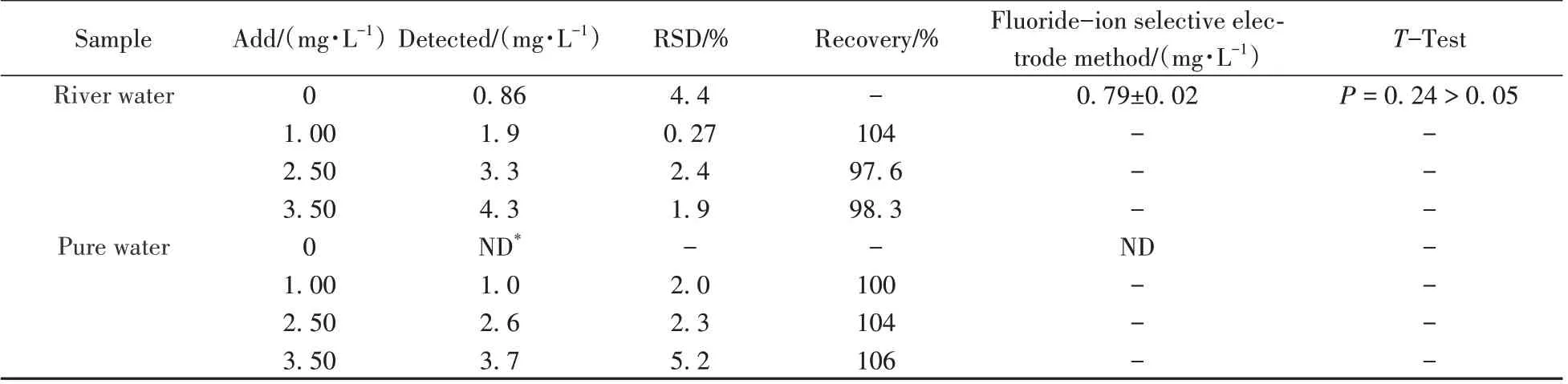
表3 实际水样中氟离子的测定(n=3)Table 3 Determination of fluoride ions in different water samples(n=3)
3 结 论
本文设计合成了一种新型Mn/Zr-MOF 纳米材料,并基于其类过氧化物酶活性及对F-的选择性识别作用,建立了一种检测F-的催化比色法。方法的线性范围为0.40~5.0 mg/L,检出限为0.16 mg/L。将该方法应用于实际水样中F-测定,加标回收率为97.6%~106%,RSD 为0.27%~5.2%,检测结果与国标法一致。本方法检测速度较快、特异性好、灵敏度高,在实际样品检测中有较好的适用性,有望进一步制成试剂盒、试纸条,与手机拍照识色功能结合进行定量分析,以更好地满足现场检测需求。此外,还可通过Mn/Zr-MOF 上金属离子的变更及官能团的修饰,实现不同待测物的特异性结合,开发其他分析物的比色检测方法或进一步拓展不同的检测模式。

