高耐蚀GO/PANI涂层的防腐蚀性能及机理
李 波,杨慧斌,何锦航,余思伍,肖仁贵,文 崎,程金科,彭盛燕,杨大宁
(1.贵州电网有限责任公司电力科学研究院, 贵阳 550002;2.贵州大学化学与化工学院, 贵阳 550025;3.海南电网有限责任公司电力科学研究院, 三亚 571159)
金属腐蚀是由金属界面的化学或电化学多相反应引起的,能够显著降低金属材料的力学性能和电气特性,这会对自然经济和产业结构造成严重威胁[1]。由于防腐蚀涂料具有操作简便的优势,金属防腐蚀普遍采用保护涂层[2]。
近年来,随着氧化石墨烯(GO)研究的深入,人们发现GO优异的物理结构能够充当一定的屏障作用,为提高GO的防腐蚀性能,通常将GO与一些导电聚合物复合,充分利用GO的片层状结构以及导电聚合物出色的电性能,提高其对金属的防护能力,但GO的制备过程存在差异,这最终会导致涂层的防护性能存在差异,甚至水性涂料在溶剂挥发后剩余的微孔不利于腐蚀保护。在与涂料物理混合的过程中,由于石墨烯表面缺乏活性基团,无法与涂层中的活性基团作用,容易出现团聚,因此各种氧化石墨烯(GO)的制备方法相继出现[3-4]。大多数研究人员在环氧树脂中加入GO或部分还原氧化石墨烯(RGO)[5],结果表明,掺杂氧化石墨烯后,环氧涂层对碳钢的保护效果得到改善。ZHU等[6]在N80钢基板上制备了含不同量还原氧化石墨烯(RGO)纳米片的增强环氧复合涂层,结果表明,加入适量还原氧化石墨烯纳米片,有效减少了环氧复合涂层中孔隙的数量和尺寸,提高了环氧复合涂层的附着力、韧性和耐蚀性,体现了较好的防腐蚀性能。
聚苯胺(PANI)由于造价低廉,制备简单,自十九世纪被发现以来,就被作为导电聚合物的宠儿进入研究者们的视线。自MacDiarmid在二十世纪八十年代提出了对钢和其他金属进行阳极保护的可能性[7],PANI在金属防腐蚀方面的研究受到人们的热烈关注。LU等[7]研究了PANI包覆的碳钢试样在人工盐水和稀盐酸环境中的腐蚀性能,研究发现,这种腐蚀保护是以电化学为动力驱动,由阳极和阴极极化产生的,这种保护能够延伸到裸钢区域。ZHANG等[8]合成了不同形式的PANI,并将其加入到环氧涂料中,结果表明,不同的PANI涂层均可以提高低碳钢的耐蚀性。HU等[9]分别研究了盐酸、对甲苯磺酸和十二烷基苯磺酸掺杂聚苯胺(PAND)/环氧树脂(EP)复合涂层在碳钢上的耐蚀性,结果表明,聚苯胺的引入可以提高环氧树脂的耐腐蚀性能。当PANI电偶联到钢上时,在PANI包覆层下的钝化氧化铁(γ Fe2O3和F3O4),能够延伸至裸露的区域2~6 mm,显而易见,它的保护区域是有限的。并且由于PANI的溶解性较差,仅能在有限的有机溶剂中溶解,且涂层与钢基体的附着力相当差。TAHERI等[10]采用电化学方法研究了锌掺杂聚苯胺对低碳钢环氧涂层保护性能的影响,结果显示,GO的高比表面积使其在抵御水和腐蚀性离子渗透到环氧涂层时具有显著的屏障作用,但氧化石墨烯的高比表面积导致了团聚。XIAO等[11]在水性富锌涂料中添加PANI/GO,利用PANI的导电性增强了富锌涂料的阴极保护作用。RAMEZANZADEH等[12]通过苯胺的原位聚合在GO表面合成了高度结晶且导电的聚苯胺纳米纤维,提高了富锌涂层的力学性能和黏合性能,改善了锌颗粒与钢基材的电接触,延长了使用寿命。
翡翠盐形式聚苯胺(ES)能够通过氧化还原反应改变腐蚀产物层的化学结构,然而因具有难溶性,ES在油性树脂或者水性树脂中的分散都较为困难,GO因其大表面能造成纳米材料的团聚,对涂层的保护作用存在消极影响,需要其他活性基团降低其表面能。因此,GO/PANI复合材料在金属防腐蚀上具有较好的应用前景[13]。
笔者利用通过Hummer法制备得到GO,以过硫酸铵为氧化剂,苯胺单体在掺杂不同质子酸条件下,通过溶液法聚合苯胺,以聚乙二醇水性化后环氧树脂为基体,制备GO/PANI环氧树脂复合涂料,用电化学方法研究了GO/PANI/WEP涂层的防腐蚀性能和机理,以期提高涂层的防腐蚀效率、减少金属腐蚀造成的损失。
1 试验
1.1 试样制备
1.1.1 Hummer法制备氧化石墨烯
将1 g鳞片石墨置于25 mL浓H2SO4中,且在恒低温条件下分散均匀,搅拌30 min后,将3 g高锰酸钾缓慢加入其中,氧化阶段的低温插层反应开始。此阶段主要是石墨层上环氧基的形成,在冰浴条件下反应一段时间(12 h,24 h)后,将反应温度升高至35 ℃,继续反应6 h。此阶段主要是环氧键断裂形成羟基或羧基的过程。待第二段反应完成后,在体系中缓慢加入去离子水,稀释氧化环境的酸度,然后再加入30%(质量分数,下同)H2O2溶液,待不产生密集的小气泡后,将其倒入预先配制的5%(质量分数,下同)稀盐酸溶液中,静置一晚,倒去上清液,并用去离子水洗涤至溶液为弱酸性,放入超声清洗机内1 h后,离心收获上清液,即可得到氧化石墨烯(GO)分散液。
1.1.2 水溶性环氧树脂乳液的制备
乳液制备过程如下:将E-44型环氧树脂放入50 ℃水浴锅中加热,待其流动性达到玻璃棒伸进树脂拿出后树脂能成股流动即可。将环氧树脂与聚乙二醇按1…4(质量比)加入配备有搅拌器和温度计的三口烧瓶中,质量即为m1,升温至100 ℃,待聚乙二醇固体完全溶解后,加入过硫酸铵,质量为8‰m1,继续升温至180 ℃,反应持续3.5 h,即可得到自制乳化环氧树脂的乳液。
乳化过程如下 :取10 g自制乳液备用,加入30 g环氧树脂,在50 ℃水浴锅中加热并持续搅拌30 min,加入26.7 g去离子水,制得固体含量约为60%(质量分数)的水溶性环氧树脂乳液(WEP)。
1.1.3 GO/PANI复合材料的制备
在苯胺氧化聚合的过程中加入制备好的GO,以实现两种物质的复合。苯胺单体在质子酸如盐酸、硫酸、磷酸的条件下,以过硫酸铵为氧化剂,在苯胺氧化过程中添加不同量GO,以此得到GO/PANI复合材料。
1.1.4 GO/PANI/WEP涂层的制备
称取一定量GO/PANI粉末,将其分散在10 g NMP(N-甲基吡咯烷酮)中,将复合物GO/PANI分散液超声30 min使其分散均匀,将不同量的GO/PANI分散液与环氧树脂(WEP)乳液共混,搅拌混合均匀后,得到分散均匀的GO/PANI质量分数分别为0,0.2%,0.4%.0.6%,0.8%,1%,2%.3%,4%,5%的GO/PANI/WEP复合乳液,将其加入到T31固化剂中,随后涂覆在金属表面。
选用不锈钢为金属基材,在涂覆乳液前对其进行预处理,先用砂纸将表面的氧化层打磨去除,并将其置于乙醇溶液中超声30 min进行脱脂处理。将处理好的钢板装进密封袋内保存。将配制好的复合乳液均匀涂覆在处理过的金属钢板上,用绝缘胶带封闭背面后,待用。
1.2 涂层的性能表征
1.2.1 胶膜耐水性测试
将配制好的复合乳液涂覆在保鲜膜上,制备成有一定厚度的胶膜,待胶膜干燥后,对其进行耐水性测试。记录干燥后胶膜质量为m1,将胶膜浸泡在去离子水中24 h后,除去表面水渍,记录质量为m2,利用公式(1)评价胶膜的耐水性。
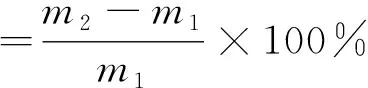
(1)
1.2.2 电化学性能测试
涂层试样的电化学性能评价采用CHI750C电化学工作站完成。试验采用标准三电极体系,其中铂电极和饱和甘汞电极(SCE)分别作为辅助电极和参比电极,试样为工作电极。在0.01~105 Hz的频率范围以及10 mV的电压振幅下对涂层试样进行电化学阻抗测试;采用5 mV/s扫描速率进行极化曲线测试,扫描范围为开路电位±0.3 V,通过ZSimDemo软件对电化学试验结果进行拟合。
涂层试样的腐蚀速率(V失)按式(2)计算
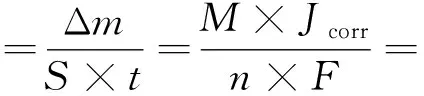
(2)
式中:Δm=MIT/nF,M为析出涂层的质量,I为电流强度,T为通电时间,F为法拉第恒量,n为化合价总数的绝对值;Jcorr为腐蚀电流密度。
在Tafel曲线中,腐蚀电位预示着腐蚀行为发生的倾向,腐蚀电位越大,电流密度越小,预示着腐蚀速率越低,材料发生腐蚀而产生破坏的程度越小。
用Tafel曲线斜率外推法研究腐蚀速率,试样的防腐蚀效率(PEF)可用式(3)表示。
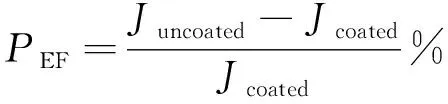
(3)
式中:Juncoated和Jcoated分别为原始试样和不同条件下所得涂层试样的腐蚀电流密度。
2 结果与讨论
2.1 胶膜的耐水性
由图1可见:胶膜的吸水率随GO/PANI含量的增加先降低后趋于稳定,当GO/PANI的含量(质量分数,下同)小于1%时,胶膜吸水率逐步降低,最低接近8%。说明该胶膜在GO/PANI含量低于1%时,随着GO/PANI量的增加,较好地填充了树脂的空隙,胶膜变得致密,水分子较难进入到胶膜内部。而后期吸水率趋于稳定,可能是因为胶膜中有少量毛细管,少量水通过毛细管现象透过GO/PANI胶膜进入树脂,即使GO/PANI含量增加,也难以阻碍水分的进入,吸水性趋于稳定。
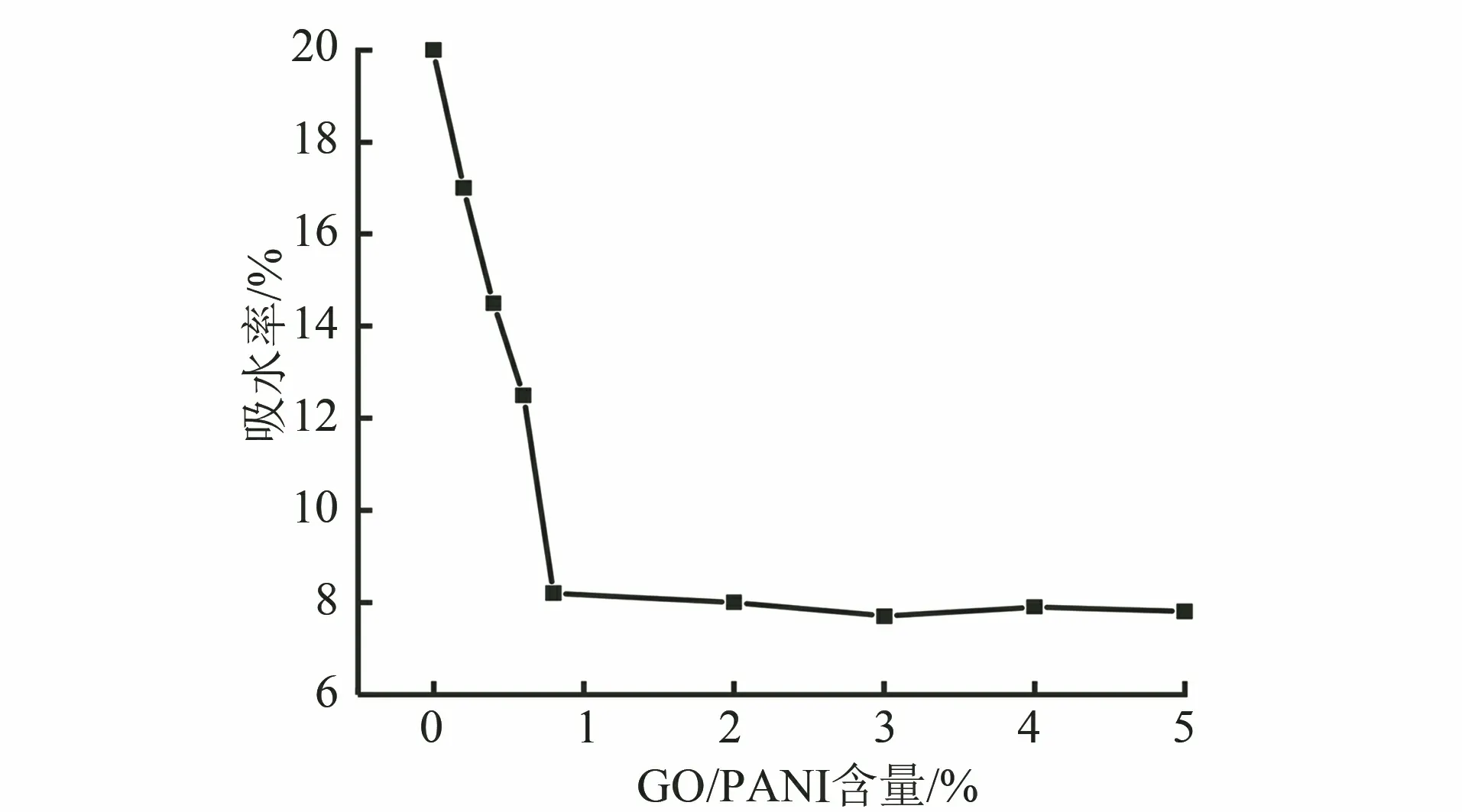
图1 含不同量GO/PANI胶膜的吸水率Fig.1 Water absorption of films containing different content of GO/PANI
2.2 含不同量GO/PANI涂层的防腐蚀性能
由图2和表1可见:与未加GO/PANI的纯水性环氧树脂(WEP)相比,随着涂层中GO/PANI量的不断增加,涂层的腐蚀电位出现先升高后降低的趋势,当GO/PANI质量分数为1%时,腐蚀电位最高。而腐蚀电流密度的变化趋势则随着GO/PANI含量的增加先降低后升高,在GO/PANI质量分数为1%时出现拐点,此时涂层的腐蚀电流密度最低,即此条件下不锈钢板的耐蚀性最好。综合拟合数据可得,当涂层中GO/PANI质量分数为1%时,涂层的防腐蚀效率最高。与未加GO/PANI的纯水性环氧树脂(WEP)相比,含1%GO/PANI涂层的腐蚀电流密度减少了2个数量级,另外,当GO/PANI质量分数为2%时,涂层的极化电阻[计算公式见式(4)]达到最大,为5.06×104Ω·cm2,防腐蚀效率为96.87%。综合来看,含1% GO/PANI涂层的防腐蚀效果最好。
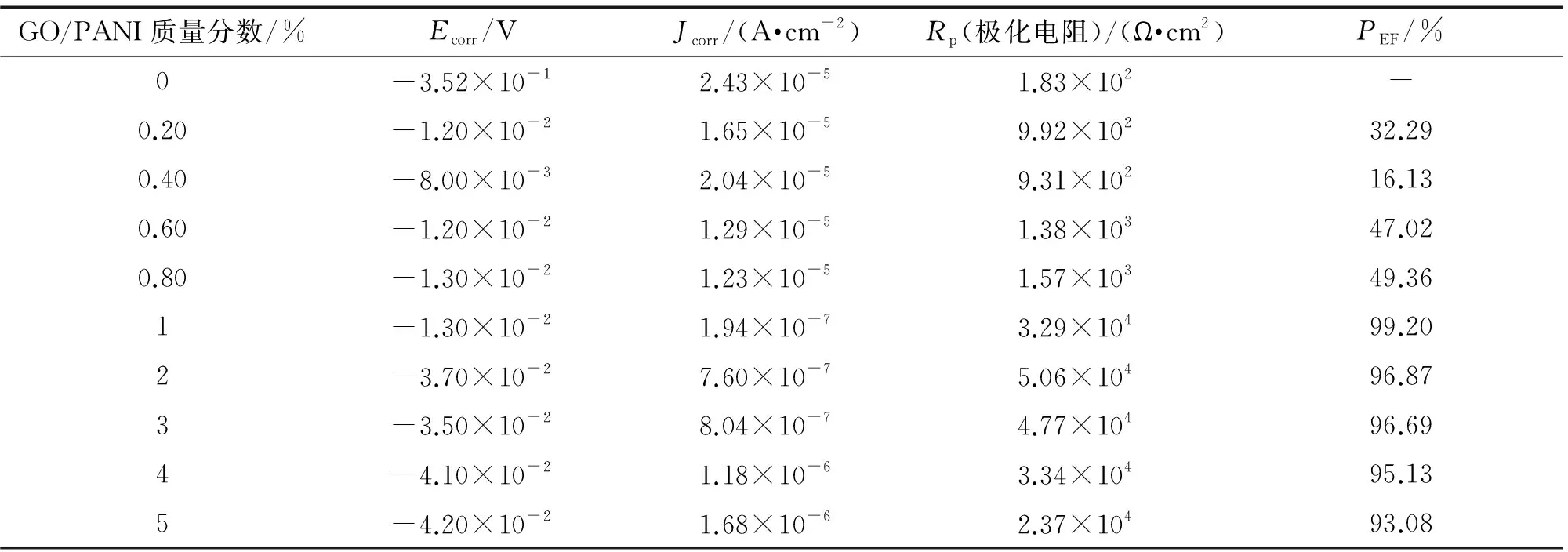
表1 含不同量GO/PANI涂层试样的Tafel结果
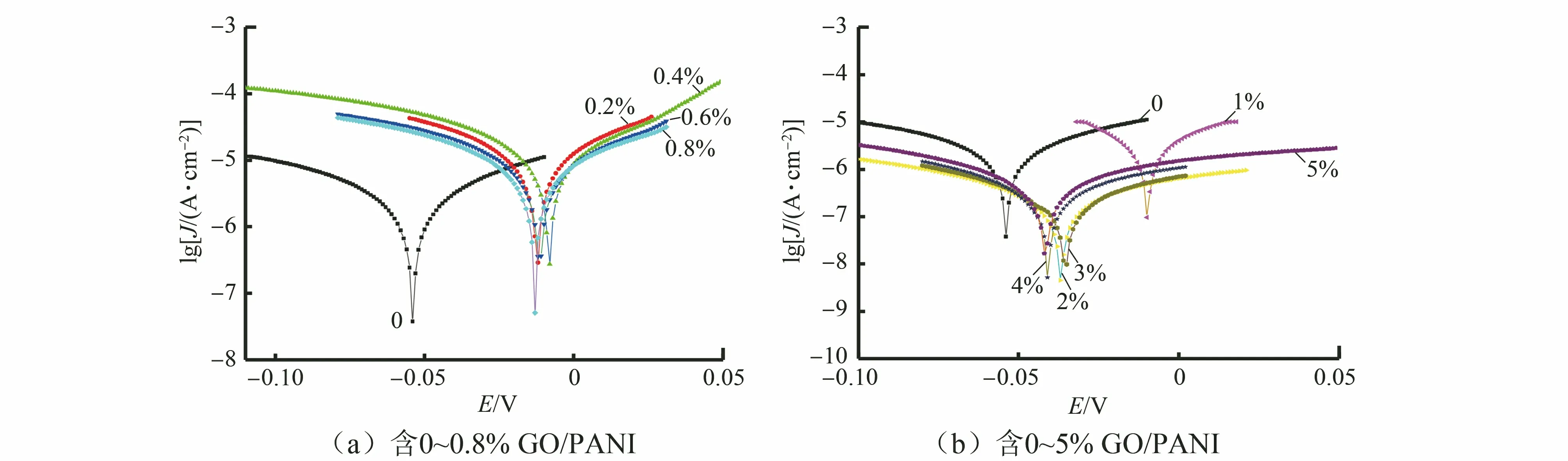
图2 含不同量 GO/PANI的涂层试样在3.5% NaCl溶液中的极化曲线Fig.2 Polarization curves of coated samples with different content of GO/PANI in 3.5% NaCl solution
(4)
式中:α,β为传递系数,ba,bc分别为Tafel曲线两侧的阳极和阴极斜率,计算公式见式(5)和(6)。
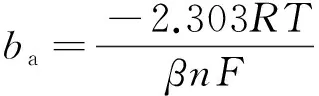
(5)
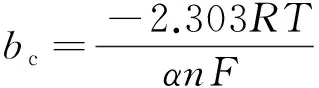
(6)
腐蚀电流密度的降低可能与中性氯化钠溶液中发生吸氧腐蚀有关。随着涂层中GO/PANI的质量分数从0增至1%,涂层的填料(GO/PANI)逐渐填补了乳液胶膜的空隙,对金属的腐蚀保护作用逐渐增强,当GO/PANI的质量分数从1%增至5%时,其腐蚀防护作用逐渐下降,这可能是随着填料含量的增加,其在涂层中的分散性较含量为1%时的有所减弱。即在最佳掺比1%条件下,涂层具有较好的表面覆盖度、较高的防腐蚀效率和较低的腐蚀电流密度。
由图3(a)可见,所有涂层试样Nyquist图展现出的容抗弧均为不规则半圆,甚至只有半弧趋势;当GO/PANI质量分数低于1%时,随着涂层中GO/PANI 量的增加,容抗弧半径逐渐增加,当GO/PANI 加入量大于1%,容抗弧的半径反而随GO/PANI 量的增加逐渐变小。与纯WEP涂层相比,GO/PANI/WEP涂层的容抗弧半径增大与填料加入量有关,即加入填料确实对金属基体有一定的保护作用,且容抗弧半径在GO/PANI 质量分数为1%时最大,容抗弧的大小一般表示系统中电阻或电容对该交流电所起的阻碍作用的强弱,一般来说,容抗弧越大,试样的防腐蚀性能越好。
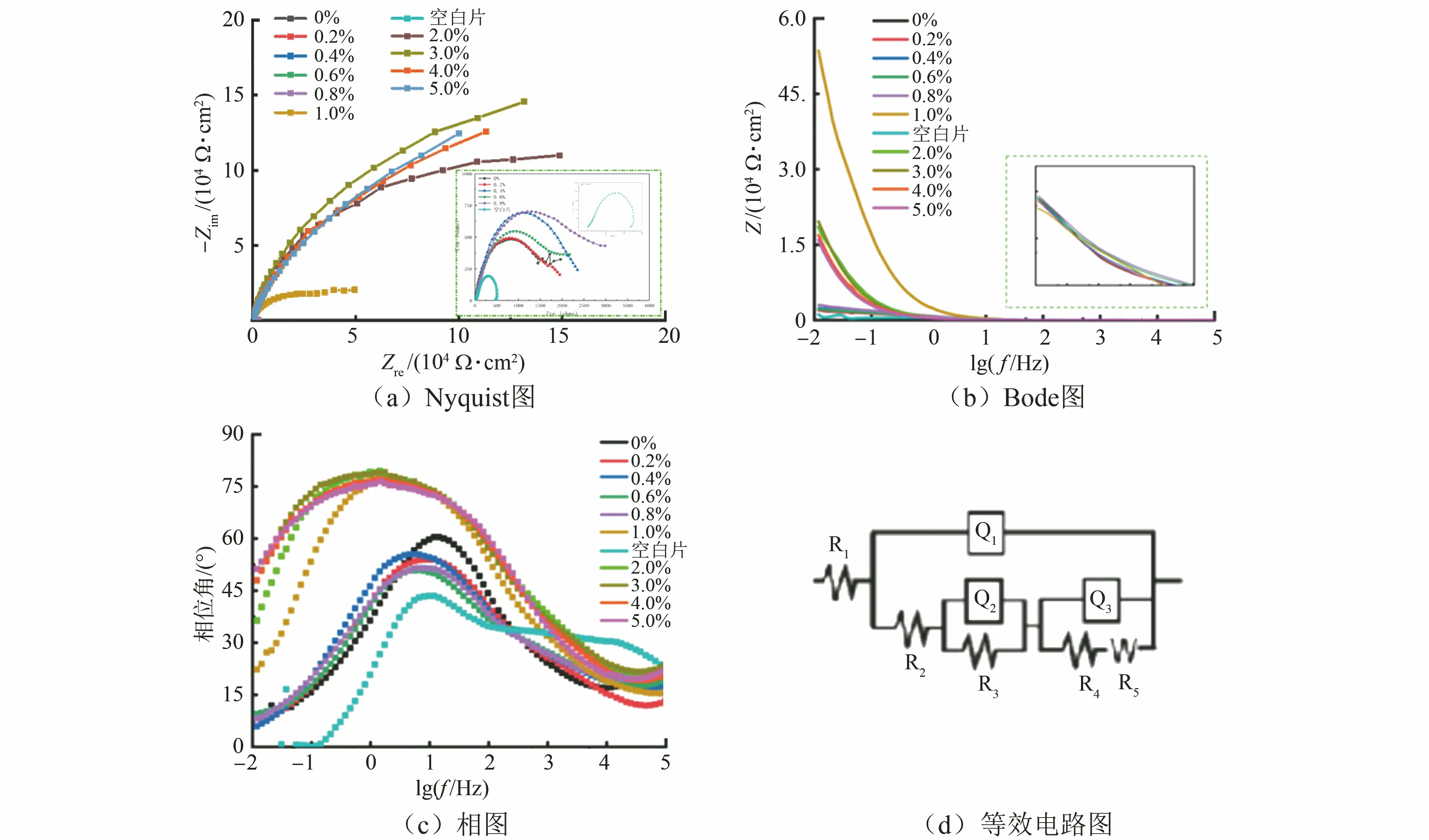
图3 含不同量GO/PANI的涂层试样在3.5% NaCl溶液中的电化学阻抗谱及其等效电路图Fig.3 EIS (a~c) and equivalent circuit diagram (d) of coated samples with different amounts of GO/PANI in 3.5% NaCl solution
由图3(b)可见:在低频条件下,涂层试样的|Z|值在GO/PANI 质量分数小于1%时较为接近。当GO/PANI 质量分数为1%时,|Z|值约为5.0×104Ω·cm2,而当GO/PANI 质量分数超过1%时,|Z|又出现下滑的趋势。由图3(c)可见:涂层试样的相位角在GO/PANI 质量分数大于等于1%时,在很宽频率范围内接近-75°,说明此条件下涂层可以较好地阻碍电解质溶液渗入金属基体表面;而当GO/PANI 质量分数小于1%时,其Bode相位角在中频时即达到该响应的相位角极值。由图3还可见:在该阻抗系统中,双电层电容对金属的腐蚀阻碍有很大影响。
与纯WEP涂层相比,GO/PANI质量分数为1%的涂层的|Z|值增加了近50倍,这是由于GO/PANI填料在WEP中得到了充分分散,有效改善了水性环氧树脂的缺陷,有效阻止了腐蚀介质的渗透,因此,该条件下涂层的防腐蚀性能最好。但是,随着GO/PANI填料含量的增多,填料在WEP中发生堆积,甚至能够为腐蚀介质给予通路扩散,涂层的防腐蚀能力反而减弱。
此外,容抗弧不是完整的半圆可能与电极结构相关,当扩散占主导,或者电容过小时,就得不到完整的半圆。经软件ZSimDemo拟合后,得到图3(d)中的等效电路,其中,R1为电极欧姆电阻,Q1为两电极间的溶液电容,R2为涂层电阻,Q2为工作电极的涂层电容,R3为溶液电阻,Q3为工作电极的双电层电容,R4为电荷传递电阻,R5为韦伯电阻,表示微孔的界面阻抗[14]。值得注意,恒相位角元件Q(CPE)的阻抗描述见式(7)。
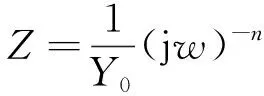
(7)
由于Q是代表双电层偏离纯电容的等效元件,因此其中一个参数Y0常取正值,另一个参数n为无量纲的指数,常被称为偏离理想状态的“弥散指数”,取值范围为0~1,n值越小,弥散效应越大,当n接近1时,它更接近于理想状态,该状态下的Q元件可看做电容元件C[15]。图3(d)中的等效电路说明,在对金属涂层进行电化学阻抗测试时,电解质由涂层表面的微孔不均匀渗入涂层甚至到达金属基体,且其界面的腐蚀电池分布不均匀[16]。而韦伯阻抗的出现表明涂层中填料分子对腐蚀介质的传质扩散有一定阻碍作用,当涂层表面的微孔逐渐成长为宏观孔时,该扩散层由涂层内转变为电极附近。
2.3 质子酸种类对GO/PANI涂层防腐蚀性能的影响
2.3.1 极化曲线
由图4可见:不同质子酸条件下制备的涂层都不同程度提高了基体金属的自腐蚀电位,其中,硫酸条件下制得GO/PANI涂层的自腐蚀电位较高,腐蚀电流密度也远低于其他两种酸条件下涂层的,为8.597×10-7A/cm2。
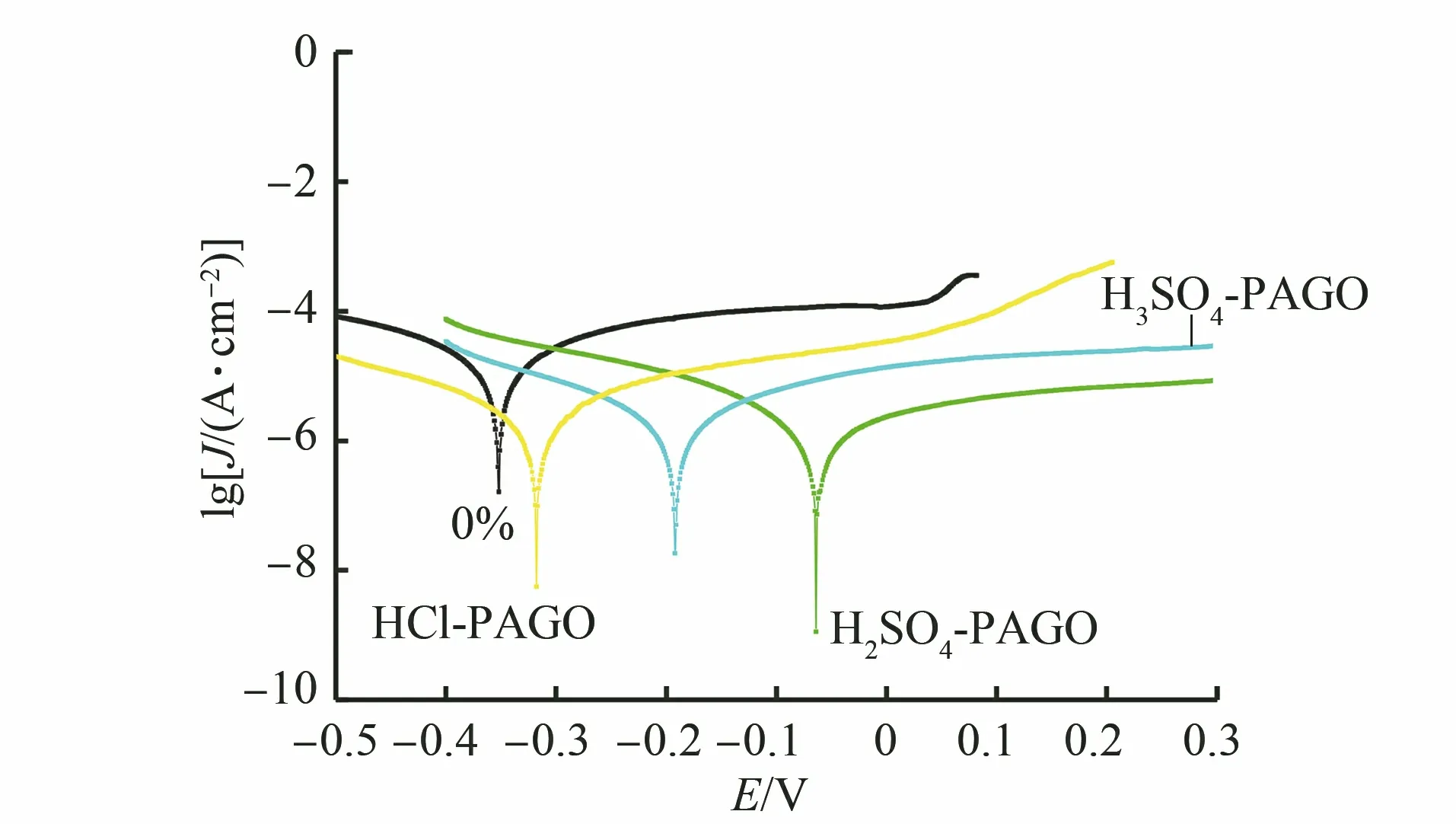
图4 不同质子酸条件下所得含1%GO/PANI涂层试样在3.5% NaCl溶液中的极化曲线Fig.4 Polarization curves of coating samples containing 1% GO/PANI under different proton acid conditions in 3.5% NaCl solution
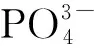

表2 极化曲线拟合结果
2.3.2 电化学阻抗谱
由图5可见:在3.5% NaCl溶液中,H2SO4-PAGO涂层试样的容抗弧半径较大,说明在本试验条件下,H2SO4-PAGO涂层对金属起到的防护作用较好,相较于HCl-PAGO和H3PO4-PAGO涂层,该涂层有效阻碍了腐蚀介质与金属基体的直接接触,防止金属发生腐蚀。不同质子酸条件下所得涂层的阻抗谱虽然相似,但半圆直径有明显差异。HCl-PAGO涂层,H3PO4-PAGO涂层以及H2SO4-PAGO涂层的阻抗分别为8 649 Ω·cm2、15 680 Ω·cm2以及75 300 Ω·cm2。
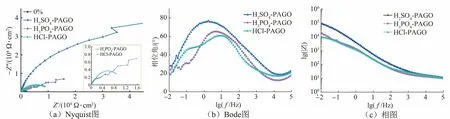
图5 不同质子酸条件下所得含1%GO/PANI涂层试样在3.5% NaCl溶液中的的电化学阻抗谱Fig.5 EIS of coating samples containing 1% GO/PANI under different proton acid conditions in 3.5% NaCl solution
在Bode图中,在低频率区,HCl-PAGO涂层,H3PO4-PAGO涂层及H2SO4-PAGO涂层的|Z|依次升高,分别为9 130×103Ω·cm2、1.714×104Ω·cm2以及8.55×104Ω·cm2。在中频区,这三种试样的相位角也依次增加,分别为61.8°、65.2°和75.9°。电化学阻抗谱结果表明,H2SO4-PAGO涂层的防腐蚀性能最好;相较于H3PO4-PAGO涂层以及HCl-PAGO涂层,H2SO4-PAGO涂层在双电层界面有较好的腐蚀介质阻碍作用,这与极化曲线结果一致。
2.4 涂层的防腐蚀机理
如图6所示:填料可以作为涂层中的屏障以隔绝外部环境,提高涂层的屏蔽性能。在GO/PANI涂层中,由于环氧树脂被水性化后,拥有了水性树脂特有的属性,即其表面会存在溶剂挥发后剩余的微孔。因此腐蚀介质在破坏涂层时,能够顺着微孔不均匀地侵入,其中一些具有氧化性的腐蚀介质如O2、H2O等,非常容易通过微孔穿透涂层,与基体表面发生反应,致使金属发生腐蚀。

图6 GO/PANI涂层的防腐蚀机理示意Fig.6 Schematic of anticorrosion mechanism for GO/PANI coating
3 结 论
在苯胺氧化过程中添加由Hummer法得到的氧化石墨烯GO,以此得到GO/PANI(聚苯胺)复合材料;以水溶性环氧树脂乳液(WEP)为载体,采用机械共混法制得GO/PANI防腐蚀涂层,耐水性结果表明,当涂层中GO/PANI质量分数为1%时,胶膜耐水性较好,其吸水率约为8%,此条件下涂层的Ecorr为-0.013 V、Jcorr为1.94×10-7A/cm2,有最高的防腐蚀效率,且在H2SO4条件下所得涂层的耐蚀性最好。

