碳黑金属酞菁原位生高价铁氧降解有机污染物
夏云 徐锦龙 陈龙

摘 要:为高效去除复杂水体环境中的有机污染物,制备过氧化物模拟酶催化剂,以双氧水为氧化剂,构建环境友好型的仿生催化体系,来催化降解水体中的地塞米松有机污染物。研究催化剂的形貌及结构特征,催化体系的催化性能、循环使用性能、催化机理、催化降解产物及最终产物。结果表明:所构筑的催化体系在温和(室温、中性)及复杂水体环境中(酸性、无机盐)对地塞米松的降解率均为100%,但在碱性条件下,该催化体系对地塞米松的降解率因双氧化水分解过快而降低了28%;该催化体系经过6次循环使用后,对地塞米松的降解率仍达到95%;过氧化物模拟酶在双氧水的作用下产生对水体有机污染物降解起主要作用的高价铁氧活性种,而羟基自由基起次要作用;经过60 min反应,该催化体系将地塞米松降解为对环境不存在二次污染的小分子有机酸。该仿生催化体系的构筑为仿生催化材料在工业废水中的应用提供了新视角。
关键词:碳黑;金属酞菁;高价铁氧活性种;降解;有机污染物
中图分类号:O643.36 文献标志码:A 文章编号:1009-265X(2023)06-0051-10
金属酞菁(MPc)与金属卟啉(MPs)均为M-N-C型金属络合物,具有极其相似的结构与性能,但金属酞菁合成简便,易大规模生产,因而是一种理想的金属卟啉的替代品[1-2]。金属酞菁可均裂双氧水(H2O2),产生羟基自由基(·OH)等活性种,·OH 是一种强氧化剂,可以瞬间氧化水体中的有机污染物(如染料、抗生素等),因而,MPc-H2O2体系的作用机理与芬顿体系的作用机理极为相似[3-4]。人们发现单一的金属酞菁分散性差且易聚合生成二聚体甚至多聚体,严重影响金属酞菁的催化活化性能。通过比表面积大的碳材料作为载体负载金属酞菁不仅可提高金属酞菁的分散性,而且金属酞菁与碳材料之间形成的п-п共轭键有助于均裂H2O2产生·OH 活性种,从而提高金属酞菁的催化活性[5-6]。但·OH 在水体中对底物的选择性差,易氧化金属酞菁,且易发生自聚反应,导致体系中氧化降解水体有机污染物的效率降低[7]。因此,将MPc-H2O2体系应用于水体有机污染物的净化治理,会受到该体系选择性差及降解效率低等问题的限制。
过氧化物酶是一种生物酶,金属卟啉为活性中心,氨基酸残基为第五配体,活性中心在配体的作用下异裂H2O2,产生高价铁氧活性种,表现出对底物的强选择性及高效的氧化降解作用[8-9]。根据过氧化物酶的作用机理,本文以结构及性能稳定的十六氯铁酞菁为活性中心,吡啶基為第五配体,具有高比表面积及使用成本低廉的碳黑为蛋白质骨架,设计过氧化物模拟酶;以H2O2为氧化剂,构建环境友好型的仿生催化体系,对水体中的地塞米松有机污染物进行催化氧化降解,研究其催化机制及降解路径。
1 实 验
1.1 实验材料与仪器
实验材料:十六氯铁酞菁(FePcCl16),实验室制备;碳黑(CB,粒径30 nm),美国卡博特公司;四氨基吡啶(4-AP,分析纯)、亚硝酸钠(NaNO2,分析纯)、浓盐酸(HCl,质量分数37%)、氢氧化钠(NaOH,分析纯)、二甲基甲酰胺(DMF,分析纯)、丙酮(AC,分析纯)、四氢呋喃(THF,分析纯)、地塞米松(DXMS,分析纯)、异丙醇(IPA,分析纯)、对苯醌(p-BQ,分析纯)、二甲基亚砜(DMSO,分析纯)、双氧水(H2O2,质量分数30%),阿拉丁试剂有限公司;5,5-二甲基-1-吡咯啉-氮-氧化物(DMPO,分析纯),东京化成工业株式会社。
实验仪器:JEM-2010高分辨透射电子显微镜(TEM),日本JEOL公司;LabRAM HR Evolution拉曼显微镜(Raman),法国HORIBA JY;K-Alpha型X射线光电子能谱(XPS),美国赛默飞公司;IKA-MAG HP 10 S025加热板,德国艾卡公司;UPLC型高效液相色谱(HPLC),美国waters公司;Agilent 700 Series电感耦合等离子体(ICP),美国安捷伦公司;A300电子顺磁共振波谱仪(EPR),德国Bruker公司;RV10型真空旋转蒸发仪,德国IKA公司;Agilent 6890N型气相色谱-质谱联用仪(GC-MS),美国安捷伦公司;UPLC/SynaptG2-S型超高液相色谱-高分辨质谱联用仪(HPLC-HDMS),美国Waters公司;Shimadu TOC-L总有机碳分析仪(TOC),日本岛津公司。
1.2 形貌和性能表征
分别将CB、吡啶基修饰的碳黑(Py-CB)、十六氯铁酞菁轴向配位的吡啶基修饰的碳黑(FePcCl16-Py-CB)分散于导电胶上,采用扫描电子显微镜对CB、Py-CB、FePcCl16-Py-CB的形貌进行观测。采用拉曼显微镜对CB、Py-CB、FePcCl16-Py-CB进行测试,扫描波长范围为1000~3000 cm-1,用532 nm的激光作为激发光源照射样品,以10%的激光功率测量得到拉曼光谱。采用X射线光电子能谱仪表征CB、Py-CB、FePcCl16-Py-CB的元素价态。
1.3 实验方法
1.3.1 过氧化物模拟酶的制备
将CB在浓HCl中浸渍5 d后,采用去离子水多次萃洗,冷冻干燥备用。将1 g CB加入100 mL的DMF中,机械搅拌使CB充分分散于DMF中;在0 ℃下,向其逐滴加入制备的吡啶重氮盐溶液,待重氮盐完全加入后,在冰浴的环境中反应3 h,在室温下机械搅拌15 h,分别采用DMF、2 M HCl溶液、2 M NaOH溶液、AC、去离子水萃洗,随后冷冻干燥即Py-CB。
将质量比为1∶1的FePcCl16与Py-CB加入到一定质量的THF溶液中,在85 ℃的温度下,在N2保护下,回流并且机械搅拌24 h;然后采用THF、去离子水多次萃洗直到萃洗液基本无色,冷冻干燥,得到FePcCl16-Py-CB,即过氧化物模拟酶。
1.3.2 催化性能测试
将20 mL 摩尔浓度为2.5×10-5 mol/L的DXMS溶液加入到40 mL的样品瓶中,加入0.025 g/L的FePcCl16-Py-CB、7.5 mmol/L的H2O2,在室温(25 ℃)的条件下进行有机污染物的催化氧化降解实验,间隔一段时间,取样并用聚四氟乙烯过滤塞过滤,过滤后在高效液相中测试其催化降解DXMS的降解率R。R的计算如式(1):
R/%=[(C0-C)/C0]×100 (1)
式中:C0为DXMS的起始浓度,C为取样时刻DXMS的浓度。
1.3.3 循环使用性能测试
将20 mL摩尔浓度为2.5×10-5 mol/L的DXMS溶液加入到40 mL的样品瓶中,加入0.025 g/L的FePcCl16-Py-CB、7.5 mmol/L的H2O2,在室温(25 ℃)的条件下反应60 min后测试样品瓶中的DXMS的降解率,为第1次实验。随后向第1次实验结束的样品瓶中加入少量高浓度的DXMS溶液,使得样品瓶中的DXMS的浓度为起始的浓度(2.5×10-5 mol/L);向其加入7.5 mmol/L的H2O2,反应60 min后测试样品瓶中的DXMS的降解率,此为第2次实验。以此类推,按照相同的方法进行循环使用性能测试。
1.3.4 催化机理测试
以IPA为·OH的捕获剂,p-BQ为超氧自由基(O·-2)的捕获剂,分别将IPA、p-BQ加入到FePcCl16-Py-CB-H2O2催化体系中,考察IPA、p-BQ对体系中DXMS降解的影响[10]。
采用EPR检测水溶液中DMPO捕获·OH的自旋信号及甲醇溶液中DMPO捕获O·-2的自旋信号[11-12],以此判断体系中是否存在·OH或O·-2。
采用GC-MS检测FePcCl16-Py-CB-H2O2催化体系中DMSO的氧化产物二甲基砜(DMSO2),以此判断体系中是否存在高价铁氧(Fe(IV)O)活性种[11]。在室温(25°C)的环境下,向FePcCl16-Py-CB-H2O2催化体系中加入DMSO,反应60 min,过滤反应液,将其在旋转蒸发仪上旋转干燥以去除水分,待水分蒸干后出现少量颗粒状固体,加入4 mL甲醇溶液,充分溶解旋转颗粒状固体,之后在GC-MS上进行检测。
1.3.5 降解中间产物及最终产物测试
采用UPLC-HDMS的正离子模式測试DXMS的中间产物,采用负离子模式测试最终产物。
2 结果与讨论
2.1 微观形貌分析
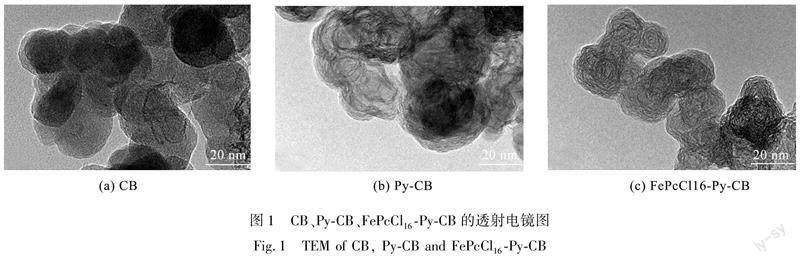
CB、Py-CB、FePcCl16-Py-CB的透射电镜图如图1所示,从图1中可以看出:Py-CB及FePcCl16-Py-CB的表面较CB并没有明显变化,表明改性剂在CB表面分散得很均匀,通过吡啶基修饰及FePcCl16的轴向配位并没有导致CB表面堆叠严重。由此推
测经过改性的CB,由于改性剂均匀分布,可以获得稳定、高效的催化性能。
2.2 拉曼光谱分析
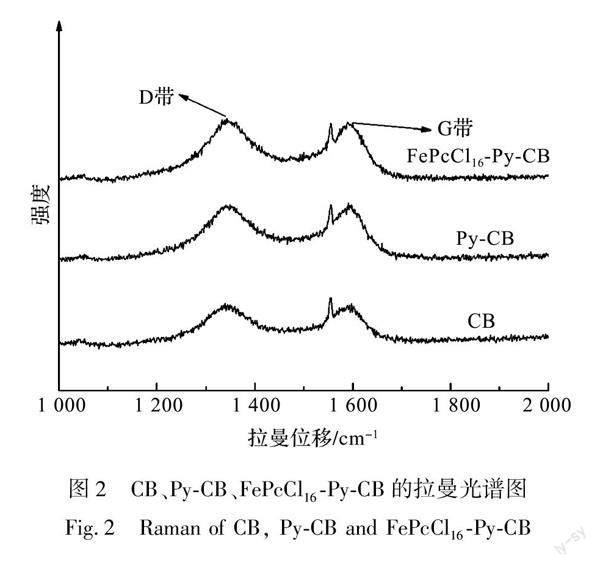
图2为CB、Py-CB、FePcCl16-Py-CB的拉曼光谱图,从图2中可以看出:在1345 cm-1处出现碳材料的D带,在1590 cm-1处出现碳材料的G带。通常采用D带的强度ID与G带的强度IG的比值,反映碳材料的缺陷程度,其值越大表示其碳材料的缺陷越明显[13]。CB、Py-CB、FePcCl16-Py-CB的ID/IG分别为0.99、1.02、1.05,说明CB、Py-CB、FePcCl16-Py-CB中碳材料的缺陷依次递增。而Py-CB及FePcCl16-Py-CB分别通过吡啶基改性CB、FePcCl16轴向配位Py-CB获得,由此表明改性使CB的结构出现了缺陷,同时证明了CB已经成功改性。
2.3 化学价键态分析
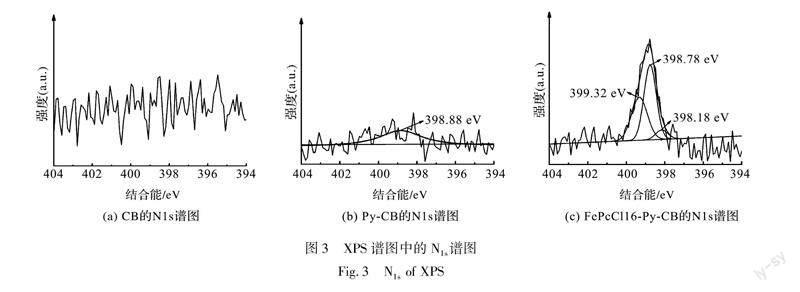
图3为CB、Py-CB、FePcCl16-Py-CB的N1s谱图,从图3中可以看出:FePcCl16-Py-CB在结合能398.18 eV、398.78 eV出现的峰分别为酞菁环中CN—C、C—N—C[14-15],表明FePcCl16已负载于CB上。从图3中可以看出CB没有出现N1s对应的峰,Py-CB在结合能398.88 eV处出现一个峰,该峰表示吡啶环中CN,该基团对应的峰在FePcCl16-Py-CB中出现在结合能399.32 eV处,结合能增加了0.54 eV。这是由于FePcCl16中的Fe与Py-CB中的N发生轴向配位,N原子孤对电子转移到Fe离子上,使得吡啶环中的N原子核外电子云密度降低,故结合能增加[14]。
2.4 催化性能
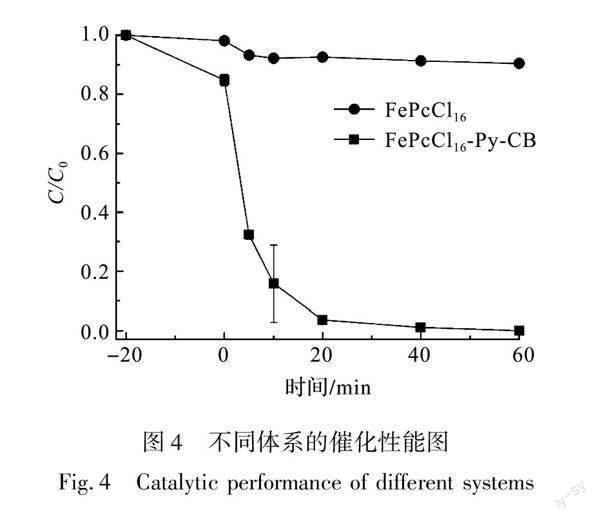
采用原子吸收光谱对FePcCl16-Py-CB中铁原子的含量进行测试,结果显示铁的含量为2.772%。因制备的FePcCl16-Py-CB的用量为0.025 g/L,通过计算得出FePcCl16-Py-CB中的FePcCl16的用量为0.014 g/L。为比较 FePcCl16-Py-CB与FePcCl16的催化效果,采用FePcCl16-Py-CB的用量0.025 g/L,FePcCl16的用量0.014 g/L,H2O2的用量均为7.5 mmol/L,DXMS的浓度均为2.5×10-5 mol/L,分别构筑催化体系,其催化结果如图4所示。从图4中可以看出:60 min,FePcCl16活化H2O2氧化降解DXMS的降解率为20%左右,而FePcCl16-Py-CB活化H2O2氧化降解DXMS的降解率为100%。这说明通过轴向配位的方式将FePcCl16负载于CB上,可以显著提高FePcCl16的催化活性。
生物酶的选择性及催化活性受到环境影响较大,故研究环境因素(如温度、pH值、无机盐等)对过氧化物模拟酶的催化性能的影响,以进一步了解过氧化物模拟酶的性能,进而拓宽模拟酶的应用领域。
2.4.1 温度的影响
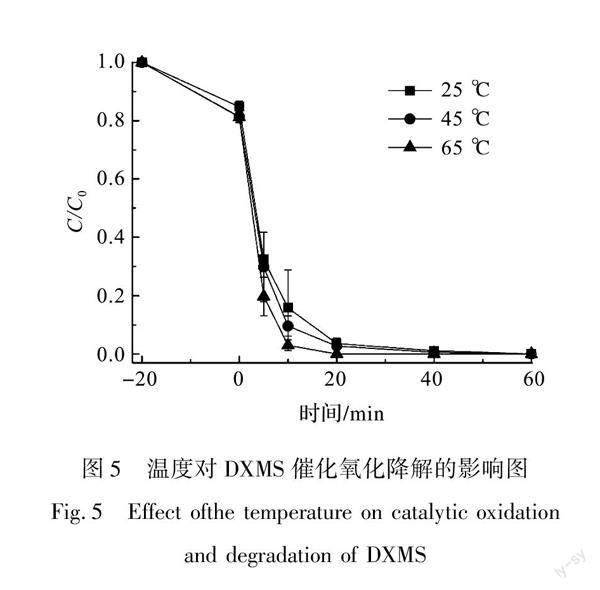
图5为温度对催化体系中催化氧化降解DXMS的影响图。从图5中可以看出,温度从25 ℃到65 ℃,体系中DXMS的降解率及降解速率并没有发生显著的变化,表明过氧化物模拟酶在较高的温度下仍然保持着优异的催化活性,该特性明显优于生物酶。从低碳发展角度考虑,过氧化物模拟酶催化选择25 ℃的条件下更为合适。
2.4.2 pH的影响
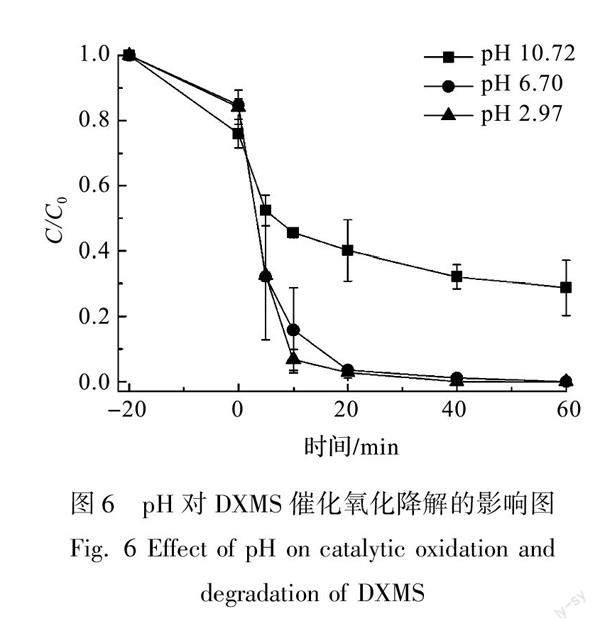
图6为pH对催化体系中催化氧化降解DXMS的影响图。由于碳材料具有优异的吸附性能,因此在进行催化氧化降解实验前进行吸附实验,故图中-20~0 min表示在催化氧化降解实验前20 min的吸附实验,在0 min加入H2O2,此刻为催化氧化降解实验的起始时刻。图6中-20~0 min吸附阶段可以看出在酸性、中性、碱性的条件下,过氧化物模拟酶的吸附性能并没有发生显著的变化。在0 min时刻,体系中加入7.5 mmol/L的H2O2,从图6中可以看出,在pH 6.70、pH 2.97的条件下,60 min内催化体系中DXMS的催化氧化降解率均达到100%,且两者降解速率并没有发生显著变化,说明该催化体系在酸性、中性的条件下均表现出优异的催化性能。而pH 10.72的条件下,60 min内DXMS的催化氧化降解率为72%,这是由于在碱性的条件下,H2O2分解过快,导致体系因H2O2量不足而降低了DXMS的降解率。
2.4.3 无机盐的影响
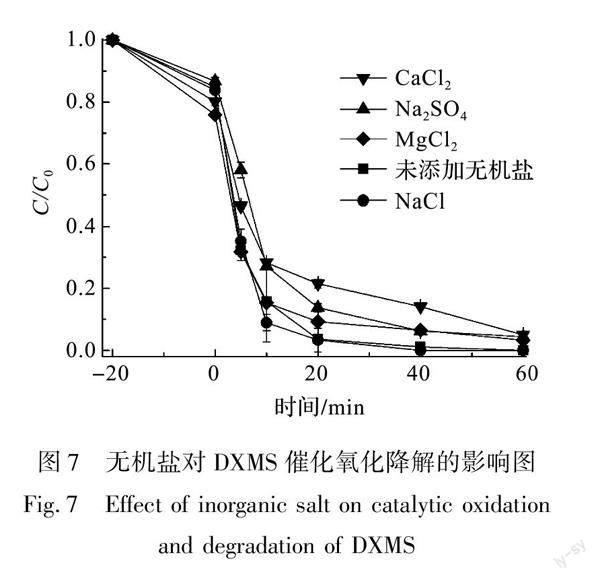
无机盐的存在在很大程度上会影响水体有机污染物的降解,因此向催化体系中加入无机盐,研究无机盐对水体有机污染物的影响以评价所构筑的催化体系对于复杂环境的适应性。在实际水体环境中,硬度是衡量水质的重要指标,而Ca2+、Mg2+的浓度决定着水体的硬度,因此选用CaCl2、MgCl2作为参考无机盐;而Na+、Cl-、SO2-4是水体中常出现的离子,因此选择Na2SO4、NaCl。图7是无机盐对DXMS催化氧化降解的影响图,从图7中可以看出:体系中加入CaCl2、Na2SO4、MgCl2、NaCl等无机盐,体系中对DXMS的降解率并没有发生明显的变化,这表明该催化体系在无机盐存在的情况下仍然具有优异的催化性能,因此该催化体系可应用于复杂的水体环境中。值得关注的是,体系中加入CaCl2、MgCl2、NaCl等无机盐,体系中存在着大量的Cl-,Cl-的存在会抑制羟基自由基(·OH)的产生[16],而体系中的催化氧化降解DXMS的性能并没有发生显著变化,由此推测该催化体系的催化机理可能为非·OH机理。
2.5 循环使用性能
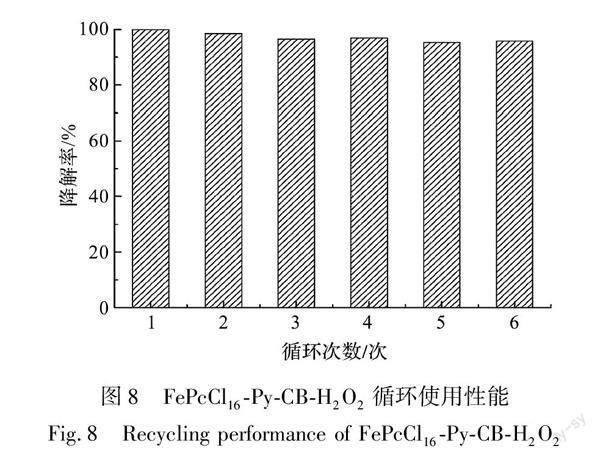
图8为FePcCl16-Py-CB-H2O2循环使用性能图,从图8中可以看出,经过6次循环使用,体系对DXMS的催化氧化降解率为95%,较第一次100%的DXMS降解率仅降低了5%。对反应前后的FePcCl16-Py-CB进行铁含量测试,反应前的铁含量为2.772%,经过6次反应后的FePcCl16-Py-CB的铁含量为2.695%,由此可以看出反应前后FePcCl16-Py-CB中的活性中心金属酞菁几乎没有损失。而经过6次循环反应后,DXMS的降解率有所降低,这可能是由于在多次循环使用过程中,过氧化物模拟酶中的活性中心有极少量的失活所致。同时说明该催化体系具有较好的循环使用性能及稳定性,可多次循环使用,具有工业化应用的潜力。
2.6 催化机制分析
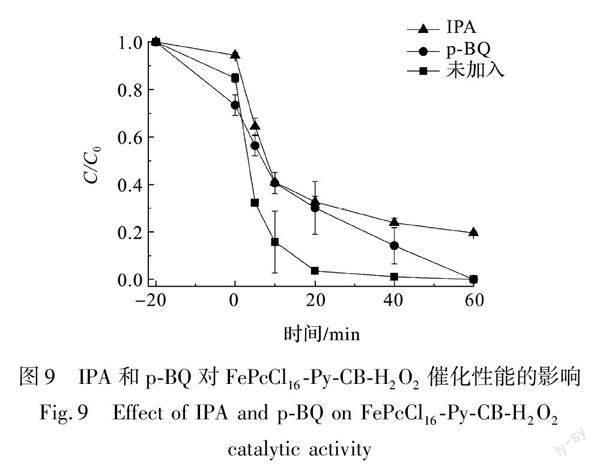
本课题组之前的研究发现,金属酞菁活化双氧水氧化降解有机污染物主要表现出·OH机理,其次有O·-2作用。为初步判断过氧化物模拟酶活化双氧水的机理,采用IPA为·OH的捕获剂,p-BQ为O·-2的捕获剂,探讨FePcCl16-Py-CB-H2O2体系中分别加入IPA、p-BQ对体系降解DXMS的影响,以初步判断所构筑的催化体系与之前的研究机理是否相同。IPA和p-BQ对FePcCl16-Py-CB-H2O2催化性能的影响如图9所示,加入p-BQ后体系60min内DXMS的降解率为100%,与未加入p-BQ的FePcCl16-Py-CB-H2O2体系相比并没有显著变化,说明O·-2对于体系中DXMS的降解未起到作用。而加入IPA后,体系60min内DXMS的降解率为80%,较未加入IPA的FePcCl16-Py-CB-H2O2体系DXMS的降解抑制了20%,说明IPA对于体系中DXMS的降解具有抑制作用,由此推测FePcCl16-Py-CB-H2O2体系中·OH起到氧化降解部分DXMS的作用,但未起到主要作用,也证实了2.4.3中所述该催化体系非·OH机理的推测。
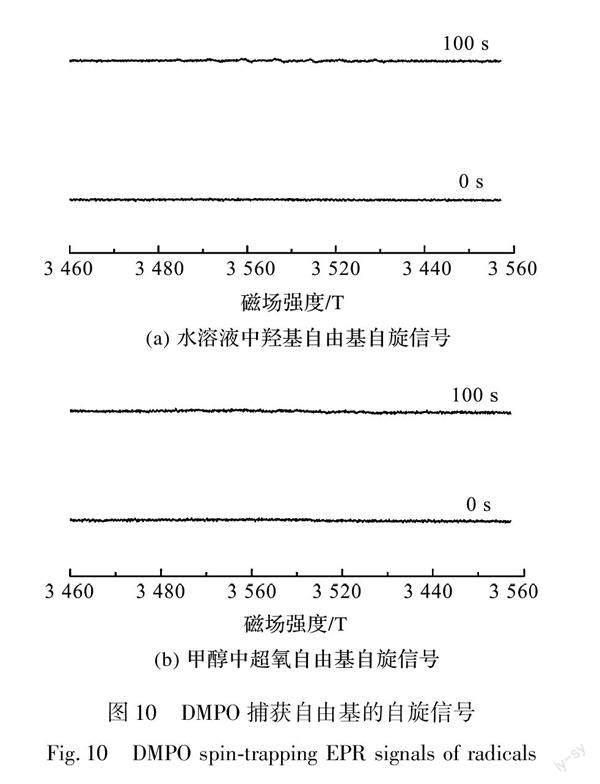
图10为DMPO捕获自由基的自旋信号图,其中:图10(a)为DMPO捕获水溶液中·OH的自旋信号,图10(b)为DMPO捕获甲醇溶液中O·-2的自旋信号。从图10(a)中可以看出,体系中存在着微弱的DMPO捕获·OH 自旋信号,说明FePcCl16-Py-CB/H2O2体系中存在着·OH ,结合图9中IPA加入体系中,DXMS的降解率抑制了20%,進一步证实了体系中·OH 起到了氧化降解DXMS的作用,但·OH 不是起氧化降解DXMS的主要活性种。而从DMPO捕获O·-2自旋信号中可以看出,图10 (b)中不存在O·-2,也与图9中p-BQ的加入对体系中对DXMS的降解不产生作用的结论相吻合。由此可以推断,体系中存在着起氧化降解DXMS的主要活性种。
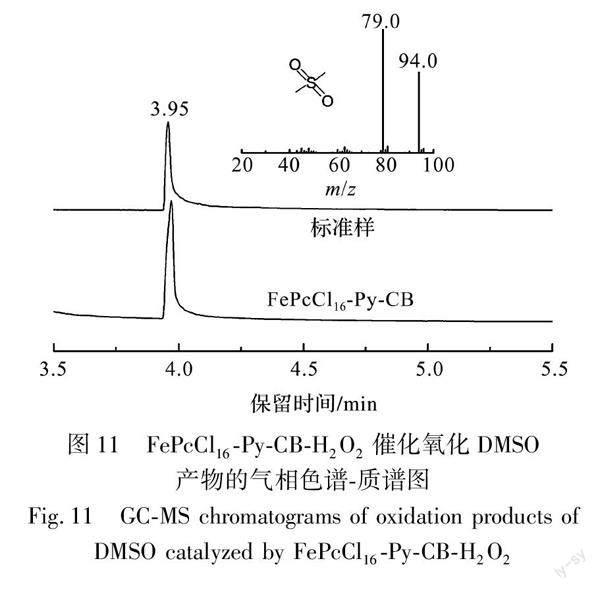
金属酞菁在配体的作用下可异裂H2O2产生高价铁氧(Fe(IV)O)活性种,推测过氧化物模拟酶活化H2O2,产生了Fe(IV)O活性种。Fe(IV)O可以将DMSO氧化成DMSO2,而·OH不能将DMSO氧化(见式(2)和式(3))[17],故通过检测体系中是否存在DMSO2以判断体系中是否存在Fe(IV)O活性种。图11为FePcCl16-Py-CB/H2O2体系催化氧化DMSO产物的气相色谱-质谱图。从图11中可以看出,FePcCl16-Py-CB/H2O2体系保留时间3.95处出现一个峰,该峰的保留时间及峰形与DMSO2吻合,同时该峰的质谱图中质荷比m/z分别在94.0 和 79.0 处出现两个质谱峰,其对应的是DMSO2和去甲基后的DMSO2分子结构片段,进一步说明了在保留时间为 3.95 min处出现的色谱峰为 DMSO2,由此可以证明 FePcCl16-Py-CB/H2O2 催化体系中存在着 Fe(IV)O 活性种[16]。
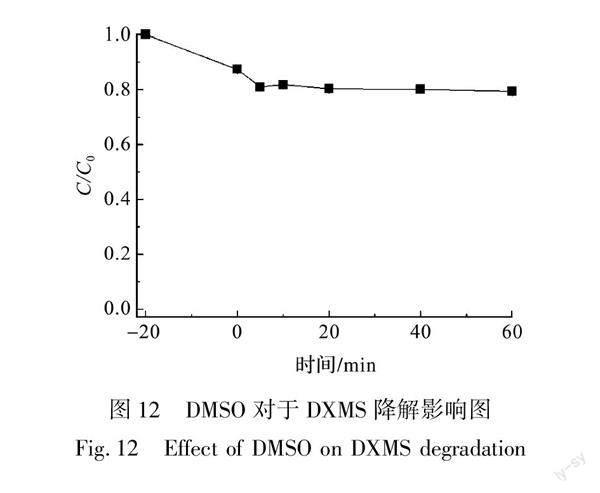
为了进一步研究Fe(IV)O对体系中催化降解DXMS的影响,以DMSO为Fe(IV)O的捕获剂,加入到体系中,研究DXMS的降解情况,其结果如如图12所示。从图12中可以看出,体系中加入DMSO后,60 min的体系中DXMS的剩余率为80%。而在图9中,60 min体系中DXMS的剩余率为0,这表明加入DMSO后,对体系DXMS的降解有明显的抑制作用。这是因为体系中加入的DMSO,与体系中的Fe(IV)O发生了反应,与体系中存在的少量·OH也发生了反应,致使体系中没有足够的活性种降解DXMS。
因此,通过向体系中分别加入·OH捕获剂IPA、O·-2的捕获剂p-BQ、EPR检测DMPO捕获·OH及DMPO捕获O·-2的自旋信号,DMSO2的气相色谱-质谱检测,DMSO对体系中DXMS降解影響可以得出,FePcCl16-Py-CB/H2O2催化体系中起降解DXMS作用的主要活性种是Fe(IV)O,其次为·OH。
2.7 降解机理分析
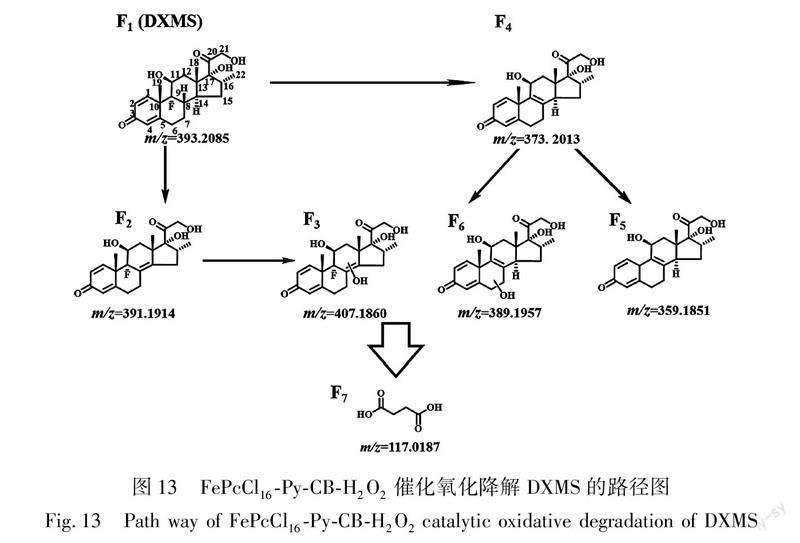
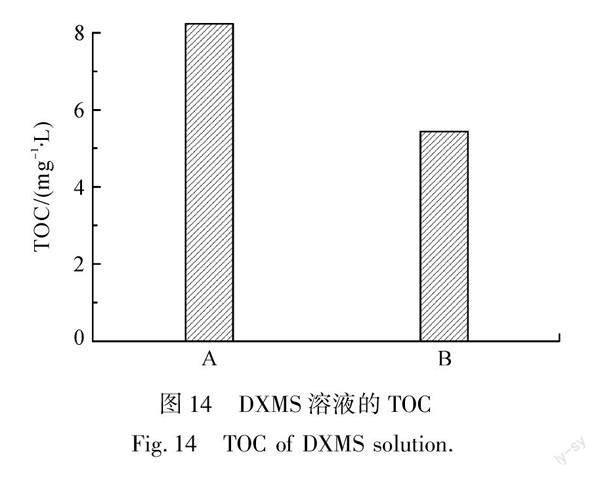
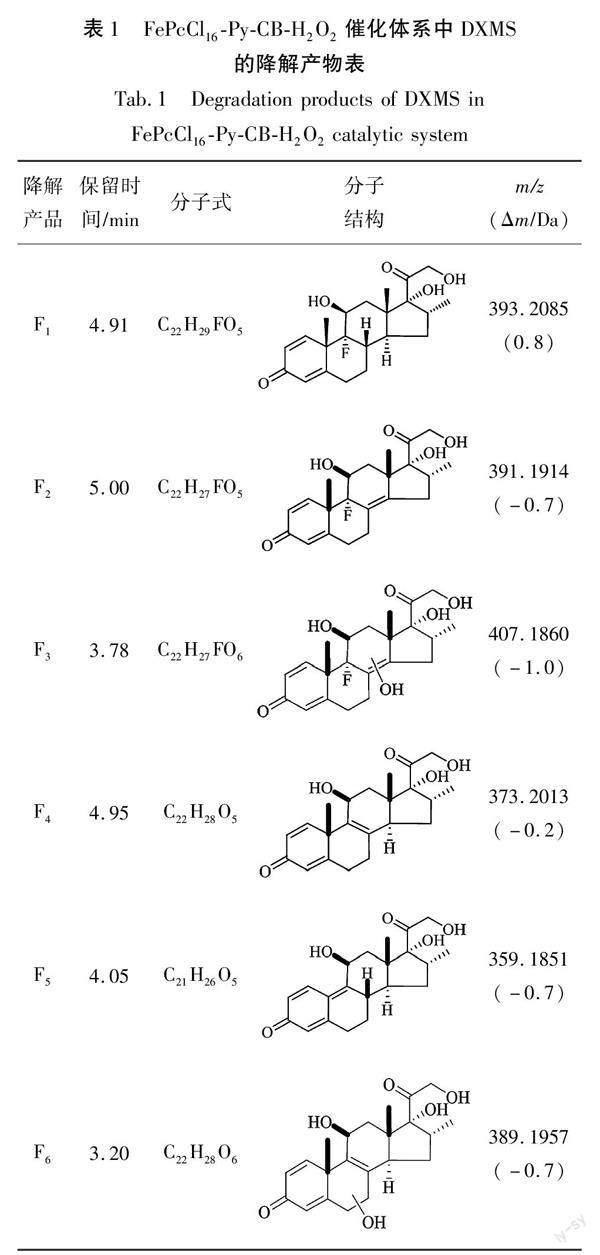
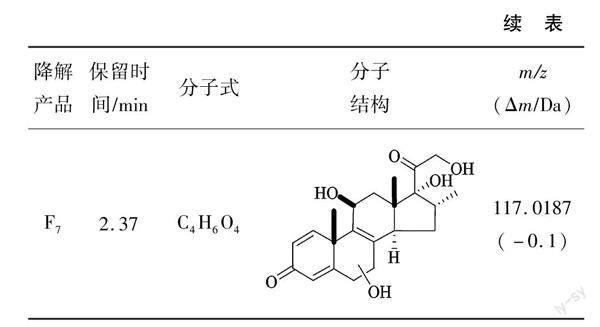
图13为FePcCl16-Py-CB-H2O2体系催化氧化降解DXMS路径图,从图13中可以看出,第1条路径是F1(DXMS)在C8、C14处脱氢生成F2,F2经过羟基化生成F3;第2条路径是F1(DXMS)在C8、C9处脱去HF生产F4,F4经过羟基化生产F6,或者F4在C19脱去甲基,生成F5,经过60 min,中间产物生成小分子有机酸F7(丁二酸)[18, 19]。图14为DXMS溶液的TOC,图中A表示DXMS原液的TOC,其值为8.28 mg/L,图中B表示经过催化氧化降解后的溶液的TOC,其值为5.45 mg/L,反应后溶液的TOC降低了34%,说明在反应过程中有CO2和H2O产生。反应的中间产物及最终产物的保留时间、分子式及可能的分子结构等如表1所示。
3 结 论
本文以FePcCl16为活性中心、吡啶基为第五配体、碳黑为蛋白质骨架,制备过氧化物模拟酶催化剂,以此催化活化H2O2原位产生Fe(IV)O为高效催化降解DXMS的主要活性种,该催化体系表现出类似于生物酶的催化机制。所构建的催化体系对温度变化具有稳定性,在无机盐及酸性的条件下仍然具有高效的催化活性,催化性能明显优于生物酶,但在碱性条件下催化活性有所减弱。FePcCl16-Py-CB-H2O2催化体系可将DXMS降解为对环境不存在危害的小分子有机酸,为模拟酶材料在工业废水治理中发挥其应用潜力提供新方向。
参考文献:
[1]CORTES-ARRIAGADA D, MIRANDA-ROJAS S, CID-MORA F, et al. First-principles study of hybrid nanostructures formed by deposited phthalocyanine/porphyrin metal complexes on phosphorene[J]. Journal of Molecular Liquids, 2021, 333(1):115948.
[2]ZHAO J, LYU H, WANG Z, et al. Phthalocyanine and porphyrin catalysts for electrocatalytic reduction of carbon dioxide: Progress in regulationstrategies and applications[J].Separation and Purification Technology, 2023, 312:123404.
[3]CHEN S, LEI S, WU B, et al. Preparation of graphene-supported-metal-phthalocyanine and mechanistic understanding of its catalytic nature at molecular level[J]. Journal of Colloid and Interface Science, 2022, 622: 708-718.
[4]FARAHMAND S, AYAZI-NASRABADI R, ALI ZOLFIGOL M. Amino-cobalt(II) phthalocyanine supported on silica chloride as an efficient and reusable heterogeneous photocatalyst for oxidation of alcohols[J]. Tetrahedron Letters, 2023, 118:154403.
[5]XU F, LAI C, ZHANG M, et al. Graphite carbon nitride coupled with high-dispersed iron (II) phthalocyanine for efficient oxytetracycline degradation under photo-Fenton process: Performance and mechanism[J]. Separation and Purification Technology, 2023, 308:122829.
[6]LU W, LI N, BAO S, et al. The coupling of metallophtha-locyanine with carbon nanotubes to produce a nanomaterial-based catalyst for reaction-controlled interfacial catalysis[J]. Carbon, 2011, 49(5):1699-1709.
[7]LI N, LU W Y, PEI K M, et al. Ordered-mesoporous-carbon-bonded cobalt phthalocyanine:A bioinspired catalytic system for controllable hydrogen peroxide activation[J]. Acs Applied Materials & Interfaces, 2014, 6(8): 5869-5876.
[8]BARREIRO D S, OLIVEIRA R N S, PAULETA S R. Bacterial peroxidases-Multivalent enzymes that enable the use of hydrogen peroxide for microaerobic and anaerobic proliferation[J]. Coordination Chemistry Reviews, 2023, 485:215114.
[9]YOSHIDA T, SUGANO Y. Unexpected diversity of dye-decolorizing peroxidases[J]. Biochemistry and Biophysics Reports, 2023, 33:101401.
[10]WANG J, LIU H, MA D, et al. Degradation of organic pollutants by ultraviolet/ozone in high salinity condition: Non-radical pathway dominated by singlet oxygen[J]. Chemosphere, 2021, 268:128796.
[11]WANG X, LU W, ZHAO Z, et al. In situ stable growth of β-FeOOH on g-C3N4 for deep oxidation of emerging contaminants by photocatalytic activation of peroxymonosulfate under solar irradiation[J]. Chemical Engineering Journal, 2020, 400:125872.
[12]WANG X Y, LU W Y, CHEN Y X, et al. Effective elimination of antibiotics over hot-melt adhesive sheath-core polyester fiber supported graphitic carbon nitride under solar irradiation[J]. Chemical Engineering Journal, 2018, 335:82-93.
[13]JIANG Y, LU Y, LV X, et al.Enhanced catalytic performance of pt-free iron phthalocyanine by graphene support for efficient oxygen reduction reaction[J]. ACS Catalysis, 2013, 3(6):1263-1271.
[14]XIA Y, LI N, LU W, et al. High-valent iron-oxo specieson pyridine-containing MWCNTs generated in a solar-induced H2O2 activation system for the removal of antimicrobials[J]. Chemosphere, 2021, 273:129545.
[15]ZHU Z, LU W, XU T, et al.High-valent iron-oxo complexes as dominant species to eliminate pharmaceuticals and chloride-containing intermediates by the activation of peroxymonosulfate under visible irradiation[J]. Catalysis Letters, 2020, 150:1355-1367.
[16]ZHU Z, LU W, LI N, et al. Pyridyl-containing polymer blends stabilized iron phthalocyanine to degrade sulfonamides by enzyme-like process[J]. Chemical Engineering Journal, 2017, 321:58-66.
[17]夏云,呂汪洋,陈文兴,等.纤维负载炭黑金属酞菁轴向配合物仿酶高效催化降解水体中有机污染物[J].高等学校化学学报,2020,41(7),1582-1590.
XIA Yun,LU Wangyang, CHEN Wenxing, etc. Fiber supported carbon black metal phthalocyanine axial complex to mimic enzyme for highly efficient catalytic degradation of organic pollutant in water[J].Chemical Journal of Chinese Universities, 2020, 41(7):1582-1590.
[18]SULAIMAN S, KHAMIS M, NIR S, et al. Stability and removal of dexamethasone sodium phosphate from wastewater using modified clays[J]. Environmental Technology, 2014, 35(15):1945-1955.
[19]CHEN Q, ZIELINSKI D, CHEN J, et al.A validated, stability-indicating HPLC method for the determination of dexamethasone related substances on dexamethasone-coated drug-eluting stents[J]. Journal of Pharmaceutical and Biomedical Analysis, 2008, 48(3):732-738.
Degradation of organic pollutants by carbon black metal phthalocyanine in situ producing high valent iron
XIA Yun 3, XU Jinlong2, CHEN Long3
Abstract: The rapid development of industry, the intensification of urbanization and the growth of population lead to human's increasing demand for clean freshwater year by year, and at the same time, human production and domestic wastewater is discharged into the environment, resulting in the scarce freshwater. Organic pollutants such as drugs, personal care products, are present at extremely low concentrations from ng/L to μg/L in water, but they can cause immeasurable damage to the environment and living organisms, which causes harm to the human body ultimately. So more and more researchers pay attention to the recycling of wastewater which comes from daily life, agricultural or industrial production.
To respond to the "dual carbon" strategic objectives, it is necessary to efficiently degrade and remove organic pollutants in water to achieve sustainable development. Biological enzymes have high catalytic activity and strong selectivity to substrates, so we can use them to catalyze degradation of organic pollutants. However, the direct extraction of enzymes from organisms will bring high extraction cost, and the change of the application environment of enzymes will significantly reduce their catalytic activity. So we designed an environmentally friendly bionic catalyst called peroxide mimicking enzyme which can catalyze the degradation of organic pollutants in water efficiently. In peroxide mimicking enzyme, iron hexadecachlorophthalocyanine (FePcCl16) worked as the active site, pyridine group (Py) acted as the fifth ligand, and carbon black (CB) served as a protein skeleton. Inspired by the principle of peroxidase metabolizing drugs, we constructed the environmentally-friendly bionic catalytic system which used peroxide simulation enzyme as catalyst, and hydrogen peroxide as oxidant to catalyze the oxidative degradation of dexamethasone (DXMS). The results showed that the bionic catalytic system maintained high efficiency and stable degradation rate of DXMS in the 25-65 ℃ temperature range, indicating that the simulated enzyme catalyst was not sensitive to temperature. The degradation rate of DXMS was 100% in 60 min in acid or neutral conditions. It can be seen that the catalytic system was better than that of the Fenton system. At the same time, the catalytic system did not change the degradation rate of organic pollutants in the presence of inorganic salts, and the degradation rate of DXMS still reached 100%, indicating that the catalytic system still had good catalytic oxidation degradation efficiency in complex water environment. However, the degradation rate of DXMS was reduced by 28% due to the rapid decomposition of H2O2 under alkaline conditions. Surprisingly, we found that the catalytic system had excellent recycling performance, and the degradation rate of DXMS was still 95% after six cycles of use. By adding isopropyl alcohol (IPA) and p-benzoquinone (p-BQ) into the system as trapping agents of hydroxyl radical(·OH) and superoxide radical (O·-2) respectively, electron spin resonance (EPR) detection of ·OH and O·-2 captured by 5,5-Dimethyl-1-pyrroline N-oxide (DMPO), gas chromatography-mass spectrometry (GC-MS) for the detection of dimethyl sulfone (DMSO) oxidation product confirmed that the main active species of DXMS in the catalytic system were high-valent iron oxo (Fe(IV)O) active sites, followed by ·OH.
Degradation path analysis showed that the first path of DXMS degradation began with the dehydrogenation of C8 and C14,followed by hydroxylation; the second path of DXMS degradation started with the removal of HF at C8 and C9, followed by hydroxylation or demethylation at C19. After 60 min, all the intermediate products generated small molecule organic acid (succinic acid) or became mineralized. The construction of the bionic catalytic system provides a new perspective for sewage treatment.
Keywords: carbon black; metal phthalocyanine; high-valent iron-oxo active species; degradation; organic pollutant
收稿日期:20230427 网络出版日期:20230804
基金项目:浙江省访问工程师项目(FG2022321);嘉兴市应用性基础研究项目(2023AY11019);嘉兴职业技术学院重点项目(jzyz202301);嘉兴职业技术學院高层次引才项目(22407030166);嘉兴职业技术学院培育项目(22407030179)
作者简介:夏云(1983—),男,江苏扬州人,讲师,博士,主要从事环境催化纤维方面的研究。

