基于CiteSpace的国内缺血性脑卒中程序性细胞死亡研究的可视化分析
陈 蕾,李子滢,秦莉花
缺血性脑卒中是由于血液供应不足导致脑组织功能短暂性或永久性丧失,并引发一连串事件,如电功能丧失、钙内流导致膜功能紊乱、致使钙依赖性兴奋性毒性、活性氧物质的产生,最终导致细胞膜破坏和细胞裂解[1]。缺血性脑卒中约占我国脑卒中的69.6%,病人死亡、残疾率高达33.3%[2]。缺血性脑卒中是国家实施“健康中国”行动中防控的四大重大慢性病之一,国务院实施健康中国行动意见中指出,要防控重大疾病,降低心脑血管疾病死亡率。缺血性脑卒中后损伤涉及多种机制,如炎症反应、氧化应激、线粒体损伤、蛋白质错误折叠等,这些机制依赖损伤和修复途径之间的平衡,若损伤大于修复,引发程序性细胞死亡机制[3]。程序性细胞死亡(programmed cell death,PCD)又称调节性细胞死亡(RCD),包括结构紧密的信号级联和分子效应机制,是细胞自杀的保守进化过程[4],包括细胞凋亡、铁死亡、细胞自噬、坏死性凋亡、细胞焦亡等11种类型[5]。程序性细胞死亡与缺血性脑卒中的发病机制及脑卒中后缺血再灌注损伤的发生密切相关[6],但目前关于缺血性脑卒中程序性细胞死亡的作用机制尚未完全明确。为探究程序性细胞死亡与缺血性脑卒中相关研究热点和发展趋势,本研究运用CiteSpace软件对该领域的文献进行可视化和文献计量学分析,以期为科研人员提供新思路。
1 资料与方法
1.1 数据来源
以中国知网、万方、维普、中国生物医学文献数据库为数据来源,检索时限为2012年1月—2022年8月10日。检索方式为主题词检索,检索主题词为“缺血性脑卒中”“程序性细胞死亡”,语种为中文,文献来源为北京大学中文核心期刊、中文社会科学引文索引(CSSCI)、中国科学引文数据库(CSCD)来源期刊和中国科技论文统计源期刊。
1.2 纳入与排除标准
纳入文献类型为article。排除重复文献、报纸、征稿通知、新闻稿、会议摘要等。
1.3 统一分析方法
从各个数据库中导出文献为RefWorks格式,将数据导入CiteSpace 6.1.R3转化数据格式。设置时间跨度为2012年1月—2022年8月10日;时间切片为1年;关键词和机构分析阈值选择为“Top N Per Slice”(n=50),作者分析阈值选择为“g-index k=25”;网络简化路径选择“Pathfinder”;网格修剪方式为“Pruning the merged network”;分析节点选择“author”“institution”“keywords”。
2 结 果
2.1 年度发文量分析
共检索到相关文献6 938篇,根据纳入与排除标准进行筛选,最终纳入文献1 604篇,其中西医类文献977篇,中医类文献627篇。对纳入的1 604篇文献进行年度发文量分析,详见图1。发文量呈曲折上升趋势,2021年达到最高峰(219篇)。

图1 2012—2022年缺血性脑卒中程序性细胞死亡年度发文量趋势
根据不同的程序性细胞死亡类型进行分析,2021年研究细胞凋亡核心期刊发文量达到最高峰为68篇,其次,2015年发文量为66篇,2015—2020年呈下降趋势;研究自噬的发文量呈逐年上升趋势。自2015年起逐渐出现坏死性凋亡、细胞焦亡及铁死亡,详见图2。
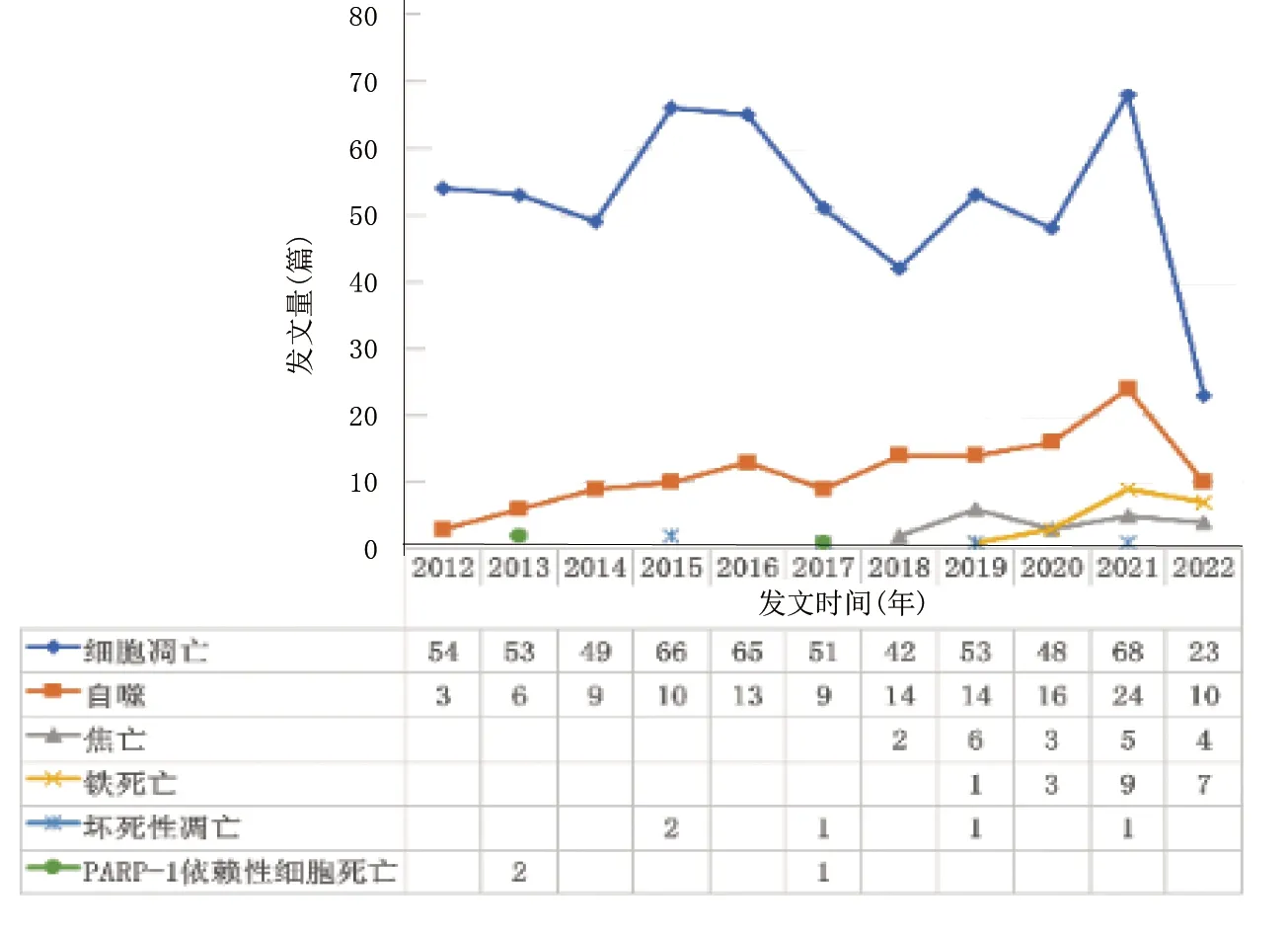
图2 2012—2022年缺血性脑卒中不同程序性细胞死亡途径相关文献发文量
2.2 作者合作网络分析

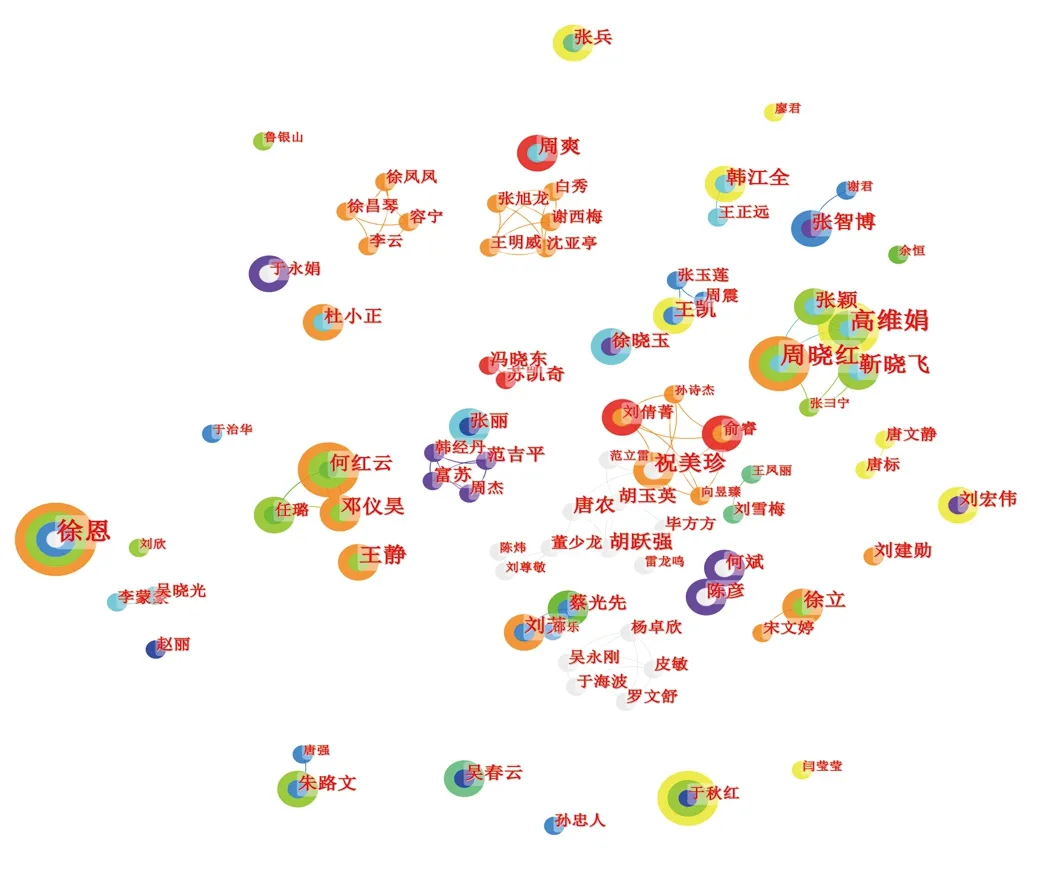
图3 作者合作网络共现图谱
对研究该领域的文献作者进行共现分析,结果显示有465名作者,作者之间的合作共512次,合作多为分散。其中祝美珍、于海波、张少芸、刘永锋、缑燕华、陈鹏典、彭君华等点度中心性排名最高(9),说明团队合作紧密。其他研究者之间合作较少,研究相对独立。
2.3 机构合作网络分析
从研究机构发文量分析,发文量排名居前10位的机构分别为湖南中医药大学(37篇)、北京中医药大学(26篇)、天津中医药大学(19篇)、北京中医药大学东直门医院(15篇)、浙江中医药大学(13篇)、哈尔滨医科大学第二附属医院(12篇)、黑龙江中医药大学(11篇)、吉林大学第一医院(11篇)、中国中医科学院(10篇)、安徽中医药大学(10篇)。研究机构平均发文量为2.8篇。
合并二级机构后进行机构共现网络分析,结果显示:研究机构数量共253个,机构之间的合作共49次,合作网络松散,详见图4。其中,北京中医药大学东直门医院、北京中医药大学、中国中医科学院的点度中心性>5,说明与其他机构合作相对密切。北京中医药大学东直门医院点度中心性最高(9),位于合作网络的中心,说明其在科研合作中有较高的影响力。

图4 机构合作网络共现图谱
2.4 关键词分析
频次最高的5个关键词分别为“细胞凋亡”“脑缺血”“脑梗死”“大鼠”“脑卒中”,中介中心性最高的关键词为“脑缺血”。“炎症反应”的西格玛值最高,说明创新性最强。频次排名居前10位的关键词见表1。

表1 程序性细胞死亡与缺血性脑卒中相关研究领域频次排名居前10位的关键词
对关键词进行聚类图谱(clusters)分析,聚类模块值(Q值)为0.610 7,聚类平均轮廓值(S值)为0.843 3,详见图5。结果表明共798个关键词,累计出现频次3 574次。关键词时间线聚类(timeline)分析中,X轴为年份,Y轴为聚类类别,时间线聚类图谱可清晰显示该研究领域的发展趋势。详见图6。
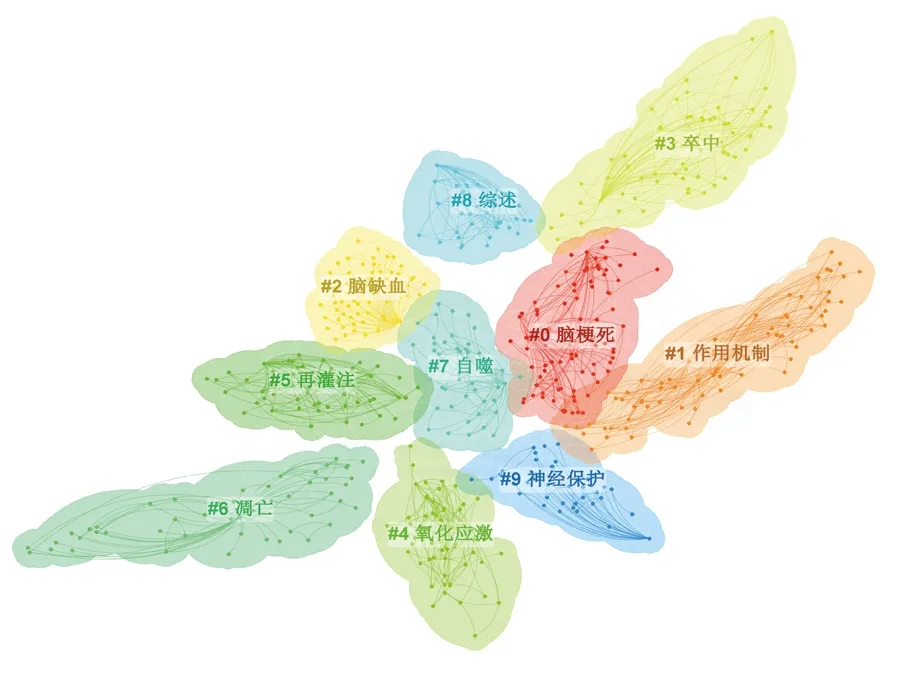
图5 关键词聚类图谱

图6 时间线关键词聚类图谱
关键词突现(burstness)是指关键词在一段时间内频次激增,可代表该领域的研究前沿。持续到2022年,突现强度排名居前3位的关键词为炎症反应、铁死亡、氧化应激。关键词突现排名居前15位的关键词见图7。
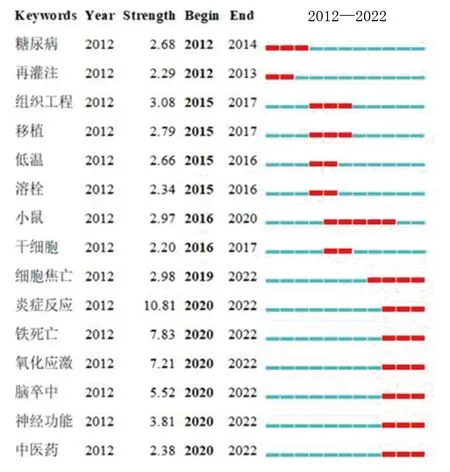
图7 关键词突现图谱
3 讨 论
3.1 研究概况
从年发文量分析,发文量呈缓慢上升趋势,且中医类文献逐渐增多,研究人员在中医方面的研究热度逐渐增加。分析与国家大力推行中医药的发展有关,国家政策的支持调动了科研积极性,推动了缺血性脑卒中程序性细胞死亡在中医领域的科研发展。程序性细胞死亡在缺血性脑卒中的研究进程主要分为两个阶段,2015年之前主要集中在细胞凋亡,2015—2022年研究方向逐渐发展到坏死性凋亡、自噬、焦亡、铁死亡及多种程序性细胞死亡途径的联合研究。
从发文作者分析,徐恩、高维娟、周晓红、祝美珍、王静、靳晓飞等在核心期刊发文较多,徐恩是缺血性脑卒中与程序性细胞死亡相关领域内核心期刊发文量最多的核心作者,可显示其致力于脑梗死的相关研究。
从研究机构分析,分布于科研合作网络中心的机构及多数科研合作主要集中在北京及省会城市,其他机构间合作较少,主要分布在同省域的高校及其附属机构之间,可能是由于地理位置较远,知识传递有阻碍导致的[7]。发文量较多的机构主要分布在一线城市或省会城市。一线城市及省会城市的科研资源较多,其高校及附属机构的科研产出能力较强,与学术方面的马太效应一致[8]。科研人员可加强跨团队和跨省域的学科交流,科研机构通过提高学科专业性,加强与其他机构间的合作,进一步提升科研机构的科研产出能力。
3.2 研究热点分析
缺血性脑卒中与程序性细胞死亡相关的研究热点作用机制集中在以下两方面:1)与程序性细胞死亡有关的缺血再灌注损伤机制,包括炎症反应、氧化应激;2)缺血性脑卒中的程序性细胞死亡途径,包括细胞凋亡、细胞焦亡、细胞自噬、铁死亡等。炎症反应的研究热点为脑梗死发生后不同阶段炎症反应损伤机制、炎症小体NOD样受体热蛋白结构域相关蛋白3(NLRP3)及小胶质细胞、T淋巴细胞[9-11]。氧化应激伴随炎症反应发生,氧化应激的研究热点为氧化应激与炎症反应、血脑屏障、细胞凋亡、自噬之间的相互作用[12-14]。焦亡机制与炎症反应密切相关,焦亡分为经典途径和非经典途径[15-17],研究热点主要包括gasdermin和Caspase(-1/-4/-5/-11)蛋白家族及炎症小体NLRP3[18],但目前非经典途径与缺血性脑卒中的关系尚未明确。自噬对脑缺血的作用机制存在争议,主要由哺乳动物雷帕霉素靶蛋白(mTOR)和单磷酸腺苷激活的蛋白激酶(AMPK)途径驱动[19],早期细胞自噬发挥着保护脑组织和神经的作用[20-22],但过度的自噬反应可引起细胞死亡[23-25]。有研究表明,铁死亡是由于缺血性脑卒中后铁代谢失衡,导致铁在细胞内大量堆积,促使大量的活性氧自由基产生,引起脂质过氧化和细胞死亡[26];同时细胞内铁离子增多加剧细胞自噬,不利于脑损伤恢复[27]。较少研究证实铁死亡与缺血性脑卒中直接相关。目前细胞焦亡、自噬及铁死亡的研究主要集中在细胞和动物实验方面,关于临床的研究证据仍有待补充。
缺血性脑卒中程序性细胞死亡的研究热点干预措施多为中医治疗,包括中药治疗、电针等。中医学将脑缺血归属于“中风”范畴,认为“气虚血瘀”为中风的关键致病原因,因此益气活血是治疗中风的重要原则。益气活血方药及其有效成分主要包括黄芪甲苷、人参皂苷、川芎嗪、脑泰方、补阳还五汤等[28],通过调节Notch、磷脂酰肌醇3-激酶(PI3K)/蛋白激酶B(AKT)、Janus激酶-信号传导子和转录激活子(JAK-STAT)、丝裂原活化蛋白激酶(MAPK)、Fas/FasL、Caspase信号通路抑制细胞凋亡[29]。黄芪甲苷通过下调核转录因子(NF)-κB蛋白表达抑制细胞凋亡,从而抑制氧化应激和炎症反应[30],并激活自噬机制减轻脑缺血再灌注损伤[31]。人参皂苷Rg1能通过抑制NADPH氧化酶异构体2-NOD样受体热蛋白结构域相关蛋白1(NOX2-NLRP1)通路、激活缺氧诱导因子-1α(HIF-1α)/血管内皮生长因子(VEGF)通路、调节跨膜受体卷曲蛋白1(FZD1)、piwi样RNA介导的基因沉默1(PIWIL1)、叉头盒蛋白M1(FOXM1)相关基因及蛋白的表达促进脑损伤恢复,改善神经功能[32-34]。川芎嗪通过抑制氧化应激和炎症反应改善细胞凋亡[35]。脑泰方通过调节SIRT1信号通路减少细胞凋亡[36],通过调控沉默休克因子1/热休克因子结合蛋白1(HSF1/HSPB1)通路抑制铁死亡,保护脑组织[37]。补阳还五汤通过AMPK/mTOR/UNC-51样激酶1(ULK1)信号通路抑制自噬,降低神经细胞凋亡率,保护大鼠神经功能[19]。电针“百会”穴可调节脑组织细胞焦亡底物蛋白消皮素D(GSDMD)表达,改善大鼠脑缺血神经损伤,通过JAK2/STAT3、MAPK信号通路下调靶蛋白减少细胞凋亡,从而减小脑梗死体积[38-40]。
综上所述,国内关于缺血性脑卒中与程序性细胞死亡领域的研究于2015年之前主要集中在细胞凋亡,因此关于坏死性凋亡、自噬、细胞焦亡、铁死亡等其他程序性细胞死亡途径对缺血性脑卒中的作用机制仍需深入探讨和完善;多数程序性细胞死亡研究仅停留在细胞和动物实验层面,临床研究存在不足。本研究仅纳入了中文文献,未纳入国外文献,缺失国外期刊发表的文献数据,因此,研究分析的准确性存在一定的偏倚。

