格拉斯哥预后评分对心力衰竭患者预后的预测价值
赵灿 王刚 刘霄燕 张娜 黄榕翀
目的:探讨格拉斯哥预后评分(Glasgow prognostic score, GPS)对心力衰竭患者预后的预测价值。
方法:回顾性分析2015年5月至2020年6月首都医科大学附属北京友谊医院收治的313例心力衰竭住院患者的临床资料并进行2年随访,按照GPS将患者分为三组:GPS 0分组(血清C反应蛋白≤10 mg/L且白蛋白≥35 g/L,n=138)、GPS 1分组(血清C反应蛋白>10 mg/L或白蛋白<35 g/L,n=115)、GPS 2分组(血清C反应蛋白>10 mg/L且白蛋白<35 g/L,n=60)。对三组患者的临床资料和2年随访结果进行统计学分析,采用Logistic回归模型分析GPS与心力衰竭患者2年全因死亡及心原性死亡风险的关系。
结果:随着GPS增加,2年全因死亡率和心原性死亡率均逐渐上升:GPS 0分组、GPS 1分组、GPS 2分组的2年全因死亡率分别为10.9%、25.2%、38.3%,2年心原性死亡率分别为7.2%、20.9%、35.0%(P均<0.001)。多因素Logistic回归分析显示,GPS较高是心力衰竭患者2年全因死亡(GPS 1分 vs. GPS 0分:OR=2.659,95% CI:1.229~5.756,P=0.013;GPS 2分 vs. GPS 0分:OR=3.858,95% CI:1.671~8.906,P=0.002)及心原性死亡(GPS 1分 vs. GPS 0分:OR=3.096,95% CI:1.244~7.703,P=0.015;GPS 2分 vs. GPS 0分:OR=4.507,95% CI:1.704~11.921,P=0.002)的独立危险因素。
结论:GPS可用于评估心力衰竭患者预后,GPS增加是心力衰竭患者2年预后的独立危险因素。
心力衰竭是各种心脏疾病的终末期阶段,是心内科常见也比较难治的一种疾病,严重影响患者的生活质量,已经成为影响我国居民健康的重要公共卫生问题。2020中国心力衰竭医疗质量控制报告显示,我国35岁以上居民中心力衰竭患病率为1.3%,估计患者数量约890万[1]。心力衰竭不仅患病率高,反复入院率、病死率也很高,因此,如何用简便的方法来评估心力衰竭患者的预后是一个值得研究的内容。
格拉斯哥预后评分(Glasgow prognostic score,GPS)是一个基于血清C反应蛋白和白蛋白两项指标的预后评分[2]。C反应蛋白及白蛋白都是临床上非常容易获取的指标,目前证据表明,GPS可预测某些癌症患者的预后[2]。然而,目前尚未证实GPS是否能预测心力衰竭患者的预后,国内相关研究甚少。鉴于此,本文旨在探讨GPS对心力衰竭患者预后的预测价值。
1 资料与方法
1.1 研究对象
选择2015年5月至2020年6月首都医科大学附属北京友谊医院心内科收治的389例≥18岁的心力衰竭患者[有心力衰竭的症状和体征,如呼吸困难、乏力、活动耐量受限及体液潴留;客观检查有心力衰竭的依据,如心脏收缩或舒张功能受损、N末端B型利钠肽原(NT-proBNP)升高]为研究对象,剔除急性炎症性疾病、自身免疫性疾病、服用免疫抑制剂、急性心肌梗死(包括ST段抬高型和非ST段抬高型心肌梗死)、急性脑卒中、先天性心脏病、妊娠患者;2年随访期间,60例患者失联,12例患者拒绝随访,4例患者因C反应蛋白数据缺失而被剔除,最终入组313例患者。本研究已获得首都医科大学附属北京友谊医院生命伦理委员会审查批准(批件号:2021-P2-415-01)。
1.2 研究方法
回顾性收集并分析所有患者的基线资料,包括年龄、性别及既往心力衰竭住院、吸烟、高血压、糖尿病、心房颤动、冠心病等病史、基本用药情况、实验室检查(包括C反应蛋白、白蛋白等)和影像学检查数据。
根据GPS标准将研究对象分组:血清C反应蛋白≤10 mg/L且白蛋白≥35 g/L为0分,设为GPS 0分组(n=138);血清C反应蛋白>10 mg/L或白蛋白<35 g/L为1分,设为GPS 1分组(n=115);血清C反应蛋白>10 mg/L且白蛋白<35 g/L为2分,设为GPS 2分组(n=60)。
对所有患者进行2年电话追踪随访,随访内容包括:2年全因死亡、心原性死亡、心力衰竭再入院情况。
1.3 统计学方法
采用SPSS 13.0软件对所有数据进行统计分析。正态分布的计量资料以均数±标准差表示,采用方差分析进行比较;不符合正态分布的计量资料以中位数(P25,P75)表示,采用非参数检验进行比较;计数资料以例(%)表示,多组间比较采用卡方检验。采用Logistic回归分析比较GPS 0分、GPS 1分、GPS 2分患者的2年全因死亡和心原性死亡风险。P<0.05为差异有统计学意义。
2 结果
2.1 三组患者的基线资料比较
313例患者的平均年龄为(69.5±12.8)岁,其中女性137例(43.8%)。GPS 0分组、GPS 1分组、GPS 2分组的中位年龄分别为69(67,71)岁、68(66,71)岁、72(69,76)岁,女性占比分别为47.1%、46.1%、31.7%(P均>0.05)。随着GPS增加,三组患者的入院心率、C反应蛋白、血肌酐、NT-proBNP水平升高,血钠、血红蛋白、白蛋白水平则下降(P均<0.05);另外,三组患者在血管紧张素转换酶抑制剂(ACEI)/血管紧张素Ⅱ受体拮抗剂(ARB)、低密度脂蛋白胆固醇方面的差异均有统计学意义(P均<0.05),在其余基线资料方面的差异均无统计学意义(P均>0.05),见表1。

表1 三组患者的基线资料比较[例(%)]
2.2 三组患者的2年随访结局比较
GPS 0分组、GPS 1分组、GPS 2分组的2年心力衰竭再入院率分别为31.9%、37.4%、33.3%,组间差异无统计学意义(P=0.647)。随着GPS增加,三组的2年全因死亡率(分别为10.9%、25.2%、38.3%)和心原性死亡率(分别为7.2%、20.9%、35.0%)均逐渐升高(P均<0.001),三组的非心原性死亡率则相似,分别为2.2%、2.6%、1.7%(P=0.921),见图1。以2年全因死亡和心力衰竭再入院作为复合终点进行分析,GPS 0分组、GPS 1分组、GPS 2分组的复合终点发生率分别为37.9%、49.6%、56.7%,差异仍有统计学意义(P<0.05);以2年心原性死亡和心力衰竭再入院作为复合终点时,三组的发生率分别为35.5%、47.0%、53.3%,差异也有统计学意义(P<0.05)。
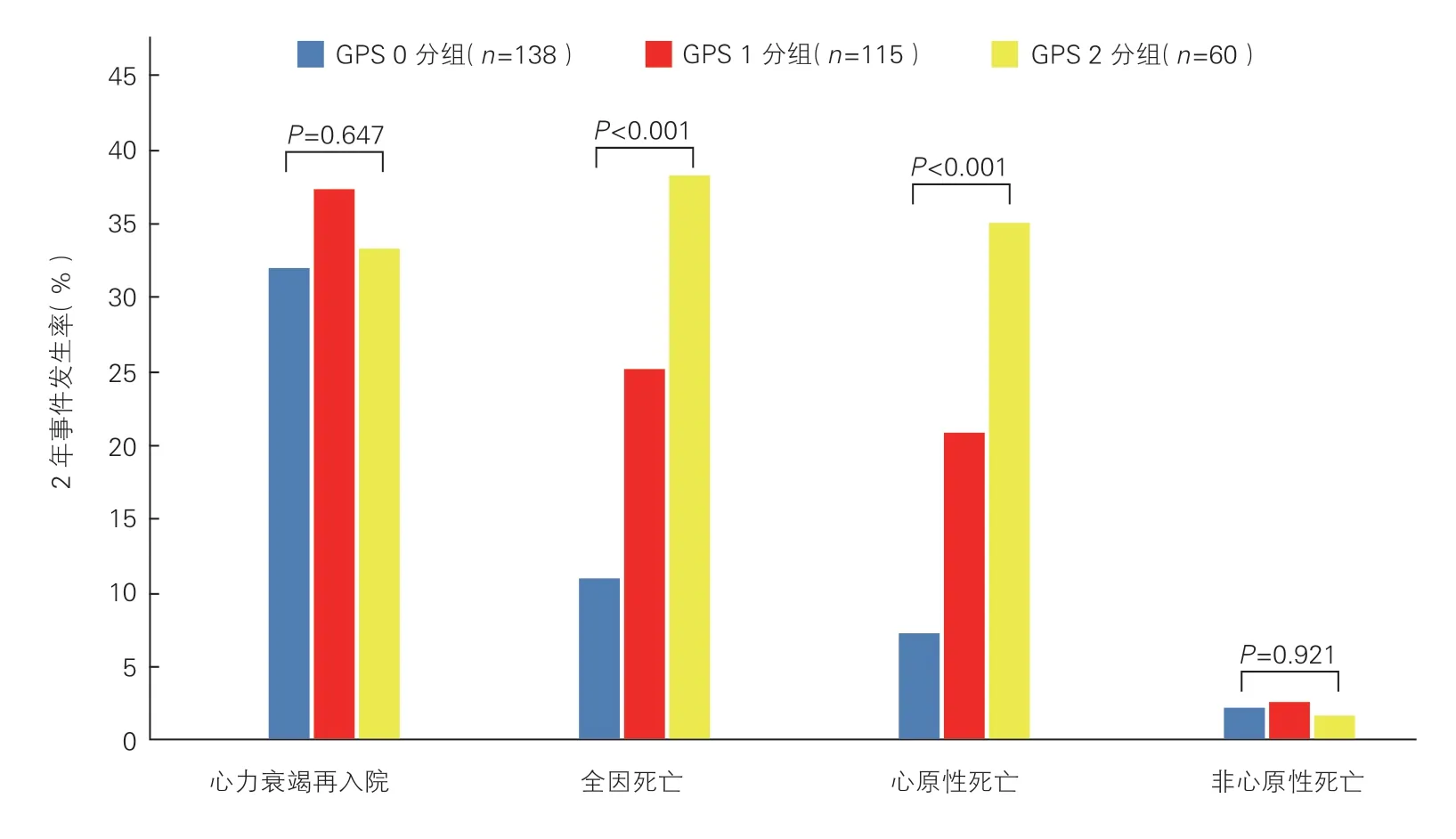
图1 三组患者的2年随访结局比较
2.3 心力衰竭患者2年全因死亡和心原性死亡的危险因素分析
单因素Logistic回归分析显示,GPS、年龄、既往心力衰竭入院、肾功能不全、NT-proBNP、β受体阻滞剂与心力衰竭患者的2年全因死亡和心原性死亡均有关,与心原性死亡有关的因素还包括高血压和体重指数。多因素Logistic回归分析显示,与GPS 0分患者相比,GPS 1分(OR=2.659,95% CI:1.229~5.756,P=0.013)和GPS 2分(OR=3.858,95%CI:1.671~8.906,P=0.002)患者的2年全因死亡风险均增加;年龄较大、既往心力衰竭入院、NT-proBNP较高也是心力衰竭患者2年全因死亡的独立危险因素,β受体阻滞剂则是保护因素(表2)。与GPS 0分患者相比,GPS 1分(OR=3.096,95% CI:1.244~7.703,P=0.015)和GPS 2分(OR=4.507,95% CI:1.704~11.921,P=0.002)患者的2年心原性死亡风险也均增加;高血压也是心力衰竭患者2年心原性死亡的独立危险因素,体重指数较高则是保护因素(表3)。
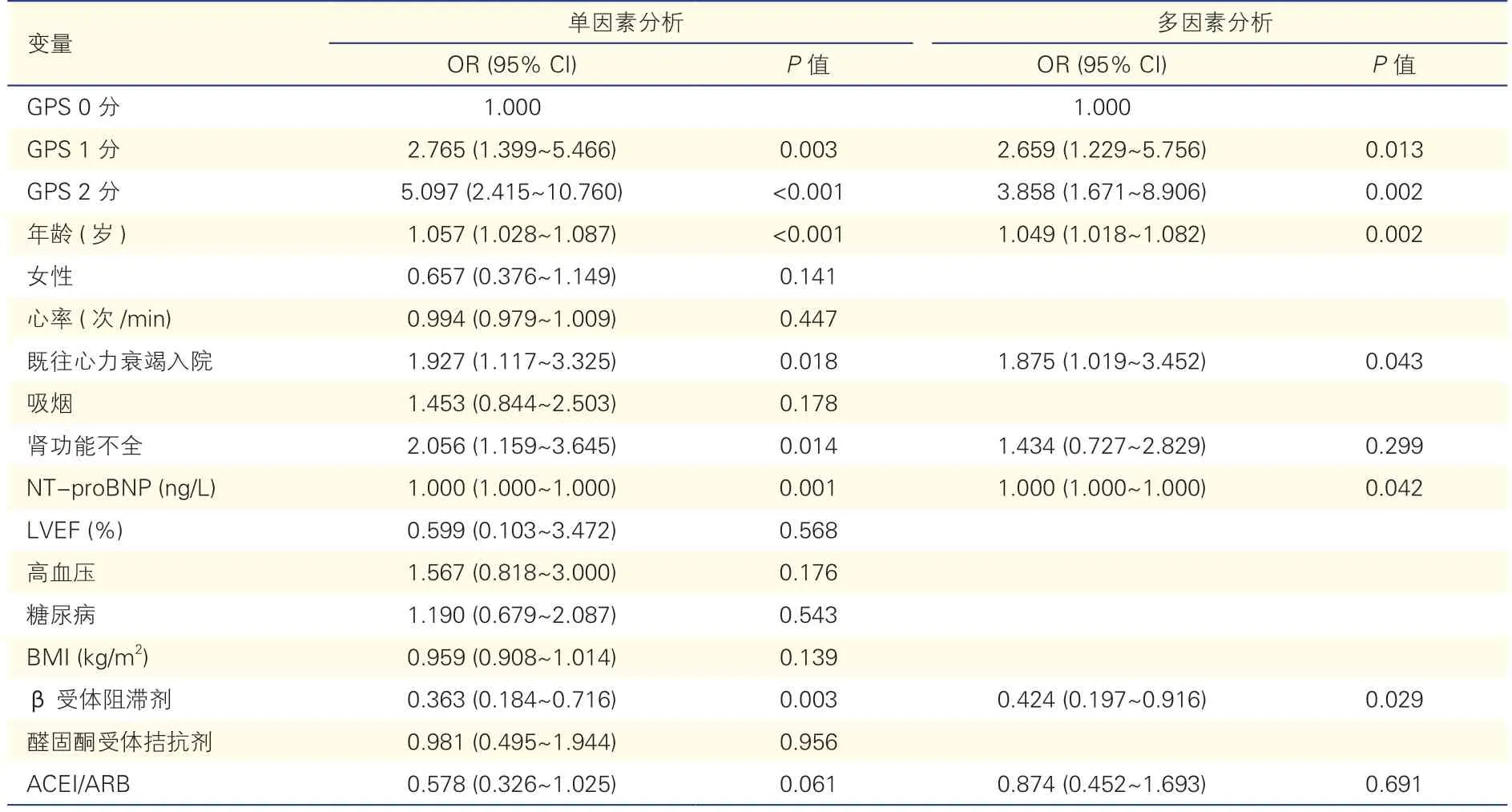
表2 心力衰竭患者2年全因死亡危险因素的单因素及多因素Logistic回归分析

表3 心力衰竭患者2年心原性死亡危险因素的单因素及多因素Logistic回归分析
3 讨论
炎症与心力衰竭密切相关,炎症机制参与心力衰竭的发生、发展过程,抑制炎症可改善心力衰竭患者的预后[3]。近年来,炎症机制及炎症相关生物标志物成为研究热点,各种炎症因子在心力衰竭病理生理过程中的作用被逐渐发现[4],比如半乳糖凝集素-3、生长分化因子15、肿瘤发生抑制蛋白2、肿瘤坏死因子α、高迁移率蛋白-1等。但这些炎症指标需要单独测定,不易获取且增加患者经济负担,多在科研中应用,而C反应蛋白是临床上非常常见且容易获取的炎症指标。
白蛋白也与心力衰竭有密切的关系,可预测心力衰竭患者的生存率。低蛋白血症在心力衰竭患者中非常常见,合并低蛋白血症的患者死亡率明显高于无低蛋白血症的患者,即使校正多个潜在混淆因素后,白蛋白水平仍可作为识别死亡风险较高的心力衰竭患者的生物标志物[5]。
C反应蛋白和白蛋白是GPS中的两个重要指标,既然C反应蛋白和白蛋白都与心力衰竭有关,GPS与心力衰竭可能也有关联。然而,目前关于GPS的研究多集中在癌症患者中开展[6],目前GPS已被确定为肺癌、胃食管癌、肝细胞癌、胰腺癌等多种癌症死亡率的可靠预测指标,成为癌症患者预后的有效评价指标[7-10]。Mohammed等[10]的研究表明,GPS越高,转移性胰腺癌患者的死亡率也越高,提示GPS有助于转移性胰腺癌患者的预后分层,避免虚弱患者过度治疗,其作为一个简单、实用的指标,可用于日常临床实践。
近年来,国外有学者开始用GPS来评价心力衰竭患者的预后[11-12]。Itagak等[12]的研究对870例心力衰竭患者进行了18个月的随访,发现随着GPS增加,心力衰竭的严重程度也增加;多因素分析显示,校正年龄、性别、血压、心力衰竭病史、血红蛋白、肾功能、血钠、B型利钠肽、左心室射血分数等因素后,与GPS 0分相比, GPS 2分与死亡风险增加有关(HR=2.92,95% CI:1.77~4.81,P<0.001),心原性死亡及非心原性死亡风险也均随着GPS增加而增加。
心力衰竭可通过室壁应激和释放细胞因子和其他炎症介质引起炎症,细胞因子和炎症介质参与心肌重构和泵功能障碍,最终导致心力衰竭进展[13]。心力衰竭患者的低蛋白血症与多个因素有关,比如代谢因素、吸收不良、对能量的需求高等,同时低蛋白血症又会通过增加外周及肺部血管的负荷,导致氧化应激及炎症反应恶化,进一步加重心力衰竭的严重程度[14]。一些客观的营养评价指标[如老年营养风险指数(GNRI)、预后营养指数(PNI)和控制营养状况(CONUT)评分]及炎症标志物(C反应蛋白等)已经被证实可克服白蛋白的缺陷[15],研究报道这些指标与心力衰竭的预后和严重程度相关,而营养评价指标和炎症标志物联用似乎对于评估心力衰竭患者的预后最有价值[12,16-17]。GPS恰好整合了营养评价指标和炎症标志物,可能会成为评估心力衰竭严重程度及预后的一种简单方法。
目前,评估GPS与心力衰竭相关性的研究较少,国内更是鲜有。本研究发现,随着GPS增加,GPS 0分组、GPS 1分组、GPS 2分组患者的C反应蛋白水平逐渐升高,这意味着评分越高,炎症反应越重;同样,随着GPS增加,三组患者的NT-proBNP水平也逐渐升高,而NT-proBNP是反映心力衰竭严重程度的指标[18],这说明GPS在一定程度上可反映心力衰竭的严重程度。2年随访结果显示,GPS 2分组的全因死亡率及心原性死亡率均高于GPS 1分组和GPS 0分组,说明GPS能评估心力衰竭患者的2年预后,GPS评分高是心力衰竭患者预后不良的独立危险因素。这提示可利用GPS来预测心力衰竭患者的全因死亡及心原性死亡风险,及早识别高风险患者并及时采取更积极的干预措施。
本研究的不足之处:(1)本研究为单中心回顾性研究,样本量偏小,且有部分患者失访,后续需增加样本量进一步研究;(2)由于随访时部分患者家属不能提供准确的死亡时间,所以未能进行COX回归分析,后续需开展前瞻性研究,以获得更好的证据。
总之,本研究结果初步表明,GPS可预测住院心力衰竭患者的预后。GPS为一个经济、简便易得的指标,临床医师可考虑利用GPS来识别高风险心力衰竭患者,从而尽早给予积极的干预措施,最终改善患者的预后。
利益冲突:所有作者均声明不存在利益冲突
——兼与亚当·斯密《道德情操论》比较

