黄铁矿与砷黄铁矿氧化浮选分离技术的研究进展
贾紫珮,宋翔宇,王文,许来福,张红涛
(郑州大学化工学院,河南 郑州 450001)
黄铁矿(又名硫铁矿,FeS2)是地壳中分布最广的硫化矿物之一,普遍存在于各种类型的岩石矿床中,世界主要产地有西班牙、捷克、斯洛伐克、美国和中国。砷黄铁矿(又名毒砂,FeAsS)是一种极为重要的含砷的黄铁矿类型,世界70%的储量集中在中国。自然界中黄铁矿和砷黄铁矿广泛共存[1],矿物加工领域内砷黄铁矿与黄铁矿的分离通常简称为砷硫分离。而金常与黄铁矿、砷黄铁矿相伴相生[2-3],冶炼过程中常会面临砷含量过高,造成空气污染等问题[4]。因此无论是黄铁矿冶炼制备硫酸还是硫化金矿冶炼提金,都需要进行砷硫分离,然后将含砷矿采用特殊冶炼工艺进行处理。
黄铁矿和砷黄铁矿拥有相似的晶体结构和表面性质,它们的可浮性相似彼此难以分离[5-6]。Allison等[4]研究发现,黄铁矿和毒砂在pH值为7的乙基钾黄药中的剩余电位相同,而黄药与两种矿物表面相互作用后都会形成产物二黄原,两种
矿物中的自然氧化速率也非常相似,这些行为使得砷硫矿物分离变得困难。
黄铁矿和砷黄铁矿一般通过抑砷浮硫的方法进行分离,为达到分离的效果会大量使用各种抑制剂[7],对环境造成了很大的污染和破坏,且存在浮选分离工艺复杂、抑制剂生产成本高等缺点。鉴于以上情况,国内外学者提出了一些新的分离技术,尤其是氧化浮选分离技术,其中包括如氧化剂浮选[8]、生物浮选、外控电位浮选。氧化浮选法是利用氧化剂或特殊氧化工艺处理砷硫矿物,使得其中某个矿物表面发生电化学反应,生成亲水或疏水反应产物,提高或降低浮选行为,实现毒砂和黄铁矿的分离。本文总结了砷硫氧化浮选分离工艺的研究现状,并对砷硫分离技术的研究进展作了重点介绍,以期望对从事砷硫分离工作的选矿技术人员有所帮助。
1 砷硫矿物晶体结构与表面特性
矿物的晶体结构与表面特性是影响矿物可浮
性极为重要的关键因素,研究矿物的结构特性、晶格特点、化学成分、表面性质的差异,对提高矿物间浮选分离水平意义重大。
1.1 黄铁矿的结构特性
普通黄铁矿晶体结构为立方体结构,属等轴晶系,其晶胞具有Th6-Pa3空间群,具有良好的对称性。其晶体结构中,每个硫原子与三个Fe原子配位并与另一个硫原子键合[9]。鉴于铁和硫的电负性不同,学者猜测黄铁矿中的键合主要是共价键。而黄铁矿中相对较短的Fe-S键距也证明了键的本质是共价键[10]。黄铁矿的理想组成S/Fe的比率应该接近2,但实际上黄铁矿中通常含有微量元素,包括Ag、As、Au等,微量元素的掺杂会使黄铁矿的性质发生改变[11]。
黄铁矿破碎解离的过程中其原子间饱和的化学键被打断,在其表面形成不饱和的悬挂键,这些不饱和键决定了黄铁矿的晶面特性。而经过解理过的黄铁矿晶体,其表面的Fe原子与S原子会产生配位不足的情况,黄铁矿表面出现大量的悬挂键,而黄铁矿周围的H2O、O2会与配位不足的Fe、S结合,从而形成表面氧化。
1.2 毒砂的结构特性
砷在环境中的存在形式主要是硫化矿物,其中砷黄铁矿是最重要含砷矿物,化学式为 FeAsS,其含砷量高达 46%。普通砷黄铁矿单晶体常以柱状呈现,属单斜晶系斜方柱晶类,其晶胞具有P21/c空间群[11]。砷黄铁矿的晶胞包含四个FeAsS单元,其中的阴离子为AsS3-,阳离子(Fe)由六个阴离子八面体配位,每个阴离子由三个Fe离子和一个其他阴离子四面体配位。毒砂与黄铁矿的主要区别在于其表面存在更多的活性砷位点。但毒砂晶体中的Fe-S键和黄铁矿表面的Fe-S键具有相似性[12],因此二者具有相近的表面特性。
2 砷硫矿物表面氧化机理
2.1 黄铁矿表面氧化机理
黄铁矿的氧化在环境保护和技术应用中有着很重要的地位,自从发现黄铁矿氧化会形成酸性矿山废水(AMD)后,在氧气和水的条件下进行了大量的研究[13],目前普遍认为的黄铁矿在氧气和水存在的环境的反应式见(1~3)
黄铁矿在水和氧气的环境下,O2、H2O会先作用于黄铁矿表面能较高的位置,表面被氧化而生成Fe2+、硫酸根离子等,生成的Fe2+继续被氧气氧化生成Fe3+,Fe3+会继续与黄铁矿表面发生反应,产生大量的Fe2+,而Fe2+又会与氧气反应为Fe3+,以此循环往复直至黄铁矿被完全反应。且Eggleston等[14]利用XPS等分析手段,提出了黄铁矿反应机制中的一个关键特征就是Fe2+和Fe3+之间发生重复转化且速率较快,而Fe转化为Fe2+或Fe3+相对较慢,因此反应式(2)控制着黄铁矿氧化的最终速率[15]。
同时又因为黄铁矿是良好的半导体材料,其氧化时会涉及电子转移,因此对黄铁矿进行了电化学研究,有学者[16]在pH值为2的电解池中,检测了黄铁矿的线性扫描伏安曲线(LSV)和循环伏安曲线(CV),LSV曲线表明抛光过的黄铁矿存在三个区域:活化区、钝化区、后钝化区(见图1),黄铁矿的CV曲线见图2。

图1 黄铁矿电极线性扫描伏安曲线Fig.1 Linear sweep voltammetry curve of a pyrite electrode
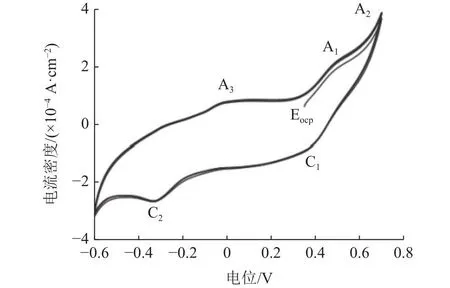
图2 黄铁矿的CV曲线Fig.2 Cyclic voltammetry curves for FeS2
从静息电位到0.5 V之间为黄铁矿的活化区,期间主要生成产物为SL(主要为S0、少量Fe1-XS2、Sn),见式(4);而电位范围在0.5~0.6 V间时,为钝化区,可以看出电流上升速度减缓,并不随着电压的升高而升高,对此现象有不同的观点,但大多数认为在活化区形成的SL会覆盖在黄铁矿表面,从而阻碍了氧化的进一步进行;随着电位升高至0.6 V以上时,形成的钝化层会发生破裂,使得黄铁矿表面重新暴露,氧化继续进行见式(5)~(6)。如果电位继续升高至0.7 V以上,黄铁矿表面生成的单质硫、多硫化物(Sn2-)、Fe(OH)3等越积越多,使得氧化速率降低。
而CV曲线结果与上述LSV曲线一致,可以看出在0.5 V左右出现了氧化峰,对应着反应式(4),即生成了SL与Fe(OH)3,尽管在早期对黄铁矿的研究认为[17],低电压下黄铁矿表面产物为S0与Fe3+,随着研究发现,黄铁矿在低电位时,Fe溶解至电解液中,同时黄铁矿表面生成一层富硫层(钝化层SL),随着电位的升高,在0.7 V左右又出现了氧化峰,电压升高,表面形成的S0与重新暴露出来的黄铁矿一同被氧化。
黄铁矿的浮选分离同样可以利用黄铁矿的表面氧化,有学者对黄铁矿进行了无捕收剂泡沫浮选实验[18],研究发现黄铁矿在表面氧化后,具有较好的可浮性,其氧化过程中生成的S0、FeSn、Fe1-XS2通常被称为富硫物种,它们被认为能增强黄铁矿的疏水性,从而使黄铁矿漂浮。
纵使对黄铁矿进行了诸多研究,但从分子水平上理解其氧化过程却仍是个挑战,根据Basolo和Pearson[19]的理论,氧化还原反应的基本步骤几乎总是一次只转移一个电子。因此二硫化物的氧化需将七个电子从每个硫原子通过半导体晶体转移到氧化剂,此过程涉及多个步骤,这也意味着对黄铁矿氧化的研究更为复杂和困难。经过大量的实验Williamson和Rimstidt等[20]得出了黄铁矿氧化的速度定律,并在此研究基础上建立了黄铁矿氧化模型,利用水氧化过程来揭示每个基本反应步骤,从而确定反应机制和速率。模型将黄铁矿的表面氧化划分为三个不同的步骤。这三个步骤分别是阴极反应、电子传输和阳极反应。
早期对黄铁矿中硫的研究认为,黄铁矿氧化时其中的硫转变为S0,尽管在实验中并没有检测到S0,研究者认为是溶液中存在的Fe3+将S0氧化成SO42-的结果。但也存在不同看法,一些观点认为[21],硫是先被氧化成S2O32-,进而被氧化为SO42-。当时的研究还有一种观点认为S的氧化取决于pH值[22],高pH值下S-SO3完全电离,使大部分S以S2O32-的形式释放到溶液中,而低pH值下,大部分S-SO3基团保持一个质子,与水反应会形成SO42-,最后SO42-被释放到溶液中。
随着计算理论的深入,对黄铁矿氧化的探究也从最初的电化学法转向基于量子力学的第一性原理理论计算法。现在对黄铁矿氧化步骤的研究多是基于密度泛函理论[23],Zhu等[24]将黄铁矿在空气中的氧化划分为四个路径。反应的初始是表面Fe(II)转化为Fe(III)–OH-;然后形成的Fe(III)-OH-将表面S(-I)氧化为S(0)–OH或S(I)=O;初始形成的Fe(III)–OH-再进一步氧化,将S(0)–OH或S(I)=O氧化为S2O32-、SO32-或SO42-;最后O2将S2O32-、SO32-氧化为SO42-。
综上所述,对于黄铁矿的氧化,在氧气和水存在的环境下,矿物表面Fe能被氧化成Fe2+、Fe3+,并且后两者之间同时存在相互转化行为,该转化反应速率决定着黄铁矿氧化的最终速率。黄铁矿光滑表面在不同电位下氧化过程中,静息电位到0.5 V和0.6~0.7 V两个范围内,表现出氧化活跃区间,氧化过程中主要生产物为SL,随着电位提高,生成的中间反应产物会覆盖在黄铁矿表面形成钝化层限制氧化进一步进行。目前研究黄铁矿氧化过程形成诸多观点:(1)溶液中存在的Fe3+将S0氧化成SO42-;(2) S氧化的速率取决于pH值;(3)中间反应物Fe(Ⅲ)-OH-在O2参与下促进S氧化为SO42-。黄铁矿氧化过程中活跃条件参数能够直接影响黄铁矿的浮选行为,因此通过控制黄铁矿的氧化过程,可以有效改善黄铁矿的浮选效果。
2.2 砷黄铁矿表面氧化机理
1988年,Buckley等[25]对砷黄铁矿氧化率先做出研究,他们认为等摩尔比的铁、砷和硫以相同速率氧化,并用以下反应式表示氧化的机制:
其中y>x;b≤1.5
但随着研究的深入,学者们提出了不同的看法,Nesbitt等[26]将砷黄铁矿暴露在空气中14 d,大约一半的Fe和As呈氧化形式,而只有不到20%的硫被氧化成硫酸盐或硫代硫酸盐,结果表明硫的氧化速率低于Fe和As的空气氧化速率。随着越来越多研究表明空气中的氧化速率为As≥Fe>S。而为了解释这个现象,Costa M等[27]对比了在空气中暴露16个月和25年的砷黄铁矿,发现其中二硫化物的百分含量与暴露14 d的砷黄铁矿变化不大,明显的二硫化物氧化在与空气反应不超过14 d后停止。而大约70%形成的所有Fe(III)-羟基氧化物是在氧化的前两周内产生的,并在16个月内完成,与S和Fe不同的是砷在25年的暴露时间中会持续与空气发生反应。目前普遍把这种差异性氧化归因于砷黄铁矿表面氧化覆层的形成。认为该包覆层由硫酸铁、亚砷酸铁和砷酸铁组成。研究表明,氧化层的形成需几周到几个月,氧化的覆盖层虽然只有几十埃厚,但一旦形成便可以防止氧气渗透到下面的毒砂中。阻止氧化的进行。
与黄铁矿相比毒砂更易发生氧化反应,而毒砂和黄铁矿的分离也多利用这一点,使毒砂产生亲水性,达到与黄铁矿分离的结果,而目前关于毒砂氧化的研究还面临许多问题,虽然在毒砂氧化的总反应方程式上已经达成共识,见式(8)[28]:
但其中As2+、As4+一般检测不到。实验结果发现,砷黄铁矿在水中氧化比在空气氧化所得砷氧化物的比例更高,两种氧化的氧化机制和氧化产物大致类似,不同是水溶液中氧化有硫酸根出现。Schaufuss A G等研究了砷黄铁矿在空气中和氧气中氧化,并进行了对比实验[30],结果显示,在氧气中氧化时,砷黄铁矿的表面被由砷和铁的氧化物质组成的层覆盖,而在空气中氧化,砷黄铁矿氧化层的顶部由Fe和O组成见图3。

图3 在氧气暴露期间形成的氧化层结构 (a) 氧气下;(b) 空气下Fig.3 Structure of oxidized layers formed during oxygen exposure (a) O2; (b) air
在氧气中氧化时,铁多以二价铁形式存在,三价铁的含量很少,其他产物分别为As(I)、As(II)、As(III)、亚硫酸盐及二硫化物,未见三价铁的氧化物和氢氧化物,在空气中氧化时,产物大多为砷的氧化物和氢氧化铁,以及少量Fe-As结合物。
综上所述,对于砷黄铁矿的氧化,在空气、水、氧气中的反应有明显差异。空气中砷最先被氧化且一直持续进行,Fe的氧化速率与As相似,但到一定时间后速率急剧下降,S氧化反应速率远低于As和Fe。水中砷黄铁矿的氧化机制和氧化产物与空气中相似,相比之下前者的砷氧化物比例更高。砷黄铁矿在氧气中氧化时,表面多被As、Fe的氧化物覆盖,而其他氧化条件下覆盖层多由Fe和O组成。因此,可以通过添加氧化剂持续加速砷黄铁矿的氧化速率,提高其亲水性,强化浮选过程中对砷黄铁矿的抑制效果。
3 砷硫矿物氧化浮选分离机理
Corkhill等[31]研究了黄铁矿(FeS2)和毒砂(FeAsS)的电子和化学结构。结果表明,黄铁矿的最高占据分子轨道(HOMO)中的Fe 3d轨道系数(0.292)远大于S 3p(0.0935),而在毒砂的HOMO中的Fe 3d轨道系数(0.323)最大,其次是As 4p(0.265),然后是S 3p(0.124)。基于HOMO的轨道系数,Fe原子将是黄铁矿与氧相互作用最活跃的位点,而Fe、S和As原子都可能成为毒砂的反应位点。与Schaufuss等[32]的结果一致,即在氧化环境中As比Fe更具反应性,因此As可能是毒砂表面最有利于氧化物质吸附的原子,从而促进砷氧化物和砷酸盐(如H3AsO3和H3AsO4)的产生。
为研究氧在毒砂表面的氧化机理,Chen等[33]计算了氧分子在毒砂表面不同吸附位点的吸附能、几何构型和电荷转移。毒砂(001)表面的氧分子具有三种稳定的构型。氧分子主要以水平构型吸附在毒砂表面的Fe和As原子。当氧分子吸附在Fe2-As2位点时,能量为-160.69 kJ/mol,吸附在Fe2-As2位点时,吸附能为-130.32 kJ/mol,吸附在 As2-Fe1 位点时,能量为-119.50 kJ/mol。Fe2-As2位点上氧分子的吸附能最大,吸附构型最稳定。因此氧分子更容易吸附在毒砂表面的Fe2-As2位点上。而毒砂表面氧分子的吸附能显着高于黄铁矿表面。
由于毒砂表面易氧化,黄铁矿具有较好的可浮性,因此,硫砷矿物的浮选分离常采用抑砷浮硫工艺。毒砂被抑制的原理可能与矿物表面氧化的增加或吸附的捕收剂物质氧化成亲水形式或与这两种机制都有关[34],Chen[35]等测量了黄铁矿和毒砂在不同氧化剂下的循环伏安曲线,根据毒砂的氧化峰,得到反应式(9~10)
反应生成的HAsO42-、H2AsO42-会在后续进一步发生反应,同时与Fe(OH)3形成亲水薄膜,使得捕收剂不能吸附在毒砂表面,达到抑制毒砂的目的[36]。
根据电镜观察,贴在弯管段不同试验贴片的表面蚀坑具有不同形态特征。用扫描电镜自带的能谱分析软件对试验贴片的化学元素做了定性分析,受20~40目粒径的砂粒冲蚀后,20号碳钢贴片表面氧元素含量较高,有明显的腐蚀增强作用。对其他粒径冲蚀的贴片进行能谱分析亦发现:20~40目砂粒冲蚀后的X80管线钢表面的氧元素与冲蚀试验之前相比有所减少,说明含砂水流在冲蚀过程中冲掉了部分腐蚀产物,此时冲蚀大于腐蚀。
4 砷硫矿物氧化浮选分离的工艺实践
随着研究的深入,传统方法暴露出很多缺陷,如污染严重、浮选分离效果不好等,现急需寻找绿色、高效的浮选分离手段。氧化法分离毒砂和黄铁矿其本质是选择性将毒砂氧化,使其表面的疏水性降低,而黄铁矿表面依旧保持较好的疏水性,使两者可浮性增大,从而达到分离的目的[37]。氧化分离法主要包括:氧化剂法、生物氧化法以及对外控电位[38]进行氧化法。
4.1 化学药剂氧化处理工艺
氧化分离法多采用氧化剂法,向矿浆中加入氧化剂或注入空气。氧化剂多为KMnO4、Ca(ClO)2、漂白粉、K2CrO7、H2O2[39]等。学者将这些氧化剂做了对比研究,发现不同的氧化剂对毒砂的抑制效果不一样且对毒砂和黄铁矿的选择性也不同。
许大洪[40]在对长坡选矿厂选锌尾矿进行有价元素的综合回收中,先采用混合浮选工艺,将含砷硫化矿与锡石和脉石矿物浮选分离,再采用腐植酸钠与H2O2的组合药剂抑制毒砂,最终实现了硫砷矿物浮选分离。硫品位由28.26%提升至46.46%,砷品位由2.05%降为0.88%,砷的回收率达84.68%。
Liu等[41]采用环保型有机氧化剂过氧乙酸(PAA, CH3C(=O)OOH),在中性pH值条件下有效抑制毒砂。氧化浮选结果表明,毒砂和PAA表面之间存在强烈的相互作用,PAA可以强烈氧化毒砂表面,生成大量含氧物质,如As(III)-O、As(V)-O、Fe(III)-O、Fe(III)-SO、SO32-、SO42-,当这些氧化物的含量分别从47.13%、14.95%、45.94%增加到88.56%、45.49%、81.57%后,单矿物浮选实验结果显示,PAA对毒砂产生较强的抑制作用,其泡沫回收率从90%降低到 3%。
Dong等[42]研究了新型氧化剂二氧化氯对毒砂的氧化,用扫描电子显微镜(SEM)拍摄的图可清晰的显示,氧化剂使光滑的毒砂表面产生裂纹、孔隙,直至被完全氧化。且低浓度的二氧化氯溶液无毒且环保,因此,二氧化氯优于其他化学氧化剂。该研究中使用的毒砂氧化法不需要高温、高压或其他耗能的实验条件,相较于在酸性毒砂矿浆中使用NaClO2产生ClO2的方法,二氧化氯反应迅速,简单易操作。这种创新的方法具有巨大的潜力。
综上而言,氧化剂法虽然简单方便,可以显著增加毒砂和其他硫化矿的可浮性差异,使毒砂的可浮性下降,但是由于氧化剂同时也作用于其他矿物和浮选药剂,从而使得浮选过程难以操作和控制,导致在工业上难以广泛运用。
4.2 生物氧化处理工艺
随着微生物技术在矿物分选领域的推广与应用,利用生物预氧化技术处理含砷硫化矿也日渐成熟。生物浮选工艺是通过微生物对矿物选择性吸附行为改变矿物表面性质,实现浮选过程中从黄铁矿中分离毒砂的方法。与黄铁矿相比,细菌在毒砂表面的粘附非常缓慢,而对黄铁矿的黏附力更高。这导致在与细胞相互作用后矿物的表面改性存在差异。在捕收剂的作用下,这些细胞能够有效地抑制黄铁矿浮选。
Chandraprabha M.N.等[43]讨论了在pH值条件下,利用氧化亚铁硫杆菌生物调节选择性抑制毒砂中的黄铁矿。TfH6菌在黄铁矿上的黏附的很坚固和迅速,即使在黄药的存在下,黄铁矿依旧保持亲水性。另一方面,即使黄铜矿与细菌细胞相互作用后,在捕收剂的作用下也能够使黄铜矿具有良好的可浮性。由于细胞与矿物表面的附着动力学较差,Cu+活化的毒砂能够在细胞存在的情况下保持其疏水性。因此,通过对细胞和收集器进行适当的调节,可以有效地将黄铁矿从黄铜矿和毒砂中抑制出来。
Zhang等[44]为含高浓度砷、硫的低品位难处理金矿石提供了一种新的预处理方法,提出了一种有效且经济的柱式生物氧化法,可显着提高金的浸出效率。此外研究还发现,在比较不同氧化时间下黄铁矿和毒砂表面的腐蚀形貌,表明毒砂比黄铁矿更容易被生物氧化。这可能是由于黄铁矿的氧化还原电位远高于毒砂的氧化还原电位。
生物浮选中对微生物的运用与浮选药剂很相似,因此微生物可作为浮选药剂作用于浮选分离的实验中,此种方法的缺陷是,当前研发出的微生物种类较少,且大多停留在理论研究方面,在工业中的应用还未曾实现。
4.3 外控电位氧化处理工艺
外控电位硫化法在硫化物和氧化物浮选中显示出前景[45],控制电位的方式有两种:氧还原药剂调控和外加电场电位调控[46],在外控电位浮选体系中,不同的电极材料具有不同的表面静电位,与硫化矿物的表面静电位腐蚀电位存在差异,浮选过程中电极与硫化矿物颗粒发生碰撞接触时形成电偶腐蚀[47]。硫化矿发生电偶腐蚀后,其表面会产生亲水性或疏水性物质,这是发生浮选分离的关键。
邓玉珍[48]在黄铁矿和砷黄铁矿的矿石选别时,加入0.5~5.5 kg/t Na2CO3,并施加电场,获得的黄铁矿精矿含硫51.62%、含砷0.55%~1.02%,同时还对比了黄铁矿在氦气、空气环境下进行电化学时的可浮性变化,发现在空气下黄铁矿天然可浮性最大值出现在集流器电位为-700 mV,与未进行电化学处理的浮选相比,其回收率增加了4.4%。王荣生[49]考查了不同矿浆pH值时外控电位处理下的黄铁矿浮选行为,通过实验发现,在乙基黄药、酸性环境下外控电位法对黄铁矿的浮选行为的影响不显著;而在乙基黄药、碱性环境下,外控电位对黄铁矿浮选行为影响显著且在400~800 mV电位间黄铁矿回收率大幅升高。机理研究表明黄铁矿可浮性改善的原因可能是表面氧化生成S0及S02;同时矿浆中矿粒表面及附近的乙基黄药氧化生成了双黄原。
外控电位法通过添加外加电极使矿物颗粒表面发生化学反应,生成具有疏水性或亲水性的氧化产物。同时也与矿浆体系中pH值关系密切,只有在合适的pH值环境下,矿物受到外控电位作用才可以呈现良好的自诱导可浮性。由于硫化矿浮选矿浆体系的复杂性影响,许多物质都可能会附着在电极上形成覆盖层,从而增加了矿浆颗粒与电极持续发生反应的难度。
综上所述,虽然各种氧化处理的氧化剂或氧化工艺各不相同,但是都是通过促使毒砂或黄铁矿颗粒表面发生电化学反应,生成亲水性或疏水性化学反应物改变矿物的浮选行为,强化黄铁矿和砷黄铁矿之间的性质差异,达到砷硫分离的目的。
5 结论与展望
黄铁矿和砷黄铁矿在密度、比磁化率、电性质、晶体结构和表面性质等方面均十分近似,采用常规的重磁浮选工艺难以实现有效分离。研究表明,二者在表面氧化性质上存在较大差异,砷黄铁矿更容易氧化,因此,研究如何充分扩大二者的氧化性差异,对实现二者的高效分离具有重要意义。目前国内外研究人员对砷硫矿物氧化分离研究取得了许多科研成果,尤其是化学药剂氧化处理工艺相对较成熟,但是仍然面临诸多问题。例如化学氧化剂选择性差,容易失效,生物氧化处理可选择的微生物种类较少,培养过程复杂,外控电位氧化工艺中矿浆体系的复杂性决定电极接触或吸附的矿物选择性较低。
目前国内外关于砷硫分离的方法仍以抑砷浮硫的浮选工艺为主,存在着抑制剂用量大、有毒、污染环境等缺点,绿色氧化浮选分离的方法能够有效克服上述缺点,是一个具有较好工业应用前景的研究方向。黄铁矿和砷黄铁矿也是常见的金的载体硫化矿物,金精矿含砷无疑会给金的冶炼提取带来困难,环保要求含砷的金精矿需要单独处理并回收其中的砷。因此,砷硫的绿色高效分离对于黄金工业也具有重要意义。

