五步法流程化腹腔镜肝右后叶切除(附47例报告)
郝星源,刘符生,刘彬,李晶华,王海涛,廖铂,常磊,何跃明,张中林,袁玉峰
武汉大学中南医院肝胆胰外科,湖北 武汉 430071
随着腹腔镜技术的推广普及和相关手术器械的更新迭代,腹腔镜肝切除的适应证在近年来不断扩大,自2007年以来,腹腔镜肝切除术的比例逐渐增多[1]。然而,右后叶、肝中叶和尾状叶等复杂困难部位肝切除术的腹腔镜操作仍然面临挑战。肝右后叶位于腹腔深部,约占肝脏体积的1/3,腹腔镜下不易显露手术视野,相比于右半肝切除术,右后叶手术切线更长,断肝平面更大,断肝过程中容易发生切线和切面偏离。右后叶切除的扇形切面涉及多支重要血管,静脉变异繁杂,除了肝右静脉之外,还包括右后下静脉等肝短静脉,术中容易发生肝右静脉及其分支静脉破裂出血,以上特征使得腹腔镜下右后叶切除术成为腹腔镜肝切除的“困难”级术式之一[2-3]。目前国内外各个肝脏中心在腹腔镜右后叶切除术中均积累了不同的手术模式和经验[4-5],这些手术方案在达到成功切除的目标下进行了多种细节的尝试和改进,以调整适应不同的手术条件及情景。笔者所在中心曾介绍了吲哚菁绿(indocyanine green,ICG)引导的腹腔镜下右后叶解剖性切除手术方案,随着手术病例和经验的积累,我们总结了本中心在腹腔镜下右后叶切除的流程化手术方案[6],以左侧卧位,优先离断尾状突处理右后肝蒂,ICG荧光引导,原位断肝,循下腔静脉前间隙和肝右静脉轴线引导肝实质离断平面为要点实施手术,可达到安全有效的手术目的。我们对近3年实施的腹腔镜下流程化肝右后叶切除手术的47例病人资料进行了回顾性分析,现报告如下。
资料与方法
一、病例选择及临床资料
回顾性收集2020年5月至2023年3月在武汉大学中南医院肝胆胰外科行腹腔镜肝右后叶切除手术病人的临床资料,分析其手术经过和围术期信息。本研究经武汉大学中南医院伦理委员会审核批准(批件号:科伦〔2020100〕),所有病人均已签署书面知情同意书。手术适应证包括:(1)位于右后叶的肝脏良、恶性病变,具有相应疾病的手术切除指征;(2)肝功能Child-Pugh分级为A级,ICG 15 min滞留率(ICG-R15)<20%;肝脏剩余体积足够,能承受腹腔镜肝切除术;(3)体力状况分级(ZPS)0~2级,Karnofsky评分≥60分。
47例病人中男性38例(80.9%),病人年龄为(55.9±11.2)岁,体重指数为(23.8±3.5) kg/m2。41例病人美国麻醉医师协会(ASA)分级为Ⅱ级,有4例病人ASA分级为Ⅲ级。所有病人美国东部肿瘤协作组(ECOG)评分均在0~2分。(表1)

表1 47例腹腔镜下流程化肝右后叶切除术病人一般信息
二、手术方法
(一)术前评估与规划
完善术前肝脏基础情况评估,包括病灶体积,肝功能分级及ICG-R15试验,术前影像学检查包括上腹部增强CT、磁共振增强(普美显)评估门静脉右支和肝右动脉分支变异情况,肝右静脉是否存在异常分支,是否存在右后下静脉或右后中静脉等肝短静脉。基于增强CT图像行肝脏三维重建,评估病灶与主要脉管的毗邻关系,制定手术切线及断面,规划手术切除范围。
(二)体位与Trocar孔布局
根据肿瘤的部位、大小制定个性化手术体位及Trocar孔布局。病变主体位于右后区予以左侧卧位、四孔或五孔Trocar布局。四孔布局:以右肋缘下10 cm腹直肌旁线交界处进10 mm Trocar作为观察孔,气腹压力维持在12~14 mmHg(1 mmHg=0.133 kPa);主操作孔位于右腋前线肋下约5 cm,辅助孔位于右腹直肌旁线肋下5 cm;再于肋缘下右腋后线处置入5 mm Trocar作辅助孔。五孔布局是在上述四孔布局的基础上于剑突下置入10 mm Trocar作辅助孔(图1A)。

图1 五步法流程化腹腔镜肝右后叶切除 A.体位及Trocar孔布局;B.优化处理尾状突(B1)及右后肝蒂(B2);C.肝右后叶荧光反染膈面观(C1)及脏面观(C2);D.循肝右静脉(D1)及荧光边界(D2)原位断肝;E.肝后下腔静脉前间隙及肝右静脉轴线引导断肝平面,由足侧向头侧(E1),由浅入深、深浅结合(E2);F.右后叶切除后肝断面
(三)ICG染色剂量
ICG使用剂量与方法遵照此前推荐的普适性推广给药方案[7],即:1/1 000 ICG原药浓度的工作液,经外周静脉注射10~20 mL,可根据目标肝段体积及不同荧光机器的ICG光敏特点酌情调整。
(四)手术步骤
优化后的程序性右后叶切除主要操作步骤如下:(1)体位摆放及Trocar孔布局。根据肿瘤主体所在位置确认适合后实施完全性左侧卧体位,建立气腹后根据视野可做进一步后仰或前俯的手术床微调,至最佳手术体位为止。Trocar孔布局采用前述四孔或五孔布局,第一个Trocar孔(观察孔)应直视下切开腹壁建立(而非直接刺入气腹针或Trocar)。(2)进入腹腔后不游离肝周韧带,直接解剖处理肝门及右后肝蒂,根据需要可优先打开肝后下腔静脉前间隙足侧入路离断尾状突,协助显露门静脉右支(图1B),置入动脉夹,经鞘外阻断右后支Glisson蒂。(3)根据需要实施ICG正染或反染(图1C)。(4)血流控制依靠低中心静脉压和肝门阻断,Pringle法进行肝门阻断,利用本中心对肝门阻断器械进行改进后的大曲度组织隧道建立及牵引装置完成重要管道结构的环绕分离、隧道建立、阻断带牵引及后续处置[6],在腹腔镜肝切除手术中更为便捷地实施包括侧卧位在内的复杂体位下的肝门阻断以及肝上下腔静脉的显露及阻断。(5)术中超声定位确定肿瘤位置及与缺血线(荧光边界)的关系,定位主要结构特别是肝右静脉或前裂静脉位置,断肝平面循荧光边界或循肝右静脉(图1D)。(6)断肝深入后,采取由尾向头,深浅结合,沿下腔静脉前间隙及肝右静脉轴线引导肝实质离断平面(图1E)。(7)离断至肝右静脉根部,根据需要保留或离断。(8)完成肝实质离断后游离右肝韧带,移除标本(图1F)。
三、统计学方法
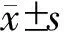
结 果
一、术中指标
手术时间为330(138,582) min,肝门阻断时间为60(15,151) min,出血量为200.0(100.0,312.5)mL。5例病人术中输血,无中转开腹病例。(表2)

表2 47例腹腔镜下流程化肝右后叶切除手术病人术中、术后资料
二、术后情况
术后出现并发症10例(21.3%),其中Clavien-Dindo评分Ⅰ级4例,观察后自行好转;Clavien-Dindo评分Ⅱ级6例,给药后好转。术后住院时间为(8.3±3.0) d;未出现围术期死亡病例。(表2)
三、病理结果
7例病人为良性疾病(表2),分别为肝血管瘤4例、肝脏非典型增生2例、肝梗死灶1例;恶性肿瘤40例,其中肝细胞癌26例,肝转移癌12例,肝内胆管癌2例,术后病理学检查结果显示,40例恶性肿瘤标本切缘均为阴性,切缘小于1 cm为3例(6.4%)。
讨 论
随着外科技术的发展,肝切除术中止血困难、术后肝衰竭等难题被逐渐克服,这一系列的进步极大地改善了肝切除术病人的预后,促进肝切除术的推广。20世纪90年代以来腹腔镜技术的发展为肝切除术提供了新思路,进入21世纪腹腔镜肝切除术的安全性和有效性已经达成广泛共识[8],研究表明,与开放手术相比,腹腔镜肝切除术可以有效减少术后并发症、术中输血率以及术后住院时间[1,9]。甚至手术难度较高的腹腔镜肝右后叶切除术也较开放肝切除具有手术时间短、手术出血量少等优势[10],然而因右后叶的位置较深,断肝平面大以及血管解剖变异等原因导致该区段肝切除术风险高、学习困难,极大地限制了腹腔镜右后叶切除术的发展。我们在之前的报道中总结了解剖性肝右后叶切除的初步经验[6],近几年来,随着手术经验的积累,笔者所在团队对腹腔镜肝右后叶切除术的手术流程进行进一步优化,以期降低右后叶切除术的难度,提高手术安全性及肿瘤学效益,促该术式的进一步推广。
腹腔镜下肝脏右后区手术,在腔镜肝切除难度评分中属于“困难”级手术,其最重要的难点在于该区域深藏于上腹腔的右后方,显露困难,在不良视野情况下管道处理及止血均面临挑战。目前,国内多数中心采用仰卧右侧垫高(40°~60°)的体位,再配合娴熟的助手牵拉以协助暴露[4]。该方法的优点是体位摆放简单,肝脏形态结构受重力影响位移较小,有利于腹腔镜术中超声对肝段管道结构的识别及术中经门静脉穿刺注射ICG等,而且操作过程中断肝平面更容易把握。缺点是手术视野的显露仍然较为困难,对手术团队的协同操作要求较高,在业务开展的初期阶段可能面临较大挑战。笔者中心在长期的腹腔镜肝脏手术探索中发现,在做到充分的手术野暴露情况下,选择适当的手术入路、调整病人体位及Trocar孔分布,利用术中超声及ICG荧光显影定位,以及恰当应用肝血流阻断和肝实质离断技术,“困难部位”肝肿瘤切除仍然是安全可行的。在肝右后叶切除的腹腔镜手术中,我们更多的采用完全左侧卧位的体位摆放,其缺点是体位摆放相对繁琐,对Trocar孔布局有一定的经验性要求,肝实质离断过程中容易发生视觉偏差和平面偏移,术中冲洗液随重力流入左侧或下腹部后腹腔不易清理;但是优点也显而易见:肝脏在重力作用下右侧肝周韧带容易分离显露,肝裸区及第二肝门更容易充分显露,即便断肝平面需达位置更深的S8段区域,仍可做到无视野盲区。肝脏右后区肿瘤病人,个体化合理评价,对肿瘤中心位于右后(特别是偏上区)的病人,使用该体位进行手术,常可达到事半功倍的效果。
在右半肝切除术中,结扎右肝蒂后可看到左右半肝出现明显的缺血线。但在右后叶切除术中,由于部分病人的S7与S8之间存在丰富的交通支,导致结扎右后肝蒂后这部分病人并没有出现理想的缺血线(或ICG荧光分界),并且会导致术中切除体积不够或切缘不足等问题。通过术前影像学检查明确S7的变异,结合术中ICG荧光染色以及术中超声定位肝右静脉,循肝右静脉切除肝脏,确定最佳肝切除范围和最大肿瘤学效应。如前所述,侧卧位的一个重大困难是重力作用下肝脏向左侧悬垂,导致断肝平面容易发生偏离,特别是在断肝至深部平面后容易偏离预定平面,偏向下腔静脉左侧,造成风险。本团队发现,侧卧体位下肝右静脉或前裂静脉平面作为解剖标志引导肝实质离断,结合肝后下腔静脉前间隙或旁间隙轴线,由浅入深,上下结合,利用腔静脉前间隙和肝右静脉轴线组成的平面断肝,即使在没有实现良好肝段荧光染色的情况下也可以完美解决平面偏移问题。
既往手术中本团队通常先游离右肝而后切除,但是发现,在左侧卧位手术时离断肝周韧带后导致S5/S6肝段失去固定,倒向左侧,严重遮挡术野,在断肝的初始阶段造成困难。2020年以来,本团队针对前述问题进行了改进:原位断肝,即在不对右肝韧带做任何游离的情况下,原位离断肝实质至下腔静脉前间隙或旁间隙,然后游离肝周韧带,移除标本。该方法既利用了右肝韧带的牵拉作用、协助显露手术视野,又更贴合“no-touch”的肿瘤学原则[11-12],减少肝切除过程中因牵拉、挤压造成的肿瘤播散转移风险。
本团队还对右后肝蒂的处理程序进行了优化。解剖性腹腔镜肝右后叶切除的难点之一是右后肝蒂的寻找和阻断。众所周知,右后肝蒂分支类型多、变化大,右后肝蒂和右尾叶肝蒂常不易分离,造成右后肝蒂寻找和显露困难。本团队在不断总结经验中发现,以尾状突和腔静脉之间的间隙作为入口,优先离断尾状突后多可轻松打开右后肝蒂后方隧道,再以Rouviere沟为解剖标志在其前方建立打开右后肝蒂前隧道(必要时切开部分肝实质),两隧道间直接插入血管夹(而不强求带线结扎),多可方便快捷地完成右后肝蒂的阻断。当然,部分病人右后肝蒂表浅、分支单一、易于解剖,并不需要上述操作。
总之,本研究通过47例腹腔镜右后叶切除术病人的手术经验总结出“五步法”流程化肝切除,即第一步,以左侧卧体位及Trocar孔布局;第二步,优化处理尾状突及右后肝蒂;第三步,ICG荧光引导;第四步,原位断肝;第五步,肝后下腔静脉前间隙和肝右静脉轴线引导校正肝实质离断平面。“五步法”流程化肝切除进一步优化了腹腔镜下肝右后叶切除的手术流程,降低了手术难度,提高了手术质量和效率,有利于手术的进一步推广应用。
利益冲突所有作者均声明不存在利益冲突

