目标导向式重复性功能训练联合局部亚低温治疗对高血压脑出血术后患者神经功能、运动功能的影响
于宗光
(青岛市即墨区第二人民医院神经外科,山东青岛 266200)
高血压脑出血是指脑部血管长期受到高血压影响而引起的出血,起病急,病情进展迅速,具有较高的致残率、病死率。高血压性脑出血的治疗核心是清除颅内血肿,大骨瓣开颅术或小骨窗微创颅内血肿清除术为常用术式,虽具有较高的血肿清除率,但对正常脑组织也有一定损伤,患者术后常伴有并发症,如深静脉血栓、神经功能障碍等。亚低温治疗可有效减少脑耗氧量,改善脑细胞代谢,促进乳酸分解,降低血脑屏障的通透性,从而有效保护脑组织和神经细胞[1]。康复训练可通过肢体运动促进血液循环,并通过刺激运动神经,促进脑组织间的代偿与重组,修复神经功能,提高患者的肢体运动功能。目标导向式重复性功能训练能够为患者制定阶段式的康复目标,帮助其循序渐进地向更高的训练目标靠近,不断增强对目标的渴求程度,使动机维持在较高水平,有利于提高训练效果[2]。基于此,本研究选取2021 年1 月—2022 年10 月青岛市即墨区第二人民医院神经外科收治的80 例高血压脑出血患者为对象,探究目标导向式重复性功能训练联合局部亚低温治疗对其术后神经功能、运动动能的影响。报道如下。
1 资料与方法
1.1 一般资料
选取青岛市即墨区第二人民医院神经外科收治的80 例高血压脑出血患者为研究对象。纳入标准:(1)符合高血压脑出血的诊断标准[3],并经颅脑影像学检查确诊;(2)发病到入院≤48 h;(3)有明确的高血压病史,且入院时血压水平较高;(4)脑出血≥30 mL;(5)发病后72 h 内接受微创颅内血肿清除术治疗;(6)患者或家属自愿签署研究知情同意书。排除标准:(1)颅内肿瘤、外伤等引起的非高血压性脑出血;(2)检查发现脑疝或脑死亡征象;(3)存在凝血功能障碍;(4)合并恶性肿瘤;(5)患有严重器质性疾病;(6)存在肢体残疾。根据双盲法将所有患者分为两组,每组40 例。对照组中男性23 例,女性17 例;年龄56~78 岁,平均年龄(67.43±5.81)岁;高血压病程4~18 年,平均病程(11.20±1.74)年;出血部位:顶叶14例,额叶10 例,枕叶11 例,颞叶5 例。观察组中男性22例,女性18 例;年龄55~78 岁,平均年龄(66.86±5.95)岁;高血压病程3~18 年,平均病程(10.83±1.86)年;出血部位:顶叶13 例,额叶10 例,枕叶10 例,颞叶7例。两组患者的各项一般资料比较,组间差异无统计学意义(P>0.05),具有可比性。本研究内容已获山东青岛即墨区第二人民医院伦理委员会批准。
1.2 方法
所有患者术后均进行对症治疗,包括营养脑细胞、控制血压、补液、止血、利尿、维持水电解质平衡、脱水、抗感染、吸氧等。
对照组采用局部亚低温治疗。选用FL-202-A 型亚低温治疗仪[哈尔滨富林科技发展有限责任公司,黑食药监械(准)字2012 第2580001 号,型号:FL-202-A],术后6 h,给患者戴上冷却帽,包裹其头部并启动减温器,用温度计检测患者颅周温度,维持脑部温度在33~34℃,连续治疗3~4 d 后开始复温,保持每1~2 天升温1℃,≤0.1℃/h 的速度。治疗期间给予患者常规护理,包括健康教育、病情观察、呼吸道护理、饮食用药指导等。
观察组在对照组基础上进行目标导向式重复性功能训练。充分评估患者病情及肢体运动功能,根据评估结果为其制定近期、中期及远期功能锻炼目标。(1)近期目标。绝对卧床期间采用仰卧位交替更换或健康侧位,为患者进行肢体按摩,并协助其进行被动训练,完成肢体拉伸及关节屈伸、内收、旋转等,由大关节至小关节,15~20 min/次,2 次/d。(2)中期目标。非卧床期间进行主动训练,指导患者在床上翻身,自行完成关节伸屈、旋转等动作,3~5 组/次,3 次/d,并指导其进行凯格尔运动,10 min/次,2 次/d。若患者耐受性良好,可进行站立平衡训练,指导其站在床边,完成向上伸直双上肢、向前移动双足、伸直膝关节等动作,10~15 min/次,2 次/d,根据患者适应性与舒适度逐渐延长站立时间。(3)远期目标。指导患者进行床边脚踏步、床边坐立、重心转移等训练,表现良好后可借助平衡杠进行步行练习,并逐渐升级难度至上下楼训练,15~20 min/次,2~3 次/d,具体视患者耐受程度调整。待患者病情稳定后,协助其进行洗漱、更衣、饮食、排便、家务劳动等训练,20~30 min/次,2~3 次/d。指导患者完成智力拼图、认字、数数、计算等任务,并进行读单词、读句子等语言能力训练,让患者记数字、讲故事强化记忆和推理能力,15~20 min/次,3 次/d。
两组均持续干预3 个月。
1.3 观察指标
(1)神经动能。干预前后,采用美国国立卫生研究院卒中量表(NIHSS)对患者进行评估,量表包括意识水平、面瘫、构音障碍、凝视、视野等10 项,总分42分,神经缺损严重程度与分值呈正相关。
(2)肢体运动功能。干预前后,采用Fugl-Meyer运动功能评定量表(FMA)对患者进行评估,量表包括不同体位的伸/屈肌协同运动、腕稳定性、协调能力、有无反射活动、反射亢进等项目,上肢66 分,下肢34分,总分100 分,分值越高表示肢体功能越好。
(3)步态。干预前后,采用Opt otrak 三维运动捕捉系统评估患者步速、步频、步长。
1.4 统计方法
采用SPSS 25.0 统计学软件进行数据分析。NIHSS评分等计量资料用()表示,采用t检验;性别等计数资料用率(%)表示,采用χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组干预前后神经功能、肢体运动功能比较
干预前,两组的NIHSS、FMA 评分比较,组间差异无统计学意义(P>0.05);干预后,两组的NIHSS、FMA 评分均改善,且观察组的NIHSS 评分低于对照组,FMA 评分高于对照组,组间差异有统计学意义(P<0.05)。见表1。
表1 两组干预前后NIHSS、FMA 评分比较[(),分]

表1 两组干预前后NIHSS、FMA 评分比较[(),分]
注:与同组干预前比较,#P<0.05
2.2 两组干预前后步态指标比较
干预前,两组的步速、步频、步长比较,组间差异无统计学意义(P>0.05);干预后,两组的各项步态指标水平均改善,且观察组的步速、步频快于对照组,步长长于对照组,组间差异有统计学意义(P<0.05)。见表2。
表2 两组干预前后步态指标比较()
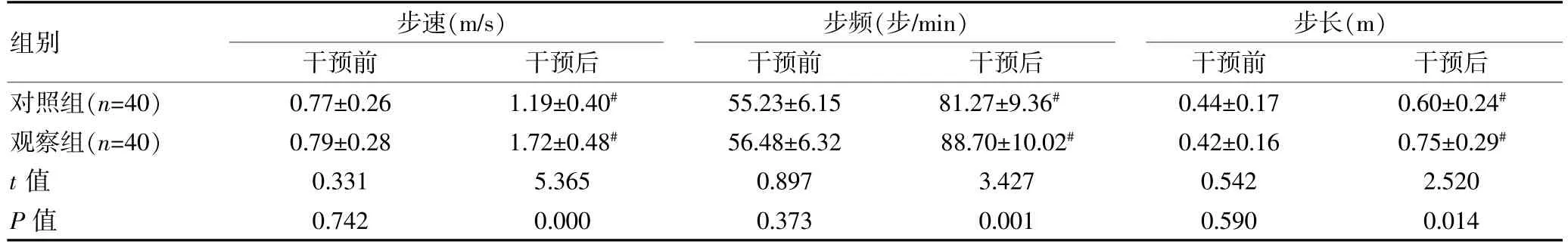
表2 两组干预前后步态指标比较()
注:与同组干预前比较,*P<0.05
3 讨论
微创颅内血肿清除术是高血压脑出血的常用治疗术式,但其对脑组织造成的创伤可导致脑耗氧量急剧增加。术后为脑部创造低温环境可降低脑氧代谢率,改善细胞能量代谢。当人体体温升高时,身体的基本新陈代谢会增加,而低温条件则有利于脑耗氧量平衡。局部亚低温治疗即是根据此原理改善脑部耗氧量和脑代谢,降低脑水肿和颅内压,避免术后缺血再灌注损伤[4]。同时,亚低温治疗可阻断脑炎性损伤,并抑制兴奋性神经递质的释放,从而减轻血-脑脊液屏障的破坏,缓解脑神经细胞凋亡,改善患者预后[5]。王载忠等[6]指出,亚低温联合血肿穿刺引流术能显著提高高血压脑出血的治疗效果。
临床研究证实,在局部亚低温治疗基础上联合功能训练,可在一定程度上促进中枢神经系统功能重组,降低神经系统后遗症的发生率[7]。本研究中,观察组患者在局部亚低温治疗基础上进行目标导向式重复性功能训练,研究结果显示,观察组干预后的NIHSS评分低于对照组,差异有统计学意义(P<0.05),这提示患者神经功能得到了更好的改善。分析原因,脑出血可导致身体失去神经的支配功能,不能自主运动,而支配躯体运动的神经为中枢神经系统,在康复训练过程刺激肢体发生肌肉收缩反射,能促使大脑皮层活化并增强神经元活动,从而修复中枢神经损伤[8]。伏瑜等[9]指出,ICU 高血压脑出血患者接受目标导向性康复护理可改善神经功能。本研究结果还显示,观察组干预后的FMA 评分高于对照组,步速、步频快于对照组,步长长于对照组,组间差异有统计学意义(P<0.05),这提示目标导向式重复性功能训练联合局部亚低温治疗可提高高血压脑出血术后患者的肢体运动功能,改善其步态。
肢体功能训练能有效刺激肌肉神经,诱发肌肉反应,促进缺损神经修复。但由于不同患者的脑损伤部位、脑出血程度均不同,个体间受年龄、病情、性格等因素影响,肢体运动能力也存在差异。目标导向式重复性功能训练相比常规康复训练更因时制宜,可根据患者的肢体运动功能评估结果为其制定近期、中期及远期功能训练目标。在近期目标中,体位调整能避免褥疮发生,肢体按摩可促进局部血液循环,肢体被动训练能通过一些简单的拉伸及关节内收外展、内旋外旋等动作刺激肌肉神经,完成神经系统的功能协调和重建过程,使神经得以正常支配运动[10]。中、远期目标根据患者的病情开展主动训练,可使其从简到繁、从易到难逐渐完成各项训练,大大提高了患者对训练的耐受性和接受度。同时,肢体训练具有促进血液循环的作用,可加快血肿消除,降低深静脉血栓的发生风险。
综上所述,高血压脑出血患者术后采用目标导向式重复性功能训练联合局部亚低温治疗有利于改善神经功能,促进肢体运动功能恢复,值得临床推广使用。

