稀酸氯盐体系转化竹浆制备5-氯甲基糠醛的研究
农贵彤, 郝唯唯, 李 铮, 唐 兴, 周宏才, 林 鹿*
(1.厦门大学 能源学院,福建 厦门 361102; 2.广东中科天元新能源科技有限公司,广东 广州 510535)
5-羟甲基糠醛(HMF)是最重要的生物质基平台化合物之一,含有羟基、醛基、呋喃环等高可塑性官能团,可通过多种催化途径进一步被转化为可再生液体燃料、高附加值化学品、材料等[1]。然而,HMF化学性质活泼、易于发生聚合反应形成腐殖质,故其大规模制备、分离与储存难度很高。近年来,拥有与HMF类似结构和反应能力的5-氯甲基糠醛(CMF)受到广泛关注。与HMF相比,CMF因分子内羟基被氯取代而具有更高的稳定性,因此,其制备、分离提纯、储存更加容易,具有更高的规模化生产潜力。CMF的下游转化途径与HMF高度类似,除经简单的水解、醇解可得HMF、乙酰丙酸及其酯类外[2-3],还可经加氢还原、氧化、羟醛缩合等多种途径制备2,5-二甲基呋喃[4]、 2,5-呋喃二甲醇[5]、 2,5-呋喃二甲醛[6]、丁烯酸内酯类染料小分子[7]等高附加值产物。因此,开发用于大规模生产的CMF合成体系十分重要。CMF的制备于1901年被首次报道[8],但其制备效率一直不高。Mascal等[9-10]建立的基于浓盐酸-二氯乙烷(DCE)双相体系首次实现了将糖类、纤维素、原生生物质等原料高效转化为CMF,其得率达70%以上。然而浓盐酸的高腐蚀性、挥发性给该体系的放大与实际生产带来了严峻的挑战。近年来,研究人员开发了一系列较温和的木质纤维原料水解氯代制备CMF的反应体系[11]。有研究[12]采用体积比4∶1的浓磷酸-浓盐酸与氯仿构建双相体系,在45 ℃将果糖以47%的得率转化为CMF,还有研究者[13]开发了一种微波辅助CMF合成方法,反应15 min后CMF得率达70%以上,但该反应仍依赖浓盐酸体系。陈泽智等[14]研究了AlCl3、LiCl等对浓盐酸-DCE双相体系制备CMF的协同催化效果,发现AlCl3的加入对CMF生成提升明显。以上CMF制备方法多采用浓盐酸/有机溶剂两相体系,浓盐酸同时提供质子作为酸催化剂,又提供Cl-作为CMF形成的氯源。但是浓盐酸容易造成设备的腐蚀、环境的污染,不符合当代绿色环保的要求。因此,有研究人员[15-16]设计了数种基于氯化胆碱、路易斯酸如AlCl3与其他添加剂的低共熔体系,在 120 ℃、 30 min的反应条件下可将葡萄糖在较低酸性下以70%的得率转化为CMF,同时对竹子、竹浆等原料也具有良好兼容性。竹子及其生产废料是理想的生物质资源,非常适合通过生物炼制转化为高值化学品。因此,本研究以竹浆为原料开发了一种基于稀酸氯盐双相体系的CMF制备工艺,旨在降低体系盐酸浓度、增加工艺环保性,并针对底物适应性、体系放大与CMF稳定性等进行了面向工业放大生产的研究探索。
1 实 验
1.1 材料、试剂与仪器
竹浆原料,本课题组采用固体碱活性氧法(CAOSA)[17]处理产自福建南平市的竹子制得,含纤维素75%,半纤维素22.5%,不溶性木质素1.04%,此外还含有少量灰分。实验所用试剂均为市售分析纯。其中二水合氯化钙、六水合氯化镁、氯化锂、四水合氯化亚铁、氯化铜、六水合氯化镍、氯化钾、甲基异丁基酮、浓盐酸、 1,2-二氯乙烷(DCE)、 1,1,2,2-四氯乙烷、氧化钙、亚硫酸氢钠和36%~38%(质量分数)盐酸等,购于西陇化工股份有限公司;六水合氯化铝、氯苯、氢氧化钠和1,1,1-三氯乙烷和1,1,2-三氯乙烷等,购于上海阿拉丁生化科技股份有限公司;氯化钴、氯化钠、氯化钡、乙酸乙酯、环己烷和微晶纤维素,购于国药集团化学试剂有限公司;四水氯化锰和二甲苯购于上海麦克林生化科技有限公司;1,3-二氯丙烷、 1,2,3-三氯丙烷和1,4-二氯丁烷,购于上海安耐吉化学有限公司。
100 mL均相罐及其反应器与1 L哈氏合金反应釜均购于烟台朗川实验设备有限公司。
1.2 稀酸氯盐催化反应体系的选择
1.2.1阴阳离子浓度的选择 本研究首先以微晶纤维素作为模型底物探索酸浓度及氯盐种类对CMF形成的影响。一般认为纤维素在酸性条件下转化为CMF分4个步骤:1) 纤维素酸催化水解为葡萄糖;2) 葡萄糖异构为果糖;3) 果糖脱水转化为HMF;4) HMF的羟基在高氯离子环境下经氯代,从而转化成CMF。具体反应途径如图1所示。反应条件: 在均相反应器中,加入2 g微晶纤维素, 40 mL DCE, 一定量的盐酸和金属氯盐(CaCl2、MgCl2、AlCl3)使得H+浓度为3 mol/L, 使Cl-浓度达到传统体系中浓盐酸提供的水平(11.64 mol/L),在130 ℃反应1 h,通过CMF得率来选择阴阳离子浓度。实验中还通过改变AlCl3加入量,考察Cl-浓度的影响。

图1 纤维素转化制备5-氯甲基糠醛(CMF)的反应途径
1.2.2氯盐种类的选择 在氯盐添加量为饱和或者近饱和状态下,考察竹浆在稀酸-氯盐双相体系中转化为CMF的反应效果,反应条件:1 g竹浆, 2 mol/L HCl, 不同种类的氯盐,8 g H2O, 20 mL DCE, 140 ℃反应1 h,氯盐选择LiCl、CaCl2、MnCl2、FeCl2、CuCl2、CoCl2、MgCl2、NiCl2、AlCl3、KCl、NaCl、BaCl2。
1.2.3原位萃取剂的选择 在1.2.2节基础上进一步考察了几种常见的与水不互溶的有机溶剂以及其他氯代烷烃作为萃取剂的作用效果,反应条件:1 g 竹浆,1.33 mol/L HCl, 6.66 mol/L CaCl2, 130 ℃反应1 h, 8 g H2O, 25 mL萃取剂。氯代烷烃类溶剂包括DCE、 1,1,1-三氯乙烷、 1,1,2-三氯乙烷、 1,1,2,2-四氯乙烷、 1,3-二氯丙烷、 1,2,3-三氯丙烷、 1,4-二氯丁烷。同时,将其萃取效果与乙酸乙酯、环己烷、甲基异丁基酮(MIBK)、氯苯和二甲苯等有机溶剂进行了对比。
1.3 在低酸浓度体系中利用竹浆制备CMF
1.3.1竹浆制CMF 在1.2节选择的稀酸氯盐催化反应体系中,选择竹浆为原料,采用一锅法制备CMF,并对其制备条件进行优化,所有反应都在均相反应器中进行。典型操作步骤如下:将1 g竹浆(即竹浆在水相质量浓度83.3 g/L,质量分数5.72%)、 2.92 g的20% HCl(即HCl浓度1.33 mol/L,以体系总体积为基准,下同)、 11.752 g 50.8%的CaCl2·2H2O(即CaCl2浓度6.66 mol/L)、 2.784 g H2O(H2O 总质量8 g、水相总质量17.456 g,水相总体积12 mL)、 20 mL DCE置于100 mL均相罐,转速30 r/min,130 ℃反应1 h后降温冷却,将反应液转移至分液漏斗并使用25 mL DCE萃取3次,合并有机相并称量总质量。有机相经CaCO3除酸、无水MgSO4除水后保存供后续检测。
实验对水解氯代反应中的HCl与CaCl2浓度、反应温度及底物浓度等条件进行优化。
1.3.2放大实验 CMF制备放大反应的典型操作如下:15 g竹浆(6.87%)、 36.5 g 20% HCl、 147.0 g CaCl2·2H2O、 34.8 g H2O、 400 mL DCE置于1 L哈氏合金反应釜,转速600 r/min,130 ℃反应1 h后降温冷却,将反应液转移至分液漏斗并使用DCE萃取3次,合并有机相并称量总质量。有机相经CaCO3除酸、无水MgSO4除水后保存供后续检测。
实验中对CMF粗提液采用减压蒸馏分离纯化CMF,并对分离纯化后的CMF进行表征。
1.4 产物分析
取2~3 mL含有CMF的DCE萃取液,分别使用CaCO3和无水MgSO4除酸、除水并过滤后,使用GC-MS定性分析,色谱柱为TR-5SilMS(30.0 m×250 μm×0.25 μm)。萃取液中的 CMF 通过 GC定量分析,色谱柱为TR-5SilMS。目标产物CMF的得率(以竹浆中纤维素为基准)通过标准品绘制的标准曲线进行定量分析,并根据以下公式计算:
(1)
式中:Y—CMF的得率,得率以理论值为基准,%;n—水解氯代实验所得CMF物质的量,mol;m—水解氯代实验竹材原料质量,g; 75%—竹浆中纤维素的质量分数; 162—纤维素的相对分子质量。
2 结果与分析
2.1 稀酸氯盐催化反应体系的构建
2.1.1阴阳离子浓度的确定 在浓盐酸/DCE体系中,浓盐酸除提供连串反应所需的酸催化条件外,还提供HMF羟基氯代反应所需的高氯离子浓度环境,即为CMF中的氯原子提供来源。因此,本研究首先以微晶纤维素作为模型底物探索酸浓度及氯盐种类对CMF形成的影响, 结果见表1。由表可知,对照反应显示当反应体系中无酸、无氯盐时,底物几乎没有转化;当盐酸浓度仅为3 mol/L时,反应体系颜色加深但有机相中未检测到目标产物CMF,这说明此时体系的酸、氯离子浓度均无法满足CMF生成的需要。当向此双相体系中分别补加常见金属氯盐(CaCl2、MgCl2、AlCl3)使氯离子浓度达到传统体系中浓盐酸提供的水平(11.64 mol/L)时,产物中可检测到CMF,且可获得较可观的CMF得率(15.4%~33.6%)。当降低AlCl3添加量时,发现CMF得率呈阶梯式降低,因此水相中饱和或者近饱和的氯离子状态对于抑制CMF重新水解为HMF及减少酸性条件下HMF向腐殖质的转化至关重要。

表1 体系中离子浓度对CMF得率的影响
2.1.2氯盐种类的筛选 根据2.1.1节结果,在氯盐添加量为饱和或者近饱和状态下,进一步考察了竹浆在稀酸-氯盐双相体系中转化为CMF的反应效果,结果如表2所示。当氯离子浓度低于6 mol/L时,CMF的得率普遍偏低(低于11%),但氯离子浓度升至8~15 mol/L时,不同阳离子氯盐展现出的催化效果差异很大。例如CuCl2、FeCl2、CoCl2存在时,CMF得率仅为2.36%、 7.90%、 13.90%,MnCl2催化时饱和浓度氯离子虽然有所升高,但对CMF得率提升却无明显优势,此时CMF得率依然较低(8.72%);而NiCl2、AlCl3催化时,CMF得率显著提升,尤其MgCl2催化时,CMF得率达到57.00%。当选用CaCl2催化时,CaCl2展现出更为优异的催化效果,CMF得率升至57.90%,虽然LiCl催化时获得最高CMF得率(59.60%),但考虑经济成本,将选用价格低廉、常见易得的CaCl2为催化剂进行工艺探索及后续研究。

表2 稀酸-氯盐/DCE双相体系中不同氯盐对CMF得率的影响
2.1.3有机原位萃取剂的筛选 DCE是CMF双相体系制备中的使用最多的有机相,但由于其沸点(83.5 ℃)较低,反应过程实际是高压反应,为反应装置的耐压、密封性能带来了一定的挑战。因此,基于以上优化条件,本研究进一步探索了几种常见的与水不互溶的有机溶剂以及其他氯代烷烃作为萃取剂的作用效果,以探索采用较高沸点溶剂来降低体系压力与溶剂挥发程度的可能性,结果见表3。由表可见,氯代烷烃类溶剂相较于乙酸乙酯、环己烷、甲基异丁基酮(MIBK)等有机溶剂展现了更加优异的效果,其对CMF具有较优的萃取性能。其中较高沸点溶剂如1,1,2-三氯乙烷、 1,3-二氯丙烷、 1,2,3-三氯丙烷做萃取剂时,CMF的得率均超过54%,因而这几种溶剂均具有取代DCE、降低反应体系压力与溶剂挥发程度的潜力。目前,本研究后续还是采用DCE作萃取剂。

表3 不同萃取剂对CMF得率的影响
2.2 水解氯代反应工艺条件的优化
2.2.1HCl与CaCl2浓度组合对CMF得率的影响 由于CaCl2在盐酸中的溶解度随HCl浓度增加而减少,而HCl浓度与CaCl2浓度又直接影响该体系下催化反应过程及目标产物的产生,因此在反应温度为130 ℃、反应时间为1 h的条件下,考察了不同HCl浓度与CaCl2浓度对CMF得率的影响,结果如图2(a)所示。

a.HCl与CaCl2浓度concentrations of HCl and CaCl2;b.反应温度reaction temperature;c.底物浓度substrate concentration
当盐酸浓度一定时,CMF得率随CaCl2浓度变化呈抛物线趋势变化,获得CMF最高得率时的CaCl2浓度随HCl浓度的增加而降低,与CaCl2溶解度对HCl浓度变化趋势一致。当HCl浓度由0.67和1.00 mol/L提升至1.33 mol/L时,CMF最高得率分别由44.8%、 48.0%跃迁至59.2%,可能过低的HCl浓度不足以提供足够的催化动力使CMF在短时间内达到较高水平,反应效率低。而进一步升高HCl浓度至2.00 mol/L时,CaCl2浓度为6.66 mol/L时即获得CMF最高得率(57.9%),较HCl浓度为1.33 mol/L催化时略微降低,原因是过量的盐酸可能促进了反应过程中副反应的发生如CMF的进一步转化等,对CMF得率的提高并无明显优势。因此,选用中等浓度(1.33 mol/L)的盐酸较为合适。此外,在此酸浓度下,CaCl2的添加量在顶点浓度(5.33~7.99 mol/L)附近时,CMF得率维持在57%以上,但是当CaCl2浓度为7.99 mol/L时,反应降温后水相中发现大量氯化钙晶体沉淀,此现象一方面不利于水相稀酸盐体系的稳定,另一方面固体的产生也增加了实际生产操作难度,综上考虑,在后续研究中将选用HCl浓度为1.33 mol/L、CaCl2浓度为5.33~6.66 mol/L为最适催化反应体系浓度。
2.2.2反应温度对CMF得率的影响 反应温度对反应速率和转化效率有重要的影响,因此在上述考察得到的最适催化反应体系浓度即HCl浓度为1.33 mol/L、CaCl2浓度为5.33 mol/L下,研究了3个不同反应温度(120、 130和140 ℃)条件下CMF得率随反应时间的变化规律,结果如图2(b)所示。当反应温度为120 ℃时,CMF随反应时间的延长得到累积,得率稳步提升,90 min后达到平衡,此时CMF得率趋于稳定,保持在51.3%~54.4%之间;当反应时间超过150 min后,进一步延长反应时间,CMF得率明显下降,说明过长的反应时间并不利于CMF的积累,这可能是由CMF在酸性条件下向HMF、乙酰丙酸(LA)以及腐殖质转移导致的。当反应温度提高至130 ℃时,反应1 h即达到平衡,反应速率明显提升,且CMF得率为57.0%,较120 ℃时也有所升高;当反应温度进一步提高至140 ℃时,反应30 min时CMF得率达到35.6%,反应速率得到进一步提高,但该温度下获得的CMF最高得率降至54.3%,且反应1 h后CMF得率下降明显。这是因为一方面过高的反应温度可能利于中间产物向HMF腐殖质的转移、CMF的下游分解反应的发生,导致了CMF得率的下降;另一方面也可能是140 ℃下CaCl2在稀酸中的饱和度增加,而1.33 mol/L的HCl浓度、 5.33 mol/L 的CaCl2浓度无法达到该反应温度下CMF对于氯离子饱和度的要求,进而促进了CMF向HMF及腐殖质的转移。由此可见,适宜的反应温度(130 ℃)和反应时间(60 min)对于CMF的积累是有益的。
2.2.3底物浓度对CMF得率的影响 在实际生产过程中,初始底物浓度决定了整条工艺路线的经济性。较高的初始底物浓度可以带来较高的产物浓度,以此提高处理效率,降低后续分离纯化过程中的能耗;但是另一方面,初始底物浓度过高,传质、传热受限,碳水化合物及呋喃类中间产物的副反应增多,反应复杂度增加,从而造成底物利用率降低,产物得率下降。因此,为了使反应底物得到充分高效利用,同时获得高浓度的产物,研究了不同初始竹浆底物浓度对CMF得率的影响。反应条件:1.33 mol/L HCl, 6.66 mol/L CaCl2, 130 ℃反应1 h, 8 g H2O, 萃取剂为25 mL DCE,结果如图2(c)所示。由图可知,当初始底物质量浓度由4 g/mL提高至8 g/mL时,CMF得率由65.7%降低至58.0%,但获得的CMF质量却由起初的0.221 5 g提高到0.390 8 g,增加了76.4%。当底物质量浓度进一步提高至12和16 g/mL时,CMF得率没有明显降低,依然保持较高水平,分别为58.1%和57.7%。与此同时,CMF质量呈阶级升高至起初的2.65和3.51倍。而当初始底物质量浓度再次提高至20 g/mL时,产物CMF的得率明显降低,仅为34.8%, 较低的CMF得率严重影响了CMF的最终质量,使得CMF总质量较初始底物质量浓度16 g/mL时不增反降,说明此时高初始底物质量浓度已严重影响反应进程,反应底物没有得到充分利用。因此综合考虑,选择16 g/mL作为初始底物质量浓度较为合适。
为了对比,实验选取了表现最好的1,1,2-三氯乙烷和1,2,3-三氯丙烷作溶剂并增加底物质量浓度为原来的2倍,结果发现CMF得率反而明显下降,由58.90%降至36.20%(表4),但是DCE做萃取剂时相同底物浓度下CMF得率依然可以保持在57.7%(图2(c))。因此,对较高底物质量浓度(12~16 g/mL)下CMF的制备DCE仍然具有优势。

表4 1,1,2-三氯乙烷和1,2,3-三氯丙烷做萃取剂的效果1)
2.2.4稀酸氯盐水相循环性能的研究 在实际生产过程中,稀酸氯盐的循环使用对于生产成本的控制、工艺流畅性至关重要,因此考察了稀酸氯盐循环使用一次后的催化效果。第一次反应回收得到的稀酸氯盐反应体系中直接添加新鲜物料进行反应时,CMF得率由原来的52.3%下降为37.8%,由纤维素转化CMF反应路径可知反应过程中H+和Cl-参与反应,消耗了稀酸氯盐催化反应体系中的部分质子与氯离子,检测体系中HCl质量分数也由初始3.34%降低至2.09%。上述研究还发现降低HCl浓度对CMF的产生是不利的,因此应当向回收得到盐酸氯盐体系补加新鲜浓盐酸至HCl浓度达到其初始浓度后再次进行催化反应,补充HCl后CMF的得率(48.3%)再次恢复到初始得率水平,这表明通过补充一定量的盐酸,本体系具有循环使用的可能性。
2.3 面向工业化竹浆制备CMF的技术开发探索
2.3.1稀酸氯盐反应体系对不同预处理原料的适用性研究 竹子具有生长速度快、分布广等特点,是
福建省重要的作物与生物质原料。因此,以将原生竹子经简单粉碎处理得到的竹粉、经不同预处理手段得到的竹粉或浆料为原料,考察了HCl-CaCl2-DCE催化反应体系对原料的适用性(表5)。由表可知,直接以竹粉为原料时,130 ℃反应温度下获得一定量的CMF,提高温度(140 ℃)或经NaOH、CaO简单预处理后,CMF的得率有所提高,但总体得率不高。经NaHSO3或固体碱活性氧蒸煮(CAOSA)得到的竹浆为原料时,CMF得率达56.0%。以上结果说明选择适当的生物质预处理技术对基于纤维素浆料的CMF制备具有至关重要的作用,是CMF工业化生产需重点考虑的上游因素。

表5 以不同预处理条件获得的竹粉为原料对CMF得率的影响
2.3.2竹浆制备CMF的15倍放大反应探索 基于以上探索结果,在1 L反应釜中探索了将反应适当放大时的反应效果,结果如表6所示。由表可见,以15 g(9.93 g/mL)竹浆为底物时,CMF的得率(57.4%)依然保持较高水平,说明将反应由均相反应器换至1 L反应釜时放大效应对该反应影响较小。当初始底物质量浓度提升至16.6 g/mL时,产物CMF得率略微降低至51.8%,但最终CMF质量依然提高了0.5倍,说明1 L反应釜为反应器时对相对较高的初始底物投入量也有较好的适应性。而再次提高底物浓度,以纤维素粉为底物反应时,产物CMF的得率显著下降至38.5%,原因可能是高底物浓度降低了催化剂与底物之间的单位接触面积,使相应的催化活性位点减少,也可能是高浓度底物影响了反应的传质传热效果,最终导致底物反应不充分,碳化严重。由此可见,该放大条件下底物质量浓度仍可保持在16.6 g/mL而不会对CMF得率带来太大影响。
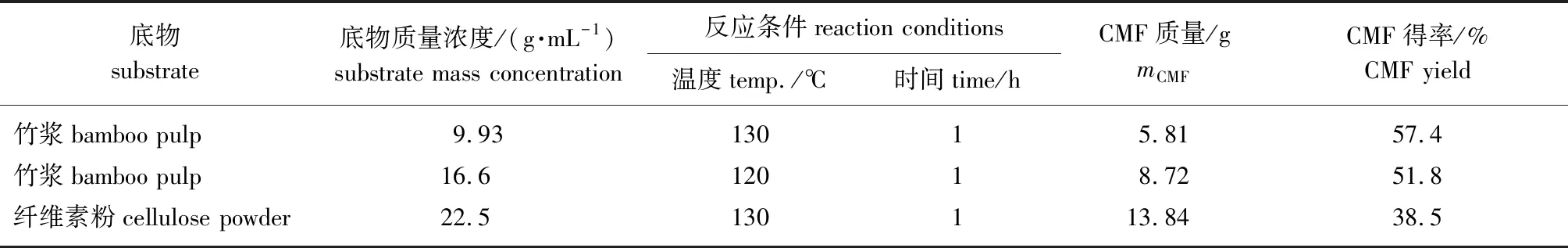
表6 稀酸氯盐体系中竹浆制备CMF的放大
2.3.3产物CMF在萃取液DCE中稳定性、分离及表征 在实际生产中,富集了CMF的有机萃取液一般会存储放置然后进行集中分离纯化。而萃取液中不可避免含有的微量酸、水等会加速产物CMF发生降解、聚合等副反应,因此,本实验通过检测两组平行萃取液中CMF的浓度变化探究了CMF在萃取液中的稳定性,如表7所示。可见,未经CaCO3除酸、MgSO4除水处理的萃取液与经过除酸、除水处理后的萃取液,密封状态于室温中分别放置4和12 d后,CMF的浓度平均变化均在2%以内,且无明显固定变化规律,故仪器测量误差应为浓度变化的主要因素。该情况说明在实验时间范围之内CMF在萃取液DCE中化学性质稳定,保存状态良好,不必进行除酸、除水处理即可满足短时间存储要求。

表7 CMF在DCE中的稳定性
CMF相对于HMF极性较弱、疏水性更强,易被有机溶剂萃取,另一方面也避免了HMF分子间易于发生的羟醛缩合等交联聚合反应,热稳定性增强。结合以上CMF分子结构特性,采用简单的减压蒸馏成功实现了萃取液中CMF的分离纯化,具体步骤如图3所示。

图3 CMF的减压蒸馏提纯
首先,CMF粗提液经45 ℃旋转蒸发浓缩得浓缩液(CMF粗产品),萃取剂DCE回收率为96.3%;然后,减压蒸馏浓缩液,收集80 ℃左右的馏分,得到纯度较高的CMF,重复此操作两次后,最终得淡黄色透明CMF液态纯品,收率为93.5%,说明减压蒸馏对于萃取液中CMF的分离提纯是可行的。分离纯化得到的CMF的1H NMR和13C NMR图谱见图4。与标准谱图对比一致[18-19],验证了经减压蒸馏得到的物质即为目标产品CMF。
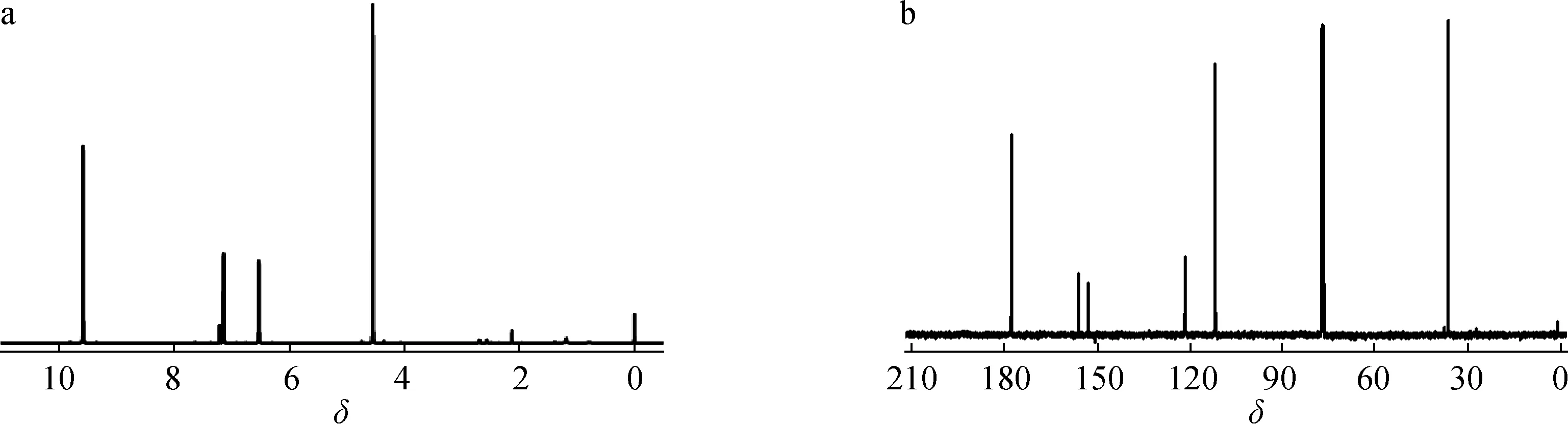
a.1H NMR; b.13C NMR
综上,本研究提供的稀酸-氯盐双相反应体系可将生物质原料如竹浆高效合成CMF,并具有良好的放大潜力,为CMF的工业化生产、分离、储存提供了极具价值的理论与实验基础。
3 结 论
3.1构建并全方面优化竹浆制备5-氯甲基糠醛(CMF)的稀酸-氯盐双相反应体系,发现水相中饱和或者近饱和的氯离子状态可有效抑制CMF与HMF化学平衡反应的右移和减少酸性条件下不稳定中间产物HMF向腐殖质的转化,进而提高体系中CMF的稳定性,CaCl2为最适催化剂,1,1,2-三氯乙烷、1,3-二氯丙烷、1,2,3-三氯丙烷均有取代1,2-二氯乙烷(DCE)的潜力。水解氯代实验结果表明:HCl浓度为1.33 mol/L、CaCl2浓度为5.33~6.66 mol/L为最适催化反应体系浓度,130 ℃和1 h为适宜的反应温度和时间,16 g/mL的初始底物浓度较为合适,通过向稀酸-氯盐体系补充适量盐酸可使其催化效果恢复。
3.2进一步放大实验研究结果表明:稀酸-氯盐双相反应体系适用于经NaHSO3或固体碱活性氧蒸煮预处理的竹浆。将体系放大15倍、原料投入量保持16 g/mL,CMF得率仍可达51.8%。此外,CMF在萃取液DCE中化学性质稳定、保存状态良好,不必进行除酸、除水处理即可满足至少4~12 d的存储要求。

