煤胶体对重金属铜与镉的吸附特征研究
王丽华,王磊,许端平,薛杨
辽宁工程技术大学环境科学与工程学院,辽宁 阜新 123000
近年来,我国土壤污染状况调查数据显示土壤重金属超标率比较高(陈付荣,2022;李海燕,2022)。2014年土壤普查显示重金属镉、铜的污染物点位超标率分别为7.0%、2.1%(全国土壤污染状况调查公报,2014)。当过量的金属或类金属进入土壤时会对土壤结构造成破坏,导致土壤质量下降(林凡华等,2007),此外重金属可以通过食物链进行生物积累和转移,产生一定的毒性作用,对人类安全构成威胁(许信等,2020;窦红宾等,2022),因此土壤重金属污染是当代社会的主要研究的环境问题之一(熊秋林等,2017;刘霞,2022)。土壤中10 μm以下的颗粒被称为土壤胶体,是土壤中最活跃的成分,其有机质含量高,比表面积大,易与重金属结合发生同步迁移,因此被认为是土壤中潜在的污染物载体(James et al.,1999;Shein et al.,2007;Syngouna et al.,2013;杜晓丽,2022),当金属或金属合金进入土壤时,它们会与土壤胶体中的细颗粒和超细颗粒发生复杂的化学反应(Liu et al.,2019),为了揭示土壤胶体促进金属在土壤中的转运机制,胶体对重金属迁移的影响成为近年来专家与学者研究的焦点(Liu et al.,2018;张蓉蓉,2020)。研究发现,胶体携带重金属的移动速度高于重金属本身在土壤中的迁移速度(丁武泉等,2017;朱一丹,2020),且不同胶体对重金属的携带迁移效果不同(龚仓等,2012;牟海燕等,2019)。
辽宁省阜新市煤炭资源丰富,保有储量探明资源量3.586×108t。海州露天煤矿是中国第一个五年计划期间156个重点建设项目之一,1950年开始建设,1953年7月1日投产,当时为亚洲最大的机械化露天煤矿。虽然煤炭对人类文明和社会进步有巨大贡献,但是矿业活动产生了大量的矿业固体废物,在长期风化和雨水淋滤等作用下,固体废物中的微量重金属元素迁移进入周围的土壤,导致土壤重金属含量增加,其中最显著的是Cu、Pb、Ni、Zn、Sn。在煤矿的开采、运输以及加工过程中产生大量的煤粉进入大气环境中,并通过沉降进入水环境和土壤环境,其中小于10 μm的细小颗粒为煤胶体(姜秀民等,2000;Nunez,2010)。煤胶体表面有不均一性,有机质含量高(Malik,2003),有机质每单位干重有许多带负电荷的基团,有很强的络合能力(王玉洁等,2021),其中的含氧官能团可以与重金属发生络合作用或螯合反应等(杨金燕等,2005;Bhattacharyya et al,2008),因此,富含有机物的煤胶体的存在可能会促进重金属在其中的迁移。但关于煤胶体对重金属迁移影响的研究较少,因此,研究土壤中煤胶体对重金属铜、镉的迁移在环境污染及修复过程中具有重要意义,对预测铜与镉在土壤中的归趋亦有重大意义。
1 实验材料与方法
1.1 煤胶体的提取
在阜新采集长焰煤,自然风干后,将煤炭粉碎,球磨成粉状。准确称取1000 g褐煤粉末于5000 mL的烧杯中,加入4 L去离子水,搅拌均匀后超声30 min(每隔5 min搅拌1次),重力沉降24 h。用虹吸法吸取20 cm的上清液,离心机以转速4000 r·min-1离心20 min,从而得到0-2 μm的煤胶体。将剩余溶液加去离子水至烧杯4000 mL刻度处,超声30 min(每5 min搅拌一次),重力沉降10 h,再用虹吸法吸取10 cm上清液,继续用4000 r·min-1转速的离心机离心20 min,得到2-5 μm的煤胶体。剩余溶液加入去离子水到烧杯4000 mL刻度处,重力沉降2 h,用虹吸法吸取20 cm的上清液,将溶液以800 r·min-1的转速离心10 min,得到5-10 μm的煤胶体。将上述3种不同粒级的煤胶体,经冷冻干燥后研磨,备用。
1.2 煤胶体的表征
分别用电子天平准确称取0.1 g不同粒级的煤胶体于100 mL的烧杯中,配制成200 mg·L-1的胶体悬浮液,放入超声清洗仪超声15 min,并用玻璃棒不断搅拌,采用激光粒度仪对煤胶体进行分析其粒径分布;采用BET法测定煤胶体的比表面积;煤胶体有机质采用国标方法《NY/T 1121.6—2006》测定(中华人民共和国农业农村部,2006)。
1.3 煤胶体对重金属的吸附动力学实验方法
分别准确称取0.05 g 3种粒级的煤胶体于50 mL离心管中,加入30 mL质量浓度为100 mg·L-1的铜、镉溶液,置于空气浴恒温振荡箱中,在35 ℃、150 r·min-1下,振荡0.25、0.5、1、2、4、8、12、24 h,以4000 r·min-1离心20 min后,取上清液,过0.45 μm纤维膜,采用原子吸收(TAS-990)测定其上清液中铜与镉的浓度。
1.4 煤胶体对重金属的等温吸附实验方法
分别准确称取不同粒级煤胶体0.05 g于50 mL离心管中,加入30 mL质量浓度分别为1、2、5、10、20、50、100、200、500 mg·L-1的铜、镉溶液,在空气浴恒温振荡箱中以25 ℃,150 r·min-1振荡24 h,以4000 r·min-1离心20 min,过45 μm纤维膜,利用原子吸收(TAS-990)测定其上清液中铜与镉的浓度,将恒温振荡箱以35 ℃,45 ℃重复上述过程。
1.5 数据处理方法
煤胶体对铜、镉的吸附量采用差量法计算,差量法计算公式如下。
式中:
qt——某时刻煤胶体吸附重金属的量(mg·kg-1);
C0——初始时刻溶液中重金属的浓度(mg·L-1);
Ct——某时刻溶液中重金属的质量浓度(mg·L-1);
V——样品体积(L);
m——吸附剂质量(kg)。
本实验通过拉格朗日准一级、拉格朗日准二级动力学方程模型进行实验数据拟合分析,一级动力学方程被描述为(2),二级动力学方程被描述为(3)。
式中:
qe——在平衡状态下的单位质量的吸附剂吸附的吸附质的量(mg·g-1);
qt——在某时刻t(时间)的单位质量的吸附剂吸附的吸附质的量(mg·g-1);
K1——拉格朗日准一级吸附速率常数(min-1)。
式中:
K2——准二级吸附速率常数(mg·g-1·min-1),和颗粒扩散系数有关;
准二级吸附模型的起始吸附速率u和吸附量达到平衡吸附量一半时所需时间t1/2根据下述方程计算:
I——与边界层厚度有关常数。
本实验使用Linear、Langmuir和Freundlich方程3种等温吸附模型进行实验数据拟合。Linear等温式被描述为(6),Langmuir等温式被描述为(7),Freundlich等温式被描述为(8)。
其中:
qc——平衡吸附量(mg·kg-1);
Ce——平衡质量浓度(mg·L-1);
K——平衡吸附系数。
其中:
kL——与吸附能有关的常数;
a——Langmuir单分子层吸附状态下的最大吸附容量(mg·kg-1)。
式中:
KF——表征吸附能力Freundlich的吸附特征常数;
n——表征吸附强度Freundlich的吸附特征常数。
为了解煤胶体对铜与镉的吸附热力学特性,计算其相关热力学参数的公式有:
式中:
Kc——平衡常数;
C0——平衡质量浓度(mg·L-1);
q——平衡吸附量(mg·kg-1);
ΔG0——自由能变(J·mol-1);
R——气体常数(J·(moL·K)-1);
T——绝对温度(K);
ΔH——焓变(KJ·mol-1);
ΔS——熵变(J·mol-1·K-1)。
2 结果与讨论
2.1 煤胶体的理化性质
采用激光粒度仪分析煤胶体的粒径分布,不同粒级煤胶体的粒径分布如图1所示:
由图1可知0-2、2-5、5-10 μm的煤胶体的质量分数依次是85.79%、75.03%和61.28%,表明所提取的煤胶体粒径基本符合预设的范围。
采用BET法测定煤胶体的比表面积,采用国标方法《NY/T 1121.6—2006》测定煤胶体有机质,其结果见表1。结果表明,随着煤胶体粒径的增加,BET比表面积逐渐减小,总孔容量逐渐减小,有机质含量逐渐减少,平均孔径逐渐增大。
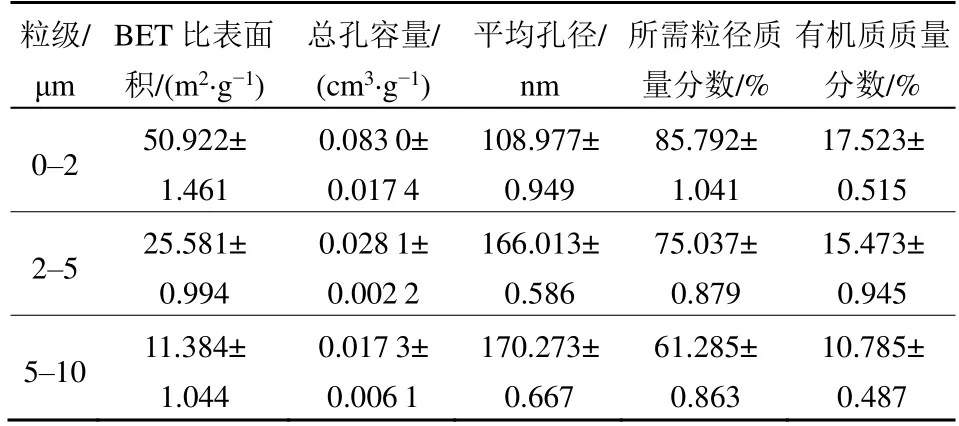
表1 煤胶体的基本理化性质Table 1 Basic physical and chemical properties of coal colloid
2.2 煤胶体对重金属吸附动力学特征
不同粒级的煤胶体对铜、镉的吸附动力学曲线如图2所示。
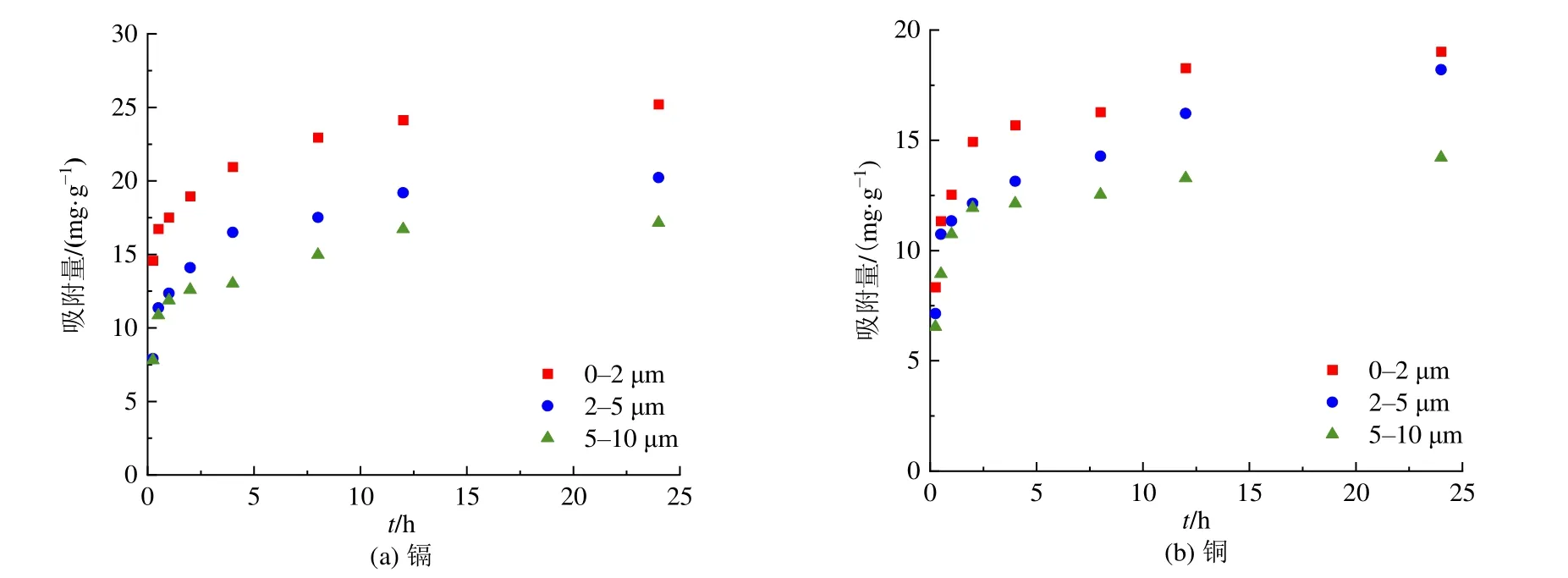
图2 煤胶体在不同粒级下(0-2、2-5、5-10 μm)对(a)镉与(b)铜的吸附动力学曲线Figure 2 Adsorption kinetic curve of coal colloid ( 0-2,2-5,5-10 μm) for (a) cadmium and (b) copper under different particle sizes
为了定量描述煤胶体对铜、镉的吸附动力学特征,讨论其吸附机理,本实验通过拉格朗日准一级、拉格朗日准二级动力学方程模型进行实验数据拟合分析(薛杨等,2017a),拟合结果见表2。
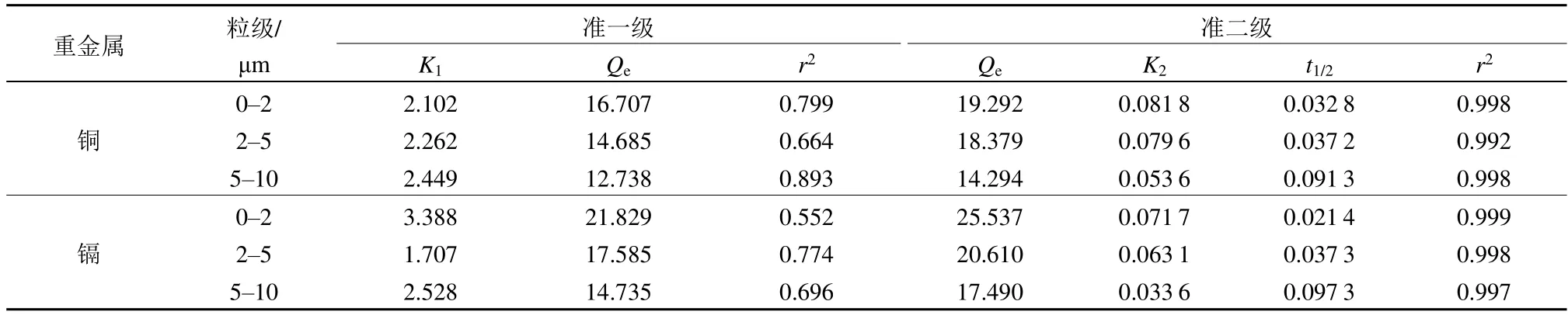
表2 不同粒级煤胶体对铜与镉吸附动力学方程拟合结果Table 2 Fitting results of adsorption kinetic equation of copper and cadmium on coal colloids of different particle sizes
由表2可知,准二级动力学方程拟合的相关系数r2均大于0.99,拟合效果比准一级动力学方程拟合效果好,说明拉格朗日准二级动力学方程能更好描述煤胶体对铜与镉的吸附动力学过程,说明吸附机理为化学吸附。铜在0-2、2-5、5-10 μm粒级煤胶体上的吸附速率常数分别为:0.0818、0.0796、0.0536;镉的分别为:0.0717、0.0631、0.0336,不同粒径的煤胶体对铜与镉的吸附实验表现为吸附速率常数K2随着粒径的增大而减小,各粒级下铜的吸附速率常数大于镉,说明铜达到吸附平衡的时间比镉短,而实验结果也显示铜先于镉到达吸附平衡。达到平衡吸附量一半时所需时间t1/2随着粒径的增大而增大,表明粒径越小,反应速率越快,达到平衡吸附量一半所需要的时间越少。由图2可知煤胶体吸附不同重金属的平衡吸附量不同,煤胶体粒级分别为0-2、2-5、5-10 μm时,铜的平衡吸附量分别为:19.292、18.379、14.294 mg·g-1,镉的平衡吸附量分别为:25.537、20.610、17.490 mg·g-1,各粒级下煤胶体对镉的平衡吸附量均大于对铜的平衡吸附量,表现为镉比铜更易于被煤胶体吸附,造成该结果的原因可能是煤胶体吸附不同重金属的配位体以及配位体浓度不同(Waychunas et al.,2005;Molnar et al.,2015)。
2.3 等温吸附特征
不同粒级的煤胶体在不同温度下对铜与镉的等温吸附曲线如图3、4所示。
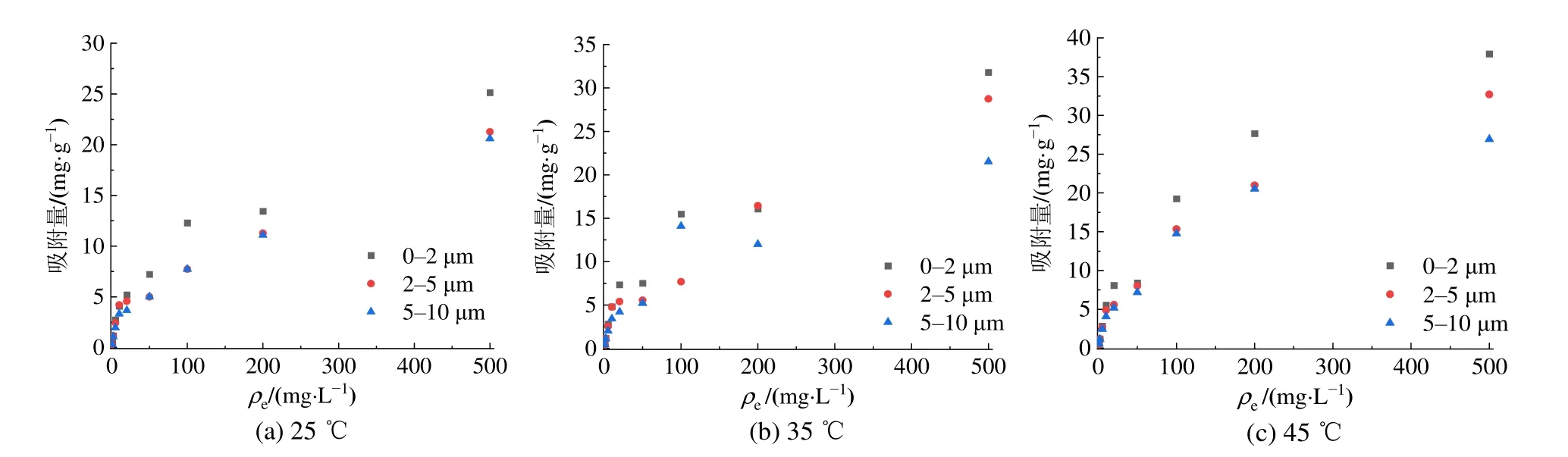
图3 0-2、2-5、5-10 μm煤胶体在不同温度下对铜的等温吸附曲线Figure 3 Isothermal adsorption curves of 0-2,2-5 and 5-10 μm coal colloids on copper at different temperatures
由图4可知各粒级各温度下煤胶体对镉的吸附量均大于其对铜的吸附量。造成煤胶体对重金属吸附量不同的原因可能与阳离子价态和水合半径有关,铜与镉的阳离子价态相同,煤胶体对其的吸附差异主要取决于水合半径,水合半径越小,越容易被胶体表面吸附(马义,2018)。Cu2+水合半径为0.419 nm,Cd2+水合半径为0.426 nm,因此,煤胶体对镉的吸附量大于其对铜的吸附量。
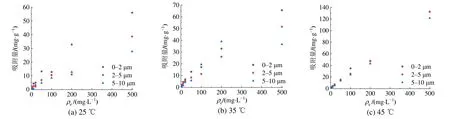
图4 0-2、2-5、5-10 μm煤胶体在不同温度下对镉的等温吸附曲线Figure 4 Isothermal adsorption curves of 0-2,2-5 and 5-10 μm coal colloids for cadmium at different temperatures
使用Linear、Langmuir和Freundlich方程(薛杨等,2017b;葛华才等,2020)3种等温吸附模型进行实验数据拟合。
煤胶体对铜、镉的等温吸附拟合分析如表3所示。
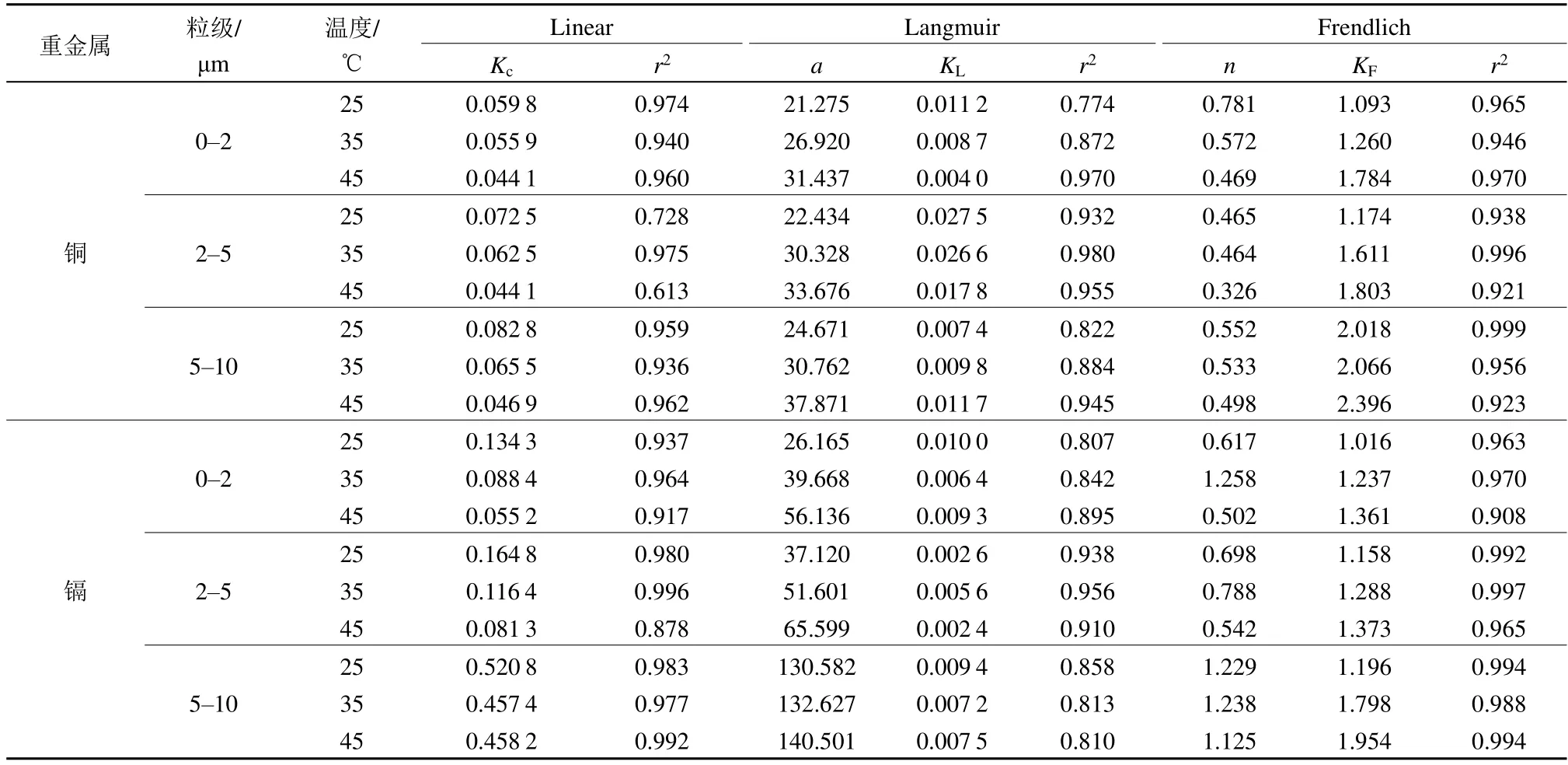
表3 煤胶体在不同温度下动力学方程拟合结果Table 3 Fitting results of coal colloid kinetic equation at different temperatures
由表4可知,在25、35、45 ℃下,不同粒级煤胶体对铜与镉的吸附实验数据经Linear方程拟合的相关系数r2拟合效果不佳;经Langmuir方程拟合的相关系数r2拟合效果较佳,经Freundlich方程拟合的相关系数r2拟合效果最佳,煤胶体对铜与镉的吸附更符合Freundlich方程吸附模型。
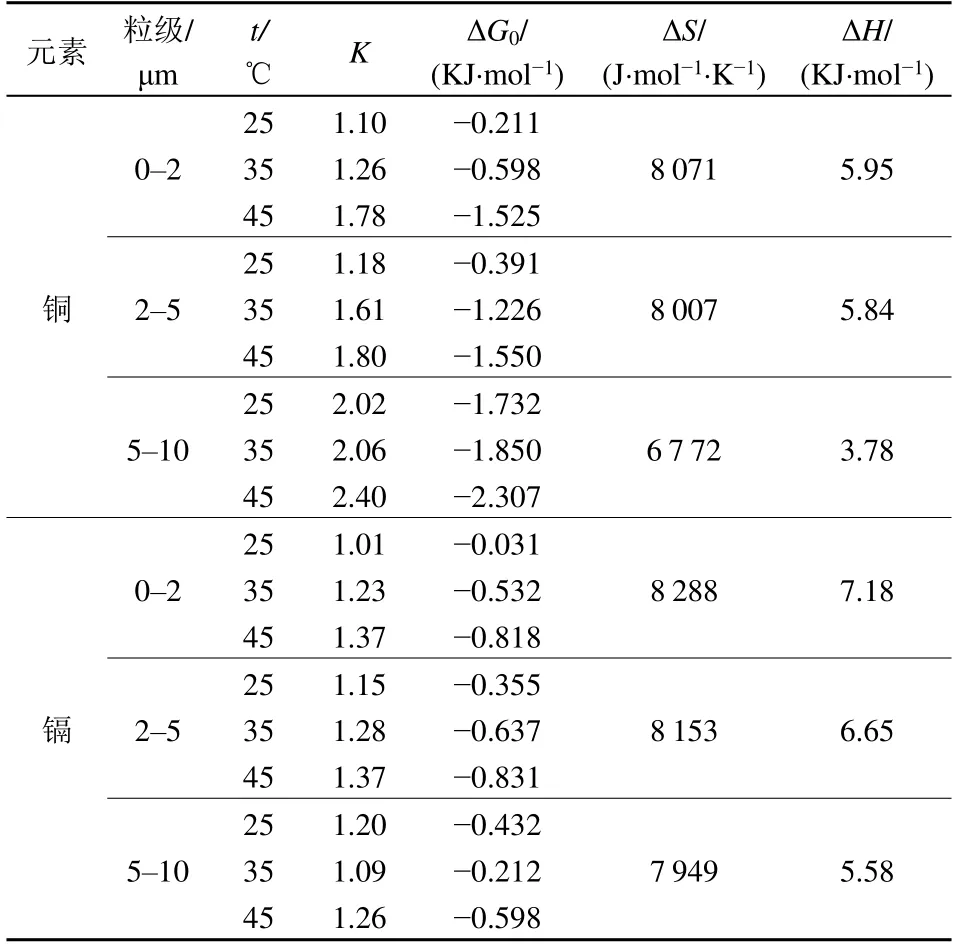
表4 煤胶体吸附铜与镉的热力学参数Table 4 Thermodynamic parameters of copper and cadmium adsorption by coal colloid
Freundlich方程中n表示土壤颗粒表面不规则程度,煤胶体对重金属吸附的n值变化不大(许端平等,2014);KF可描述吸附能力的强弱,KF越大,煤胶体与重金属离子结合强度越大,吸附效果越好,由表4可以看出,温度越高、粒径越小,KF越大,越有利于煤胶体对重金属的吸附。
对于同一粒级的煤胶体,随着温度的升高,煤胶体对铜、镉吸附量增加,表明煤胶体对铜、镉的吸附反应为吸热反应。温度的升高使重金属离子及其吸附剂的运动速率加快,因此重金属更容易被煤胶体吸附(车轶夫,2017)。
对于同一温度的煤胶体,随着粒径的增大,煤胶体对铜、镉的吸附量减少。可能是由于煤胶体粒径增大,其比表面积减小,与铜、镉的接触面积也减小,煤胶体对铜、镉的吸附量减少。
2.4 煤胶体对铜与镉吸附热力学参数计算
为了解煤胶体对铜与镉的吸附热力学特性,计算其相关热力学参数,煤胶体吸附铜与镉的热力学参数见表4。
由表4可知,ΔG0<0,说明煤胶体吸附反应为沿着正反应方向进行的自发反应,ΔG0的数值大小可表示吸附过程中驱动力的强弱,表4表现为随着温度的升高,吸附驱动力增大,说明了温度在胶体吸附能力方面的正效应(徐伟慧等,2018),为化学吸附;煤胶体粒径的减少也会增加煤胶体对铜与镉的吸附。ΔS>0,熵值增大,煤胶体对铜、镉吸附的混乱程度增加,反应更容易进行,由表4知增加温度、减小煤胶体粒径利于反应的进行;ΔH>0,说明煤胶体吸附为吸热反应,温度升高,反应更容易进行。
不同焓变对应的不同作用力见表5。

表5 不同作用引起的吸附反应焓变(薛杨,2017b)Table 5 Enthalpy change of adsorption reaction caused by different actions kJ·moL-1
Cu在0-2、2-5、5-10 μm粒级的煤胶体的ΔH分别为5.950、5.841、3.783;Cd在0-2、2-5、5-10 μm粒级的煤胶体的ΔH分别为7.179、6.654、5.580。由表5推断0-2 μm、2-5 μm的煤胶体吸附铜与0-5 μm的煤胶体吸附镉的吸附机理可能是范德华力、氢键、偶极键共同作用;而5-10 μm煤胶体吸附铜的吸附机理可能是氢键和偶极键共同作用;2-5 μm的煤胶体吸附铜、5-10 μm的煤胶体吸附镉的作用机理还可能是疏水作用,又有研究显示ΔH>0,ΔS>0为疏水力作用,ΔH较小,ΔS>0为静电力作用(Ross et al.,1981),本实验数据符合该规律。
3 结论
(1)随着煤胶体粒径增加,煤胶体的BET比表面积减小,孔径增大,总孔容量减小,有机质含量减少。
(2)吸附动力学实验表明,准二级动力学方程能够更贴切的描述煤胶体对铜、镉的吸附动力学过程(r²>0.99),吸附机理为化学吸附。铜的吸附速率常数大于镉,镉的平衡吸附量大于铜,随着煤胶体粒径的减小,吸附速率变快、平衡吸附量增大。
(3)等温吸附实验表明,Freundlich吸附模型能够更好的拟合煤胶体对重金属铜与镉吸附过程。温度越高,煤胶体对铜与镉的吸附能力越强,煤胶体吸附铜与镉是吸热反应,温度越高,煤胶体对铜与镉的吸附能力越强。
(4)煤胶体对铜、镉的吸附热力学参数均为ΔG0<0,ΔS>0,ΔH>0,说明其吸附可自发进行,为熵增的吸热反应。温度升高有利于煤胶体吸附铜与镉,为化学吸附。煤胶体粒径的减小也提高对铜与镉的吸附能力。

