非抑郁脑梗死患者卒中后疲劳的现状及影响因素分析
陈玉培 邹华 龚亚驰 冯扣兰 陈燕 彭美娣
(1.南通大学医学院护理学院,江苏 南通 226001;2.南通大学附属南通第三医院 南通市第三人民医院,江苏 南通 226006)
卒中后疲劳(post-stroke fatigue,PSF)是脑卒中常见的后遗症,临床主要表现为患者精神萎靡,在简单活动下即出现不成比例的疲惫感并且休息后不能缓解[1-2]。若未及时发现和处理,PSF不仅会影响患者康复进程及健康相关生活质量,还会增加患者自杀的风险[3]。但目前PSF的病理生理学尚未阐明,对其可能的影响因素研究也在探索中。抑郁与疲劳均属于情感障碍,并且卒中后抑郁的发病率高达18%~33%[4]。尽管PSF已被从卒中后心理情感的后遗症中区分出来[5],然而目前仍较少报道将抑郁症状从PSF中独立出来,因此可能会出现PSF被抑郁症状掩盖的情况。本研究探讨非抑郁脑梗死患者PSF发生现状及影响因素,现报告如下。
1 资料与方法
1.1一般资料 选取2021年4月-2022年6月收治于我院院神经内科、老年医学科的脑卒中患者199例。样本量估算采用 GPower 3.1.9软件进行,运行后得到所需样本量至少为158例,本研究纳入199例符合样本量要求。纳入标准:(1)符合《中国急性缺血性脑卒中诊治指南2018》[6]中的诊断标准并经脑CT/MRI 确诊。(2)住院期间汉密尔顿抑郁量表(hamilton depression scale,HAMD)[7]评分<8分。(3)生命体征稳定。(4)认知能力正常,简易智力状态检查量表(mini-mental state examination,MMSE)评分≥24分。(5)签署知情同意书,自愿参加本研究。排除标准:(1)卒中前疲劳。(2)既往有严重疾病者(心、肺、肝、肾功能障碍)等。(3)不配合及资料不全者。本研究已通过南通市第三人民医院医学伦理委员会批准(审批号:EK2021008)。
1.2方法
1.2.2研究工具
1.2.2.1一般资料与疾病相关资料 (1)一般资料:采集患者的血压、身高、体重、BMI、年龄、性别、婚姻状况、文化程度、是否有医保等。(2)疾病史:采集患者高血压、糖尿病、冠心病、卒中及房颤史。(3)影像学资料:CT或磁共振检查[10]。(4)血样指标:中性粒细胞、淋巴细胞、单核细胞、血红蛋白量、血小板值、总胆固醇、甘油三酯、低密度脂蛋白、高密度脂蛋白、空腹血糖等。
1.2.2.2疲劳及相关指标 (1)疲劳程度:采用疲劳严重度量表(fatigue severity scale,FSS),其由9个条目组成,每个条目根据患者对疲劳严重程度的评价将结果评为1~7分,总分为9~63分。≥36分判断为PSF[11],该量表具有较好的内部一致性。(2)神经功能缺损程度:应用美国国立卫生研究院卒中量表(national institute of health stroke scale,NIHSS)[7]对患者神经功能情况进行评估,NIHSS评分越高,说明患者神经功能缺损症状越严重。 (3)疼痛程度:采用数字等级评定量表(numerical rating scale,NRS)[9]评分,以0~10分代表不同程度的疼痛,让患者自行选择代表疼痛的数值,0分为无痛,1~3分为轻度疼痛,4~6分为中度疼痛,7~10分为重度疼痛。(4)吞咽功能:采用洼田饮水试验,判断患者喝下30 mL温开水所需时间及呛咳情况,分为1~5级,1级为正常吞咽,≥3级即吞咽功能障碍。(5)睡眠质量:应用匹兹堡睡眠质量指数(pittsburgh sleep quality index,PSQI)[12]评价,该量表包括7个维度,共18个条目,每个维度计0~3分,累加总分为0~21分,得分越高表示睡眠质量越差。Cronbach′s α=0.83,具有较好的内部一致性。(6)日常生活活动能力(activities of daily living ,ADL):采用Barthel指数[5]评定,包括10条条目,总分为0~100分,≤60分则表现为依赖。(7)肌少症:采用肌少症简易5项评分问卷(SARC-F)[13],包括5个条目,根据患者的身体情况进行评分,每个条目分别计0~2分,总分≥4分为肌少症。
1.2.3资料收集方法 入院时收集患者的一般资料、疾病病史及影像学资料[8];入院次日清晨采空腹血样本。抑郁等精神疾病,请精神科医生确诊。FSS、NIHSS、PSQI等问卷于患者入院后病情稳定后进行采集[9];PSF在发病后2周内进行评估。
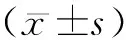
2 结果
2.1非抑郁脑梗死患者发生PSF状况及单因素分析 纳入的199例脑梗死患者中,PSF组71 例(35.6%),非PSF组128例(64.4%),见表1。
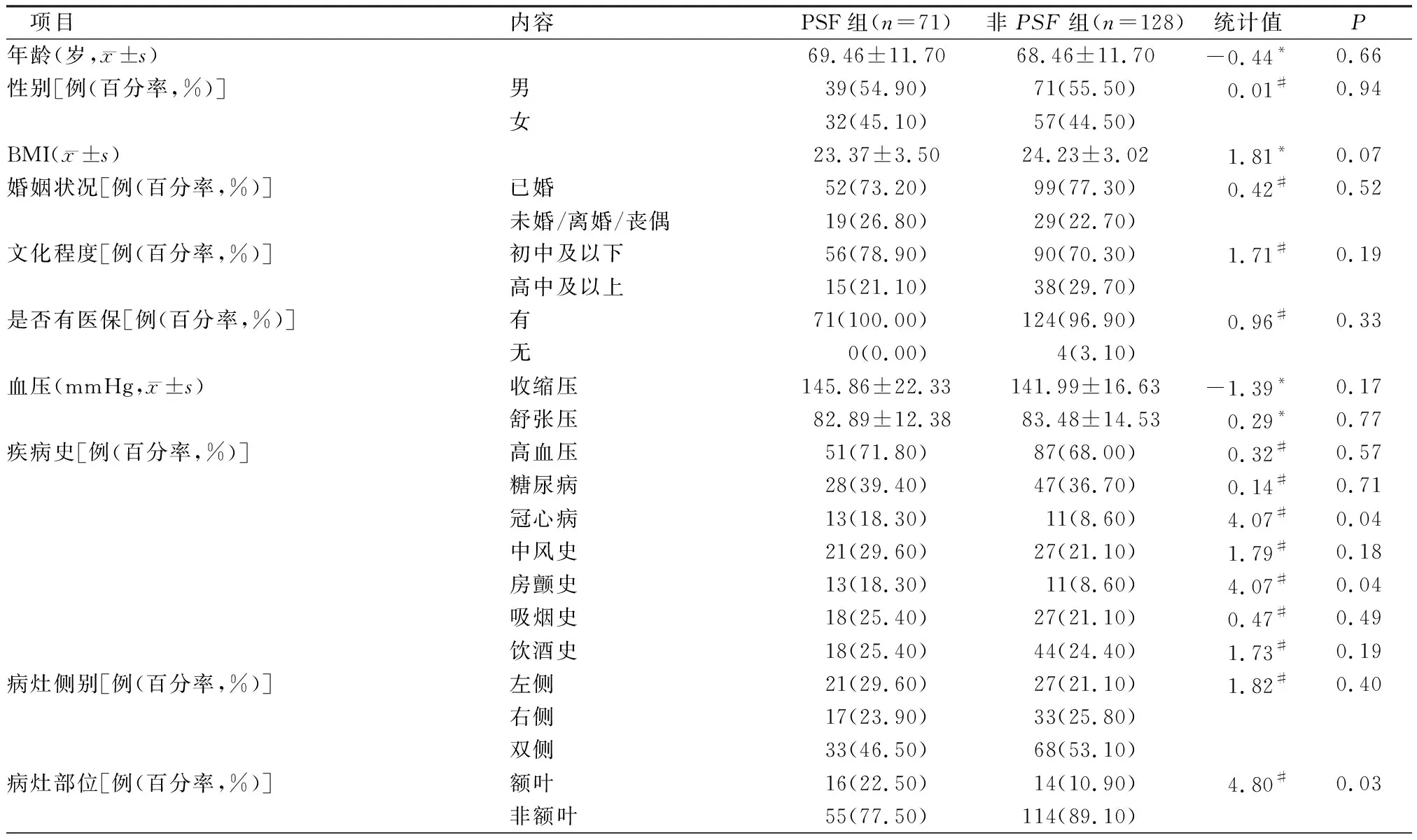
表1 非抑郁脑梗死患者发生PSF状况及单因素分析(n=199)
2.2非抑郁脑梗死患者发生PSF的多因素分析 以患者是否发生PSF(否=0,是=1)作为因变量,将单因素分析中10个P<0.1的因素(BMI、冠心病史、房颤史、病灶部位、神经功能缺损程度、吞咽功能、ADL、疼痛程度、睡眠质量、肌少症)作为自变量进行logistic回归分析。结果显示,病灶部位:额叶、PSQI总分、肌少症为独立影响因素,自变量赋值表,见表2。PPSF的多因素logistic回归分析,见表3。

表2 自变量赋值表
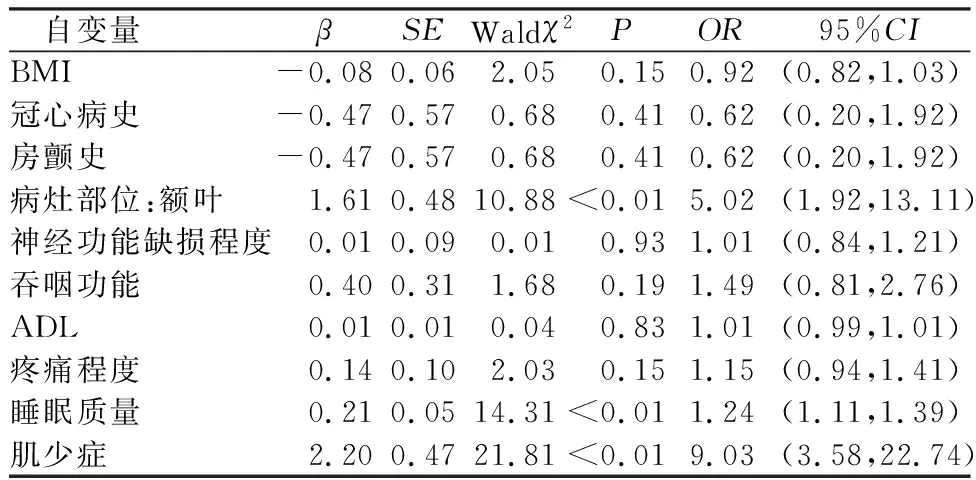
表3 PSF的多因素logistic回归分析
2.3非抑郁脑梗死患者睡眠特征比较 将PSQI中的7个维度与PSF做单因素分析,结果表显示:睡眠质量(P<0.001)、入睡时间(P=0.032)、日间功能(P<0.001)差异有统计学意义,见表4。

表4 非抑郁脑梗死患者PSF组与非PSF组的睡眠特征比较[n=199,分,M(P25,P75)]
3 讨论
3.1非抑郁脑梗死患者发生PSF的现状 本研究PSF的发生率为35.67%,在25%~85%的发病率范围内[14]。低于Ho等[15]研究结果(52.7%),可能由于本研究仅纳入了非抑郁的脑梗死患者。曾有综述[16]表明PSF与抑郁发病机制类似,均是由炎症细胞因子介导,从而影响单胺神经递质的合成和活性,本研究已规避抑郁对PSF的影响。
3.2非抑郁脑梗死患者PSF影响因素
3.2.1病灶部位:额叶 本研究结果显示,与非PSF脑梗死患者相比,额叶梗死具有统计学意义(P=0.001),额叶梗死是PSF的独立影响因素,这与吴春薇[17]等研究一致。额叶的主要功能与精神、语言以及随意运动有关,额叶损伤会严重影响神经回路的完整性,降低情绪信息传递的速度,因而患者更容易出现情感障碍。
3.2.2睡眠质量 本研究PSF患者的睡眠情况表现均低于非PSF患者(P<0.05),且PISQ总分是PSF的独立影响因素。这与Ho等[15]研究结果一致。卒中引起的脑部变化可能会改变个体的睡眠-觉醒周期和睡眠昼夜节律,并且影响睡眠的质量[18],造成各种睡眠障碍,而较差的睡眠质量及睡眠障碍会通过大脑活动促使疲劳的发生。本研究中睡眠特征单因素分析显示,睡眠质量、入睡时间、日间功能2组比较差异有统计学意义(P<0.05),提示医护人员可针对这3方面采取对应措施以提高患者的睡眠指数。如为患者提供安静舒适的环境,减少患者入睡期间的操作治疗;与患者及家属制定每日生活规划,鼓励其养成健康的生活习惯;提倡适当运动,缩短患者白天卧床时间等[19]。
3.2.3肌少症 本研究结果显示,肌少症是非抑郁脑梗死患者PSF的独立影响因素(P<0.05)。Neefjes等[20]报道骨骼肌质量下降是疲劳的潜在原因,突触前运动神经元和突触后肌纤维的改变可能导致肌肉去神经化,损耗神经肌肉功能从而导致疲劳[21]。在一项关于癌因性疲劳研究[14]中表明,增加肌肉质量的运动干预可以有效减轻患者的疲劳感。Suya等[22]曾建立了基于95例患者的PSF风险模型,该研究在没有排除抑郁的前提下得出与本研究相似结论。由于肌少症是慢性疾病,且不容易被发现。此对肌少症患者,医护人员应增加健康宣教,鼓励其保持营养均衡,加强运动锻炼。
综上所述,本研究表明病灶部位为额叶、睡眠质量、肌少症为非抑郁脑梗死PSF患者的独立影响因素。然而,本研究为单中心研究,样本量较小,影响因素可能未完全覆盖。接下来笔者团队将进行多中心,大样本量的调查,使用循证方法进行全面的文献检索及结合临床调查情况,采用理论模型对影响PSF的因素进行系统归纳,以便临床及早识别及干预。

