基于HPLC-Q-TOF-MS/MS技术解析苏木配方颗粒的化学物质组成及裂解规律
颜继忠,吴亚梦,曾结林,白 芮,张 慧
(浙江工业大学 药学院,浙江 杭州 310014)
苏木为豆科植物苏木CaesalpiniasappanL.的干燥心材[1],原产于东南亚和南印度,常用作天然红色染料、食用色素,以及作为中药用于镇痛消炎和促进血液循环。研究证实这种药用植物还具有促进血管舒张、抗动脉粥样硬化、抗氧化、抗菌和抗炎等作用[1]。苏木化学成分复杂,其含有大量的黄酮类成分[2],主要包括黄酮类(Flavones)、黄酮醇类(Flavonol)、二氢黄酮类(Dihydroflavone)、二氢黄酮醇类(Dihydroflavonol)、异黄酮类(Isoflavone)、查尔酮类(Chalcones)、黄烷酮类(Flavanes)、花色素类(Anthocyanidins)和高异黄酮类(Homoisoflavonoids)等[2],以及其他药理活性成分,如原苏木素类(Protosappanins)。
苏木配方颗粒是由苏木饮片经过提取、浓缩、干燥和制粒等工序,供医生临床配方使用的单味中药浓缩颗粒。目前,关于苏木的文献报道主要集中在醇提物的化学成分以及药理作用研究,对苏木水提液中的化学成分研究较少,且尚未见苏木配方颗粒的化学组成文献报道。笔者利用HPLC-Q-TOF-MS/MS技术对苏木配方颗粒进行化学成分分析和裂解规律研究,归纳了查尔酮类、高异黄酮类和原苏木素类化合物在负离子模式下的裂解规律,为后续苏木配方颗粒的质量控制提供理论基础。
1 仪器与材料
1.1 仪 器
Agilent 1290型高效液相色谱仪(美国Agilent科技有限公司);ACQUITY UPLC(美国Waters公司)-Triple TOFTM 5600+型高分辨质谱系统(美国AB Sciex公司);电子天平(YP502N,上海菁海仪器有限公司),万分之一电子天平(BS124,赛多利斯科学仪器北京有限公司);旋转蒸发仪(R210+V700,瑞士Buchi公司);数控超声波清洗器(KQ-250DE,巩义市予华仪器有限公司)。
1.2 材 料
色谱级甲醇(TEDIA);色谱级乙腈(TEDIA);娃哈哈纯净水;(±)原苏木素B(购于成都普思生物科技股份有限公司,批号:PS0359-0020);巴西苏木素对照品(购于成都普思生物科技股份有限公司,批号:PS0358-0025);苏木配方颗粒(批次:19507)由浙江贝尼菲特药业有限公司提供。
2 方 法
2.1 检测条件
2.1.1 色谱条件
以十八烷基硅烷键合硅胶为填充剂。以乙腈为流动相A,以纯水为流动相B,梯度洗脱:0~<15 min,15% A;15~<30 min,15%~30% A;30~40 min,30%~100% A;流速1.0 mL/min;检测波长285 nm;柱温30 ℃;进样量10 μL。
2.1.2 质谱条件
采用Triple TOF 5600+质谱仪。在ESI正、负离子模式下对供试品溶液进行检测。一级质谱扫描范围m/z为100~1 500,二级质谱扫描范围m/z为50~1 500;负离子模式,雾化气(GSI)为50 Psi;气帘气(CUR)为35 Psi;离子源温度(TEM)为550 ℃;离子源电压(IS)为-4 500 V;一级扫描去簇电压为80 V;碰撞能量为5 V。正离子模式,雾化气(GSI)为50 Psi;气帘气(CUR)为35 Psi;离子源温度(TEM)为600 ℃;离子源电压(RS)为+5 500 V;一级扫描去簇电压为80 V;碰撞能量为5 V。
2.2 溶液的配制
取苏木配方颗粒适量,研细,取0.1 g,置于具塞锥形瓶中,加甲醇50 mL后称定质量,超声处理(功率250 W,频率40 kHz)20 min,放冷,再次称定质量,用甲醇溶液补足减失质量,0.22 μm微孔滤膜过滤备用。
3 结果与分析
3.1 基于HPLC-Q-TOF-MS/MS的苏木配方颗粒化学成分定性表征
通过优化裂解电压、扫描参数,确定最佳质谱分析条件,对苏木配方颗粒在正、负离子条件下进行检测,总离子流图如图1所示。检测结果表明:在负离子模式下苏木配方颗粒的响应值较高,特征吸收峰较多,因此,主要研究负离子模式下的化学成分以及推导负离子模式下的质谱裂解规律。通过对照品、参考文献及相关数据库的比对分析,共鉴定了61个化合物:包括24个黄酮类成分、6个酚酸类成分、5个巴西苏木素类成分、4个原苏木素类成分、4个查尔酮类、4个高异黄酮成分、2个糖类成分、2个生物碱成分、3个二苯类成分、2个香豆素类、3个未知成分、1个苯丙素类和1个氨基酸;其中有12个化合物是首次在苏木中鉴定的成分;化学成分信息结果如表1所示。按照成分的不同母核结构,将苏木中的查尔酮类、高异黄酮类和原苏木素类化合物进行归纳总结(图2),并将对这3类典型药理活性化合物进行裂解规律解析。
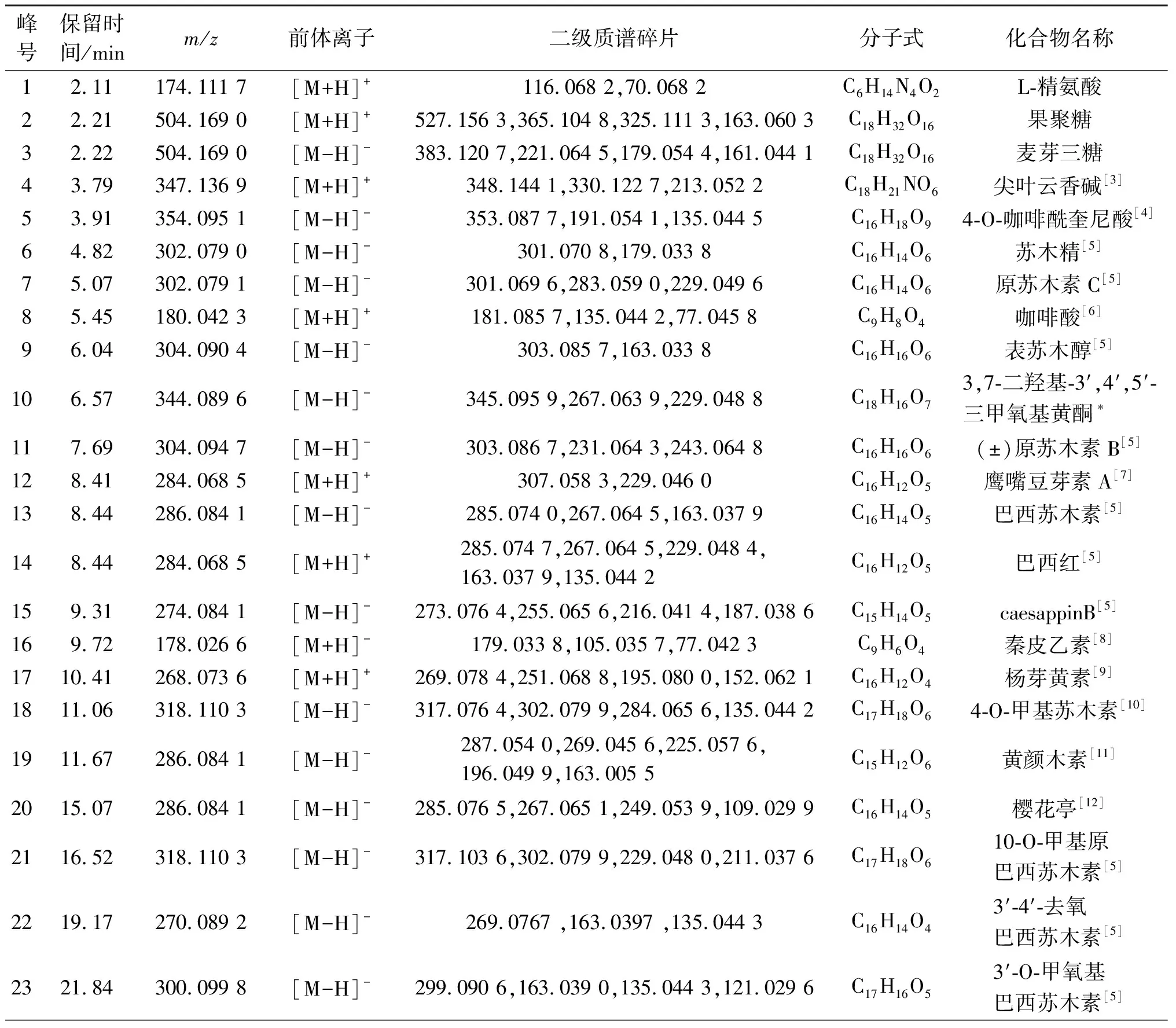
表1 苏木配方颗粒化学成分信息表

图1 苏木配方颗粒总离子流图
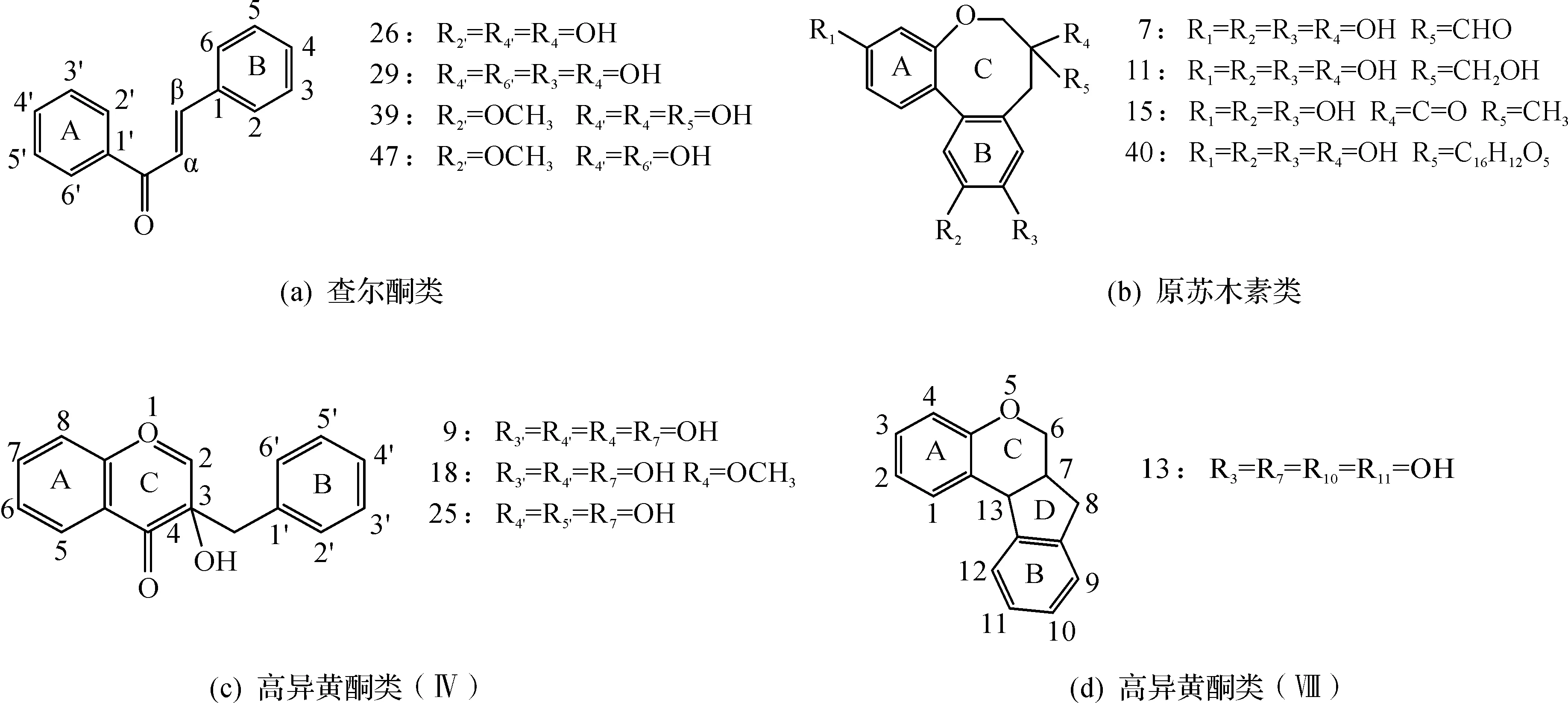
图2 苏木中查尔酮类、原苏木素类和高异黄酮类成分的基本骨架
3.2 查尔酮化合物的裂解规律解析
查尔酮化合物被认为是黄酮类化合物和异黄酮类化合物的前体,属于芳香族烯酮类化合物,基本结构为1,3-二苯基-2-烯-1-酮[29]。苏木配方颗粒中共鉴定4个查尔酮类化合物,分别为化合物26,29,39,47。查尔酮类裂解时会有典型的中性丢失,包括H2O(18Da)、CO(28Da)等,同时会产生m/z为135[C8H7O2]-和91[C6H3O]-的典型碎片离子。B环取代基和位置均相同时区别在于A环取代基的类型和位置,从而影响裂解。对于B环上含有羟基取代的查尔酮类,由于间位羟基与环外的双键以及羰基的共轭受阻,从而使得生成的负离子稳定性不强,因而C-3羟基优先丢失。若A环上连有甲氧基,甲氧基作为推电子基团,提高了B环的电子云密度,增强了共轭效应,因而相对稳定,优先丢失H2O(18Da),后续进一步脱去·CH3碎片离子且易与B环一起发生断裂。受2′位置羟基的影响,B环易丢失,若A环上存在羟基,首先其氢重排后再失去CO(28Da)碎片离子,且取代基种类会影响碎片的丰度。
化合物29(Butein,紫铆因)在负离子模式下丢失一分子H,得到的准分子离子峰m/z为271.060 3[M-H]-,在准分子离子峰的基础上,α裂解产生m/z为135.043 9[M-H-C7H4O3]-或91.020 9[M-H-C9H8O4]-的碎片离子,与化合物39的裂解途径基本相似。化合物39(Sappanchalcone,苏木查尔酮)在负离子模式下丢失一分子H,产生准分子离子峰m/z为285.075 8[M-H]-,在准分子离子峰的基础上,B环失去一分子·CH3所产生的m/z为270.052 2[M-H-CH3]-,B环丢失得到m/z为161.023 2[M-H-C7H8O2]-的碎片离子。同时也有可能断裂产生m/z约为135[C8H7O2]-或91[C6H3O]-的碎片离子。可能裂解途径如图3所示。

图3 苏木中查尔酮类在负离子模式下的裂解规律
3.3 高异黄酮类化合物的裂解规律解析
高异黄酮类是比异黄酮类的B、C环之间多1个亚甲基的特殊黄酮类,因亚甲基的存在容易导致C-3处的断裂,从而产生失去B环的特征碎片离子[30]。取代基一般为—OH、—OCH3,共有8种类型,其中高异黄酮类(Ⅳ)的结构特征为母体结构为3-羟基二氢高异黄酮,A环7位为羟基取代;高异黄酮类(Ⅷ)的结构特征为母体结构是由A、B、C和D四环构成,并且C-4没有连接羰基。在苏木中,根据C-4位取代基的不同而划分为苏木酮类和苏木醇类。苏木配方颗粒中共鉴定出4个高异黄酮类成分,分别为化合物9,13,18,25。高异黄酮类发生的中性碎片丢失如CO(28Da)、CH3(15Da)和H2O(18Da)等,生成m/z为135[C8H7O2]-、163[C9H7O3]-和179[C9H7O4]-等典型碎片离子。当C环上有甲氧基取代时,则会产生中性丢失CH3(15Da),且优于B环(Ⅷ型)发生丢失。当C环上无甲氧基取代时,容易发生C环的断裂,C环开环变为五元环,以及A环本身也会发生裂解反应。
化合物9(Episappanol,表苏木醇)在负离子模式下丢失一分子H,得到的准分子离子峰m/z为303.085 7[M-H]-,在准分子离子峰的基础上,B环(Ⅳ)直接断裂得到m/z为179.033 4[M-H-C7H8O2]-和123.044 2[M-H-C9H8O4]-的碎片,B环丢失,产生m/z为148.016 0[M-H-C8H10O3]-的亚稳离子,经诱导裂解后产生m/z为135.044 4[M-H-C8H7O4]-的碎片离子,失去一分子·CH2,所产生的m/z为121.021 9[M-H-C9H9O4]-。化合物18(4-O-Methylsappanol,4-O-甲基苏木素)在负离子模式下丢失一分子H,得到的准分子离子峰m/z为317.076 4[M-H]-,失去一分子·CH3得到302.079 9[M-H-CH3]-,失一分子H2O得到284.065 6[M-H-CH3-H2O]-的碎片离子,C环开环断裂得到m/z为135.044 2[M-H-C9H10O4]-的碎片离子。化合物25(Sappanone B,苏木酮B)在负离子模式下丢失一分子H,得到的准分子离子峰m/z为301.071 1[M-H]-,在准分子离子峰的基础上,B环(Ⅳ型)断裂得到m/z为179.033 4[M-H-C7H6O2]-,和丰度较低m/z为135.044 7[M-H-C8H6O4]-的碎片离子。失去一分子CO后得到151.039 0[M-H-C8H6O3]-。m/z为179.033 8[M-H-C7H6O2]-失去·C2H2得到m/z为109.030 5[M-H-C10H8O4]-的碎片离子。化合物13(Brazilin,巴西苏木素)在负离子模式下丢失一分子H得到的准分子离子峰m/z为285.074 7[M-H]-,在准分子离子峰的基础上,丢失一分子H2O,得到m/z为267.064 5[M-H-H2O]-的碎片离子,m/z为163.037 9[M-H-C7H6O2]-由六元环C环与五元环D环直接断裂形成。丢失一分子CO,所产生的m/z为135.044 2[M-H-C8H6O3]-,同时也有可能C环开环断裂产生m/z为121.028 9[M-H-C9H8O3]-和163.037 9[M-H-C7H6O2]-的碎片离子。易发生断裂的母核位置以及可能裂解途径如图4所示。
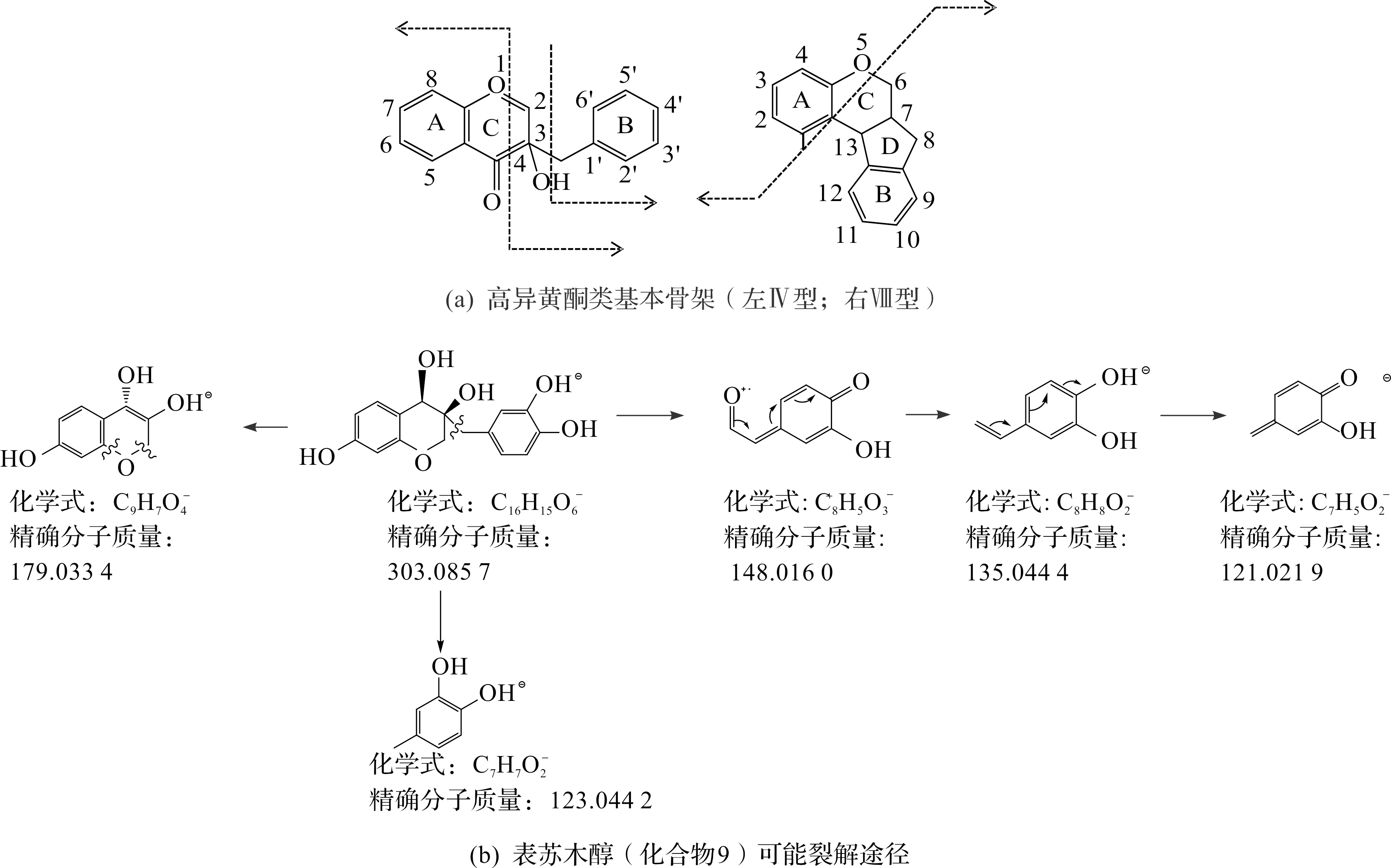
图4 苏木中高异黄酮类在负离子模式下的裂解规律
3.4 原苏木素类化合物的裂解规律解析
原苏木素类是苏木中特有的一类成分,它们具有一个基本的母核结构。苏木配方颗粒中共鉴定出4个原苏木素类成分,分别为化合物7,11,15,40。其中,化合物21是化合物11的衍生物,化合物40由化合物7与化合物11聚合形成。原苏木素类发生的中性碎片丢失主要以H2O(18Da)为主,且会产生特征碎片离子,其m/z为229[C13H9O4]-或211[C13H7O3]-。C环上的R基团并未与苯环共轭,因此性质相对于其他环上的基团较为活泼,容易丢失。同时C环由于跨环张力,八元环相对不是很稳定,易发生开环行为,或形成六元环化合物。当C环上连有甲氧基时,则优于其他R基团发生中性丢失,或者同时发生断裂。
化合物11(Protosappanin B,原苏木素B)在负离子模式下丢失一分子H,得到的准分子离子峰m/z为303.086 7[M-H]-,在准分子离子峰的基础上,丢失一分子H2O,得到m/z为285.076 6[M-H-H2O]-的碎片离子,C环断裂成得到m/z为231.064 3[M-H-C3H4O2]-和243.064 8[M-H-C2H4O2]-的碎片离子,m/z为243.064 8[M-H-C2H4O2]-闭环得到m/z为211.039 1[M-H-C3H8O3]-的碎片离子。化合物7(Protosappanin C,原苏木素C)在负离子模式下丢失一分子H,得到的准分子离子峰m/z为301.069 6[M-H]-,在准分子离子峰的基础上,丢失一分子H2O,得到m/z为283.059 0[M-H-H2O]-的碎片离子,C环断裂所生成的m/z为229.049 6[M-H-C3H4O2]-,丢失一分子H2O,得到m/z为211.038 8[M-H-C3H6O3]-的碎片离子。化合物40(Protosappanin E1/E2,原苏木素E1/E2)在负离子模式下丢失一分子H,得到的准分子离子峰m/z为585.140 2[M-H]-,在准分子离子峰的基础上断裂,得到m/z为283.060 0[M-H-C16H14O6]-的碎片离子,与化合物7中的m/z为283[M-H-H2O]-相吻合,C环开环断裂形成m/z为229.049 4[M-H-C19H16O7]-的碎片离子。易发生断裂的母核位置以及可能裂解途径如图5所示。
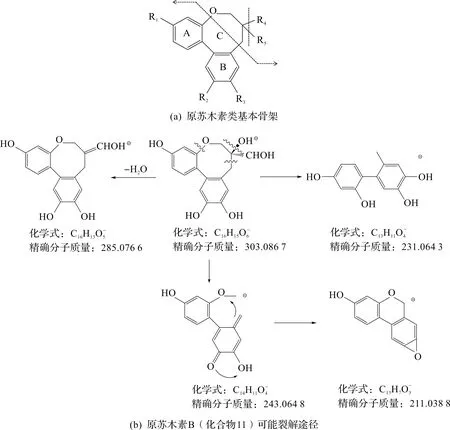
图5 苏木中原苏木素类在负离子模式下的裂解规律
4 结 论
采用HPLC-Q-TOF-MS/MS技术解析了苏木配方颗粒中化学成分以及裂解规律。根据化合物的一级、二级质谱信息,通过对照品、参考文献及相关数据库的比对分析,共鉴别了61个化合物,包括24个黄酮类成分、4个原苏木素类成分、4个高异黄酮类成分和4个查尔酮类成分等。总结推导了查尔酮类、高异黄酮类和原苏木素类的质谱裂解规律。查尔酮类主要的裂解途径为脱掉中性分子以及丢失B环,主要产生m/z为135[C8H7O2]-或91[C6H3O]-的特征碎片离子;高异黄酮类主要的裂解途径为脱去H2O,脱去甲氧基、B环断裂,产生m/z为135[C8H7O2]-、163[C9H7O3]-和179[C9H7O4]-等特征碎片离子;原苏木素类主要的裂解途径为脱去H2O、C环断裂,产生m/z为229[C13H9O4]-或211[C13H7O3]-的特征碎片离子。还推导出了查尔酮类、原苏木素类化合物在负离子模式下的裂解规律,并总结了3类化合物在负离子模式下的特征碎片离子,研究成果将有助于苏木配方颗粒的化学物质基础研究,同时为该品种的科学质量控制奠定基础。
本文得到了浙江工业大学研究生实践基地建设项目(GZ21231160006,GZ21881160011)的资助。

