CT联合Hcy、Ca2+对ICH预后效果评估分析*
陈振雄,周 巍
(咸宁市第一人民医院,湖北 咸宁 437000)
脑出血(intracerebral hemorrhage,ICH)是指非外伤性脑实质内血管破裂引起的出血。该病的年均发病率为24.6/10万人,亚洲人群年发病率51.8/10万人,且20余年来持续上升[1-2]。ICH在30d内死亡率可达到30~50%,一年内超过75%患者可能残疾或死亡;仅有不到20%患者预后良好[3]。ICH的发病机制复杂,目前针对ICH患者病情及预后的快速检测指标尚未完全明确,亟需设计具有较高证据等级的临床研究来填补指南空白,从而更好地指导临床实践[4-5]。目前,有学者指出Hcy、Ca2+表达是影响ICH患者预后重要指标,但目前国内关于应用CT联合生化指标对患者进行预后评估相关研究较少。笔者就此进行研究,报道如下。
1 资料与方法
1.1 一般资料
研究对象选取2018年9月至2021年9月在我院神经外科收治的ICH患者合计240例进行研究。纳入标准:①符合《高血压性脑出血中国多学科诊治指南》的诊断标准,并行临床头颅计算机断层摄影术(CT)检查明确诊断(均为幕上出血);②年龄在30~65岁;③患者或家属认知功能正常;④无相关影像学检查禁忌症,或造影剂过敏反应情况,影像学检查过程中能够积极配合者;⑤抽血化验前未行手术治疗;⑥发病至行头颅CT检查<8h;⑦发病至血生化检查时间<24h;⑧临床资料收集完整无缺失;⑨患者及其家属签署本研究知情同意书,并经我院医学伦理会批准认证。排除标准:①合并严重的心律失常、心肌炎、心力衰竭,严重肝肾疾病、糖尿病、呼吸系统疾病、恶性肿瘤、严重感染等病史者;②伴有严重精神障碍者;③近期(1d内)服用过影响血清Hcy、CRP、D-D、Ca2+水平代谢药物者;④溶栓或脑血管造影,继发于动脉或静脉脑梗塞、动脉瘤、脑肿瘤相关脑出血的出血;⑤外伤后脑出血;⑥丘脑出血;⑦并发脑室铸型及梗阻性脑积水;⑧幕下出血;⑨合并严重感染者;⑩血液系统疾病或恶性肿瘤导致的出血。
1.2 方法
所有患者入院后建立病案资料并整合为患者数据库,收录数据包括人口统计学资料(年龄、性别等基线资料)、合并疾病(高血压、糖尿病、高脂血症等常见合并疾病)、卒中或出血病史、不良生活习惯(抽烟、饮酒、熬夜等)、血压、血脂、哥斯拉昏迷量表评分、血肿特征、血常规、影像学检测[混合征、黑(空)洞征]、入院时Hcy、Ca2+水平。所有患者资料入库后由科室负责人确认资料库建库完成,并于同一计算机上进行调用及资料管理。根据预后将所有ICH患者分为预后良好组(MRS评分≤2分)149例及预后不良组(MRS评分>2分)91例。
影像学检查方法:检测仪器采用80排160层CT检测。参数设置:管电压120kv,管电流200~300mA,层厚0.625mm,层间距0.625mm,旋转速度0.5r/s,准直器320×0.625,螺距1。重建层厚0.7mm,重建层间距0.5mm,使用迭代算法计算。检测完成后使用惠普Z600工作站进行横轴位多平面图像重建。影像学分析均由影像科医生完成,分析患者血肿体积、血肿形状及影像学表达特征等。
Hcy:取患者外周静脉血,3000r/min离心15min,取上清液,采用循环酶法检测。试剂盒购自上海酶联生物科技有限公司。Ca2+:患者样本获取同上,使用全自动生化分析仪检测。
对患者所有资料进行分析比较,采用单因素分析与多因素回归分析方法寻找患者发病及预后影响因素,并利用危险因素进行模型回归:以分组为基础,将单因素分析中筛选出的差异项作为回归自变量,以分组作为回归因变量进行多因素回归分析。根据回归分析结果中相关系数β建立多指标联合评估模型。模型公式Y=ex/(1+ex)。
1.3 观察指标
①不同预后患者基线资料比较。②不同预后患者影像学资料比较。③不同预后患者Hcy、Ca2+水平比较。④预后不良危险因素相关性分析。⑤联合模型预后评估效能验证。
1.4 统计学方法

2 结 果
2.1 不同预后患者基线资料比较
预后不良组患者收缩压、舒张压高于预后良好组,差异具有统计学意义(P<0.05),两组患者年龄、合并疾病、性别组成、卒中病史、出血部位组成、血脂等指标差异不具统计学意义(P>0.05),见表1。
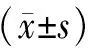
表1 不同预后患者基线资料的比较
2.2 不同预后患者影像学资料的比较
预后不良组患者血肿体积高于预后良好组,血肿形状不规则、混合征、黑(空)洞征、卫星小血肿检出率高于预后良好组,差异具有统计学意义(P<0.05),见表2。

表2 不同预后患者影像学资料的比较
2.3 不同预后患者Hcy、Ca2+水平比较
预后不良组患者Hcy高于预后良好组,Ca2+水平低于预后良好组,差异具有统计学意义(P<0.05),见表3。
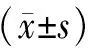
表3 不同预后患者Hcy、Ca2+水平比较
2.4 预后不良危险因素相关性分析
根据ICH患者预后单因素分析结果,筛选出收缩压、舒张压、血肿体积、Hcy、Ca2+等因素作为患者预后不良危险因素自变量,变量赋值情况如表4所示。以患者预后分组作为相关性分析因变量,进行二元Logistic回归分析,结果显示:收缩压、舒张压、血肿体积、Hcy水平升高,Ca2+降低及、混合征、卫星小血肿是患者预后不良独立危险因素,具体如表5所示。本研究结果获得的ICH发病相关因素的Logistic回归模型如公式所示:X=0.183Hcy-0.447Ca2+0.032收缩压+0.049舒张压+0.420血肿体积+1.065混合征+0.996卫星小血肿。

表5 患者预后不良危险因素二元Logistic相关性分析
2.5 联合模型预后评估效能验证
绘制上述模型的ROC曲线,如图1所示。并利用该模型对入组的患者进行预后评估,结果显示:联合模型对患者预后评估具有更优效能,曲线下AUC为0.865,高于单独应用影像学检测或单独指标评估,具体结果见表6。
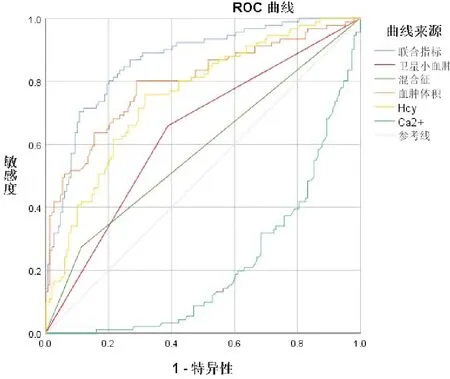
图1 联合模型评估患者预后ROC曲线(注:联合模型曲线下面积0.865)
3 讨 论
ICH是指非外伤性脑实质内血管破裂引起的出血。ICH占全部脑卒中的20%~30%,急性期病死率为30%~40%[6]。ICH具有发病急、病情进展迅速、致残率高等特点,对病情分级及预后的尽早评估有助于患者治疗方案及时调整,改善患者预后。本研究通过对患者基线资料、影像学治疗及血清Hcy、Ca2+水平与ICH预后关系进行分析,整合多指标联合诊断评估模型,旨在为脑出血患者预后评估方案完善及进一步研究提供参考。
本研究可见,在患者基线资料中,仅有血压与患者预后呈现相关性,合并疾病、年龄等与患者预后无相关性。分析原因,血压较高患者血流压力及血管腔内压力较高,发生脑出血后,患者二次出血及持续出血风险更高,患者血肿扩大可能性随之升高。这可能因为血压影响患者预后的最主要作用机制之一;其次,高血压还会引起患者血管粥样硬化等脑血管疾病,这也可能是血压升高引起患者不良预后的原因。但本研究发现,合并高血压却不是不良预后的危险因素,分析原因可能为人体血压本身存在波动,轻微高血压并不会引起患者血管腔压力及血管病变的显著波动和变化,因此,对于合并高血压患者而言,控制其病情是促进患者转归的重要手段。目前,CT检测是脑出血患者最主要病情评估方式,能直观反映患者脑内血肿体积、形状等参数,其中混合征、黑(空)洞征及合并卫星小血肿均是患者不良预后的重要影响因素。
Hcy是从蛋氨酸中提取的一种含琉基氨基酸,可引起血脑屏障通透性增加,损害血管完整性,是动脉粥样硬化形成的重要影响因素之一,同时也参与ICH病情发展进程。本研究发现,高Hcy表达是ICH患者预后不良的独立危险因素,结合既往研究,笔者分析,其作用机制可能为[7-10]:①Hcy对ICH患者血管内皮细胞毒性作用:高水平Hcy可引起患者血管内壁内皮细胞损伤,导致患者血管功能降低,同时高水平Hcy还能损伤患者血管内壁胶原纤维及弹力层,降低患者脑血管内皮细胞分裂及稳定性,引起血脑屏障损伤,细胞通透性增加,导致细胞间组织液增加,从而引起血浆溢出及血肿吸收能力减弱,加重患者脑神经损伤症状。②高Hcy引起患者血管结构变化:Hcy具有加快胶原纤维溶解及减弱患者血管壁弹力作用,其高水平表达可引起患者血管壁纤维化,导致血管复原能力减弱,引起血管重构,引发血流微循环紊乱等症状,从而减缓患者血肿吸收速度,加重因血肿压迫等引起的神经损伤。③高Hcy影响患者血管舒张功能:Hcy可上调ET-1合成及分泌并抑制NO释放,打破患者血管舒张/收缩平衡,引起患者脑血管舒张及收缩反应异常,影响患者出血量并增加二次出血风险。④高Hcy引起氧化应激激活:血清Hcy会促进过氧化氢、超氧化物及促炎因子等一系列活性氧自由基合成,而上述合成物质可促进氧化修饰型低密度脂蛋白合成及分泌,并抑制一氧化氮的合成和降解,破坏血管细胞功能及形态,形成以一氧化氮为介导的依赖性血管舒张功能障碍,继而导致血肿吸收受限,增加血肿压迫神经功能程度及时间,加重神经功能损伤,影响患者病情进展。
人体内钙离子具有血脑屏障黏附性及通透性作用,对受损的血脑屏障具有一定影响。本研究结果显示,血清钙离子水平与患者预后具有密切联系。使用血清钙离子水平评估患者预后具有一定价值。进一步分析钙离子对患者预后的影响作用机制可能为:①影响患者血压调控。研究表明[11],钙摄入量少的人群罹患高血压风险较高,低血钙可能通过影响血管内皮功能,导致患者血压调控机制异常,血肿体积增加。②影响血脑屏障稳定性。研究表明[12],钙离子水平会影响血脑屏障稳定性,当细胞外钙离子浓度降低时,会导致血脑屏障中细胞黏附中断,当发生高血压性脑出血后会影响神经功能。③影响凝血功能。钙离子是参与凝血过程的重要物质,参与组织因子的激活及血小板黏附过程。研究表明[13],血清钙离子降低大鼠的血液凝固时间明显延长,推测入院时低血钙可能会影响凝血功能,导致血肿体积增加。④血清钙水平降低增加神经细胞凋亡。研究发现[14],当发生高血压性脑出血时,可以导致神经细胞钙通道开放,引发钙离子内流,细胞内钙离子超载,引起神经细胞凋亡。
关于ICH患者病情及预后影响因素及评估模型建立,近年来国内也有相关报道,但不同学者关注侧重点均有差异,如赵子涵等[15]中性粒细胞与淋巴细胞比值(NLR)和高敏 C-反应蛋白(hs-CRP)及患者一般资料进行了分析,提出NLR、hs-CRP水平是影响ICH患者预后的重要因素,使用此两者对患者进行预后评估具有较高效能;张丽侠等[16]则对脑出血患者NSE、D-D、Hcy水平进行了观察,结果发现脑出血患者NSE、D-D、Hcy水平相较健康患者升高,且与患者病情严重度、脑出血量呈正相关;李琼等[17]通过患者CTA点征、GCS评分和基线脑室出血量联合建立了脑出血患者脑室出血量增加预测模型,灵敏度和特异度分别为68.2%和94.5%,具有较高诊断效能。本研究对Hcy、Ca2+水平进行了整合并建立了联合评估模型,ROC曲线结果显示,联合模型对患者预后评估具有更优效能,高于单独应用影像学检测或单独指标评估。证实多个指标联合评估具有更优效能,有助于提高预测效能,希望能为临床进一步研究提供参考。
根据本研究所得到的结果,以及病例筛选、研究过程回顾等,本研究仍存在一些局限性。首先,本研究的所有样本均取自我院所收治的病例样本,属于单中心、回顾性队列研究,虽然在试验设计和执行时,通过质量控制手段以及干扰因素的剔除(如所有纳入病例的样本采取时间控制在一定范围内,血液样本抽取时间段以及抽取量严格固定,资料收集以及记录过程中始终交由同一工作人员等),进而尽可能保证了结果的准确性与科学性,但队列研究本身的局限性使其无法避免一些混杂因素的存在。
综上所述,Hcy、Ca2+水平表达及CT表现与ICH患者预后均有密切联系,通过对患者Hcy、Ca2+水平监测及CT表现观察有助于及时了解患者病情,评估患者预后。但本研究选取样本较少,且全为我院患者,可能对本研究可信度造成一定影响,此结论有待多中心、大样本实验证实。

