塞来昔布自微乳的制备及体外溶出研究
杨雪华,毛楷凡,刘正平,,李大伟,*,张岱州,*
(1. 山东省药学科学院 新型缓控释制剂与药物靶向递送系统山东省工程研究中心,山东 济南250101;2. 国家药监局药物制剂技术研究与评价重点实验室,山东 济南 250101; 3. 山东福瑞达医药集团有限公司 山东省黏膜与皮肤给药技术重点实验室,山东 济南 250101)
塞来昔布(celecoxib,CXB)是新一代非甾体抗炎药(nonsteroidal anti-inflammatory drug,NSAID),可通过选择性抑制环氧化酶2来抑制前列腺素的生成,继而发挥抗炎镇痛作用[1]。与其他NSAID相比,CXB同样用于治疗骨关节炎、类风湿性关节炎和急性疼痛,但不同的是,CXB治疗效果更好,且上消化道溃疡及其他并发症的发生率最低[2]。然而根据生物制药分类系统,CXB属于II类药物(高渗透性和低溶解性),其有限的水溶性极大地影响了其口服生物利用度。因此,亟需通过各种增溶技术来增加CXB的水溶性。近年,研究人员将CXB制备成固体分散体、纳米混悬液及脂质体等来改善其水溶性,但这些手段增溶有限,且都存在制备工艺复杂、难以放大生产的缺点[3]。
自微乳药物递送系统(self-microemulsifying drug delivery system,SMEDDS)是由油相、乳化剂、助乳化剂混合而成的液态或类固态制剂[4]。SMEDDS口服后能在胃肠道的蠕动下与胃液、肠液融合,自发分散形成粒径小于100 nm的O/W型乳液,可极大地提高药物的溶解度和口服生物利用度[5]。且SMEDDS具有生物相容性好、稳定性高及容易放大生产的优点[6]。因此,本研究拟将CXB制备成SMEDDS,以期实现增加CXB溶解度、改善胃肠道吸收、提高口服生物利用度的目的。
1 仪器与材料
1.1 仪器
Agilent 8454型紫外分光光度计(美国安捷伦公司);LOGAN 860DL型智能溶出仪(美国LOGAN公司);MS204TS/02型电子天平(美国梅特勒-托利多仪器有限公司);C-MAG HS4型磁力搅拌器(德国IKA公司);Nano-ZS90型马尔文激光粒度分布与电势分析仪(英国Malvern公司);Talos F200s型透射电子显微镜(FEI公司);KQ-500E型超声波清洗器(昆山市超声设备有限公司)。
1.2 材料
塞来昔布原料药(自制,批号:210304);中链甘油三酯(MCT,批号:177185,法国嘉法狮公司);聚氧乙烯35蓖麻油(ELP35,批号:7778402UO,北京凤礼精求医药有限公司);丙三醇(批号:B2108262,西陇科学股份有限公司);甲醇(批号:20211118),无水乙酸钠(批号:20180307),磷酸二氢钠(批号:20161011),十二烷基硫酸钠(SDS,批号:20170904),盐酸(批号:20190320,国药集团化学试剂有限公司);醋酸(批号:20170712,天津市科密欧化学试剂有限公司);氢氧化钠(批号:20210504,天津市大茂化学试剂厂)。
2 方法与结果
2.1 CXB-SMEDDS的制备
分别以中链甘油三酯(MCT)、聚氧乙烯35蓖麻油(ELP35)、丙三醇作为油相、乳化剂及助乳化剂。参考相关文献[7]确定了CXB-SMEDDS的制备工艺,即先称取一定量的MCT、ELP35及丙三醇,磁力搅拌10 min后得到空白SMEDDS,称取一定量的CXB加入空白SMEDDS中,磁力搅拌10 min,得到CXB-SMEDDS。
2.2 处方筛选
先通过伪三元相图的绘制确定能发生乳化的处方比例范围,再通过单纯形网格法进行处方优化。
2.2.1 伪三元相图的绘制 按乳化剂与助乳化剂的质量比为1:9,2:8,3:7,4:6,5:5,6:4,7:3,8:2,9:1,分别称取相应量的ELP35与丙三醇,再将此混合乳化剂与油相MCT按9:1~5:5的质量比分别混匀,然后将CXB按25 mg/g的载药量加入上述空白SMEDDS中,混匀,即得系列CXB-SMEDDS。将0.5 g CXB-SMEDDS在磁力搅拌条件下(100 r/min)缓慢加入50 ml 37 ℃蒸馏水中,观察各CXB-SMEDDS能否发生自乳化。乳化的标准分为5个等级:A:乳化时间<1 min,溶液呈澄清或略泛蓝光;B:乳化时间<1 min,略浊,呈蓝白色;C:乳化时间1~2 min,呈亮白色不透明液体;D:乳化时间>2 min,色泽暗,呈灰白色,略带油状;E:难乳化,一直有油滴存在[8]。记录形成A、B等级微乳时MCT、ELP35及丙三醇各自的质量分数,并以各组分为三元相图顶点,利用origin软件绘制三元相图。图1为根据实验结果绘制的伪三元相图,由图1可知,能发生乳化的各组分比例范围为,MCT 10 %~40 %,ELP35 9 %~81 %,丙三醇6 %~81 %。

图1 CXB-SMEDDS的伪三元相图
2.2.2 单纯形网格法优化处方 固定处方中MCT、ELP35、丙三醇的总比例为100 %,以2.2.1项下各组分比例范围为基础,结合单纯形网格法比例约束及各组分一般用量,确定M C T 比例范围为10 %~40 %,ELP35为30 %~60 %,丙三醇为30 %~60 %。以CXB-SMEDDS的平均粒径(Y1)、多分散指数(PDI,Y2)、乳化时间(Y3)为评价指标,采用Design Expert软件中Simplex Lattice对处方进行设计,见表1。按表1称取各组分,磁力搅拌10 min,得空白SMEDDS,按25 mg/g的比例称取CXB,加入空白SMEDDS中,磁力搅拌10 min,得CXB-SMEDDS。称取1 g CXB-SMEDDS,磁力搅拌条件下(100 r/min)缓慢加入到100 ml 37 ℃蒸馏水中。记录乳化时间,并取部分乳液用马尔文激光粒度分布仪测定其粒径和PDI。

表1 单纯形网格法优化实验设计及结果
单纯形网格法优化处方实验结果见表1。采用Design Expert软件,以Y1、Y2、Y3为评价指标,通过模型拟合得响应方程分别为:Y1=182.01A+18.16B+25.87C-265.30AB-232.02AC-2.08BC-2238.07A2BC+1381.37AB2C+1281.95ABC(P<0.0001,R2=0.9994);Y2=0.2405A+0.0707B+0.0964C-0.3584AB-0.2005AC+0.0209BC(P<0.0001,R2=0.9660);Y3=70.85A+8.79B+9.15C+65.78AB-63.83AC-0.5055BC-347.69A2BC+253.15AB2C+65.98ABC2(P<0.0001,R2=0.9999)。对上述回归模型进行方差分析,结果表明,模型的P值均小于0.0001,远小于 0.05,表明模型显著可靠;模型的回归方程系数R2及校正决定系数(adjustR2)均大于 0.95,表明模型相关系数较高,非线性拟合的效果良好。
根据上述回归模型,绘制三维效应面图,见图2。由图2可见,MCT用量对3个评价指标的影响最大,随着MCT比例的增大,粒径、PDI和乳化时间都逐渐增大,可能是因为随着油相比例增大,乳化过程变得困难,导致乳化时间延长,形成的乳液粒径较大,粒径均一性也较差。ELP35用量对3个评价指标的影响弱于MCT,但也有一定影响,粒径、PDI和乳化时间都随着ELP35比例的增大而减小,表明随着乳化剂用量的增加,CXBSMEDDS在水中更易自发形成粒径较小的乳液。而助乳化剂丙三醇对3个评价指标的影响比较小,其主要起增溶药物、促进微乳形成并增加微乳稳定性的作用。
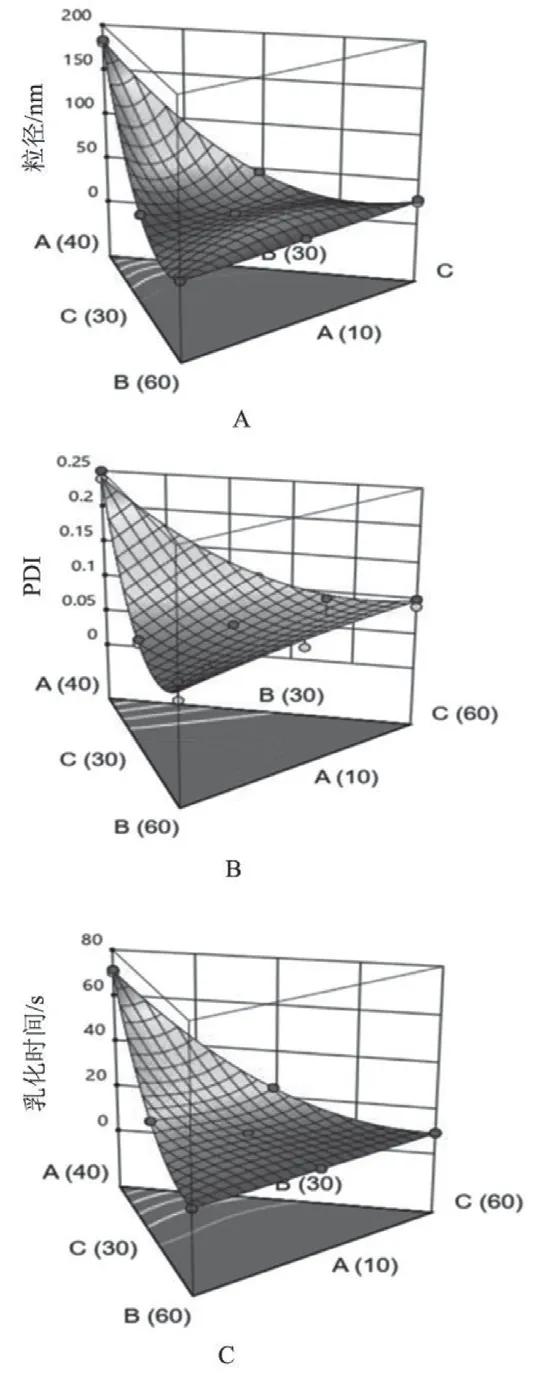
图2 各组分比例对CXB-SMEDDS的粒径(A)、PDI(B)及乳化时间(C)影响的三维效应面图
2.2.3 最优处方确定与验证 CXB-SMEDDS的粒径越小,比表面积越大,药物溶出与吸收就越快;自乳化时间越短,乳化效果越好;PDI值小于0.2时,乳液的分散性较好。综合3个指标,通过软件预测得最优处方为MCT 10 %、ELP35 59.45 %、丙三醇30.55 %。为便于实验操作,将处方调整为MCT 10 %、ELP35 60 %、丙三醇30 %。根据预测的最优处方制备 3 批CXB-SMEDDS,测定其粒径、PDI与乳化时间,计算预测值与实测值之间的偏差,结果见表2。结果表明,各评价指标的预测值与实测值之间的偏差较小,说明所建立的数学模型具有良好的预测效果。
表2 最优处方验证实验结果( ±s,n=3)
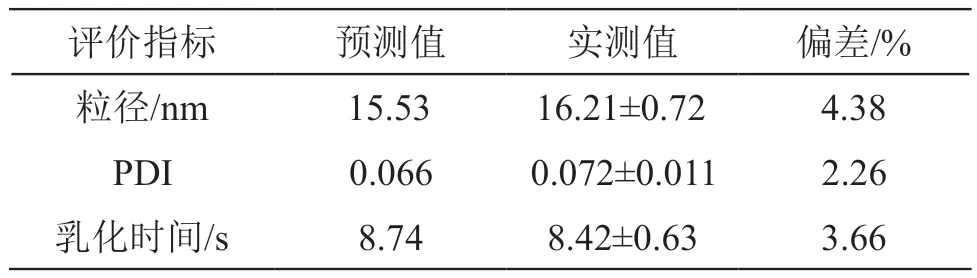
表2 最优处方验证实验结果( ±s,n=3)
评价指标预测值实测值偏差/%粒径/nm15.5316.21±0.724.38 PDI0.0660.072±0.0112.26乳化时间/s8.748.42±0.633.66
2.3 CXB-SMEDDS的质量评价
2.3.1 外观性状 将新鲜制备的CXB-SMEDDS置于西林瓶中,肉眼观察其外观性状,见图3。称取CXB-SMEDDS 1 g,磁力搅拌条件下(100 r/min)缓慢加入到100 ml 37 ℃蒸馏水中,观察乳液的外观性状。由图3A可见,CXB-SMEDDS在室温(25 ℃)下呈无色透明溶液,流动性较好。由图3B可见,CXB自乳化后能形成略泛蓝光的溶液。

图3 CXB-SMEDDS自乳化前(A)和自乳化后(B)的外观性状
2.3.2 微观形态 采用透射电子显微镜观察CXBSMEDDS的微观形态。称取CXB-SMEDDS 1 g,磁力搅拌条件下(100 r/min)缓慢加入37 ℃蒸馏水100 ml中,得到CXB乳液。将该乳液滴在覆有支持膜的铜网上,静置10 min,再滴加1 %磷钨酸溶液于铜网上,负染2 min后用滤纸片吸干,过夜干燥,透射电镜下观察,结果见图4。结果表明,CXBSMEDDS 自乳化后形成的乳滴呈均一的圆球形,粒径为20 nm左右。

图4 CXB-SMEDDS的透射电镜图
2.3.3 粒径与电位分布 称取CXB-SMEDDS 1 g,磁力搅拌条件下(100 r/min)缓慢加入到100 ml 37 ℃蒸馏水中,得到CXB乳液。用Malvern激光粒度分布与电势分析仪测定该乳液平均粒径及Zeta电位分布,结果见图5。结果表明,CXB-SMEDDS自乳化后形成的乳滴的平均粒径为(16.21±0.72)nm,粒径较小。PDI为0.072±0.011,表明粒度分布比较均匀。电位为(-15.8±1.2)mV。

图5 CXB-SMEDDS和CXB原料药在水(A)、pH 1.2盐酸溶液(B)、pH 4.5醋酸盐溶液(C)和pH 6.8磷酸盐溶液(D)中的溶出曲线
2.3.4 载药量与包封率
2.3.4.1 CXB的含量测定 采用紫外分光光度法测定CXB的含量。精密称取CXB原料药细粉30.00 mg,置于100 ml量瓶中,加适量甲醇超声溶解,并用甲醇稀释至刻度,配成300 µg/ml的储备液。精密移取200 μl储备液至10 ml量瓶,用甲醇稀释至刻度,得6 µg/ml的溶液,紫外扫描确定CXB的最大吸收波长。精密移取储备液50,100,200,300,400,500 µl至10 ml量瓶,用甲醇稀释至刻度,于最大波长条件下测定吸光度,以吸光度A为纵坐标,质量浓度C(µg/ml)为横坐标绘制标准曲线。按上述步骤配制低、中、高3种不同浓度的溶液,测定吸光度,计算回收率和精密度。结果显示,CXB在甲醇中的标准曲线为y=0.0563x-0.0143,R2=0.9998,表明CXB在1.5~15 µg/ml范围内线性关系良好。回收率和精密度试验的结果也表明,本含量测定方法的回收率与精密度良好。
2.3.4.2 载药量与包封率的测定 精密称取1.0000 g CXB-SMEDDS(其中含CXB的量为W0),置于100 ml量瓶中,加适量甲醇超声溶解,并用甲醇稀释至刻度,配成储备液。精密移取500 µl储备液至10 ml量瓶,加甲醇稀释至刻度,于最大波长条件下测定其吸光度,按2.2.4.1 项下方法计算其药物含量(W1)。精密称取1.0000 g CXB-SMEDDS,磁力搅拌条件下(100 r/min)缓慢加入100 ml 37 ℃蒸馏水中,得CXB乳液。取该乳液2 ml,置于离心管中,10 000 r/min离心 15 min,精密移取上清500 µl至10 ml量瓶中,用甲醇稀释至刻度,于最大波长条件下测定其吸光度,按2.2.4.1 项下方法计算其药物含量(W2)。根据公式:载药量=W1/W0,包封率=W2/W1,计算相应的载药量与包封率。最终测得CXB-SMEDDS的载药量为标示量的101.42 %±0.29 %,包封率为98.05 %±0.18 %,均符合要求。
2.4 CXB-SMEDDS的体外溶出评价
2.4.1 CXB溶出度测定方法的建立 建立CXB在4种不同溶出介质(水、pH 1.2盐酸溶液、pH 4.5醋酸盐溶液、pH 6.8磷酸盐溶液)中的含量测定方法。精密称取CXB原料药细粉 15.00 mg,置于100 ml量瓶中,加适量溶出介质(含SDS)超声溶解,并稀释至刻度,配成150 µg/ml储备液。精密移取400 µl储备液至10 ml量瓶,用溶出介质稀释至刻度,得6 µg/ml的溶液,紫外扫描确定CXB的最大吸收波长。精密移取储备液100,200,400,600,800,1000 µl至 10 ml量瓶,用溶出介质稀释至刻度,于最大波长条件下测定吸光度,以吸光度A为纵坐标,质量浓度C(µg/ml)为横坐标绘制标准曲线。按上述步骤配制低、中、高3种不同浓度的溶液,测定吸光度,计算回收率和精密度。结果见表3。由表3可知,本方法回收率与精密度良好,CXB在各溶出介质中线性关系良好。
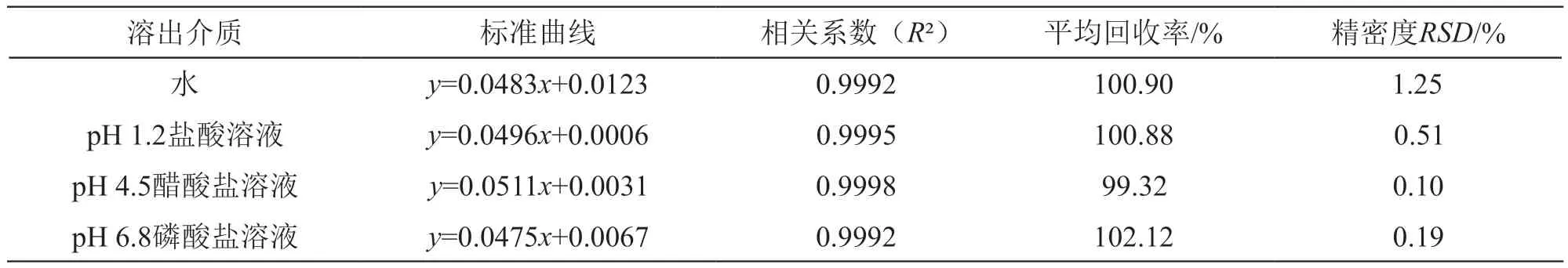
表3 CXB在各溶出介质中的标准曲线、精密度与回收率测定结果
2.4.2 CXB-SMEDDS体外溶出度的测定 按《中国药典》2020年版溶出度测定法第二法(桨法)进行CXB-SMEDDS的溶出度测定。溶出度测定要求为:溶出介质为水、pH 1.2盐酸溶液、pH 4.5醋酸盐溶液及pH 6.8磷酸盐溶液,溶出介质的体积为500 ml,转速为 50 r/min,温度为(37±0.5)℃。精密称取原料药12.50 mg和CXB-SMEDDS 0.5000 g,分别投入溶出杯中,分别于 5,10,15,30,45,60,90,120 min取样7 ml,并及时补入同温度介质7 ml,所取样品用0. 45 μm微孔滤膜滤过。按2.4.1项下方法,测定溶出量,绘制溶出曲线。
CXB-SMEDDS和CXB原料药在各介质中的溶出曲线见图5。由图5可见,CXB原料药在各介质中的溶出都比较少,24 h内累积溶出度均小于10 %,表明原料药较差的水溶性限制了其溶出。而CXB-SMEDDS在4种溶出介质的溶出均较快,5 min内平均溶出度大于43.94 %,45 min的累积溶出度达到了87.48 %以上,此后一直维持在这个水平,溶出较完全。CXB-SMEDDS在各个介质中溶出行为没有差异,可以预测CXB-SMEDDS口服后在胃以及小肠、十二指肠等部位的溶出行为也相似,都能实现较快较完全的溶出。综上,与CXB原料药相比,CXB-SMEDDS的溶出度大大提高,由此推测,将CXB制成CXB-SMEDDS后可改善CXB的胃肠道吸收,大大提高CXB的口服生物利用度。
3 讨论
SMEDDS体系通常由油相、乳化剂及助乳化剂组成,油相对SMEDDS的形成十分重要。本研究选择MCT作为油相,是因为MCT是脂溶性药物强大的增溶剂,CXB在MCT中的溶解度可达到载药量的要求,同时MCT脂肪链较短,易微乳化,消化吸收快。且MCT还具有很多其他优良性质,如安全性高、预防肥胖、抗疲劳及提高免疫力等[9]。
筛选最佳处方是制备SMEDDS的中心环节。SMEDDS一般先通过伪三元相图的绘制,确定能发生自乳化的各因素的比例范围,再通过单纯网格优化确定各因素的最佳比例。当实验因素总量恒定时,单纯形网格法仅需确定各因素比例范围就可准确预测实验区域内其他点的性能,被广泛用于SMEDDS制剂处方优选[7]。与其他方法相比,单纯形网格法可通过较少的实验次数,确定最优处方,大大简化了实验操作,且预测性良好[10]。使用单纯形网格法优化处方时,把粒径、PDI、乳化时间作为参考因素,这是因为SMEDDS粒径越小,比表面积越大,越容易被吸收;较小的PDI可保证乳液的分散性;乳化时间越短,自乳化过程越容易进行。总之,合适的粒径、PDI、乳化时间可保证SMEDDS优良的体内外性质。
体外溶出试验结果表明与C X B 原料药相比,CXB-SMEDDS的溶出度大大提高,据此预测,CXB-SMEDDS可提高CXB的口服生物利用度。体外溶出试验可以一定程度上预测药物的体内行为,但体外溶出并不能完全模拟药物的体内吸收情况,因此后续试验还可以进行CXB-SMEDDS的药动学试验,通过测定CXB原料药和CXB-SMEDDS的血药浓度,进一步验证CXB-SMEDDS确实能大大提高CXB的体内吸收[11]。同时,还可比较体内体外试验的结果,进行体内外相关性研究。

