Cu-ZnIn2S4/Ti3C2高效光催化还原水中Cr(Ⅵ)
刘 坤,杨 鑫,茆 平,孙爱武,沈锦优,丁 宁
(1. 淮阴工学院 化学工程学院,江苏 淮安 223003;2. 南京理工大学 环境与生物工程学院,江苏 南京 210094)
在冶金、电镀、制革等工业过程中,常释放出重金属铬污染物,其中六价铬(Cr(Ⅵ))的毒性、致癌性以及化学稳定性远高于三价铬(Cr(Ⅲ)),对生态环境危害极大[1]。常见的Cr(Ⅵ)处理方法有吸附、膜分离、离子交换、电化学、光催化等,其中光催化技术因操作简单、无二次污染等优点受到广泛关注[2-3]。然而,TiO2和ZnO等传统光催化剂因可见光激发能力差、稳定性差、活性位点暴露不足等缺陷,导致其光催化性能仍不尽人意[4]。三元硫化物(如ZnIn2S4,以下简称ZIS)是一种新型的可见光驱动光催化剂,带隙能可调(2.06~2.85 eV),其层状结构表现出良好的光催化活性和稳定性,具有广泛的应用前景[5]。金属掺杂虽可进一步提升其光催化性能[6],但针对性能稳定的Cr(Ⅵ)的还原,金属掺杂效果仍不理想。MXene(如Ti3C2)是一种新型过渡金属碳化物、氮化物和碳氮化物二维材料,可通过从MAX相材料(一种新型三元层状化合物,由前过渡金属(M)、A族元素(A)以及碳或氮(X)组成,如Ti3AlC2)中选择性蚀刻A元素得到[7]。由于MXene的层状结构和特殊的表面官能团(—OH,—O和—F),使其表现出优异的亲水性和与其他半导体材料的亲和力,同时MXene拥有优异的电子导电性,便于光生电子的分离和转移[8]。
本工作将ZIS与廉价的Cu和助催化剂Ti3C2复合,考察了复合材料对水中Cr(Ⅵ)的可见光光催化还原性能,利用表征分析和光电化学测试研究了其光催化还原机理,并对其光催化活性的提升进行了解释。
1 实验部分
1.1 试剂
钛碳化铝(Ti3AlC2)、六水合硝酸铜(Cu(NO3)2·6H2O)、二水合醋酸锌(Zn(OAc)2·2H2O)、四水合氯化铟(InCl3·4H2O)、氟化锂(LiF)、乙二醇、N,N-二甲基甲酰胺、硫代乙酰胺(TAA)、重铬酸钾、乙醇、盐酸:均为分析纯。
1.2 光催化剂的制备和表征
1.2.1 单层Ti3C2的制备将2 g LiF溶于20 mL 9 mol/L盐酸中,随后边搅拌边加入0.5 g Ti3AlC2粉末,于室温下搅拌反应24 h,得到悬浮液。离心分离,用去离子水洗涤固体至pH大于等于6,于60 ℃下真空干燥12 h。将干燥后的样品再分散于去离子水中,冰浴下超声1 h后3 500 r/min离心1 h。收集上清液,于-50 ℃下冷冻干燥24 h,得到单层Ti3C2。
1.2.2 Cu-ZnIn2S4的制备将一定量(0.02,0.10,0.30,0.50 mL)0.1 mol/L Cu(NO3)2·6H2O溶液分散于25 mL乙二醇和25 mLN,N-二甲基甲酰胺混合溶液中,再依次加入0.50 mmol Zn(OAc)2·2H2O、1.00 mmol InCl3·4H2O和2.00 mmol TAA,超声搅拌30 min。随后将上述溶液倒入100 mL聚四氟乙烯内衬的高压反应釜中,并于180 ℃下加热反应24 h。离心分离,用去离子水和乙醇洗涤固体多次,于60 ℃下真空干燥24 h,得到Cu-ZIS复合材料。将加入0.02,0.10,0.30,0.50 mL Cu(NO3)2·6H2O溶液制备的复合材料分别记为0.2%Cu-ZIS、1%Cu-ZIS、3%Cu-ZIS和5%Cu-ZIS。为便于比较,通过不添加Cu(NO3)2·6H2O制备了纯ZIS。
1.2.3 Cu-ZIS/Ti3C2的制备Cu-ZIS/Ti3C2的制备流程如图1所示。将一定量(1,5,10 mg)的单层Ti3C2分散于25 mL乙二醇和25 mLN,N-二甲基甲酰胺混合溶液中,依次加入0.01 mmol Cu(NO3)2·6H2O,0.50 mmol Zn(OAC)2·2H2O,1.00 mmol InCl3·4H2O和2.00 mmol TAA,超声搅拌30 min,后续操作同1.2.2节,得到1%Cu-ZIS/Ti3C2复合光催化剂。将加入1,5,10 mg Ti3C2制备的复合光催化剂分别记为1%Cu-ZIS/MX1,1%Cu-ZIS/MX5和1%Cu-ZIS/MX10。

图1 Cu-ZIS/Ti3C2的制备流程
1.2.4 光催化剂的表征
采用配备CuKα辐射源的X射线衍射仪(XRD)(AXS公司,Brucker-D8型)对样品进行物相分析。采用X射线光电子能谱仪(XPS)(Thermo公司,Escal AB 250型)获取材料的表面元素信息,用C 1s的结合能(284.6 eV)校准其他结合能。采用扫描电子显微镜(SEM)(日立公司,S-4800型)对样品进行微观形貌表征。采用全谱直读电感耦合等离子体发射光谱仪(ICP)(PE公司,OPTIMA7000DV型)测定样品中各元素的含量。采用紫外-可见分光光度计(UV-Vis)(Varian公司,Cary 300型)测试样品的光吸收性能。采用荧光光谱仪(PL)(Edinburgh Instruments公司,FLS980型)考察样品的电子-空穴对分离状况。采用电化学工作站(北京华科普天公司,CHI660E型)分析样品的光电化学性能。
1.3 光催化实验方法
将12.5 mg制备好的样品加入到50 mL质量浓度为50 mg/L的Cr(Ⅵ)溶液中,除分析pH影响的实验外,其他实验的初始pH均为7。在暗室条件下搅拌60 min,达到吸附平衡,再利用氙灯(300 W,波长大于420 nm)进行可见光照射。每隔一段时间取5 mL悬浮液,用0.22 μm滤膜过滤去除杂质后,采用二苯碳酰二肼分光光度法[9]测定Cr(Ⅵ)浓度,根据Cr(Ⅵ)的测定结果和初始浓度计算其去除率。
2 结果与讨论
2.1 光催化剂的表征结果
2.1.1 SEM
利用SEM研究了光催化剂的微观结构和形貌,结果如图2所示。ZIS呈现出由片状组成的直径约400 nm的微球花状结构(图2a)。随着Cu掺杂进ZIS(图2b~2d),Cu-ZIS复合材料基本仍保持微球结构,但片层间逐渐布有颗粒,当硝酸铜溶液用量增至0.50 mL时片层间已充满颗粒。图2e表明,经刻蚀得到片状的Ti3C2。当复合Cu和ZIS后(图2e),Ti3C2片状表面变得粗糙,局部放大图可以看出其表面布满了Cu-ZIS球状结构。这是因为Ti3C2表面带负电和不同的官能团,使其具有亲水性[10],导致其能够固定溶液中的阳离子(In3+、Zn2+和Cu2+);而Ti3C2的层状结构可使金属离子在其表面被吸附,随后向更深的插层位置扩散;同时,TAA的S2-与吸附的In3+和Zn2+发生反应,使得Cu-ZIS微球原位生长于Ti3C2上。

图2 光催化剂的SEM照片a ZIS;b 0.2%Cu-ZIS;c 1%Cu-ZIS;d 5%Cu-ZIS;e Ti3C2;f 1%Cu-ZIS/MX5
2.1.2 XRD
利用XRD分析了光催化剂的晶体结构,结果如图3所示。图3a中,经LiF和HCl混合溶液刻蚀处理后,Ti3AlC2位于39°的特征衍射峰消失,表明Ti3AlC2中的Al元素被去除;Ti3AlC2(002)晶面对应的9.6°峰向低角度偏移,转变为Ti3C2(002)晶面对应的8.9°峰,进一步证明Ti3AlC2已成功转化为Ti3C2[11]。图3a和图3b中,21.5°和47.1°的衍射峰属于ZIS的特征峰(JCPDS 65-2023),但由于Cu和Ti3C2的掺杂量较低,与ZIS相比,Cu-ZIS和Cu-ZIS/MX5复合材料的XRD谱图未见明显变化[12]。

图3 光催化剂的XRD谱图
2.1.3 XPS和ICP
利用XPS分析了光催化剂表面的元素组成,结果如图4所示。由图可知,Cu和Ti3C2被成功掺杂到ZIS中。随着Cu和Ti3C2的掺杂,S 2p的结合能从162.8 eV蓝移到162.4 eV,In 3d的结合能从445.5 eV、453.0 eV分别蓝移到445.1 eV、452.7 eV和444.9 eV、452.5 eV,Zn 2p的结合能从1 044.8 eV、1 021.8 eV分别蓝移到1 044.4 eV、1 021.4 eV和1 044.2 eV、1 021.2 eV,这表明掺杂的金属元素与ZIS发生了强烈的界面相互作用。Cu 2p谱图中:较小的峰面积表明掺杂量较低;此外,Cu峰的结合能位置表明,复合材料中的Cu主要以单质铜为主[10,13]。

图4 光催化剂的XPS谱图
利用ICP测定了1%Cu-ZIS/MX5中各金属元素的含量,经计算样品中Cu、Ti3C2和ZnIn2S4的质量分数分别为1.38%、5.83%和92.79%。
2.1.4 UV-Vis DRS
利用UV-Vis DRS(紫外-可见漫反射光谱)对光催化剂的捕光性能进行了测试,结果如图5所示。
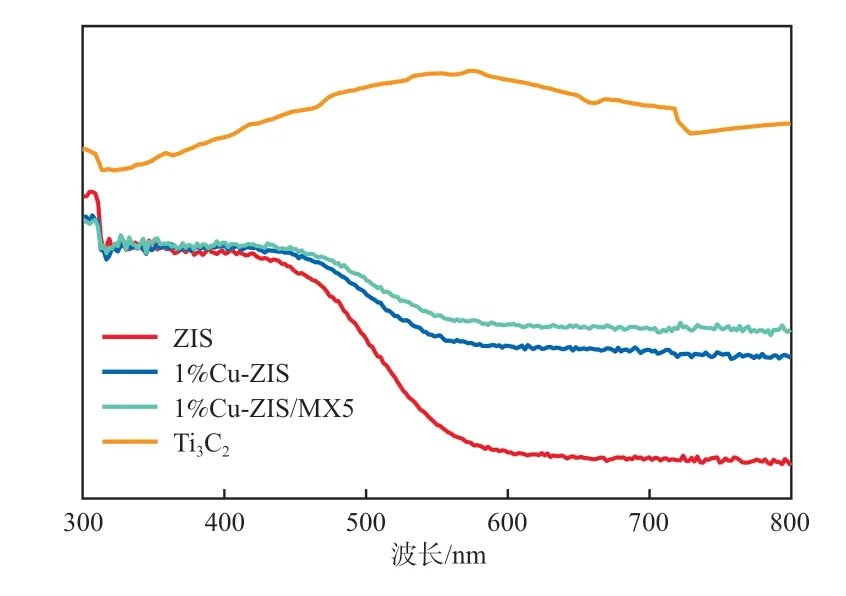
图5 光催化剂的UV-Vis DRS谱图
由于Ti3C2的颜色较深,因而其在可见光波段范围(300~800 nm)表现出较高的吸收带[14]。纯ZIS仅在550 nm以下区域有较强的吸收带。当Cu掺杂进ZIS后,样品颜色逐渐由黄色变为红色,因而在510~800 nm范围内的吸光性能明显增强,这意味着Cu-ZIS复合光催化剂可能具有更强的光能利用率。继续引入Ti3C2后,吸光性能得到进一步提升,这归因于Ti3C2的全光谱吸收和独特的分层分支结构[15]。
2.2 光催化性能评价
考察了不同光催化剂对Cr(Ⅵ)的可见光催化还原能力,结果如图6所示。

图6 不同光催化剂对Cr(Ⅵ)的光催化还原效果对比
Ti3C2基本没有吸附性能,吸附性能最佳的是ZIS;随着Cu和Ti3C2掺杂量的增加,材料的吸附性能逐渐下降,但由于掺杂量较低,下降的幅度较小。Cr(Ⅵ)的稳定性较好,可见光光照后,其浓度基本无变化。光照60 min,ZIS对Cr(Ⅵ)的去除率可达44.3%。掺杂Cu后的Cu-ZIS还原效率显著提升,最佳配比的1%Cu-ZIS光照60 min后的Cr(Ⅵ)去除率达69.5%。Cu的掺杂有助于ZIS能带引入受体和施主态,从而大幅提高了载流子密度和电荷传输效率[16];并且,标准氧化还原电位φ⊖(Cu2+/Cu)(+0.337 eV)小于φ⊖(Cr2O72-/Cr3+)(+1.33 eV),因而Cu可直接还原Cr(Ⅵ)为Cr(Ⅲ)。进一步引入Ti3C2后,材料的还原效率再次得到提升,最佳配比的1%Cu-ZIS/MX5光照60 min后的Cr(Ⅵ)去除率基本达到100%。这主要是因为与Ti3C2复合后,半导体ZIS与Ti3C2间的强界面作用有效延长了光生载流子的寿命[5]。相比于前人报道的ZnIn2S4类光催化剂(表1),1%Cu-ZIS/MX5光催化剂在用量较低的情况下,仍拥有与其他ZnIn2S4光催化剂同样优异的光催化性能。

表1 ZnIn2S4系列光催化剂还原Cr(Ⅵ)的性能对比
溶液pH对1%Cu-ZIS/MX5光催化还原Cr(Ⅵ)性能的影响见图7。由图7可见,酸性和中性环境有利于Cr(Ⅵ)的还原,随着pH的增大,Cr(Ⅵ)的去除率逐渐下降。Cr(Ⅵ)在酸性和中性环境下主要以Cr2O72-或HCrO4-形式存在,碱性环境下则为CrO42-,而Cr2O72-和HCrO4-比CrO42-更易被吸附和光催化还原[22]。此外,碱性环境下,金属易被氧化为金属氧化物或氢氧化物[23],因而其光催化还原性能有所下降。

图7 溶液pH对Cr(Ⅵ)光催化效果的影响
除了高效的光催化性能外,复合材料的循环稳定性也是实际应用中的一项重要指标。催化剂完成一次光催化性能测试,经水洗、烘干后即可进行下一次光催化性能测试,每次光照时间120 min。经过5次循环后,1%Cu-ZIS/MX5对Cr(Ⅵ)的去除率仍可达90.3%(前4次为100%,98.5%,96.3%,93.6%),说明其具有较高的稳定性。此外,1%Cu-ZIS/MX5 5次光催化循环反应后的XRD谱图(见图3c)几乎未发生变化,说明其结构未发生改变,进一步证明其具有良好的循环稳定性。
2.3 光催化机理分析
2.3.1 PL分析
利用PL分析光催化剂的电荷分离效率,结果如图8所示。在470 nm激发波长下,纯ZIS显示出较高的荧光强度,说明ZIS半导体中的电荷在光催化还原过程中容易复合,寿命较短。Cu掺杂大幅减弱了光催化剂的荧光强度。随着Ti3C2的引入,复合光催化剂的荧光强度进一步下降,这归因于具有良好导电性的Ti3C2纳米片为光生载流子提供了一个快速通道,加速了Cu-ZIS/MX中电子的传输和迁移。
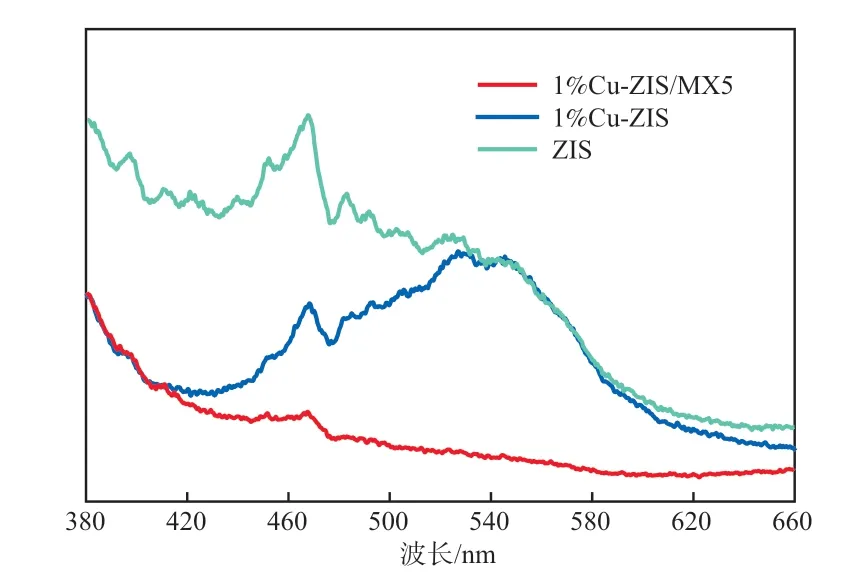
图8 光催化剂的PL谱图
2.3.2 光电化学性能
为了解Cu和Ti3C2的引入对提高光催化活性的作用,对光催化剂进行了光电化学性能测试。图9a为光催化剂的瞬态光电流响应曲线。在有光照的情况下光电流密度迅速增加并达到饱和,而在无光照的情况下立即降至几乎为零。1%Cu-ZIS/MX5具有最高的光电流密度,而1%Cu-ZIS的光电流密度也明显大于纯ZIS,说明Cu和Ti3C2的引入均可提高光电流密度。这进一步证实了Cu和Ti3C2的引入可促进光生载流子的分离和延长其存在时间,从而有助于提高ZIS的光催化活性。光催化剂的电化学阻抗谱(图9b)显示:掺杂Cu后,1%Cu-ZIS的电弧半径比纯ZIS小,说明掺杂Cu后电子转移速率更快;引入Ti3C2后,1%Cu-ZIS/MX5的电弧半径进一步减小,说明Cu和Ti3C2的引入可共同提高材料的导电性能,即加速界面电荷转移[16]。

图9 光催化剂的瞬态光电流响应曲线(a)和电化学阻抗谱(b)
2.3.3 活性物种
异丙醇(I PA)、A g N O3和乙二胺四乙酸(EDTA)分别可以掩蔽光催化体系中的羟基自由基(·OH)、电子(e-)和空穴(h+),引入这3种掩蔽剂进行1%Cu-ZIS/MX5光催化实验(光照120 min),研究各活性物种在光催化过程中的作用,结果如图10所示。添加AgNO3后,1%Cu-ZIS/MX5对Cr(Ⅵ)的去除率从100%大幅降至60.4%,表明e-是主要的光催化活性物种。当添加IPA和EDTA时,Cr(Ⅵ)去除率分别降至90.1%和95.8%,表明·OH和h+在降解过程中的作用可忽略不计。
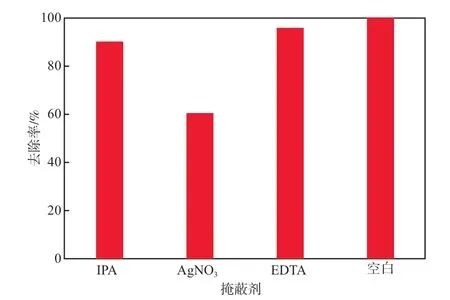
图10 掩蔽剂对Cr(Ⅵ)去除率的影响
2.3.4 机理推测
根据上述分析,推测Cu-ZIS/MX复合光催化剂光催化还原Cr(Ⅵ)的机理如图11所示。

图11 Cu-ZIS/MX光催化还原Cr(Ⅵ)的机理示意图
复合材料中,ZIS为主催化剂,Cu和Ti3C2为助催化剂。可见光照射下,ZIS价带(VB)上的电子被激发到导带(CB),由于ZIS的CB电位比Ti3C2的费米能级更负,光生电子可以迅速从ZIS转移到Ti3C2表面。同时,引入Ti3C2后,相间的强界面作用有效延长了光生载流子的寿命,使得积累在Ti3C2上的光生电子更有效地将溶液中的Cr(Ⅵ)还原为Cr(Ⅲ)。此外,Cu的掺杂有助于ZIS能带引入受体和施主态,从而大幅提高了载流子密度和电荷传输效率。ZIS和Cu-ZIS的CB电位(-0.65 V和-0.77 V)均比φ⊖(Cr2O72-/Cr3+)(+1.33 V)、φ⊖(HCrO4-/Cr3+)(+1.35 V)和φ⊖(CrO42-/Cr3+)(-0.13 V)低,因而复合材料中的光生电子具有足够的负电位驱动Cr(Ⅵ)还原为Cr(Ⅲ)。
3 结论
a)利用水热反应在超薄纳米片Ti3C2上原位生长Cu-ZIS复合微球,合成出Cu-ZIS/MX复合材料。复合材料中的Cu主要以单质铜的形式存在,但含量较低;复合材料对可见光的吸收性能较ZIS显著提升。
b)得益于Cu的掺杂提高了载流子密度和电荷传输效率以及其直接还原Cr(Ⅵ)的性能,1%Cu-ZIS复合光催化剂在60 min内对Cr(Ⅵ)的去除率可达69.5%,高于ZIS的44.3%。
c)引入Ti3C2后,复合材料的强界面作用有效延长了光生载流子的寿命,使得最佳配比的1%Cu-ZIS/MX5光照60 min后拥有对Cr(Ⅵ)近100%的去除率。1%Cu-ZIS/MX5具有良好的循环稳定性,经5次循环后仍具有较高的光催化性能,且结构未发生改变。
——潘桂棠光生的地质情怀

