镁合金生物材料在动物体内的实验研究进展
李晋香,喻正文,张 剑
遵义医科大学口腔医学院,贵州 遵义 563000
镁(Magnesium,Mg)及镁合金具有良好的力学性能和生物相容性。一方面,Mg 是人体必需元素之一,它参与多种蛋白质合成,多种酶的激活等。此外,Mg 是人体细胞内第二重要的阳离子,对于维持生物膜电位有着重要作用。另一方面,Mg 及镁合金力学性能优良,有着与人骨相似的杨氏模量(37.5~65 GPa),比强度与比刚度、抗拉强度较陶瓷材料和高分子生物材料高[1],见表1。这些特征使得其能够很好缓解骨科植入物的应力遮挡效应[2-3]。然而,Mg及镁合金在体内降解速度过快,这是阻碍镁合金进入临床应用的最大困难[4]。本文主要介绍了近年来相关重要镁合金在各领域应用的动物体内研究进展。
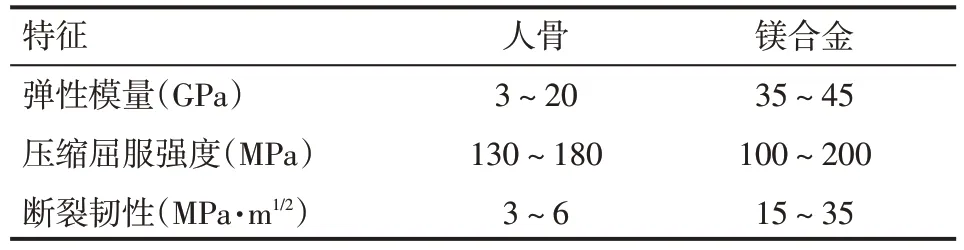
表1 镁合金植入物与人骨的对比情况
1 镁合金生物材料在医学领域的临床前期研究
1.1 骨科领域应用
现有证据表明,镁离子可以促进骨再生,且对新血管和骨组织的形成起着有益的作用,加速骨疾病的愈合[5],此外,Mg 降解产生的碱性和高镁微环境可以有效地抑制破骨细胞分化和骨吸收。骨科领域是目前镁合金研究的主要且最多方向之一,在国内外研究且取得了一定的临床进展有Mg-Y-RE-Zr(WE43)合金、Mg-5Ca-1Zn 合金和纯镁[6]。最近在我国,由Kai Xie 等[7]将(Ca-P 涂层)的Mg-Nd-Zn-Zr(JDBM)合金螺钉治疗内踝骨折,观察1至2 年。结果显示,所有患者术后内踝骨折愈合,功能恢复。上述临床试验局部均只产生少量气体且临床效果良好,这可能是与植入部位均不负重且体积较小有关。考虑到未来镁合金需要提供强大支撑力或扭转力在长骨上,因此是否能够提供足够的机械强度仍然需探索。合金化是提高Mg的机械和物理性能及其耐腐蚀性的重要步骤。Mao G等[8]在 纯Mg 中 加 入 微 量 的 锌 和 钙,轧 制 得 到Mg-2Zn-0.05Ca 合金。在体内和体外实验中表明,该合金有效地平衡机械强度和耐腐蚀性,具有潜在的骨植入应用前景。Holweg P 等[9]也制备了微量Mg-0.45Zn-0.45Ca 合金,应用于具有截骨(模拟骨折)的生长绵羊模型上,与非骨折的组相比,在骨折愈合过程中,合金体积未变化,表明其降解率得到控制。保护性涂层和表面处理则可以用来改善镁合金的耐蚀性,并潜在地增强镁合金的生物相容性和活性。Lin Z 等[10]采用等离子体离子浸没注入(PIII)技术在WE43 镁植入体表面构建了功能化的TiO2/Mg2TiO4纳米层。纳米层的应用显著提高了镁基体的耐腐蚀性,而且由于镁离子的控制释放,也提高了成骨细胞在体外的分化能力。Rendenbach C 等[11]则是将WE43 进行MAO处理,也与未处理对比,结果表明该处理有效地控制了WE43镁植入物在体内的降解行为,同时有适度的骨刺激作用,对骨膜下区域新骨形成增加。现在Mg 及镁合金表面防护处理技术繁多,但是其成本较高,而且也仍未得知最具有突出性能的表面防护处理技术。
1.2 心血管领域应用
现心血管领域镁合金主要产品为血管支架、血管缝合线及血管夹。心血管支架是研究最广的,而镁合金支架的耐腐蚀性差、血管内皮化不足导致血栓、炎症和再狭窄的发生,限制了其预期的临床应用。
合金化策略通常是为了解决镁合金的退化问题。比如,在止血夹的设计上,Ding P 等[12]采用制备了Mg-3Zn-0.2Ca 合金止血夹,均能成功结扎颈动脉,术后无一例发生血漏。且没有观察到周围炎症和少量的氢气形成,各项生化指标均正常。Yu X等[13]在此基础上添加钇元素不仅提高了合金的耐蚀性,还得到一样的良好结果,而且在长期的应用中(8个月),该夹子完全降解。但从临床应用的角度来看,合金的综合力学性能,特别是弹性模量和延展性还有待进一步提高。Bian 等[14]最近研究了一种高延展性Mg-8.5Li (wt.%)合金,在猪体内未产生血栓,对周围组织具有耐受性。在体外表明总体降解率的控制较好,但在猪体内降解率升高,显示搭建时间不足,即使如此该合金在1个月内内皮细胞也能覆盖。然而,合金元素的需求量大,成本也更高。此外,相关的体内降解机制还需要进一步研究和澄清。表面改性作为另一种候选策略,是改善镁合金支架性能的有效策略。最近两年的研究来看,Li JA等[15]在氢氧化钠钝化的Mg-Zn-Y-Nd合金表面制备了不同分子量的聚多巴胺(PDA)/透明质酸(HA)涂层,体内外实验表明,适量分子量涂层的合金具有良好的血液相容性、促内皮化、抗增生和抗炎功能。Wang P 等[16]开发了一种用于Mg-Zn-Y-Nd 合金单宁酸(TA)涂层的多功能表面,结果表明该涂层后的合金具有优异的抗氧化和抗血小板能力。此外,钽(Tantalum,Ta)涂层支持内皮细胞的生长和增殖。在大鼠皮下植入试验中,TA涂层未观察到明显的炎症反应。Mao等[17]在JD⁃BM合金表面制备片层宽度约为1~5 um的Mg3(PO4)2涂层体外证实,该涂层对人脐静脉内皮细胞的保护作用使合金的耐蚀性提高了约25%,此外溶血率也较低和良好的抗血小板黏附性能。
1.3 口腔领域应用
在口腔领域的应用中,可降解镁合金除了在颌骨内固定系统、骨缺损充填等骨科方面的应用外,在口腔种植体系统、颌面外科伤口的缝合装置以及在抗菌方面也是可降解镁合金临床应用方向。Zhao X 等[18]研究团队在之前的研究中已表明铜含量最低的Mg-0.03Cu可以提高细胞存活率、碱性磷酸酶活性以及成骨相关蛋白的表达。在最近研究中,该团队还表明了Mg-Cu合金作为潜在的植骨材料可以有效地预防牙周炎中常见的厌氧菌牙龈卟啉单胞菌和伴放线聚集杆菌手术中的感染。在目前正畸中,常用于支抗的是微型螺钉种植体(MSI)和用于外科正畸治疗的骨固定 板(BFP)。Kawamura N 等[19]比 较 了 镁 铝 锌 合 金(AZ31)与钛合金(TIA),试验表明,AZ31可获得明显高于TIA 的骨-种植体界面强度。此外,AZ31 在成骨方面优于TIA。动物实验未见严重炎症反应,对活体无损伤。所以AZ31适用于MSI和BFP。然而,该AZ31合金未在12周的实验期后降解,因此,需要更长期的研究。口腔缝线的要求很高,因为在口腔窄而深,操作不便而且口腔免疫系统强大,愈合能力及黏膜再生能力强。Li W 等[20]开发了Mg-2Zn 合金作为一种潜在的口腔缝合材料,并表明0.5 mm 的尺寸的缝合材料最适合,但在接下来研究目的中,降解率的控制还需要进一步提高。
1.4 其他领域应用
在肝胆外科中,Mg 及镁合金支架的研究主要在于对胆道狭窄及肝胆癌的干预。Guo L等[21]研究表明JDBM支架比TIA 支架更适合应用于胆管,且若用MgF2–PDLLA涂层的JDBM支架在体内的降解率下降,虽然涂层的JDBM支架尚不能满足良性胆管狭窄的支持时间,但表明了镁合金的在肝胆外科中潜在临床应用及提供了未来研究方向提供了思路,即降低镁合金的降解率。Li T 等[22]和Peng H等[23]都用高纯Mg与钛(Ti)支架对比,在体内及体外研究表明Mg 的降解产物能显著抑制肝胆区癌细胞的生长并促进其凋亡,这些结果进一步为镁在胆道外科领域的应用提供了理论支持。
在泌尿系统的应用中,Zhang S 等[24-25]将Mg-Zn(6wt.%)合金和ZK60 合金(Mg5.6wt%Zn0.5wt%Zr)与纯镁对比研究表明,三者均有良好的生物相容性,在体外(SBF溶液、人工尿液中)、体内(大鼠膀胱)中前两者的降解速率均比纯镁快,但与输尿管支架的平均临床留置时间为8~12 周相比,这项实验时间较短,也未提出更佳的镁合金植入材料。为此在最近的研究中,Tian Q 等[26]在体外研究人尿路上皮细胞与抗菌性能较好的Mg-4Zn-1Sr(ZJ41)合金生物相容性最好,但应进一步降低镁合金的降解率。当然,此合金尚需体内实验进一步研究。因此该团队,Di Tie等[27]首次在大型动物(广西巴马小型猪)中对该合金输尿管支架植入物进行体内研究,表明与目前广泛使用的不锈钢支架相比,该合金具有相似的生物相容性,但抗菌活性明显增强。
2 结论与展望
综合以上论述,镁及镁合金作为植入物材料的最大限制是其快速的降解速率,严重损害了镁植入物保持其结构的能力。众多研究者通过合金化,表面改性等途径合成的新型镁合金在性能上都得到了不断提高,证明了镁及合金作为未来生物植入物的理想候选者的潜力,但是这些技术虽然有效改善了镁合金的机械性能及降解速率,但要想完全满足镁合金临床植入期望,仍需要不断改进,而且现今对于哪种元素是镁合金最佳的合金元素,哪种镁合金在临床上综合性能最好都无定论。今后的工作重点还是应放在提高镁合金生物相容性、机械性能及腐蚀性能上,通过对找到最合适的合金化元素、添加量以及在表面改性的技术上更加优化,相信在不久的将来镁合金的应用及适用性更加广泛。

